¿CÓMO LO HARÍA?
Los autores presentan un interesante caso de una paciente de 10 años, con antecedentes familiares de enfermedad de Rendu-Osler-Weber, que presenta cianosis, poliglobulia y saturación basal del 85%, secundarias a una malformación arteriovenosa pulmonar (MAVP) grande y compleja, que genera desaturación sistémica por la existencia de un cortocircuito derecha-izquierda significativo.
Las MAVP son comunicaciones directas entre ramas arteriales, generalmente de arteria pulmonar, y venas pulmonares, sin que exista un lecho capilar normal, unidas mediante un saco aneurismático, que puede estar parcialmente septado en su interior. Se dividen en simples, cuando reciben sangre de una única arteria aferente, y complejas, cuando la aferencia es múltiple.
La mayoría son de origen congénito y en más del 70% de los casos se asocian a enfermedad de Rendu-Osler-Weber, o telangiectasia hemorrágica hereditaria. Esta es una enfermedad autosómica dominante que, aunque se puede confirmar por estudio genético, dispone de unos criterios diagnósticos, denominados criterios de Curaçao1, que permiten su diagnóstico:
Epistaxis recurrente.
Múltiples telangiectasias en localizaciones típicas: labios, cavidad oral, dedos y nariz.
Malformaciones vasculares viscerales: gastrointestinales, pulmonares, hepáticas, cerebrales o espinales.
Familiar en primer grado con la enfermedad.
Si se cumplen 3 o más criterios, el diagnóstico es definitivo, y se considera posible con la existencia de 2 de ellos.
La mayoría de las veces es asintomática, y la presencia de clínica va a depender del tamaño y del número. Los síntomas asociados a las MAVP son:
Relacionados con la desaturación, por el cortocircuito derecha-izquierda, con saturaciones en sangre periférica inferiores al 90%, que conlleva la presencia de cianosis, acropaquias y policitemia reactiva.
Debidos a la fragilidad de las paredes de las MAVP, que pueden romperse hacia el lecho bronquial, generando hemoptisis, o hacia el espacio pleural, produciendo hemotórax.
Debido a la ausencia de filtro capilar pulmonar, pueden ocurrir embolias paradójicas y es posible la formación frecuente de abscesos cerebrales.
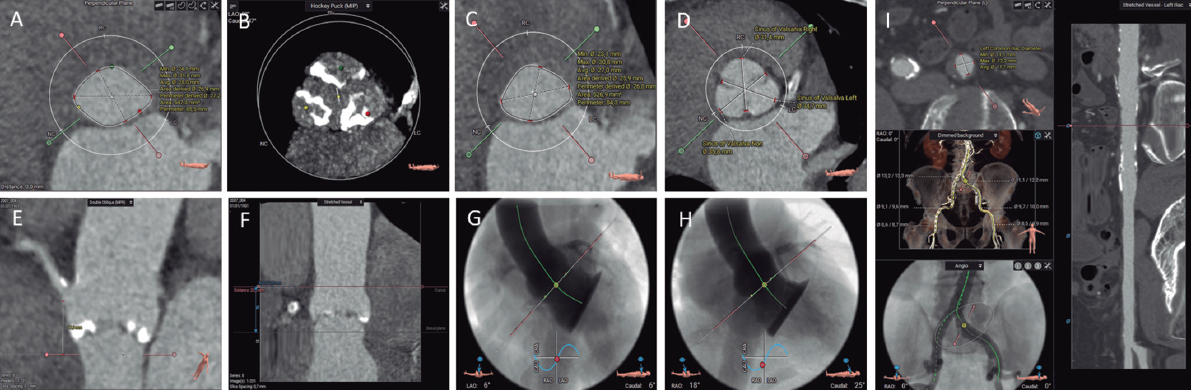
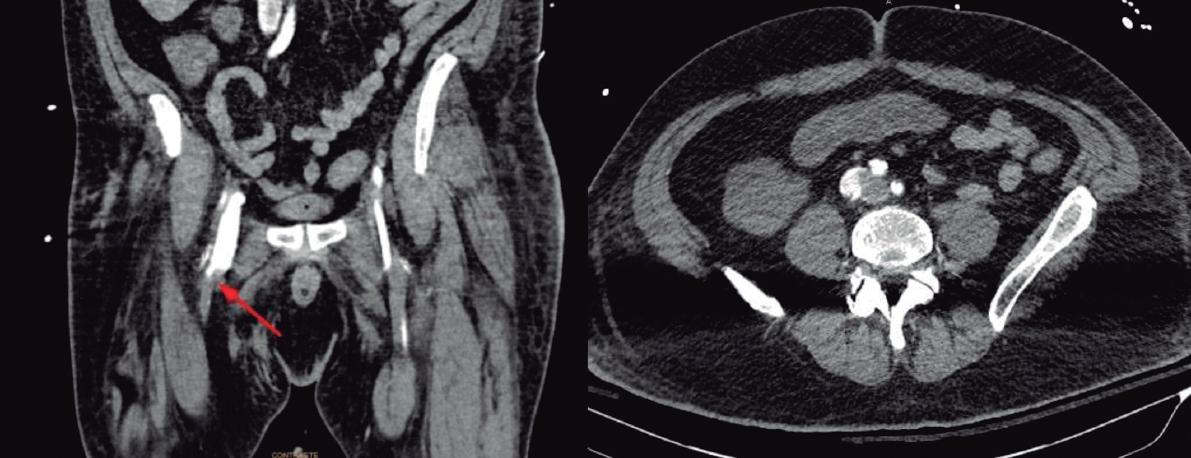
El diagnóstico se basa en la existencia de signos clínicos sugestivos. La radiografía de tórax muestra alteraciones en más del 95% de los pacientes. En la ecocardiografía con solución salina agitada se observa el paso de burbujas al cabo de 3-5 segundos (3 a 8 ciclos cardiacos). Hoy en día la tomografía computarizada es la prueba de referencia; permite un estudio anatómico preciso y es útil en la planificación de la embolización y en el seguimiento evolutivo.
Aunque inicialmente se indicaba la resección quirúrgica, el tratamiento de elección es la embolización endovascular. Se considera indicado2 cuando la arteria aferente es ≥ 3 mm, ya que con este tamaño el riesgo de embolia paradójica es mayor del 1,5% anual. Gracias a la mejora en los materiales es posible realizar el procedimiento con seguridad en arterias aferentes menores de 2 mm, por lo que en los casos entre 2 y 3 mm se recomienda la valoración individualizada del paciente.
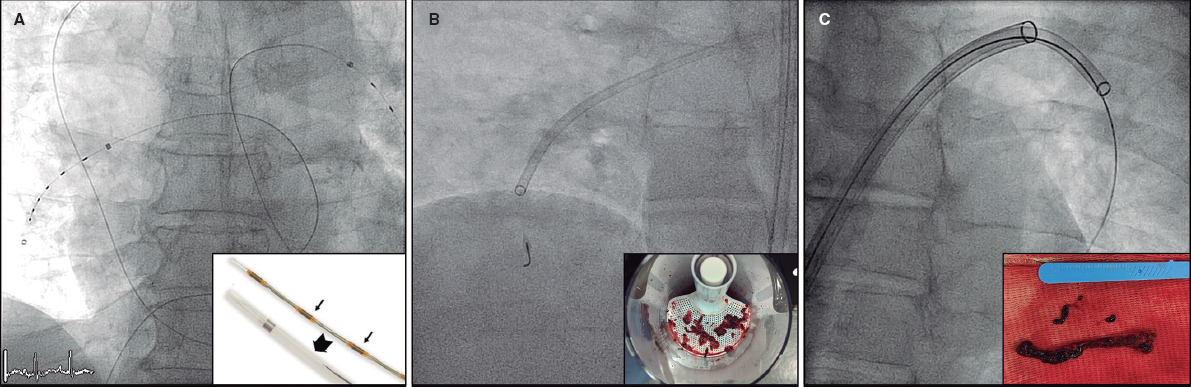
Para realizar la embolización se pueden emplear espirales metálicas (coils), descritas por Gianturco et al.3 en 1975. En nuestro caso usamos MReye Flipper Detachable Embolization Coil (Cook, Estados Unidos). Para empezar la embolización con una espiral de liberación controlada, del tamaño adecuado, se recomienda seleccionarla al menos un 30% mayor que el diámetro del vaso diana, y liberarla lo más distal posible en la arteria aferente. Tras la primera espiral se añaden otras hasta completar la oclusión. Otra opción es emplear para la embolización tapones vasculares, que son dispositivos de nitinol. En nuestro caso usamos dispositivos de la familia Amplatzer Vascular Plug (Abbott, Estados Unidos), seleccionando el tamaño un 30-50% mayor que el diámetro del vaso a ocluir y liberándolo lo más distal posible en la arteria aferente, evitando interferir con otras ramas que nazcan hacia el parénquima sano. La elección de uno u otro material muchas veces depende de la experiencia y de las preferencias del operador.
En el caso que se nos presenta, la indicación de cierre se debe a la importancia del cortocircuito, que genera desaturación, y a las com- plicaciones por el tamaño de la malformación, de embolia paradójica y de rotura.
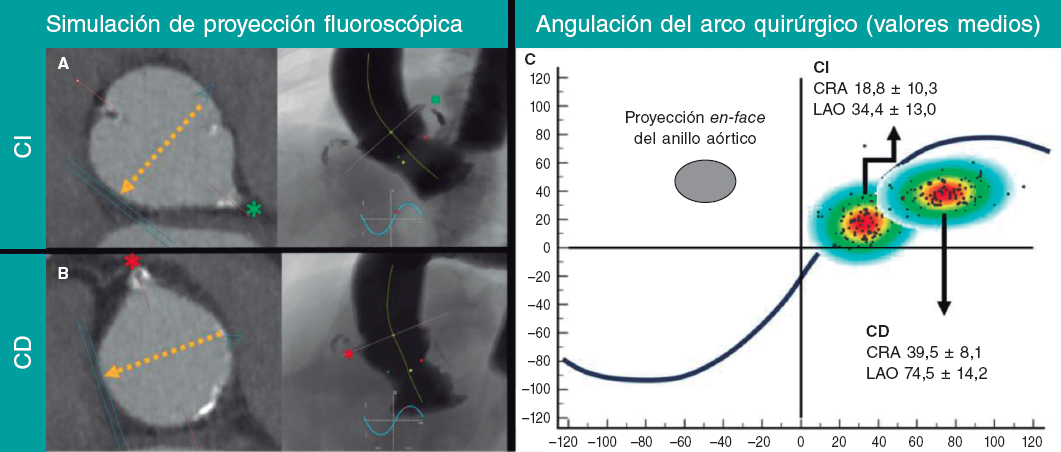
En nuestra experiencia, el análisis previo de la tomografía computarizada permite estudiar las zonas objetivo de embolización, anticipar los dispositivos a usar y los ángulos de trabajo más favorables, así como controlar la existencia de ramas que perfunden tejido sano que se deben evitar interferir con los dispositivos.
En cuanto al procedimiento, realizado bajo anestesia general, por acceso venoso femoral derecho, con un introductor de 6 Fr, se ascendería un catéter Wedge (Teleflex, Estados Unidos) hasta la rama pulmonar derecha. Desde ahí se avanzaría selectivamente hacia las arterias aferentes apoyado en catéteres diagnósticos de 4 o 5 Fr, curvas multipropósito, Judkins Right 4,0, Cobra o Vertebral, usando guías hidrófilas de 0,018 a 0,035 pulgadas (Radiofocus Guide Wire, Terumo, Japón) o guías workhorse coronarias de 0,014 pulgadas. Realizamos angiografías selectivas en cada arteria aferente para confirmar las características del vaso diana de la embolización. Una vez avanzado hasta el nido de la malformación, se intercambia a la vaina transportadora. En este escenario, mi preferencia es por dispositivos autoexpandibles de nitinol tipo Amplatzer Vascular Plug (AVP), Amplatzer Vascular Plug II (AVP II) o Amplatzer Vascular Plug IV (AVP 4) (Abbott, Estados Unidos). En ocasiones usamos espirales y tapones en el mismo paciente en función de las características anatómicas de cada aferente. En este caso, abordaría una por una las 3 arterias aferentes en el mismo procedimiento e iría liberando los dispositivos, tras confirmar su correcta posición y su estabilidad. Dada la ausencia de un lecho capilar limitante, existe la posibilidad de migración a las cavidades izquierdas, y por lo tanto es importante un adecuado dimensionamiento de los dispositivos. En caso de producirse esta complicación, desde un abordaje arterial, generalmente femoral, se alcanzaría el dispositivo y se capturaría con un lazo para su extracción, mediante una vaina de 2 Fr mayor que la empleada en la liberación.
Tras la oclusión, en el seguimiento evolutivo, se recomienda realizar un control con tomografía computarizada a los 6 meses para confirmar el cierre efectivo y descartar la recanalización de las arterias embolizadas o la aparición de nuevas malformaciones. Asimismo, se recomiendan controles posteriores periódicos.
FINANCIACIÓN
Ninguna.
CONFLICTO DE INTERESES
Ninguno.
BIBLIOGRAFÍA
1. Shovlin CL, Guttmacher AE, Buscarini E, et al. Diagnostic criteria for hereditary hemorrhagic telangiectasia (Rendu-Osler-Weber syndrome). Am J Med Genet. 2000;91:66-67.
2. Faughnan ME, Mager JJ, Hetts SW, et al. Second International Guidelines for the Diagnosis and Management of Hereditary Hemorrhagic Telangiectasia. Ann Intern Med. 2020;173:989-1001.
3. Gianturco C, Anderson JH, Wallace S. Mechanical devices for arterial occlusion. Am J Roentgenol Radium Ther Nucl Med. 1975;124:428-435.
* Autor para correspondencia: Servicio de Cardiología, Hospital Universitario Cruces, Pza. de Cruces s/n, 48903 Barakaldo, Bizkaia, España.
Correo electrónico: blancomata@yahoo.es (R. Blanco Mata).