RESUMEN
Introducción y objetivos: El implante percutáneo de válvula aórtica (TAVI) se introdujo en 2007 como una alternativa a la cirugía a corazón abierto para tratar a pacientes con estenosis aórtica grave sintomática, y desde entonces han aumentado las indicaciones autorizadas. Recientemente, el Placement of Aortic Transcatheter Valve Study (PARTNER) 3 ha demostrado beneficios clínicos con el TAVI con la válvula SAPIEN 3 frente al reemplazo quirúrgico de válvula aórtica (RVAo) en pacientes seleccionados con bajo riesgo de mortalidad quirúrgica. Utilizando los datos del PARTNER 3 junto con datos económicos de España, se evaluó la relación coste-efectividad del TAVI en comparación con el RVAo en pacientes con estenosis aórtica grave sintomática con bajo riesgo de mortalidad quirúrgica.
Métodos: Se utilizó un modelo en dos etapas para estimar los costes directos sanitarios y los datos de calidad de vida relacionadas con la salud para TAVI con la válvula SAPIEN 3 y RVAo. Los eventos adversos tempranos relacionados con TAVI del PARTNER 3 se incluyeron en un modelo de Markov, que capturó los resultados a más largo plazo tras TAVI o RVAo.
Resultados: El TAVI con SAPIEN 3 mejoró los años de vida ajustados por calidad por paciente (+1,00), con un aumento en el coste frente al RVAo de 6.971 € por paciente. Esto representó una ratio coste-efectividad incremental por año de vida ganado ajustado por calidad de 6.952 € por paciente. Los resultados fueron robustos en los diversos análisis de sensibilidad realizados, en los que el TAVI con SAPIEN 3 se mantiene como una opción coste-efectiva.
Conclusiones: El TAVI con SAPIEN 3 es coste-efectivo en comparación con el RVAo en pacientes con estenosis aórtica grave sintomática con bajo riesgo de mortalidad quirúrgica. Estos resultados pueden informar a los decisores políticos en España para facilitar el desarrollo de políticas sobre la selección de opciones terapéuticas en esta población de pacientes.
Palabras clave: España. Implante percutáneo de válvula aórtica. Cirugía cardiaca. Prótesis valvular cardiaca. Reemplazo quirúrgico de válvula aórtica. Análisis coste-beneficio. Análisis coste-efectividad. Estenosis aórtica. Bajo riesgo.
ABSTRACT
Introduction and objectives: Transcatheter aortic valve implantation (TAVI) was first introduced in 2007 as an alternative to open heart surgery to treat patients with severe symptomatic aortic stenosis (sSAS) with various indication expansions since that date. Recently, the PARTNER 3 study (Placement of aortic transcatheter valve) demonstrated clinical benefits with TAVI with the SAPIEN 3 valve vs surgical aortic valve replacement (SAVR) in selected low surgical mortality risk patients. We reviewed data from the PARTNER 3 and economic data from Spain to assess the cost-effectiveness ratio of TAVI vs SAVR in patients with sSAS and low surgical mortality risk.
Methods: A 2-stage model was used to estimate direct healthcare costs and health-related quality of life data regarding TAVI with the SAPIEN 3 valve and SAVR. Early adverse events associated with TAVI from the PARTNER 3 were fed into a Markov model that captured longer-term outcomes after TAVI or SAVR.
Results: TAVI with SAPIEN 3 improved quality-adjusted life years per patient (+ 1.00) with an increase in costs vs SAVR (€6971 per patient). This meant an incremental cost-effectiveness ratio/quality-adjusted life year of €6952 per patient. The results were robust with TAVI with the SAPIEN 3 valve remaining cost-effective across several sensitivity analyses.
Conclusions: TAVI with the SAPIEN 3 valve is cost effective compared to SAVR in patients with sSAS and low surgical mortality risk. These findings can inform policymakers to facilitate policy development in Spain on intervention selection in this patient population.
Keywords: Spain. Transcatheter aortic valve replacement. Heart procedures and surgeries. Prosthetic heart valve. Surgical aortic valve replacement. Cost-benefit analysis. Cost-effectiveness analysis. Aortic stenosis. Low-risk.
Abreviaturas
AVAC: años de vida ajustados por calidad. EAGs: estenosis aórtica grave sintomática. ICER: ratio coste-efectividad incremental. RVAo: reemplazo quirúrgico de válvula aórtica. TAVI: implante percutáneo de válvula aórtica.
INTRODUCCIÓN
La estenosis aórtica afecta a casi el 3% de la población adulta de más de 65 años.1 Suele tener un periodo latente asintomático inicial, pero a medida que la enfermedad avanza, se hacen evidentes los signos de insuficiencia cardiaca, angina o síncope1,2. Se recomienda sustituir la válvula aórtica en la mayoría de los pacientes sintomáticos con evidencias ecocardiográficas de estenosis aórtica significativa, así como también en ciertos pacientes asintomáticos1,2.
Desde que se realizó el primer implante percutáneo de válvula aórtica (TAVI) como opción terapéutica para tratar una estenosis aórtica grave sintomática (EAGs) hace casi 20 años, las evidencias de los ensayos clínicos han seguido avalando el uso de este procedimiento3. En 2013, el TAVI se convirtió en el tratamiento de elección para pacientes inoperables con EAGs y pacientes con riesgo alto de mortalidad quirúrgica. En los últimos tiempos, este tratamiento de elección se ha ido ampliando hasta incluir a pacientes con un riesgo intermedio/bajo de mortalidad quirúrgica4,5.
El estudio PARTNER 3 (Placement of aortic transcatheter valve study), publicado recientemente, forma parte de la cada vez mayor y más sólida evidencia clínica disponible. Se trata de un estudio pivotal controlado, aleatorizado y multicéntrico de pacientes con EAGs y un riesgo bajo de mortalidad quirúrgica6,7. Este estudio comparó los diferentes resultados de tratamiento obtenidos con el reemplazo quirúrgico de válvula aórtica (RVAo) y el TAVI con la prótesis valvular cardiaca percutánea SAPIEN 3 mediante abordaje transfemoral6,7. Comparado con el RVAo, el TAVI con la válvula SAPIEN 3 redujo el riesgo en la variable agregada compuesta por muerte, accidente cerebrovascular o rehospitalización en el seguimiento a 1 y 2 años6,7. Gracias a estos avances clínicos tan satisfactorios, las guías elaboradas conjuntamente por la European Society of Cardiology (ESC)/European Association for Cardio-Thoracic Surgery (EACTS) recomiendan, ahora, el RVAo en pacientes más jóvenes de bajo riesgo y el TAVI como tratamiento de elección en pacientes de mayor edad. También se puede considerar en todos los pacientes con EAGs tras una minuciosa evaluación de las características clínicas, anatómicas y quirúrgicas de cada paciente por parte del equipo multidisciplinar5.
Aunque en España no se cuenta con guías de tratamiento específicas sobre el uso del TAVI, la Sociedad Española de Cardiología, como miembro de la ESC, avala las guías de ésta, siendo las que se siguen por los profesionales sanitarios españoles5. Con independencia de estas guías, en España, el TAVI sigue empleándose poco en comparación con otros países europeos. A pesar de contar con una mayor infraestructura8, definida como el número de centros TAVI por millón de habitantes, los índices de intervenciones TAVI realizadas varían mucho de una región española a otra9. En 2021, casi 5.000 pacientes se beneficiaron en España de esta transformadora tecnología mínimamente invasiva. Según un estudio publicado recientemente10, el número anual de pacientes aptos para recibir el TAVI en España se sitúa en torno a los 15.783 pacientes, incluidos los de riesgo bajo. Si a esto le sumamos los cada vez mayores y evidentes beneficios clínicos del TAVI en pacientes con EAGs, parece relevante realizar un análisis coste-efectividad del uso del TAVI frente al RVAo en pacientes con EAGs de bajo riesgo quirúrgico para quienes el TAVI está ahora recomendado en las últimas guías publicadas5. Además, comparado con el RVAo, el TAVI transfemoral con la válvula SAPIEN 3 ha demostrado ser coste-efectivo en población española de riesgo intermedio y alto11. Esto no hace sino poner de manifiesto que se necesitan más evidencias sobre el análisis coste-efectividad del TAVI con la válvula SAPIEN 3 en la población española de pacientes de riesgo quirúrgico bajo con EAGs. Así pues, el objetivo de este artículo es revisar los resultados del PARTNER 3 y los datos económicos de España para evaluar el coste-efectividad del uso del TAVI frente al RVAo en pacientes con EAGs y riesgo bajo de mortalidad quirúrgica.
MÉTODOS
Se desarrolló un análisis coste-utilidad empleando metodología validada para poblaciones francesas12 e italianas13 para calcular cualquier cambio tanto en los costes sanitarios directos y calidad de vida relacionada con la salud derivados del uso del TAVI con la válvula SAPIEN 3 frente al RVAo en pacientes con EAGs y riesgo bajo de mortalidad quirúrgica (puntuación en la Society of Thoracic Surgeons < 4%) desde la perspectiva del Sistema Nacional de Salud de España. Los costes se calcularon según la cotización del euro de 2021 y los beneficios se midieron en años de vida ajustados por calidad (AVAC) ganados. La ratio coste-efectividad incremental (ICER) se calculó dividiendo la diferencia de costes entre los 2 grupos de tratamiento por la diferencia en AVAC. Al igual que en otros estudios publicados11,14, se empleó una ICER < 30.000 € por AVAC ganado como el umbral de disponibilidad a pagar (DAP) de un coste-efectividad aceptable.
Estructura del modelo
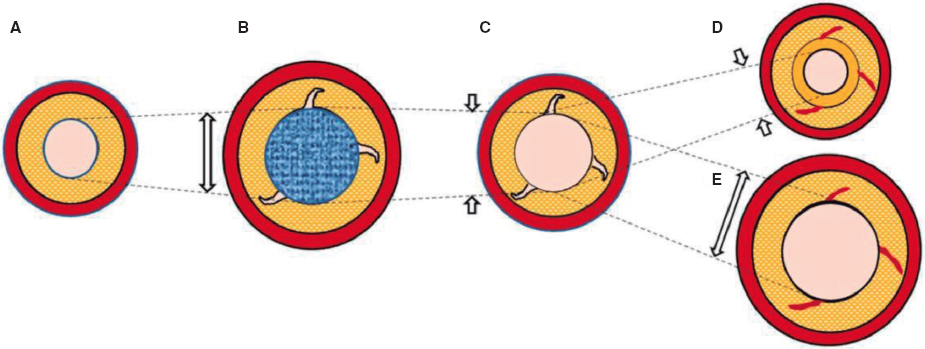
Los detalles de la estructura del modelo en 2 etapas ya se han descrito en la población francesa12. En resumen, se incorporaron en un árbol de decisión los eventos adversos tempranos secundarios al TAVI obtenidos de los datos del estudio PARTNER 3 a 30 días6 (figura 1A). Posteriormente, estos datos fueron incorporaron a un modelo de Markov que incluyó 4 estados de salud distintos (‘vivo y estable’, ‘fibrilación auricular [FA] tratada’, ‘accidente cerebrovascular discapacitante’ y ‘muerto’) para reflejar los resultados clínicos a más largo plazo de pacientes tratados mediante TAVI o RVAo (figura 1B). Todos los autores consideraron el modelo apto para el contexto español según sus conocimientos en materia clínica y económica.

Figura 1. Figura central. El modelo de coste-efectividad tiene 2 etapas: a) los EA tempranos del PARTNER 3 se incorporaron a un árbol de decisión que se usó para alimentar b) un modelo de Markov que incorporó los resultados a más largo plazo de pacientes clasificados en 4 estados de salud: ‘Vivo y Estable’ = pacientes intervenidos que sobrevivieron con solo algún EA a corto plazo o sin ningún EA; los pacientes de este estado de salud pueden pasar a ‘accidente cerebrovascular discapacitante’, ‘FA en tratamiento’ o ‘muerto’ en cualquier momento durante el tiempo de duración del modelo. ‘FA en tratamiento’ = pacientes intervenidos que sobrevivieron y terminaron desarrollando FA que precisó tratamiento específico. Esto puede ocurrir durante los primeros 30 días o durante el resto del tiempo de duración del modelo. Los pacientes de este estado de salud pueden pasar a ‘accidente cerebrovascular discapacitante’ o ‘muerto’ en cualquier momento durante el tiempo de duración del modelo. ‘Accidente cerebrovascular discapacitante’ = pacientes intervenidos que sobrevivieron y terminaron sufriendo un accidente cerebrovascular discapacitante. Esto puede ocurrir durante los primeros 30 días o durante el tiempo de duración del modelo. Los pacientes de este estado de salud sólo pueden pasar al estado ‘muerto’ en cualquier momento durante el tiempo de duración del modelo. ‘Muerto’ = este es el estado absorbente del modelo: todos los pacientes del modelo corren el riesgo de fallecer por mortalidad general de cualquier causa; los pacientes con FA en tratamiento y accidente cerebrovascular corren un mayor riesgo de muerte.
Reproducido con permiso de Gilard M, et al. Value Health 202112 bajo los términos de la licencia Creative Commons.44 EA: evento adverso; FA: fibrilación auricular; RVAo: reemplazo quirúrgico de válvula aórtica; TAVI: implante percutáneo de válvula aórtica.
Dado que el tratamiento de elección de la EAGs durante la supervivencia consiste en el reemplazo valvular, se escogió un periodo de tiempo de esperanza de vida máximo de 50 años para realizar el análisis coste-utilidad, con un factor anual de descuento del 3% aplicado a costes y beneficios futuros, según las recomendaciones específicas para España15. Se optó por este marco temporal para reflejar todas las posibles consecuencias para pacientes con EAGs a lo largo de la vida. Tanto los costes sanitarios como la calidad de vida relacionada con la salud se calcularon empleando AVAC.
Inputs del modelo
Resumen del estudio
El modelo se construyó sobre la base de la población del estudio PARTNER 3 que excluyó a pacientes con fragilidad clínica, válvulas aórticas bicúspides o cualquier otra característica anatómica que aumentara el riesgo de complicaciones asociadas a la cirugía o al TAVI. El PARTNER 3 reclutó a 1.000 pacientes, 503 de los cuales fueron aleatorizados a recibir TAVI y 497 RVAo con grupos ‘tratados’ de 496 y 454 pacientes, respectivamente6. El objetivo primario del estudio fue una variable agregada compuesta de mortalidad por cualquier causa, accidente cerebrovascular o rehospitalización al año tras la intervención.
Eventos clínicos
Las probabilidades de los eventos clínicos empleados en el modelo (tabla 1 del material adicional) se basaron en un árbol de decisión que incorporó todos los eventos adversos tempranos experimentados en el PARTNER 3 hasta 30 días después de la intervención. Se calcularon las probabilidades de transición mensual entre los diferentes estados de salud del modelo de Markov. Para calcular la transición entre los estados ‘vivo y estable’ y ‘FA en tratamiento’, se emplearon datos del PARTNER 3 sobre FA en tratamiento de nueva aparición entre 30 días y 1 año6. Otras fuentes bibliográficas ofrecieron cálculos más realistas sobre las otras 2 transiciones debido a la escasez de estos eventos en el PARTNER 3. Se usaron datos sobre la carga de accidentes cerebrovasculares en España (Stroke Alliance for Europe)16 para la transición de ‘vivo y estable’ a ‘accidente cerebrovascular discapacitante’ y datos de una revisión sistemática/metanálisis de 104 estudios de cohortes elegibles para la transición de FA en tratamiento’ a ‘accidente cerebrovascular discapacitante’17. El infarto de miocardio, el accidente isquémico transitorio y las hemorragias graves o amenazantes para la vida se reflejaron como eventos clínicos intercurrentes ocurridos entre 30 días y 1 año según datos del PARTNER 36. También se tuvieron en cuenta otros eventos importantes tales como las tasas de rehospitalización según datos del PARTNER 36, reintervención por deterioro de la válvula (datos de seguimiento del PARTNER 3 hasta los 2 años)6,7 y los resultados a 20 años de la bioprótesis valvular aórtica de los 3 años en adelante18 (tabla 1 del material adicional). En el caso base se empleó la misma tasa de reintervenciones tanto para el grupo TAVI como para el RVAo, este supuesto simplificador permitió usar mejor los datos disponibles. En el escenario 1 se asumieron tasas más altas de reintervención para el TAVI con la válvula SAPIEN 3 que para el RVAo según los datos a 5 años del PARTNER 219. En el escenario 2, en cambio, se asumió un mayor riesgo de accidentes cerebrovasculares, lo cual coincide con los resultados del PARTNER 3.
Extrapolación de la supervivencia
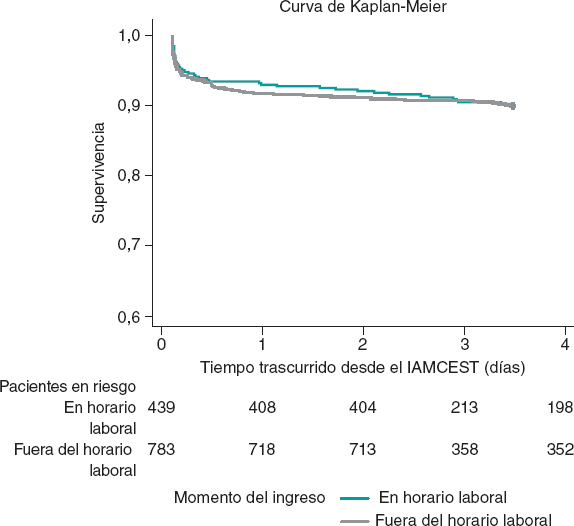
Hubo 2 opciones en lo referente a la extrapolación de la supervivencia. En la opción 1 las probabilidades de transición de un estado a otro se tomaron de la literatura médica (riesgo relativo de muerte con FA y con accidente cerebrovascular discapacitante de 1,517 y 2,0520, respectivamente). En la opción 2 el ajuste paramétrico de la supervivencia se realizó empleando los datos del modelo de Kaplan-Meier extraídos del PARTNER 3. Se emplearon 3 distribuciones paramétricas (Weibull, Exponential, Gompertz) que se ajustaron a la supervivencia de toda la población española. Por lo tanto, en el caso base, la supervivencia se calculó teniendo en cuenta las probabilidades de transición por la inmadurez de los datos de supervivencia del estudio. El riesgo anual de mortalidad para el estado ‘vivo y estable’, así como otros riesgos relativos para diferentes estados de salud se muestran en la tabla 2 del material adicional. La opción 2 (análisis paramétrico de la supervivencia) se exploró empleando hazard ratios (HR) alternativos en el escenario 3: HR = 0.75 según datos del PARTNER 3 a los 2 años ajustados por la mortalidad global de la población española. Un 4º escenario adicional eliminó cualquier posible beneficio sobre la supervivencia con la válvula SAPIEN 3 (HR = 1).
Utilidades de salud
Hubo 2 opciones para determinar el decremento de las utilidades de salud: la opción 1 empleó decrementos de las utilidades de salud según la literatura médica ajustados por edad y estándares de la población española21. Esta fue la opción preferida dados los pocos eventos descritos el PARTNER 3 y porque las estimaciones a partir de la literatura médica se consideraron realistas. Los decrementos ajustados por estándares etarios y poblacionales fueron 0,1622 y 0,42 para la FA y el accidente cerebrovascular discapacitante, respectivamente23. La opción 2 empleó las opciones de tratamiento del PARTNER 3 y se analizó dentro del escenario 5. En la opción 2 cada decremento en las utilidades de salud se extrajo individualmente del PARTNER 3 en el momento basal, a los 30 días, 6 meses y 1 año; después, se convirtieron a utilidades de salud españolas24.
Inputs en materia de costes
Los costes asociados al TAVI y al RVAo (intervención, complicaciones y largo plazo) se muestran en la tabla 3 del material adicional. La información de los costes del procedimiento se extrajo del SERGAS25. Se debe mencionar que el coste del SERGAS incluye tanto el valor de mercado de la válvula como el precio del material complementario. Los costes de personal se calcularon como coste por hora para los distintos profesionales sanitarios. Los costes correspondientes a las complicaciones y a los estados de salud se extrajeron de la literatura médica y de grupos relacionados por el diagnóstico (GRD). El coste desglosado del TAVI y el RVAo se muestra en la tabla 4 del material adicional. Los micro-costes se obtuvieron del estudio realizado por Bayón et al.26 y fueron actualizados para reflejar la actual práctica TAVI en pacientes españoles de bajo riesgo con EAGs. Como los costes varían según la región española de que se trate, se exploraron 3 escenarios adicionales: 6A, 6B y 6C con información sobre costes que se ajustó para reflejar la práctica clínica habitual en Murcia, Huelva y País Vasco. También se incluyó un 7.º escenario con el coste de los eventos adversos tempranos a 30 días.
Outputs del modelo
Los principales outputs del modelo fueron los costes globales por paciente y los AVAC de cada brazo y la ICER.
Análisis de sensibilidad
Para calcular la incertidumbre, se realizaron análisis de sensibilidad determinísticos variando diferentes inputs empleando intervalos de confianza y rangos descritos en la literatura médica, si los hubiere y, en su defecto, rangos plausibles (tabla 5 del material adicional). Se modificaron diversos parámetros y se analizó el impacto en los resultados. La incertidumbre global de los parámetros se abordó empleando 1 análisis de sensibilidad probabilístico (ASP) (tabla 6 del material adicional). Se analizaron diferentes escenarios para estudiar el impacto de los principales supuestos estructurales tal y como se muestran en la tabla 7 del material adicional. Todos los análisis se realizaron empleando la hoja de cálculo Excel de Microsoft (Microsoft Corporation, Estados Unidos).
RESULTADOS
Caso base
El TAVI con la válvula SAPIEN 3 mejoró los AVAC por paciente (+ 1,0) a un mayor coste que el RVAo (alrededor de 6.971 € por paciente). Esto supuso una ICER de 6.952 € por AVAC, inferior al umbral de DAP de 30.000 €/AVAC referenciado habitualmente en el contexto español. Los resultados a 50 años del caso base se muestran en la tabla 1. El desglose de los costes del TAVI frente al RVAo confirmó que aunque, en el modelo, los costes iniciales de la intervención fueron más altos para el TAVI, los costes del ‘accidente cerebrovascular discapacitante’ y la ‘FA en tratamiento’ fueron algo más bajos (tabla 1 y figura 1 del material adicional).
Tabla 1. Resultados del caso base con costes agudos y durante la supervivencia
| Resumen de resultados | TAVI con SAPIEN 3 | RVAo | Incremental |
|---|---|---|---|
| Coste por paciente | 39.052 € | 32.081 € | 6.971 € |
| Año de vida ganado (no descontado) | 14,08 | 13,22 | 0,86 |
| Mediana de supervivencia (años) | 16,50 | 14,50 | 2,00 |
| AVAC por paciente | 8,66 | 7,66 | 1,00 |
| Ratio coste-efectividad incremental (ICER) | 6.952 € | ||
| Beneficio monetario neto incremental (NMB) | 23.111 € | ||
| Beneficio de salud neto incremental (NHB) | 0,77 | ||
| Coste fase aguda (primera hospitalización y rehabilitación) | |||
| Primera Hospitalización | 24.781 € | 13.779 € | 11.003 € |
| Rehabilitación | 114 € | 461 € | - 347 € |
| Implante de marcapasos | 506 € | 311 € | 195 € |
| Costes derivados de la fase aguda | 25.401 € | 14.550 € | 10.656 € |
| Costes adicionales al año | |||
| IM | 181 € | 92 € | 89 € |
| Costes derivados de complicaciones asociadas al implante de marcapasos | 38 € | 23 € | 15 € |
| Costes de hospitalización | 212 € | 316 € | -104 € |
| Costes de reintervención | 117 € | 147 € | -30 € |
| Costes del estado de salud «vivo y estable» | 1.258 € | 844 € | 415 € |
| Costes del estado de salud «FA en tratamiento» | 48 € | 376 € | -328 € |
| Costes del estado de salud «accidente cerebrovascular discapacitante» | 11 € | 221 € | -210 € |
| Costes derivados de la mortalidad | 0 € | 0 € | 0 € |
| Coste global a 1 año | 27.267 € | 16.570 € | 10.698 € |
| Costes adicionales durante la supervivencia | |||
| Costes derivados de complicaciones asociadas al implante de marcapasos | 433 € | 251 € | 182 € |
| Costes de hospitalización | 374 € | 353 € | 21 € |
| Costes de reintervención | 4.464 € | 4.941 € | -477 € |
| Costes del estado de salud «vivo y estable» | 4.120 € | 2.590 € | 1.530 € |
| Costes del estado de salud «FA en tratamiento» | 970 € | 3.963 € | -2.993 € |
| Costes del estado de salud «accidente cerebrovascular discapacitante» | 1.424 € | 3.414 € | -1.990 € |
| Costes adicionales durante la supervivencia | 11.785 € | 15.512 € | -3.727 € |
| Costes totales durante la supervivencia | 39.052 € | 32.081 € | 6.971 € |
| AVAC: años de vida ajustados por calidad; FA: fibrilación auricular; IM: infarto de miocardio. | |||
Análisis de sensibilidad determinísticos
Los análisis de sensibilidad univariados se muestran en el diagrama de tornado (figura 2). El TAVI con la válvula SAPIEN 3 siguió siendo coste-efectivo con independencia de cualquier posible cambio sobre parámetros individuales del modelo (nota: se muestran en el diagrama los 20 parámetros con mayor influencia sobre el modelo). El modelo fue más sensible a la edad, a los costes del RVAo y al riesgo de accidente cerebrovascular a los 30 días asociado al TAVI.
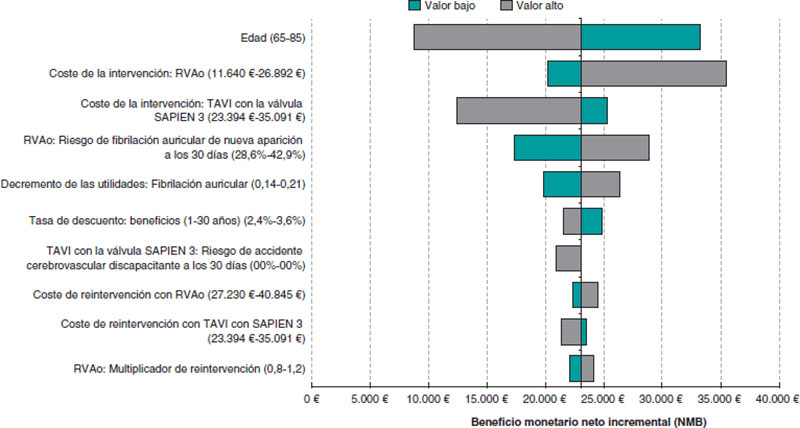
Figura 2. Diagrama de tornado con los 20 parámetros de más influencia del modelo (análisis de sensibilidad determinístico).
Análisis de sensibilidad probabilístico
Los resultados del ASP vienen a confirmar los resultados del análisis del caso base. En el umbral convencional de DAP de 30.000 €/AVAC, el TAVI con la válvula SAPIEN 3 sigue siendo coste-efectivo comparado con el RVAo en el 100% de las simulaciones realizadas en el modelo (figura 3A). Además, la curva de aceptabilidad indica que el tratamiento con TAVI con la válvula SAPIEN 3 tiene una probabilidad del 99,9% de ser coste-efectivo con un umbral de DAP de 30.000 €/AVAC (figura 3B). Los supuestos del ASP se muestran en la tabla 5 del material adicional.
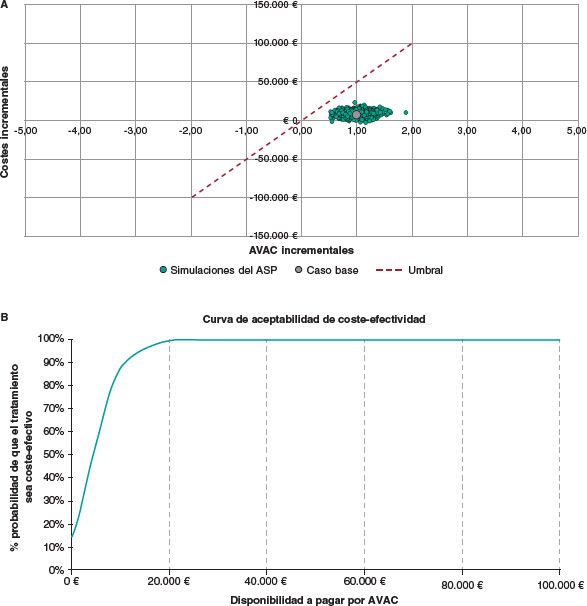
Figura 3. Análisis de sensibilidad probabilístico: A: Diagrama de dispersión del coste-efectividad y B: Curva de aceptabilidad del coste-efectividad. ASP: análisis de sensibilidad probabilístico; AVAC: años de vida ajustados por calidad.
Análisis de los escenarios
Se analizaron varios escenarios para ver qué impacto tendría cambiar distintos supuestos sobre los resultados del modelo y la solidez del mismo. El TAVI con la válvula SAPIEN 3 sigue siendo coste-efectivo comparado con el RVAo en casi todos los escenarios descritos (tabla 6 del material adicional) incluidos aquellos con marcos temporales distintos (10, 15, 20 y 30 años). Los resultados de los análisis de los distintos escenarios vienen a confirmar la solidez comparativa del modelo descrito.
DISCUSIÓN
Este análisis sugiere que, en España, el TAVI con la válvula SAPIEN 3 probablemente sea una opción coste-efectiva de reemplazo valvular para pacientes con EAGs y un riesgo bajo de mortalidad quirúrgica. El TAVI con la válvula SAPIEN 3 mejoró los AVAC (+ 1,0) que se asocian a costes algo mayores que el RVAo (unos 6.971 € por paciente). Los beneficios de la ICER para el TAVI con la válvula SAPIEN 3 descritos en este modelo nos hablan de una intervención muy coste-efectiva (ICER/AVAC, 6.952 €) en el actual sistema español con un umbral de DAP de 30.000 €/AVAC. La incertidumbre se estudió en varios análisis de sensibilidad y los resultados fueron sólidos.
Los hallazgos de este estudio vienen avalados por otros estudios de coste-efectividad que aseguran que el TAVI con la SAPIEN 3 es dominante o coste-efectivo en pacientes de bajo riesgo de mortalidad quirúrgica27-31. Los hallazgos españoles también coinciden con otros análisis de coste-efectividad del TAVI con la SAPIEN 3 frente al RVAo realizados en Francia12 e Italia13 con la misma estructura de modelo.
Este análisis es importante porque el TAVI ofrece a los pacientes una opción de tratamiento mínimamente invasiva con un menor riesgo de complicaciones y/o rehospitalizaciones, tasas más altas de recuperación y una mejor calidad de vida. Desde la perspectiva de los proveedores sanitarios, el TAVI también es eficiente porque reduce el uso de recursos sanitarios, minimiza las complicaciones posoperatorias y acorta la estancia hospitalaria (incluso en unidades de cuidados intensivos [UCI])32. Acortar las estancias hospitalarias significa tratar a más pacientes en el mismo hospital, algo importante en un ya de por sí colapsado sistema sanitario y con largas listas de espera. Estas eficiencias del TAVI también reducen el riesgo de infección y contaminación33, algo apreciado durante la reciente pandemia de la COVID-19. Por último, el TAVI reduce el periodo de recuperación y la vuelta a las actividades diarias normales, aspectos que no se incluyeron en este análisis. También puede que haya otros beneficios indirectos no considerados en este análisis que se sumen a los beneficios globales de esta tecnología, como actividades de voluntariado, cuidado de nietos o menor necesidad de ayuda de cuidadores34.
Los resultados de este análisis pueden ayudar a que un mayor número de pacientes españoles con EAGs puedan tener acceso al TAVI. Estudios recientes confirman el perfil de seguridad y eficacia del TAVI transfemoral en España9. Esto, sumado a las guías europeas publicadas recientemente, sugiere que el número de TAVI irá en aumento y hará que muchos pacientes de bajo riesgo quirúrgico con EAGs sean pacientes aptos para recibir esta intervención. Además, con el tiempo, el TAVI probablemente se simplifique aún más con tiempos de ingreso más cortos35, lo cual debería reducir los costes del TAVI en el futuro. A este respecto, los resultados de este estudio pueden ser de utilidad para los decisores políticos y sanitarios en lo referente al manejo de pacientes con EAGs en España.
Limitaciones
Este estudio no está exento de limitaciones. La primera tiene que ver con ciertos inputs del modelo y con la elaboración de supuestos. En este modelo, los datos de las hospitalizaciones se basaron en los datos a 1 y 2 años del estudio PARTNER 3 asumiendo que esta tasa se mantenía constante durante el marco temporal del modelo después de 2 años. El impacto que tuvo este supuesto se desconoce porque los sujetos de ambos grupos a tratamiento del modelo siguieron estando en riesgo de hospitalización. La tasa de reintervenciones se mantuvo constante después de 22 años; el impacto que tuvo esta asunción sobre los resultados del modelo se consideró mínimo ante la expectativa de que casi el 11% de los pacientes seguirían vivos en el modelo después de este tiempo con una necesidad limitada de tener que ser reintervenidos. A pesar de esto, no puede descartarse la incertidumbre en torno a la durabilidad a más largo plazo del dispositivo TAVI ni los subsiguientes índices de reintervenciones en pacientes más jóvenes. No se incluyeron desutilidades para ningún evento intercurrente porque se puede correr el riesgo de duplicarlas tras haberse aplicado las utilidades a pacientes de los estados de salud ‘FA en tratamiento’ y ‘accidente cerebrovascular discapacitante’. Se trató de una asunción conservadora pues, aparte de las complicaciones asociadas al marcapasos, los índices de eventos intercurrentes suelen ser más bajos para el TAVI con la válvula SAPIEN 3 que para el RVAo.6-
Una segunda limitación del estudio es la extrapolación de los resultados. Las conclusiones no pueden extrapolarse a la población general con estenosis aórtica porque, entre otros, los pacientes con anatomías coronarias desfavorables fueron excluidos del estudio PARTNER 3. Además, se ha de actuar con cautela a la hora de extrapolar cualquier hallazgo de este modelo a poblaciones fuera del territorio español.
Por último, se debe mencionar que los costes quirúrgicos en las distintas regiones españolas son heterogéneos. En este estudio, se emplearon datos públicos de una región española y nuestro abordaje fue conservador pues dio cuenta de la práctica clínica habitual. También se analizaron distintos escenarios con otros datos de costes disponibles.
CONCLUSIONES
Los datos del PARTNER 3 sugieren que el uso del TAVI con la válvula SAPIEN 3 es más favorable, a nivel clínico, que el RVAo en pacientes con EAGs y bajo riesgo de mortalidad quirúrgica. Los resultados de este modelo de coste-efectividad nos indican que, en España, el TAVI podría ser una opción coste-efectiva con respecto al RVAo en esta población con un valor ICER/AVAC estimado muy por debajo del umbral nacional. El modelo fue sólido y la incertidumbre se valoró en diferentes análisis de sensibilidad. Los resultados de este análisis de coste-efectividad servirán para que tanto los decisores políticos y sanitarios como los responsables de los presupuestos sanitarios optimicen el manejo de pacientes españoles con EAGs.
FINANCIACIÓN
Edwards Lifesciences SA, Suiza financió este estudio económico, y formó parte del análisis y la redacción de este manuscrito.
CONTRIBUCIÓN DE LOS AUTORES
J.M. Vázquez recopiló los datos económicos, participó en la validación del modelo y en el proceso de revisión del manuscrito. E Pinar recopiló los datos económicos y participó en la validación del modelo. J. Zamorano participó en la recopilación de datos, así como en el proceso de validación del modelo. J. Burgos participó tanto en el proceso de recopilación de datos como en la validación del modelo. J. Díaz participó tanto en el proceso de recopilación de datos, así como en la validación del modelo. B. García del Blanco participó tanto en el proceso de recopilación de datos, así como en la validación del modelo. A. Sarmah participó en la recopilación y análisis de datos, la preparación de los resultados, así como en la redacción y revisión del manuscrito. P. Candolfi participó en el análisis de costes y en la redacción del manuscrito. J Shore participó en el proceso de desarrollo del modelo, así como en la revisión del manuscrito. M. Green participó, también, en el proceso de desarrollo del modelo y en el proceso de revisión del manuscrito.
CONFLICTO DE INTERESES
J.M. Vázquez Rodríguez declaró que su departamento recibió becas de formación o investigación de Edwards Lifesciences, Medtronic y Boston Scientific y él dijo haber recibido honorarios como consultor de Medtronic y Boston Scientific. J.L. Zamorano declaró que su centro recibió becas de investigación de Abbott y Medtronic y él, por su parte, honorarios como conferenciante de Edwards Lifesciences, Bayer, Novo Nordisk y Daiichi Sankyo. J. Moreu Burgos declaró haber recibido honorarios de Biosensors, Boston Scientific, Cardiva, Edwards Lifesciences y Medtronic. A. Sarmah declaró ser empleado de Edwards Lifesciences y tener opciones sobre acciones. P. Candolfi declaró ser empleado de Edwards Lifesciences y tener opciones sobre acciones. J. Shore declaró haber recibido honorarios como consultor para el desarrollo del modelo económico. M. Green declaró haber recibido honorarios como consultor para el desarrollo del modelo económico. Ni E. Pinar, J.F. Díaz-Fernández ni B. García del Blanco declararon ningún conflicto de intereses.
AGRADECIMIENTOS
La redacción de este manuscrito ha sido posible gracias al apoyo de Zenith Healthcare Communications Ltd (Chester, Reino unido) y a la financiación de Edwards Lifesciences.
¿QUÉ SE SABE DEL TEMA?
- Un reciente ensayo clínico confirma los beneficios clínicos del TAVI con la válvula SAPIEN 3 en una población de bajo riesgo quirúrgico frente al RVAo. Además, a raíz de las últimas actualizaciones de las guías europeas y norteamericanas, el TAVI puede considerarse ya una opción terapéutica viable para pacientes de bajo riesgo quirúrgico con EAGs. No obstante, con respecto a la evidencia económica, únicamente se ha demostrado que el TAVI con la válvula SAPIEN 3, comparado con el RVAo, es coste-efectivo en pacientes españoles de riesgo alto e intermedio con EAGs.
¿QUÉ APORTA DE NUEVO?
- Los datos del PARTNER 3 sugieren que el uso del TAVI con la válvula SAPIEN 3 fue más favorable, a nivel clínico, que el RVAo en pacientes con EAGs y bajo riesgo de mortalidad quirúrgica. Los resultados de este sólido análisis de coste-efectividad indican que, en España, el TAVI podría ser más coste-efectivo que el RVAo en esta población de pacientes con un valor ICER/AVAC estimado muy por debajo del umbral nacional. Conjuntamente, los datos del PARTNER 3 sumados a los de este análisis de coste-efectividad servirán para que tanto los decisores políticos y sanitarios como los responsables del presupuesto sanitario optimicen el manejo de pacientes españoles con EAGs.
BIBLIOGRAFÍA
1. Grimard BH, Larson JM. Aortic Stenosis: Diagnosis and Treatment. Am Fam Physician. 2016;93:371-378.
2. Marquis-Gravel G, Redfors B, Leon MB, Généreux P. Medical treatment of Aortic Stenosis. Circulation. 2016;134:1766-1784.
3. Cribier A. Development of Transcatheter Aortic Valve Implantation (TAVI): A 20-year Odyssey. Arch Cardiovasc Dis. 2012;105:146-152.
4. Falk, V, Baumgartner H, Bax, JJ, et al. 2017 ESC/EACTS Guidelines for the management of valvular heart disease. Eur J Cardiothorac Surg. 2017;52:616-664.
5. Beyersdorf F, Vahanian A, Milojevic M, et al. 2021 ESC/EACTS Guidelines for the Management of Valvular Heart Disease. Eur J Cardiothorac Surg. 2021;60:727-800.
6. Mack MJ, Leon MB, Thourani VH, et al. Transcatheter Aortic-Valve Replacement With a Balloon-Expandable Valve in Low-Risk Patients. N Engl J Med. 2019;380:1695-1705.
7. Leon MB, Mack MJ, Hahn RT, et al. Outcomes 2 Years After Transcatheter Aortic Valve Replacement in Patients at Low Surgical Risk. J Am Coll Cardiol. 2021;77:1149-1161.
8. Ali N, Faour A, Rawlins J, et al. ‘Valve for Life’: tackling the deficit in transcatheter treatment of heart valve disease in the UK. Open Heart. 2021;8:e001547.
9. Íñiguez-Romo A, Javier Zueco-Gil J, Álvarez-Bartolomé M, et al. Outcomes of transcatheter aortic valve implantation in Spain through the Activity Registry of Specialized Health Care. REC Interv Cardiol. 2022;4:123-131.
10. Durko, AP, Osnabrugge RL, Van Mieghem NM, et al. Annual number of candidates for transcatheter aortic valve implantation per country: current estimates and future projections. European Heart Journal. 2018;39:2635-2642.
11. Pinar E, García de Lara J, Hurtado J, et al. Análisis coste-efectividad del implante percutáneo de válvula aórtica SAPIEN 3 en pacientes con estenosis aórtica grave sintomática. Rev Esp Cardiol. 2021;75:325-333.
12. Gilard M, Eltchaninoff H, Lung B, et al. Cost-Effectiveness Analysis of SAPIEN 3 Transcatheter Aortic Valve Implantation Procedure Compared with Surgery in Patients with Severe Aortic Stenosis at Low Risk of Surgical Mortality in France. Value Health. 2022;25:605-613.
13. Mennini FS, Meucci F, Gabriele Pesarini G, et al. Cost-effectiveness of transcatheter aortic valve implantation vs surgical aortic valve replacement in low surgical risk aortic stenosis patients. Int J Cardiol. 2022;357:26-32.
14. Sacristán JA, Oliva J, Del Llano J, Prieto L, Pinto JL. What is an efficient health technology in Spain? Gac Sanit. 2002;16:334-343.
15. Lopez-Bastida J, Oliva J, Antoñanzas F, et al. Spanish recommendations on economic evaluation of health technologies. Eur J Health Econ. 2010;11: 513-20.
16. SAFE 2017. The Burden of Stroke in Spain. Disponible en: https://www.safestroke.eu/wp-content/uploads/2017/12/SAFE_STROKE_SPAIN.pdf. Acessed 22 May 2022.
17. Odutayo A, Wong CX, Hsiao AJ, et al. Atrial fibrillation and risks of cardiovascular disease, renal disease, and death: systematic review and meta-analysis. BMJ. 2016;354:i4482.
18. Bourguignon T, Bouquiaux-Stablo A-L, Candolfi P, et al. Very long-term outcomes of the Carpentier-Edwards Perimount valve in aortic position. Ann Thorac Surg. 2015;99:831-837.
19. Makkar RR, Thourani VH, Mack MJ, et al. Five-Year Outcomes of Transcatheter or Surgical Aortic-Valve Replacement. N Engl J Med. 2020;382:799-809.
20. de Andrés-Nogales F, Álvarez M, de Miquel MÁ, et al. Cost-effectiveness of mechanical thrombectomy using stent retriever after intravenous tissue plasminogen activator compared with intravenous tissue plasminogen activator alone in the treatment of acute ischaemic stroke due to large vessel occlusion in Spain. Eur Stroke J. 2017;2:272-284.
21. Szende A, Janssen B, Cabases J, editors. Self-Reported Population Health: An International Perspective based on EQ-5D. Dordrecht (NL): Springer; 2014. p. 30.
22. Oyagüez I, Suárez C, López-Sendón JL, et al. Cost-Effectiveness Analysis of Apixaban Vs Edoxaban in Patients with Atrial Fibrillation for Stroke Prevention. Pharmacoecon Open. 2020;4:485-497.
23. Lopez-Bastida J, Oliva Moreno J, Worbes Cerezo M, et al. Social and economic costs and health-related quality of life in stroke survivors in the Canary Islands, Spain. BMC Health Serv Res. 2012;12:315.
24. Ramos-Goñi JM, Craig BM, Oppe M, et al. Handling Data Quality Issues to Estimate the Spanish EQ-5D-5L Value Set Using a Hybrid Interval Regression Approach. Value Health. 2018;21:596-604.
25. SERGAS 2014. DECRETO 56/2014, de 30 de abril, por el que se establecen las tarifas de los servicios sanitarios prestados en los centros dependientes del Servicio Gallego de Salud y en las fundaciones públicas sanitarias. DOG 96. 2014. Disponible en: https://www.xunta.gal/dog/Publicados/2014/20140521/AnuncioC3K1-140514-0001_es.html. Consultado 22 May 2022.
26. Bayón Yusta JC, Gutiérrez Iglesias A, Mateos del Pino M, IIbarrola Gutiérrez MI, Gómez Inhiesto E, Acaiturri Ayesta MT. Análisis coste-efectividad del recambio valvular aórtico mediante prótesis valvular percutánea frente al tratamiento quirúrgico habitual. Ministerio de Sanidad, Servicios Sociales e Igualdad; Servicio de Evaluación de Tecnologías Sanitarias del País Vasco. Informes de Evaluación de Tecnologías Sanitarias: OSTEBA (2014). Disponible en: https://www.euskadi.eus/contenidos/informacion/biblioteca_central/es_9528/scp/215765.pdf. Consultado 22 May 2022.
27. Tam DY, Azizi PM, Fremes SE, Chikwe J, Gaudino M, Wijeysundera HC. The Cost-Effectiveness of Transcatheter Aortic Valve Replacement in Low Surgical Risk Patients With Severe Aortic Stenosis. Eur Heart J Qual Care Clin Outcomes. 2021;7:556-563.
28. Zhou JY, Liew D, Duffy SJ, Walton A, Htun N, Stub D. Cost-Effectiveness of Transcatheter Vs Surgical Aortic Valve Replacement in Low-Risk Patients with Severe Aortic Stenosis. Heart Lung Circ. 2021;30:547-554.
29. Health Information and Quality Authority (HIQA) Health Technology Assessment of transcatheter aortic valve implantation (TAVI) in patients with severe symptomatic aortic stenosis at low and intermediate risk of surgical complications. 2019. Disponible en: https://www.hiqa.ie/sites/default/files/2019-12/TAVI_HTA.pdf. Consultado 22 May 2022.
30. Norwegian Institute of Public Health (NIPH) Transcatheter aortic valve implantation (TAVI) vs surgical aortic valve replacement (SAVR) for patients with severe aortic stenosis and low surgical risk and across surgical risk groups: a health technology assessment. 2021. Disponible en: https://www.fhi.no/en/publ/2021/TAVI-vs-SAVR-for-patients-with-severe-aortic-stenosis-and-low-surgical-risk-and-across-surgical-risk-groups/. Consultado 22 May 2022.
31. Haute Autorité de Santé (HAS) Traitement de la sténose aortique sévère symptomatique en France chez les patients à faible risqué chirurgical. 2021. Disponible en: https://www.has-sante.fr/upload/docs/application/pdf/2021-04/sapien3_9022021_avis_economique_vf2.pdf. Consultado 22 May 2022.
32. Valdebenito, M, Massalha E, Barbash IM et al. Transcatheter aortic valve implantation during the COVID-19 pandemic. Am J Cardiol. 2021;145:97-101.
33. Noad RL, Johnston N, McKinley A, et al. A pathway to earlier discharge following TAVI: Assessment of safety and resource utilization. Catheter Cardiovasc Interv. 2016;87:134-142.
34. Huygens SA, van der Kley F, Bekkers JA, Bogers AJJC, Tekkenberg JJM, Rutten-van Mölken MPMH. Beyond the clinical impact of aortic and pulmonary valve implantation: health-related quality of life, informal care and productivity. Eur J Cardiothorac Surg. 2019;55:751-759.
35. Martínez-Sellés M. Coste-efectividad del implante percutáneo de válvula aórtica en 2022. Rev Esp Cardiol. 2022;75(10):853.
36. Instituto Nacional de Estadística. National Life Tables Spain (2019) Disponible en: https://www.ine.es/dyngs/INEbase/en/operacion.htm?c=Estadistica_C&cid=1254736177004&menu=ultiDatos&idp=1254735573002. Consultado 22 May 2022.
37. de Andrés-Nogales F, Vivancos Mora J, Barriga Hernández FJ, et al. Use of healthcare resources and costs of acute cardioembolic stroke management in the Region of Madrid: The CODICE Study. Neurología. 2015;30:536-544.
38. Esquivias, GB, Albaladejo GE, Zamorano JL, et al. Cost-effectiveness analysis comparing apixaban and acenocoumarol in the prevention of stroke in patients with nonvalvular atrial fibrillation in Spain. Rev Esp Cardiol. 2015;68:680-690.
39. Rubio-Terrés, C, Graefenhain de Codeset R, Rubio-Rodríguez D, Evers T, Grau Cerrato SG. Cost-effectiveness analysis of rivaroxaban vs acenocoumarol in the prevention of stroke in patients with non-valvular atrial fibrillation in Spain. JHEOR. 2016;4:19-34.
40. Alvarez-Sabín J, Quintana M, Masiuan J, et al. Economic impact of patients admitted to stroke units in Spain. Eur J Health Econ. 2017;18:449-458.
41. Ministerio de Sanidad de España. GRD APR 190/191 (2019). Registro de Altas de los Hospitales Generales del Sistema Nacional de Salud. CMBD. Norma Estatal de Años Anteriores Disponible en: https://www.sanidad.gob.es/estadEstudios/estadisticas/cmbdAnteriores.htm. Consultado 22 May 2022.
42. Crespo C, Linhart M, Acosta J, et al. Optimisation of cardiac resynchronisation therapy device selection guided by cardiac magnetic resonance imaging: cost-effectiveness analysis. Eur J Prev Cardiol. 2020;27:622-632.
43. Leon MB, Smith CR, Mack MJ, et al. Transcatheter or Surgical Aortic-Valve Replacement in Intermediate-Risk Patients. N Engl J Med. 2016; 374: 1609-1620.
44. Attribution 4.0 International (CC BY 4.0). Disponible en: https://creativecommons.org/licenses/by/4.0/. Consultado 25 Ago 2022.
* Autor para correspondencia.
Correo electrónico: archita_sarmah@edwards.com (A. Sarmah).
@jmvazrod; @CorazonHuvr; @pepp183; @PascalCandolfi; @CIBER_CV