RESUMEN
La insuficiencia mitral funcional auricular (IMFA) ha sido recientemente el foco de atención de muchos artículos y revisiones originales. El envejecimiento de la población, el aumento de la prevalencia de insuficiencia cardiaca con fracción de eyección preservada y fibrilación auricular así como el desarrollo de las técnicas transcatéter para la reparación de la válvula mitral han resaltado la IMFA, un fenotipo de insuficiencia mitral que presenta desafíos diagnósticos específicos y para el cual actualmente las guías no tienen recomendaciones sólidas para su tratamiento. Existe una importante acumulación de datos que sugieren que el pronóstico de los pacientes con IMFA grave es malo si no se tratan. Sin embargo, las nuevas terapias para la insuficiencia cardiaca y las técnicas mínimamente invasivas pueden tener un impacto positivo en el prognóstico de esos pacientes.
Palabras clave: Insuficiencia mitral funcional atrial. Diagnóstico. Ecocardiografía. Reparación de borde a borde. Reparación mitral transcatéter.
ABSTRACT
Atrial functional mitral regurgitation (AFMR) has recently been the focus of numerous original articles and reviews. This entity has been highlighted by population aging, the increasing prevalence of heart failure with preserved ejection fraction and atrial fibrillation, and the advent of the transcatheter techniques for mitral valve repair. AFMR is phenotype of mitral regurgitation that presents specific diagnostic challenges and current guidelines do not provide strong recommendations for its management. Cumulative data show that the outcomes of patients with severe AFMR are poor if left untreated. However, new heart failure therapies and minimally invasive techniques may have a positive impact on the outcomes of these patients.
Keywords: Atrial functional mitral regurgitation. Diagnosis. Echocardiography. Edge-to-edge repair. Transcatheter mitral valve repair.
Abreviaturas IMFA: insuficiencia mitral funcional auricular.
La tríada propuesta por el Prof. Carpentier se suele emplear para caracterizar el mecanismo de la insuficiencia mitral: etiología, lesión y disfunción1. La deficiencia fibroelástica, la enfermedad mixomatosa, la cardiopatía reumática y la endocarditis son etiologías que provocan, directamente, lesiones en la válvula mitral tales como la rotura de las cuerdas tendinosas, tejido excesivo en las valvas, engrosamiento y calcificación de éstas y del aparato subvalvular y perforación de las valvas. Como consecuencia, la insuficiencia mitral resultante se conoce como orgánica o primaria. La cardiopatía isquémica, la miocardiopatía dilatada y la fibrilación auricular son etiologías que dan lugar a la dilatación del anillo mitral y a una restricción del movimiento de las valvas. Estas lesiones se consideran secundarias al proceso de remodelado tanto del ventrículo izquierdo como de la aurícula. En este sentido, la insuficiencia mitral resultante se considera secundaria o funcional. El abordaje para la reparación quirúrgica varía dependiendo de si se trata de insuficiencia mitral primaria o secundaria. En la primaria, las técnicas de reparación implican la resección del festón redundante de la valva mitral, el implante de neocuerdas, el uso de un parche pericárdico (en la perforación de las valvas) y una anuloplastia mitral para restablecer una coaptación normal. En la secundaria, la técnica que suele usarse es la anuloplastia mitral restrictiva.
La llegada de técnicas de reparación percutánea de la válvula mitral pone de manifiesto lo importante que es valorar la etiología de la insuficiencia mitral y caracterizar el aparato valvular mitral con especial atención al área valvular mitral, a la longitud y movimiento de las valvas, a la profundidad y longitud de coaptación y a la localización de la mayor vena contracta del chorro regurgitante2. Estos factores son clave a la hora de seleccionar a aquellos pacientes con insuficiencia mitral en quienes la reparación mitral percutánea de borde a borde tendrá éxito. Las guías actuales describen las características de la válvula mitral que definen las anatomías óptimas, complejas y no adecuadas de la válvula mitral a la hora de realizar una reparación mitral percutánea de borde a borde con garantías de éxito3. En pacientes de alto riesgo quirúrgico o considerados inoperables con insuficiencia mitral primaria y un aparato valvular mitral anatómicamente adecuado, se puede considerar la reparación mitral por catéter de borde a borde (clase IIb). En aquellos de alto riesgo quirúrgico o considerados inoperables y que no precisan revascularización coronaria y con insuficiencia mitral secundaria y un aparato valvular mitral anatómicamente adecuado, la reparación mitral percutánea de borde a borde tiene una recomendación clase IIa. En la actualidad, en este último escenario clínico, hay muchos pacientes con insuficiencia mitral secundaria debido a la dilatación auricular y del anillo mitral; se trata de pacientes distintos de aquellos en quienes la insuficiencia mitral está provocada por una dilatación y disfunción del ventrículo izquierdo. El riesgo quirúrgico de pacientes con insuficiencia mitral funcional auricular (IMFA) suele ser menor que el de aquellos con insuficiencia mitral funcional ventricular, si bien la evidencia que avale el uso de la reparación quirúrgica frente a percutánea de la valvular mitral sigue siendo escasa.
La IMFA aparece en un contexto de fibrilación auricular permanente o insuficiencia cardiaca con fracción de eyección mantenida4-6 y se caracteriza por la dilatación y disfunción del anillo y por una pérdida de sincronía auricular7. En pacientes con insuficiencia cardiaca y fracción de eyección mantenida, el remodelado del ventrículo izquierdo, caracterizado por una hipertrofia concéntrica y una mayor rigidez, resulta en presiones altas de llenado del ventrículo izquierdo que se transmiten a la aurícula izquierda. En respuesta a estas subidas de presión, la aurícula izquierda se dilata como mecanismo compensatorio para equilibrar esta subida de presión y que no pase a la circulación pulmonar. No obstante, el remodelado crónico de la aurícula izquierda conduce a la disfunción auricular y a la dilatación del anillo mitral y contribuye a una coaptación fallida de las valvas7.
La incidencia de la IMFA entre pacientes con fibrilación auricular se calcula en un 7%, aunque esta cifra puede aumentar hasta el 53% en pacientes con insuficiencia cardiaca y fracción de eyección mantenida8. Además, los datos de la Base de Datos Nacional de Eco de Australia (NEDA) informaron incidencias significativas de la IMFA llegando al 8% en pacientes con fibrilación auricular y sin cardiopatía estructural subyacente, al 28% en pacientes con fibrilación auricular de larga data y al 20% en aquellos con insuficiencia cardiaca y fracción de eyección conservada9.
Según diferentes series, se sabe que la IMFA suele afectar a mujeres ancianas con antecedentes de fibrilación auricular e hipertensión arterial10. Se debe mencionar que tanto la fibrilación auricular como la insuficiencia cardiaca con fracción de eyección conservada suelen coexistir, lo cual provoca un mayor remodelado cardiaco, más sintomatología y peores resultados clínicos11. Se suele llegar al diagnóstico de IMFA, principalmente, mediante ecocardiografía transtorácica y transesofágica8. Las principales características ecocardiográficas de la IMFA incluyen una morfología y movimiento normales de las valvas mitrales con una coaptación alterada secundaria a la dilatación del anillo mitral, a menudo con diferentes grados de calcificación. Cuantificar el grado de IMFA puede ser todo un desafío al tratarse de una disfunción que depende de las condiciones de carga de los pacientes. Además, la presencia de fibrilación auricular añade complejidad a la cuantificación de la IMFA por la variabilidad latido a latido. Es importante tener en cuenta el papel que juega la ecocardiografía de esfuerzo, capaz de revelar la presencia de síntomas y detectar la IMFA grave durante la realización de ejercicio máximo. La inducción de insuficiencia tricuspídea significativa e hipertensión pulmonar también son habituales en el esfuerzo. La ecocardiografía de esfuerzo puede ser un segundo paso previo a otras técnicas de imagen, como la resonancia magnética cardiaca, para identificar a aquellos pacientes con IMFA grave.
Las implicaciones clínicas de la IMFA se han descrito recientemente8. El pronóstico de la IMFA grave bajo tratamiento médico es similar al de la insuficiencia mitral funcional del ventrículo izquierdo. En una comparativa con pacientes con insuficiencia mitral primaria, la IMFA se asoció a una peor supervivencia y a más hospitalizaciones por insuficiencia cardiaca. Es importante destacar que se suelen derivar menos a pacientes con IMFA para reparación o reemplazo quirúrgico de la válvula mitral que a pacientes con insuficiencia mitral funcional del ventrículo izquierdo o insuficiencia mitral primaria12. Esto probablemente se deba a la fisiopatología de la IMFA: las guías recomiendan, primero, prescribir el tratamiento médico óptimo (en este caso para la insuficiencia cardiaca con fracción de eyección conservada) y lograr controlar el ritmo cardiaco (en presencia de fibrilación auricular) antes de la intervención3. La evidencia que existe sobre el beneficio de supervivencia de la reparación quirúrgica de la válvula mitral aislada en el manejo de la IMFA es escasa. La reparación quirúrgica de la válvula mitral mediante anuloplastia con anillo rígido completo ha reportado índices bajos tanto de reintervenciones como de recurrencia de la insuficiencia mitral tras 5 años de seguimiento13.
Basándose en un gran registro, la inteligencia artificial ha sido capaz de identificar 4 grupos de pacientes con insuficiencia mitral tratados mediante reparación percutánea de la válvula mitral de borde a borde con resultados clínicos dispares14. Los pacientes del grupo 1 (insuficiencia mitral aislada), caracterizados por la presencia de dilatación auricular izquierda, fracción de eyección del ventrículo izquierdo conservada y una fibrilación auricular del 60% son los que tuvieron la supervivencia más alta. Por otro lado, los pacientes del grupo 4 (dilatación biauricular), caracterizados por la presen- cia de aurículas izquierda y derecha sumamente dilatadas, una fracción de eyección del ventrículo izquierdo en el límite inferior de la normalidad y todos con fibrilación auricular, fueron los que tuvieron peores resultados14. Estos resultados fueron confirmados en una cohorte externa. No obstante, no se especificó en el estudio qué lesión de la válvula mitral es la que provocaba insuficiencia mitral. En este sentido, podría haber pacientes con insuficiencia mitral primaria. En la actualidad, ningún ensayo clínico aleatorizado ha comparado los resultados de la reparación quirúrgica frente a la reparación percutánea de borde a borde de la válvula mitral en pacientes con IMFA.
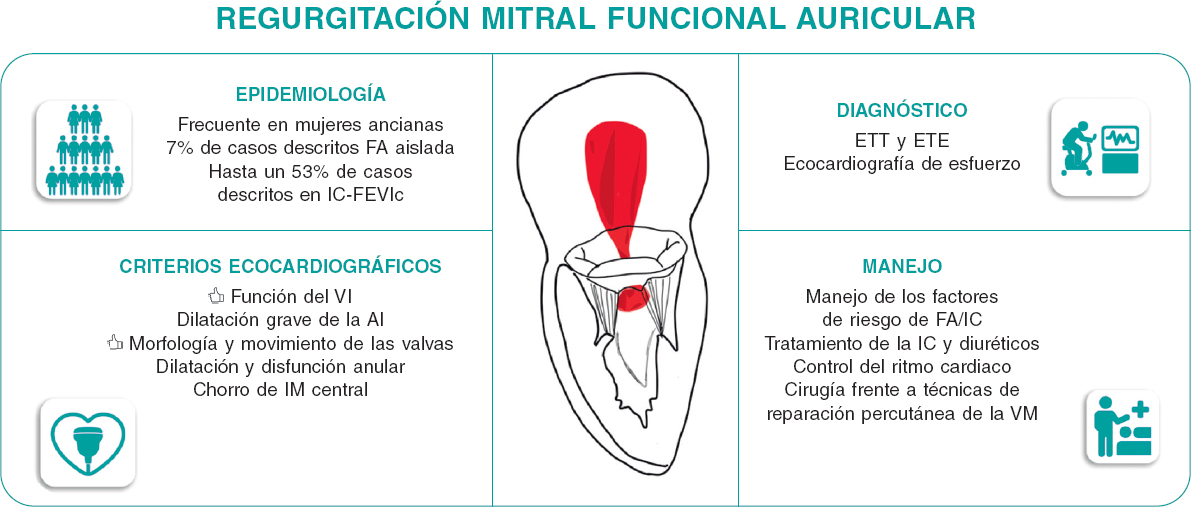
El campo de la IMFA va a atraer mucha atención porque la prevalencia de la insuficiencia cardiaca con fracción de eyección conservada y fibrilación auricular, las principales etiologías fisiopatológicas subyacentes de la IMFA, irán en aumento de forma simultánea al envejecimiento poblacional. Nuevos y eficaces tratamientos tales como los inhibidores del cotransportador de sodio-glucosa tipo 215, los agonistas del péptido similar al glucagón-116 y las técnicas tempranas de ablación de la fibrilación auricular17, pueden influir en la prevalencia de la IMFA. No obstante, necesitaremos nuevos ensayos centrados en la IMFA, aunque, quizás, antes debamos mejorar el abordaje de esta entidad que lleva demasiado tiempo descuidándose y considerándose un mero espectador de otras patologías. Se necesita un diagnóstico y caracterización precisos de la IMFA (figura 1). También se necesitan grandes registros que informen sobre los resultados de la IMFA a tratamiento médico y con técnicas quirúrgicas y de reparación percutánea de la válvula mitral para acotar y diseñar nuevos ensayos clínicos aleatorizados que perfeccionen las recomendaciones establecidas en las guías clínicas En este sentido, establecer la IMFA como una nueva entidad fue una necesidad clínica no satisfecha para dar un tratamiento óptimo y personalizado a cada paciente con insuficiencia mitral.
Figura 1. Caracterización y manejo de la insuficiencia mitral funcional auricular. AI: aurícula izquierda; ETE: ecocardiografía transesofágica; ETT: ecocardiografía transtorácica; FA: fibrilación auricular; IC-FEVIm: insuficiencia cardíaca con fracción de eyección del ventrículo izquierdo mantenida; IC: insuficiencia cardiaca; IM: insuficiencia mitral; VM: válvula mitral.
FINANCIACIÓN
Ninguna.
DECLARACIÓN SOBRE EL USO DE INTELIGENCIA ARTIFICIAL
No se han utilizado herramientas basadas en inteligencia artificial para redactar este manuscrito ni generar la figura.
CONTRIBUCIÓN DE LOS AUTORES
Los autores confirman las siguientes aportaciones a este artículo. Idea y diseño del artículo: V. Delgado, S. Danojevic, M. De Raffele y L. Niro. Metodología: V. Delgado, S. Danojevic. Validación, M. De Raffele y L. Niro. Búsqueda bibliográfica: S. Danojevic, M. De Raffele y L. Niro. Preparación y redacción del borrador original: S. Danojevic. Redacción, revisión y edición: V. Delgado, M. De Raffele y L. Niro. Supervisión: V. Delgado. Todos los autores han leído y aceptado la versión publicada del manuscrito.
CONFLICTO DE INTERESES
V. Delgado declaró haber recibido honorarios como conferenciante de Edwards Lifesciences, GE Healthcare, Novartis y Philips y como consultor de Novo Nordisk, MSD y Edwards Lifesciences. Los demás autores no declararon ningún conflicto de intereses.
BIBLIOGRAFÍA
1. Carpentier A. Cardiac valve surgery--The “French correction”. J Thorac Cardiovasc Surg. 1983;86:323-37.
2. Mauri L, Garg P, Massaro JM, et al. The EVEREST II Trial:Design and rationale for a randomized study of the evalve mitraclip system compared with mitral valve surgery for mitral regurgitation. Am Heart J. 2010;160:23-29.
3. Vahanian A, Beyersdorf F, Praz F, et al. 2021 ESC/EACTS Guidelines for the management of valvular heart disease. Eur Heart J. 2022;43:561-632.
4. Zoghbi WA, Levine RA, Flachskampf F, et al. Atrial Functional Mitral Regurgitation:A JACC:Cardiovascular Imaging Expert Panel Viewpoint. JACC Cardiovasc Imaging. 2022;15:1870-1882.
5. Levine RA, Schwammenthal E. Ischemic mitral regurgitation on the threshold of a solution:From paradoxes to unifying concepts. Circulation. 2005;112:745-758.
6. Ennezat PV, Maréchaux S, Pibarot P, Le Jemtel TH. Secondary mitral regurgitation in heart failure with reduced or preserved left ventricular ejection fraction. Cardiology. 2013;125:110-117.
7. Gertz ZM, Raina A, Saghy L, et al. Evidence of atrial functional mitral regurgitation due to atrial fibrillation:Reversal with arrhythmia control. J Am Coll Cardiol. 2011;58:1474-81.
8. Deferm S, Bertrand PB, Verbrugge FH, et al. Atrial Functional Mitral Regurgitation:JACC Review Topic of the Week. J Am Coll Cardiol. 2019;73:2465-2476.
9. Moonen A, Ng MKC, Playford D, Strange G, Scalia GM, Celermajer DS. Atrial functional mitral regurgitation:Prevalence, characteristics and outcomes from the National Echo Database of Australia. Open Heart. 2023;10:e002180.
10. Dziadzko V, Dziadzko M, Medina-Inojosa JR, et al. Causes and mechanisms of isolated mitral regurgitation in the community:Clinical context and outcome. Eur Heart J. 2019;40:2194-2202.
11. Lam CSP, Rienstra M, Tay WT, et al. Atrial Fibrillation in Heart Failure With Preserved Ejection Fraction:Association With Exercise Capacity, Left Ventricular Filling Pressures, Natriuretic Peptides, and Left Atrial Volume. JACC Heart Fail. 2017;5:92-98.
12. Mesi O, Gad MM, Crane AD, et al. Severe Atrial Functional Mitral Regurgitation:Clinical and Echocardiographic Characteristics, Management and Outcomes. JACC Cardiovasc Imaging. 2021;14:797-808.
13. Wagner CM, Brescia AA, Watt TMF, et al. Surgical strategy and outcomes for atrial functional mitral regurgitation:All functional mitral regurgitation is not the same!J Thorac Cardiovasc Surg. 2022;167(2):647-655.
14. Trenkwalder T, Lachmann M, Stolz L, et al. Machine learning identifies pathophysiologically and prognostically informative phenotypes among patients with mitral regurgitation undergoing transcatheter edge-to-edge repair. Eur Heart J Cardiovasc Imaging. 2023;24:574-587.
15. Gulsin GS, Graham-Brown MPM, Squire IB, Davies MJ, McCann GP. Benefits of sodium glucose cotransporter 2 inhibitors across the spectrum of cardiovascular diseases. Heart. 2022;108:16-21.
16. Kosiborod MN, Abildstrøm SZ, Borlaug BA, et al. Semaglutide in Patients with Heart Failure with Preserved Ejection Fraction and Obesity. N Engl J Med. 2023;389:1069-1084.
17. Yamauchi R, Morishima I, Okumura K, et al. Association Between Catheter Ablation for Nonparoxysmal Atrial Fibrillation and Functional Mitral Regurgitation in Patients With Heart Failure With Preserved Ejection Fraction. Am J Cardiol. 2023;207:192-201.
* Autor para correspondencia.
Correo electrónico: (V. Delgado).
@VDelgadoGarcia; @icorcat; @suzidanojevic; @Doc_Niro; @MartinaRaffele;