RESUMEN
Introducción y objetivos: El abordaje sistemático en pacientes con angina con arterias coronarias no obstruidas (ANOCA) o con isquemia con arterias coronarias no obstruidas (INOCA) no está bien protocolizado.
Métodos: Todos los pacientes con diagnóstico de INOCA o ANOCA se trasladaron a una clínica ambulatoria específica para evaluar su elegibilidad para el programa NOCA. Si eran elegibles, se sometían a una angiografía coronaria programada con pruebas de función coronaria y provocación intracoronaria con acetilcolina. La terapia médica se optimizó en consecuencia. Todos los pacientes tuvieron un seguimiento a 1, 3, 6 y 12 meses. Al inicio y a los 3 meses se aplicaron los cuestionarios SAQ y EuroQol-5D.
Resultados: De 77 pacientes se excluyeron 23 (29,9%) y se incluyeron 54 (70,1%) (29 [53,7%] con INOCA y 25 [46,3%] con ANOCA). Se diagnosticó angina microvascular a 19 (35,2 %) pacientes, angina vasoespástica a 12 (22,2 %), angina microvascular y angina vasoespástica a 18 (33,3 %), y dolor torácico no coronario a 5 (9,3 %). Hubo un aumento significativo en el uso de bloqueadores beta, bloqueadores del calcio y nitratos. Se presentaron complicaciones en 3 (5,5%) pacientes. No hubo diferencias en la puntuación media del EQ-5D a los 3 meses y se observó una mejora significativa en la puntuación SAQ respecto a la limitación física, la estabilidad de la angina y la percepción de enfermedad, sin diferencias en la frecuencia de angina y la satisfacción con el tratamiento. No se registraron eventos al año.
Conclusiones: Un protocolo diagnóstico y terapéutico específico podría implementarse de manera fácil y segura en la práctica clínica diaria, y con ello mejoraría la calidad de vida de los pacientes.
Palabras clave: INOCA. ANOCA. Diagnóstico. Terapia. Protocolo.
ABSTRACT
Introduction and objectives: : A systematic approach to patients with angina with no obstructed coronary arteries (ANOCA) or ischemia with no obstructed coronary arteries (INOCA) patients is not routinely implemented.
Methods: All consecutive patients diagnosed with ANOCA/INOCA were referred to a designated outpatient clinic for a screening visit to assess their eligibility for a NOCA program. If eligible, patients underwent scheduled coronary angiograms with coronary function testing and intracoronary acetylcholine provocation testing. Medical therapy was optimized accordingly. All patients were then followed up at 1, 3, 6, and 12 months. Baseline and 3-month follow-up assessments included the Seattle Angina Questionnaire (SAQ) and EuroQol-5D questionnaire.
Results: Of 77 patients screened, 23 (29.9%) were excluded and 54 (70.1%) were included (29 [53.7%] with INOCA and 25 [46.3%] with ANOCA). Microvascular angina was diagnosed in 19 (35.2%) patients, vasospastic angina in 12 (22.2%), both microvascular angina and vasospastic angina in 18 (33.3%), and noncoronary chest pain in 5 (9.3%). There was a notable increase in the use of beta-blockers, calcium channel blockers and nitrates. Complications occurred in 3 (5.5%) patients. Compared with baseline, there was no difference in the mean EQ-5D score at the 3-month follow-up, but there was a significant improvement in the SAQ score related to physical limitations, angina stability, and disease perception, with no differences in angina frequency or treatment satisfaction. No events were recorded at the 1-year follow-up.
Conclusions: A specific diagnostic and therapeutic protocol can be easily and safely implemented in routine clinical practice, leading to improvement in patients’ quality of life.
Keywords: INOCA. ANOCA. Diagnosis. Therapy. Protocol.
Abreviaturas
ANOCA: angina sin arterias coronarias obstructivas. INOCA: isquemia sin arterias coronarias obstructivas.
INTRODUCCIÓN
La cardiopatía isquémica es la principal causa de discapacidad y mortalidad en todo el mundo y se caracteriza comúnmente por la presencia de enfermedad coronaria (EC) obstructiva (definida como cualquier estenosis de las coronarias ≥ 50% de diámetro)1. No obstante, entre el 60 y el 70% de los pacientes con angina y/o isquemia miocárdica documentada carecen de evidencias angiográficas de EC2. Esta enfermedad se define como un cuadro de angina sin arterias coronarias obstructivas (ANOCA) o isquemia sin arterias coronarias obstructivas (INOCA) cuando se asocia a evidencias de isquemia miocárdica3. Se debe mencionar que, comparado con individuos sanos, a pesar de la ausencia de EC, estos pacientes corren un mayor riesgo de sufrir eventos cardiovasculares en el futuro tales como síndrome coronario agudo, hospitalización por insuficiencia cardíaca, accidente cerebrovascular y múltiples intervenciones cardiovasculares4,5. En este sentido, un manejo adecuado en términos de diagnóstico y tratamiento es de suma importancia para mejorar el pronóstico y los resultados de los pacientes6. El estudio CorMicA (Coronary microvascular angina) demostró que una estrategia de pruebas invasivas adyuvantes para el tratamiento de trastornos de la función coronaria y una terapia médica estratificada pueden llegar a mejorar los resultados (reducir la gravedad de la angina y mejorar la calidad de vida)7,8. No obstante, la correcta implementación en la práctica del mundo real de un enfoque diagnóstico y terapéutico sistemático en pacientes con INOCA y ANOCA sigue siendo objeto de debate, al ser algo que podría afectar los resultados y la calidad de vida de los pacientes.
Se informa de nuestra experiencia en un único centro sobre la implementación en la práctica clínica de un protocolo de diagnóstico y tratamiento específico (programa NOCA [arterias coronarias no obstructivas]) en pacientes con INOCA y ANOCA.
MÉTODOS
Criterios de elegibilidad para el programa NOCA
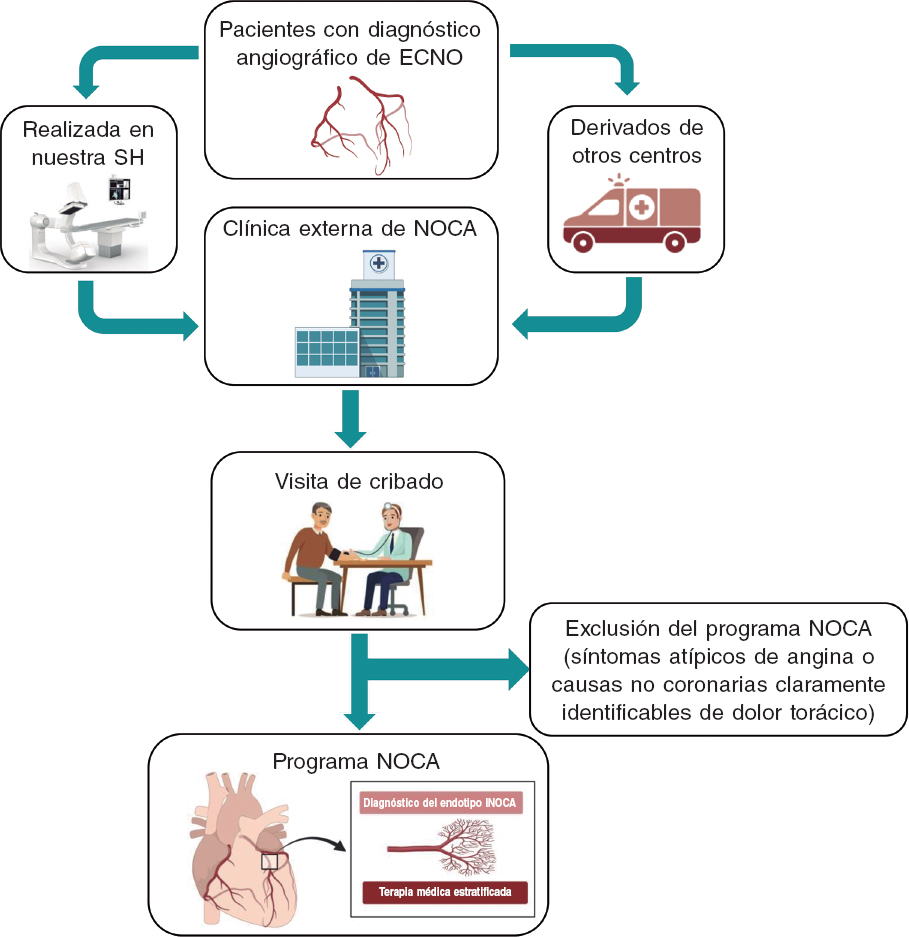
Todos los pacientes consecutivos diagnosticados en nuestro hospital o en centros de referencia con angina o isquemia con EC no obstructiva según la coronariografía se derivaron a una clínica ambulatoria específica (la clínica NOCA del Hospital Clínic de Barcelona) para una visita de cribado. La EC no obstructiva se definió como la evidencia angiográfica de coronarias normales o ateroesclerosis difusa con estenosis < 50% o una reserva fraccional de flujo (RFF) > 0,80 con un porcentaje de estenosis del 50-70%. Durante la visita de cribado, un equipo de cardiólogos expertos confirmó la elegibilidad de los pacientes para el programa NOCA según los siguientes criterios: a) diagnóstico de ANOCA, definido como síntomas típicos de angina crónica estable (como dolor torácico secundario a esfuerzo físico o estrés emocional y aliviado con reposo o nitroglicerina); b) diagnóstico de INOCA, definido como la confirmación de isquemia miocárdica identificada mediante pruebas no invasiva con pruebas de esfuerzo farmacológicas o de esfuerzo tales como tomografía computarizada por emisión de fotón único, resonancia magnética cardiaca, electrocardiograma de esfuerzo o ecocardiografía3. Los criterios de exclusión fueron: a) síntomas atípicos de angina y b) causas no coronarias claramente identificables del dolor torácico (figura 1). El protocolo del estudio se adhirió a la Declaración de Helsinki y el estudio fue aprobado el comité de revisión de nuestro centro. Todos los pacientes dieron su consentimiento informado por escrito antes de ser incluidos tanto en el programa NOCA como en el estudio. El comité de ética clínica dio su aprobación para el análisis retrospectivo de los datos recopilados.
Figura 1. Figura central. Diagrama de flujo para la inclusión de pacientes en el programa NOCA. INOCA: isquemia sin arterias coronarias obstructivas; NOCA: arterias coronarias no obstructivas; ECNO: enfermedad coronaria no obstructiva; SH: sala de hemodinámica.
Programa NOCA: abordaje diagnóstico
Tras la inclusión de los pacientes en el programa NOCA, cardiólogos y enfermeras expertos dieron asesoramiento especializado. Se informó minuciosamente a todos los pacientes sobre su enfermedad, la importancia de alcanzar un diagnóstico específico y de implementar una terapia personalizada. Durante las sesiones de asesoramiento, se explicaron, en detalle, los beneficios previstos y los bajos riesgos asociados a una intervención invasiva para el estudio específico de la microcirculación coronaria y el vasoespasmo. Todos los pacientes dieron su consentimiento informado por escrito antes de someterse a la coronariografía y las pruebas de vasorreactividad coronaria mediante la infusión de acetilcolina (ACh).
Posteriormente, a todos los pacientes se les hizo una coronariografía programada con una evaluación diagnóstica integral consistente en: a) pruebas de la función coronaria para medir la reserva de flujo coronario (RFC) y el índice de resistencia microcirculatoria (IRM); b) pruebas de provocación intracoronaria con ACh para valorar la presencia de trastornos de la vasomoción coronaria tales como espasmo epicárdico o espasmo microvascular.
Las pruebas de la función coronaria se llevaron a cabo con una guía con sensor de presión y temperatura (guía PressureWire X y sistema cardiovascular Coroventis CoroFlow, Abbott Vascular, Estados Unidos) que se colocó en la descendente anterior (DA) (el vaso diana predefinido) reflejando su masa miocárdica subyacente y dominancia coronaria. Se indujo hiperemia en estado estable mediante la infusión de adenosina intravenosa (140 μg/kg/min). Ante la presencia de tortuosidad grave de la DA o evidencia de isquemia miocárdica en una región distinta del territorio de la DA, la guía se colocó en la coronaria derecha o en la circunfleja izquierda a criterio del operador. La RFC se calculó mediante termodilución, definida como el tiempo de tránsito medio en reposo dividido por el tiempo de tránsito medio en hiperemia (los valores anómalos de la RFC se definieron como ≤ 2,5). El IRM se calculó como el producto de la presión coronaria distal en hiperemia máxima multiplicado por el tiempo de tránsito medio en hiperemia (valores normales < 25)6,9.
Las pruebas de provocación intracoronaria con ACh se hicieron siguiendo un protocolo estandarizado con infusiones seriadas de ACh durante 20 segundos a concentraciones crecientes (2-20-100 μg en la descendente anterior a intervalos de 2-3 minutos entre cada inyección), con evaluación concomitante de los síntomas del paciente, documentación electrocardiográfica y escaneos angiográficos. Los pacientes a tratamiento con fármacos vasoactivos tales como bloqueadores de los canales de calcio y nitratos tuvieron un periodo de eliminación de, como mínimo, 48 horas antes de la prueba de provocación10,11,12. El espasmo coronario epicárdico se definió como una reproducción del dolor torácico y cambios isquémicos en el electrocardiograma asociados a un descenso del diámetro coronario ≥ 90% con respecto a los valores basales en cualquier segmento de la arteria coronaria epicárdica13. Se diagnosticó espasmo microvascular ante la presencia de cambios típicos en el segmento ST isquémico (desviación ≥ 1 mm) y angina en ausencia de constricción coronaria epicárdica (reducción de diámetro < 90%)14.
Después, se estratificó a los pacientes en 4 endotipos: a) angina microvascular (AMV) (evidencia de disfunción microvascular coronaria [DMC] definida como la presencia de valores anómalos en la RFC [< 2,5], IRM [≥ 25] o espasmos microvasculares); b) angina vasoespástica (AV) (RFC ≥ 2,5, IRM < 25 y espasmos epicárdicos); c) AMV y AV (evidencia de DMC y espasmos epicárdicos); y d) dolor torácico de origen no coronario (RFC ≥ 2,5 y IRM < 25, sin espasmos microvasculares ni epicárdicos)6.
Se documentaron todas las complicaciones sobrevenidas durante el trabajo de diagnóstico invasivo, incluidas bradiarritmias, fibrilaciones auriculares, taquicardias o fibrilaciones ventriculares, perforaciones coronarias, mortalidad por cualquier causa, así como cualquier otra complicación.
Programa NOCA: abordaje terapéutico farmacológico y psicológico
Una vez identificado el endotipo, el tratamiento médico de cada paciente se optimizó convenientemente (tabla 1). En pacientes con AMV, se inició tratamiento o aumentó la dosis de bloqueadores beta y bloqueadores de los canales de calcio (BCC). Se añadió ranolazina cuando los síntomas anginosos no podían controlarse completamente con bloqueadores beta y BCC. En pacientes con AV, se inició tratamiento o aumentó la dosis de BCC no dihidropiridínicos y nitratos de acción prolongada. En pacientes con AMV y AV, se inició tratamiento o aumentó la dosis de BCC no dihidropiridínicos o beta-bloqueadores. En pacientes con dolor torácico de origen no coronario, se suspendieron los fármacos vasoactivos salvo que estuvieran clínicamente indicados por otras razones. También se inició tratamiento o aumentó la dosis de inhibidores de la enzima convertidora de angiotensina/bloqueadores de los receptores de angiotensina y estatinas en todos los pacientes. Si un paciente mostraba intolerancia o tenía contraindicaciones para un fármaco determinado (como, por ejemplo, asma para los bloqueadores beta, edema perimaleolar para los BCC, bradicardia grave tanto para los bloqueadores beta como para los BCC), el tratamiento se adaptaba y modificaba en consecuencia.
Tabla 1. Tratamiento médico según el endotipo específico de ANOCA/INOCA
| Mecanismo patogénico del MINOCA | Implicaciones terapéuticas |
|---|---|
| AMV | Bloqueadores beta (Nebivolol 2.5-10 mg al día) |
| BCC (amlodipino 10 mg/día o verapamilo 240 mg/día o diltiazem 90 mg 2 veces al día) | |
| Ranolazina (375-750 mg 2 veces al día) | |
| AV | BCC no dihidropiridínicos (verapamilo 240 mg al día o diltiazem 90 mg 2 veces al día) |
| Nitratos de acción prolongada (mononitrato de isosorbida 30 mg) | |
| AMV y AV | BCC (verapamilo o diltiazem) o bloqueadores beta |
| Dolor torácico no coronario | Bloqueadores beta o BCC dihidropiridínicos con indicación clínica (por ejemplo, en caso de hipertensión) |
| IECA o BRA con indicación clínica | |
| Estatinas con indicación clínica | |
|
AMV: angina microvascular; ANOCA: angina sin arterias coronarias obstructivas; AV: angina vasoespástica; BCC: bloqueadores de los canales de calcio; BRA: bloqueadores de los receptores de angiotensina; IECA: inhibidor de la enzima de conversión de la angiotensina; INOCA: isquemia sin arterias coronarias obstructivas; MINOCA: infarto agudo de miocardio sin enfermedad coronaria ateroesclerótica obstructiva. |
|
Como el estrés es un factor desencadenante importante para los síntomas anginosos, se derivó a todos los pacientes a un equipo de psicólogos expertos para recibir apoyo psicológico15.
Programa NOCA: valoración de los resultados clínicos y la calidad de vida
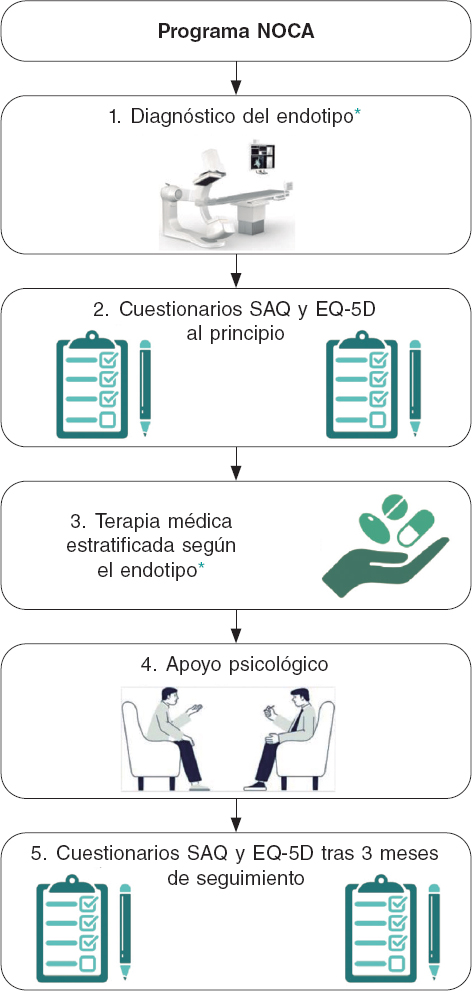
Todos los pacientes tuvieron un seguimiento de 1, 3, 6 y 12 meses para la titulación del tratamiento y valoración de los resultados clínicos. En la coronariografía basal y en el seguimiento de 3 meses se entregó a todos los pacientes los cuestionarios de angina de Seattle (SAQ) y de calidad de vida (EuroQol-5D [EQ-5D]). El primero es un cuestionario validado de 19 ítems autoadministrado que mide 5 dimensiones de la EC: limitación física, estabilidad de la angina, frecuencia de los episodios anginosos, satisfacción con el tratamiento y percepción de la enfermedad16. El segundo es un cuestionario estandarizado no específico de enfermedad que se emplea para describir y valorar el estado de salud de los pacientes y cuyo objetivo principal fue complementar otras mediciones de la calidad de vida17. La figura 2 nos ofrece una representación visual de todos los pasos dados en pacientes incluidos en el programa NOCA.
Figura 2. Representación visual del programa NOCA. EQ-5D: EuroQol-5D; NOCA: arterias coronarias no obstructivas; SAQ: cuestionario de angina de Seattle. * Consultar el texto para tener más información.
Análisis estadístico
La distribución de los datos se valoró con la prueba de Kolmogorov. Las variables continuas se compararon con la prueba t de Student no emparejada o la prueba U de Mann-Whitney, según corresponda. Los datos se expresan como media ± desviación estándar (DE) o como mediana e intervalo intercuartílico [RIQ]. Los datos categóricos se expresan como números y porcentajes y se evaluaron con la prueba de la X2 o la prueba exacta de Fisher, según corresponda. Se consideró significativo un valor de p bilateral < 0,05. Todos los análisis se realizaron con el paquete de software estadístico SPSS, versión 21 (SPSS, Estados Unidos).
RESULTADOS
Características basales de la población del estudio
Durante el periodo comprendido entre enero de 2021 y diciembre de 2021, se cribó a un total de 77 pacientes en la clínica NOCA para determinar su elegibilidad para el programa NOCA. Tras la selección inicial, se excluyó a 23 pacientes (29,9%), 12 de ellos por presentar síntomas anginosos atípicos y 11 por causas no coronarias claramente identificables. Finalmente, se incluyó a 54 pacientes en el programa NOCA, con una media de edad de 64,4 ± 9,4 años, 39 de los cuales eran mujeres (63,9%), de los cuales se diagnosticó a 29 (53,7%) de INOCA y a 25 (46,3%) de ANOCA. Las características clínicas y angiográficas de la población del estudio se muestran en la tabla 1.
Programa NOCA: diagnóstico del endotipo específico y complicaciones
Los resultados de la valoración funcional invasiva se muestran en la tabla 2. Los valores medios tanto del IRM como de la RFC fueron 21,2 ± 10,6 y 2,3 ± 1.4, respectivamente. Se diagnosticó de AMV a 19 pacientes (35,2%), a 12 (22,2%) de AV y a 18 de AMV y AV (33,3%). Finalmente, se diagnosticó a 5 pacientes (9,3%) de dolor torácico no coronario.
Tabla 2. Características clínicas y angiográficas de pacientes incluidos en el programa NOCA
| Características | Población del estudio (n = 54) |
|---|---|
| Características clínicas | |
| Edad | 64,4 ± 9,4 |
| Sexo femenino | 39 (72,2) |
| Presentación clínica | |
| ANOCA | 25 (46,3) |
| INOCA | 29 (53,7) |
| Diabetes mellitus | 12 (22,2) |
| Hipertensión | 35 (64,8) |
| Dislipemia | 28 (51,9) |
| Exfumadores | 3 (5,7) |
| Fumadores en la actualidad | 14 (25,9) |
| Antecedentes familiares de EC | 5 (9,3) |
| Antecedentes de EC | |
| IAM previo | 7 (13,0) |
| ICP previa | 8 (14,8) |
| CABG previa | 0 (0,0) |
| EPOC | 1 (1,9) |
| IRC (TFGe < 60 ml/min/m2) | 4 (7,4) |
| Depresión | 15 (27,8) |
| Ansiedad | 19 (35,2) |
| Valoración funcional invasiva | |
| Vasos explorados | |
| DA | 48 (88,9) |
| CXI | 3 (5,6) |
| CD | 3 (5,6) |
| IRM | 21,2 ± 10,6 |
| Valores elevados del IRM (≥ 25) | 18 (33,3) |
| RFC | 2,3 ± 1,4 |
| Valores bajos de la RFC (< 2,5) | 33 (61,1) |
| Valores elevados del IRM (≥ 25) y valores bajos de la RFC (< 2,5) | 13 (24,1) |
| Diagnóstico (endotipo) | |
| AMV | 19 (35,2) |
| AV | 12 (22,2) |
| AMV y AV | 18 (33,3) |
| Dolor torácico no coronario | 5 (9,3) |
|
AMV: angina microvascular; ANOCA: angina de arterias coronarias no obstructivas; AV: angina vasoespástica; CABG: cirugía de revascularización aortocoronaria; CD: coronaria derecha; CXI: circunfleja izquierda; DA: descendente anterior; EC: enfermedad cardiovascular; EPOC: enfermedad pulmonar obstructiva crónica; IAM: infarto agudo de miocardio; ICP: intervención coronaria percutánea; IRM: índice de resistencia microcirculatoria; INOCA: isquemia de arterias coronarias no obstructivas; IRC: insuficiencia renal crónica; RFC: reserva de flujo coronario; TFGe: tasa de filtración glomerular estimada. Los valores expresan nº (%), media ± desviación estándar o mediana [intervalo intercuartílico]. |
|
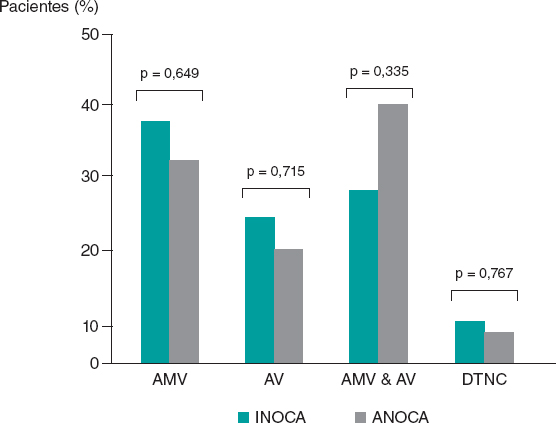
Entre los pacientes con INOCA, se diagnosticó AMV en 11 pacientes (37,9%), AV en 7 (24,1%), AMV y AV en 8 (27,6%) y dolor torácico no coronario en 3 (10,3%). Entre aquellos con ANOCA, se diagnosticó AMV en 8 pacientes (32,0%), AV en 5 (20,0%), AMV y AV en 10 (40,0%), y dolor torácico no coronario en 2 (8,0%). No hubo diferencias estadísticamente significativas en la prevalencia de ningún endotipo entre los pacientes con INOCA y ANOCA (todos los valores de p > 0,05, figura 3).
Figura 3. Prevalencia de los diferentes endotipos entre pacientes con INOCA y ANOCA. AMV: angina microvascular; ANOCA: angina con arterias coronarias no obstructivas; AV: angina vasoespástica; DTNC: dolor torácico no coronario; INOCA: isquemia con arterias coronarias no obstructivas.
Hubo complicaciones en 3 pacientes (5,5%) durante la prueba de provocación intracoronaria con ACh: 2 pacientes (3,7%) experimentaron bradiarritmias transitorias y 1 paciente (1,8%) fibrila- ción auricular paroxística que revirtió espontáneamente al ritmo sinusal.
Programa NOCA: Optimización del tratamiento según el endotipo específico
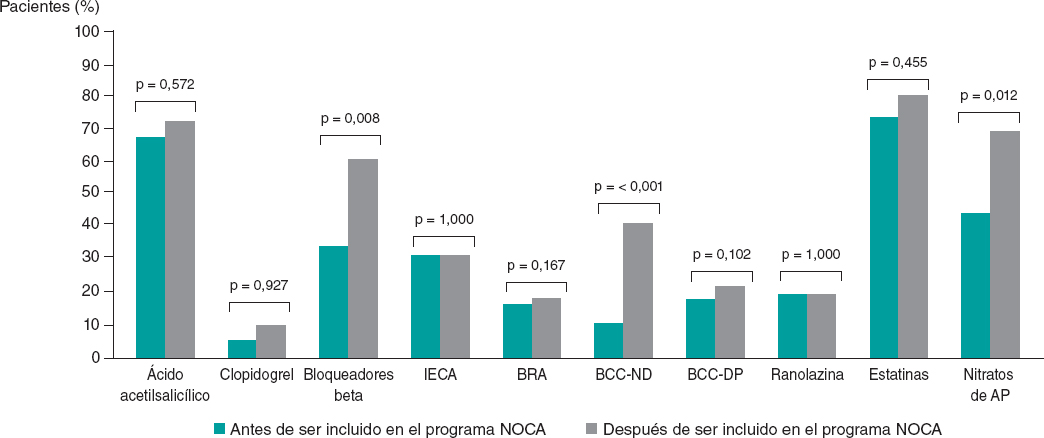
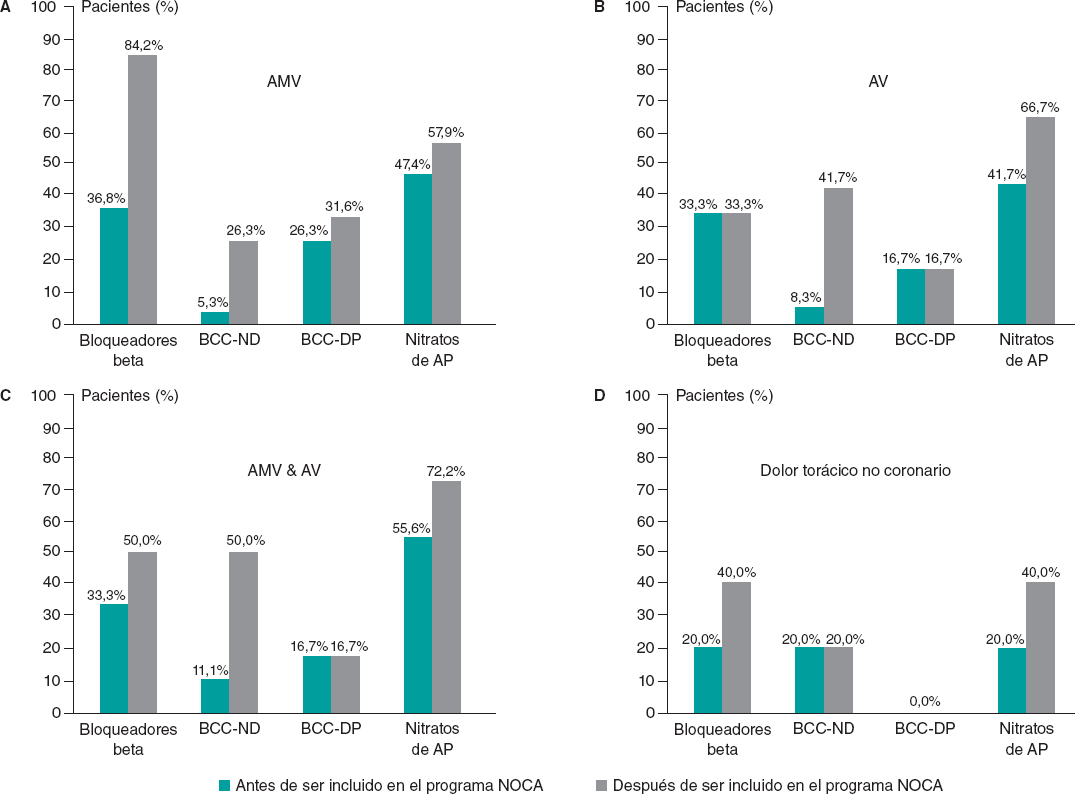
La inclusión en el programa NOCA provocó cambios estadísticamente significativos en los fármacos tras el diagnóstico del endotipo específico. Aumentó significativamente el uso de bloqueadores beta (33,3 antes frente al 57,4% después; p = 0,008), BCC no dihidropiridínicos (9,3 antes frente al 37,0% después; p < 0,001) y nitratos de acción prolongada (46,3 antes frente al 63,0% después; p = 0,012). No hubo diferencias estadísticamente significativas en ningún otro fármaco antes ni después de la evaluación invasiva (todos los valores de p > 0,05; figura 4). Todos los cambios de fármacos adaptados al endotipo específico de ANOCA/INOCA se muestran en la figura 5.
Figura 4. Diferencias en el tratamiento médico antes y después de la inclusión de los pacientes en el programa NOCA. AP: acción prolongada; BCC-DP: bloqueadores de los canales de calcio dihidropiridínicos; BCC-ND: bloqueadores de los canales de calcio no dihidropiridínicos; BRA: bloqueadores de los receptores de angiotensina; IECA: inhibidor de la enzima de conversión de la angiotensina.
Figura 5. Cambios en la medicación en función de endotipo específico de ANOCA/INOCA. A: pacientes con AMV. B: pacientes con AV. C: pacientes con AMV y AV. D: pacientes con dolor torácico no coronario. AMV: angina microvascular; AP: acción prolongada; AV: angina vasoespástica; BCC-DP: bloqueadores de los canales de calcio dihidropiridínicos; BCC-ND: bloqueadores de los canales de calcio no dihidropiridínicos.
Programa NOCA: valoración de los resultados clínicos
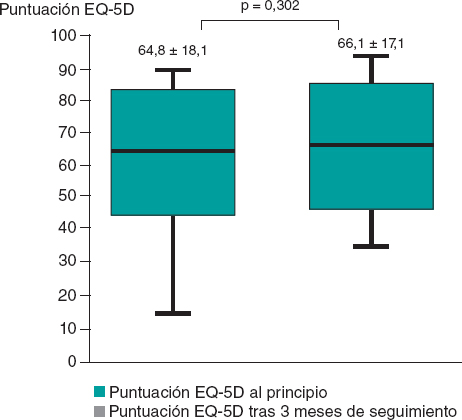
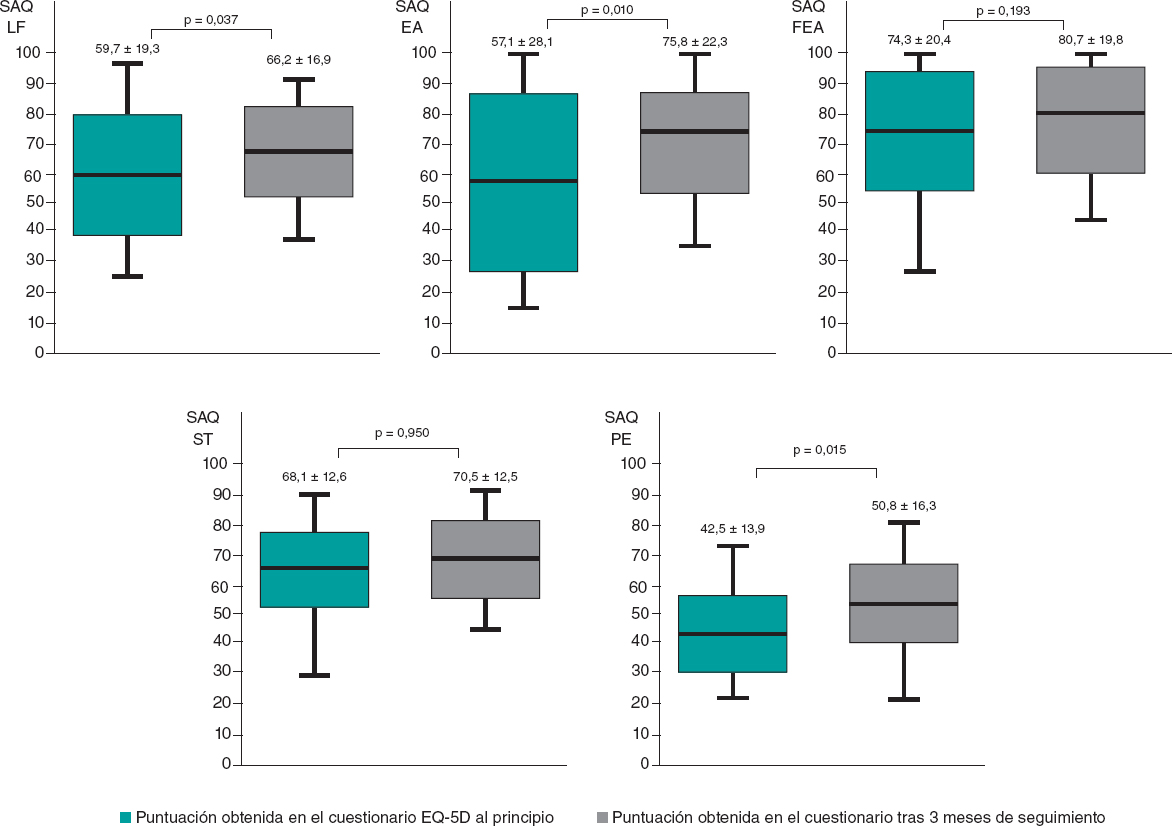
A los 3 meses de seguimiento, no se observó ninguna diferencia estadísticamente significativa en la puntuación media obtenida en el EQ-5D frente a los valores basales (64,8 ± 18,1 al principio frente a 66,1 ± 17,1 a los 3 meses de seguimiento; p = 0,302) (figura 6), No obstante, sí hubo una mejoría estadísticamente significativa en la puntuación obtenida en el SAQ en las limitaciones físicas (59,7 ± 19,3 al principio frente a 66,2 ± 16,9 a los 3 meses de seguimiento; p = 0,037), la estabilidad de la angina (57,1 ± 28,1 al principio frente a 75,8 ± 22,3 a los 3 meses de seguimiento; p = 0,010), así como en la percepción de la enfermedad (42,5 ± 13,9 al principio frente a 50,8 ± 16,3 a los 3 meses de seguimiento; p = 0,015), No se hallaron diferencias estadísticamente significativas en la frecuencia de los episodios anginosos (74,3 ± 20,4 al principio frente a 80,7 ± 19,8 a los 3 meses de seguimiento; p = 0,193) ni en la satisfacción con el tratamiento (68,1 ± 12,6 al principio frente a 70,5 ± 12,5 a los 3 meses de seguimiento; p = 0,950) (figura 7). Tampoco se registraron reacciones adversas tras 1 año de seguimiento.
Figura 6. Diferencias en la puntuación obtenida en el cuestionario EuroQol-5D (EQ-5D) al principio y a los 3 meses de seguimiento.
Figura 7. Diferencias en la puntuación obtenida en el cuestionario SAQ al principio y a los 3 meses de seguimiento. EA: estabilidad de la angina; EQ-5D: EuroQol-5D; FEA: frecuencia de los episodios anginosos; LF: limitaciones físicas; PE: percepción de la enfermedad; SAQ: cuestionario de angina de Seattle; ST, satisfacción con el tratamiento.
DISCUSIÓN
Los principales resultados de nuestra experiencia se pueden resumir de la siguiente manera: a) la implementación de un protocolo diagnóstico y terapéutico específico (programa NOCA) en pacientes diagnosticados de EC no obstructiva es factible y permitió un uso eficiente de los recursos médicos; b) un estudio diagnóstico integral de pacientes con INOCA y ANOCA resulta seguro y tiene un índice bajo de complicaciones leves y transitorias (5,5%); c) la inclusión de pacientes en el programa NOCA provocó cambios significativos en los fármacos y mejoró notablemente los síntomas anginosos de los pacientes tras 3 meses de seguimiento, sin eventos adversos al cabo 1 año.
A pesar de que la evidencia acumulada ha venido a confirmar que un abordaje que englobe una valoración diagnóstica integral y una terapia médica estratificada en pacientes con INOCA y ANOCA se antoja esencial a la hora de mejorar el pronóstico de los pacientes, dicho abordaje todavía está lejos de poderse implementar de manera rutinaria en la práctica clínica7,8. Todavía preocupa la relación coste-beneficios, el mayor tiempo asociado la intervención, los mayores costes asociados y el riesgo de posibles complicaciones. Además, en las guías más recientes publicadas por la Sociedad Europea de Cardiología, las pruebas invasivas de la función coronaria han recibido una recomendación de clase IIa («debería considerarse»), cuando las pruebas de provocación con ACh vienen respaldadas por una recomendación de clase IIb («puede considerarse») para la valoración del espasmo microvascular y una recomendación de clase IIa en pacientes con AV3. Como resultado, el tratamiento de estos pacientes suele dejarse a criterio médico o a la experiencia de cada centro. Como consecuencia, el diagnóstico de un endotipo NOCA específico se suele pasar por alto y el tratamiento médico no se suele optimizar, lo que a su vez, influye muy negativamente tanto en la calidad de vida y los resultados clínicos de los pacientes como en el gasto médico por la necesidad de nuevas hospitalizaciones o intervenciones invasivas18.
Al participar nuestra propia experiencia, demostramos que un protocolo diagnóstico y terapéutico específico (es decir, el programa NOCA) en pacientes con un diagnóstico previo de EC no obstructiva se puede implementar fácilmente en la práctica clínica. Una innovación clave de nuestro estudio frente a publicaciones previas, es la creación e implementación de un protocolo específico para la población de INOCA/ANOCA. Además, nuestro enfoque incorpora visitas de cribado a equipos de cardiólogos expertos para pacientes con sospecha diagnóstica de INOCA/ANOCA. Este enfoque mejora la identificación de estos pacientes y, según nuestra experiencia, excluyó a casi un tercio de los pacientes (29,9%) por la presencia de síntomas anginosos atípicos o causas no coronarias claramente identificables de dolor torácico. Esta es otra novedad de nuestro estudio que podría ser sumamente relevante para el manejo de estos pacientes. La selección de pacientes para incluir en el programa permitiría dirigir los recursos clínicos a aquellos pacientes más propensos a beneficiarse evitando, así, tener que repetir intervenciones invasivas y riesgos de pacientes con indicaciones poco claras. Además, el asesoramiento especializado proporcionado por cardiólogos y enfermeras durante las visitas de cribado, sumado al apoyo psicológico, probablemente sean un componente vital en el abordaje y tratamiento de pacientes con INOCA/ANOCA. De hecho, estudios recientes han demostrado que factores psicológicos tales como el estrés crónico, la ansiedad, la depresión y los factores de estrés social están implicados en la patogénesis tanto de la AMV como de la AV19-23. El estrés mental ha demostrado ser determinante, sobre todo en la DMC a través de mecanismos dependientes del endotelio y de la disfunción endotelial24. Asimismo, al activar áreas del cerebro implicadas en la regulación de los sistemas neuroendocrino y nervioso autónomo, el estrés mental puede provocar hiperreactividad de las células musculares lisas vasculares, disfunción del sistema nervioso autónomo, estrés oxidativo, inflamación vascular y disfunción endotelial, todo ello conducente a una mayor propensión a sufrir vasoespasmos coronarios25-27.
Coincidiendo con lo descrito en otros estudios publicados28-30, nuestra experiencia demuestra que una valoración diagnóstica invasiva integral encaminada a diagnosticar endotipos específicos en pacientes con INOCA y ANOCA es segura y tiene un índice bajo de complicaciones leves y transitorias. Por tanto, médicos y pacientes deben estar tranquilos ante la ausencia de complicaciones graves y se debe alentar a los cardiólogos a implementar programas de diagnóstico y tratamiento específico de estos pacientes. La disponibilidad de dicho programa para pacientes con INOCA y ANOCA puede tener importantes implicaciones clínicas y terapéuticas, ya que, según nuestra experiencia, provocó cambios sustanciales en los fármacos y mejoras significativas en el cuestionario SAQ a los 3 meses en lo referente a las limitaciones físicas, frecuencia de los episodios anginosos y percepción de la enfermedad. Las mejoras más leves y menos significativas descritas en otros parámetros (por ejemplo, frecuencia de los episodios anginosos y satisfacción con el tratamiento) serían atribuibles a valores de referencia altos per se (74,5 ± 19,9 y 69,6 ± 11,9, respectivamente). Asimismo, la falta de mejoras significativas en el cuestionario EQ-5D a los 3 meses podría deberse al corto periodo de seguimiento o que es un cuestionario no específico de la enfermedad diseñado para describir y evaluar el estado de salud de los pacientes que se ha de complementar con otras mediciones de la calidad de vida31.
Limitaciones del estudio
Se deben reconocer algunas limitaciones propias de este estudio. En primer lugar, se trata de un estudio unicéntrico con un tamaño de muestra relativamente pequeño y un seguimiento corto. En segundo lugar, como no se realizó un análisis de costes, no se puede especular sobre el impacto que tuvo el programa NOCA en los costes de la atención sanitaria. Se necesitan más estudios en poblaciones más grandes con ANOCA e INOCA. Finalmente, la ausencia de un grupo de control impidió una valoración integral de la mejora en la calidad de vida de estos pacientes.
CONCLUSIONES
Nuestra experiencia viene a demostrar que un protocolo diagnóstico y terapéutico específico (programa NOCA) puede implementarse de manera fácil y segura en la práctica clínica habitual. Dicho protocolo garantizaría mejores cuidados para pacientes con INOCA y ANOCA, mejoras en la calidad de vida y evitar tratamientos inadecuados e investigaciones incompletas. Es imprescindible disponer de nuevas evidencias de futuros ensayos clínicos aleatorizados o de recomendaciones procedentes de guías clínicas internacionales que respalden la implementación de un protocolo específico en estos pacientes.
FINANCIACIÓN
Ninguna.
CONSIDERACIONES ÉTICAS
El protocolo del estudio se realizó de conformidad con lo dispuesto en la Declaración de Helsinki y el estudio fue aprobado por nuestro Comité de Revisión Institucional. Todos los pacientes dieron su consentimiento informado por escrito antes de ser incluidos en este programa y estudio. El comité de ética clínica dio su aprobación para un análisis retrospectivo de los datos recopilados. En este trabajo, se han tenido en cuenta las posibles variables de sexo y género.
DECLARACIÓN SOBRE EL USO DE INTELIGENCIA ARTIFICIAL
No se utilizaron herramientas de inteligencia artificial durante la preparación de este trabajo.
CONTRIBUCIÓN DE LOS AUTORES
R. Rinaldi, F. Spione y F.M. Verardi: extracción y análisis de datos y redacción del manuscrito; R. Rinaldi, F. Spione y S. Brugaletta: diseño y revisión del manuscrito; P. Vidal Calés, V. Arévalos, R. Gabani, D. Cánovas, M. Gutiérrez, M. Pardo, R. Domínguez, L. Pintor, X. Torres, X. Freixa, A. Regueiro, O. Abdul-Jawad Altisent y M. Sabaté: revisión del manuscrito. Todos los autores han leído y aceptado la versión publicada del manuscrito.
¿QUÉ SE SABE DEL TEMA?
- Entre el 60 y 70% de los pacientes con angina y/o evidencia documentada de isquemia miocárdica no presentan evidencias angiográficas de enfermedad coronaria obstructiva. Esta patología se define como un cuadro de angina sin arterias coronarias obstructivas (ANOCA) o isquemia sin arterias coronarias obstructivas (INOCA) ante posibles evidencias de isquemia miocárdica. Sigue preocupando la implementación en la práctica clínica real de un abordaje diagnóstico y terapéutico sistemático en pacientes con INOCA y ANOCA que pudiese influir tanto en los resultados como en la calidad de vida de los pacientes.
¿QUÉ APORTA DE NUEVO?
- La implementación de un protocolo específico (programa NOCA) en pacientes diagnosticados de EC no obstructiva es factible y permitió un uso eficiente de los recursos médicos. La valoración diagnóstica invasiva integral en pacientes con INOCA o ANOCA resulta segura y se asocia a un índice bajo de complicaciones leves y transitorias. La disponibilidad de un programa diagnóstico y terapéutico específico para pacientes con INOCA y ANOCA podría tener importantes implicaciones clínicas y terapéuticas, ya que, según nuestra experiencia, condujo a cambios farmacológicos significativos y a una notable mejoría tras 3 meses de seguimiento en el cuestionario SAQ en lo referente a las limitaciones físicas, la frecuencia de los episodios anginosos y la percepción de la enfermedad.
CONFLICTO DE INTERESES
Ninguno.
AGRADECIMIENTOS
F. Spione ha recibido una beca de investigación dentro del programa de doctorado Cardiopath.
BIBLIOGRAFÍA
1. Roth GA, Mensah GA, Johnson CO, et al. Global Burden of Cardiovascular Diseases and Risk Factors, 1990-2019:Update From the GBD 2019 Study. J Am Coll Cardiol. 2020;76:2982-3021.
2. Patel MR, Peterson ED, Dai D, et al. Low diagnostic yield of elective coronary angiography. N Engl J Med. 2010;362:886-895.
3. Neumann FJ, Sechtem U, Banning AP, et al. 2019 ESC Guidelines for the diagnosis and management of chronic coronary syndromes. Eur Heart J. 2020;41:407-477.
4. Jespersen L, Hvelplund A, Abildstrøm SZ, et al. Stable angina pectoris with no obstructive coronary artery disease is associated with increased risks of major adverse cardiovascular events. Eur Heart J. 2012;33:734-744.
5. Taqueti VR, Solomon SD, Shah AM, et al. Coronary microvascular dysfunction and future risk of heart failure with preserved ejection fraction. Eur Heart J. 2018;39:840-849.
6. Kunadian V, Chieffo A, Camici PG, et al. An EAPCI Expert Consensus Document on Ischaemia with Non-Obstructive Coronary Arteries in Collaboration with European Society of Cardiology Working Group on Coronary Pathophysiology &Microcirculation Endorsed by Coronary Vasomotor Disorders International Study Group. Eur Heart J. 2020;41:3504-3520.
7. Ford TJ, Stanley B, Good R, et al. Stratified Medical Therapy Using Invasive Coronary Function Testing in Angina:The CorMicA Trial. J Am Coll Cardiol. 2018;72:2841-2855.
8. Ford TJ, Stanley B, Sidik N, et al. 1-Year Outcomes of Angina Management Guided by Invasive Coronary Function Testing (CorMicA). JACC Cardiovasc Interv. 2020;13:33-45.
9. Candreva A, Gallinoro E, van 't Veer M, et al. Basics of Coronary Thermodilution. JACC Cardiovasc Interv. 2021;14:595-605.
10. Montone RA, Meucci MC, De Vita A, Lanza GA, Niccoli G. Coronary provocative tests in the catheterization laboratory:Pathophysiological bases, methodological considerations and clinical implications. Atherosclerosis. 2021;318:14-21.
11. Ford TJ, Ong P, Sechtem U, et al. Assessment of Vascular Dysfunction in Patients Without Obstructive Coronary Artery Disease:Why, How, and When. JACC Cardiovasc Interv. 2020;13:1847-1864.
12. Gutiérrez E, Gómez-Lara J, Escaned J, et al. Assessment of the endothelial function and spasm provocation test performed by intracoronary infusion of acetylcholine. Technical report from the ACI-SEC;REC Interv Cardiol. 2021;3:286-296.
13. Beltrame JF, Crea F, Kaski JC, et al. International standardization of diagnostic criteria for vasospastic angina. Eur Heart J. 2017;38:2565-2568.
14. Ong P, Camici PG, Beltrame JF, et al. International standardization of diagnostic criteria for microvascular angina. Int J Cardiol. 2018;250:16-20.
15. Jespersen L, Abildstrøm SZ, Hvelplund A, Prescott E. Persistent angina:highly prevalent and associated with long-term anxiety, depression, low physical functioning, and quality of life in stable angina pectoris. Clin Res Cardiol. 2013;102:571-581.
16. Chan PS, Jones PG, Arnold SA, Spertus JA. Development and validation of a short version of the Seattle angina questionnaire. Circ Cardiovasc Qual Outcomes. 2014;7:640-647.
17. Herdman M, Gudex C, Lloyd A, et al. Development and preliminary testing of the new five-level version of EQ-5D (EQ-5D-5L). Qual Life Res. 2011;20:1727-1736.
18. Jespersen L, Abildstrom SZ, Hvelplund A, et al. Burden of hospital admission and repeat angiography in angina pectoris patients with and without coronary artery disease:a registry-based cohort study. PLoS One. 2014;9:e93170.
19. Smaardijk VR, Lodder P, Kop WJ, van Gennep B, Maas AHEM, Mommersteeg PMC. Sex- and Gender-Stratified Risks of Psychological Factors for Incident Ischemic Heart Disease:Systematic Review and Meta-Analysis. J Am Heart Assoc. 2019;8:e010859.
20. Mehta PK, Hermel M, Nelson MD, et al. Mental stress peripheral vascular reactivity is elevated in women with coronary vascular dysfunction:Results from the NHLBI-sponsored Cardiac Autonomic Nervous System (CANS) study. Int J Cardiol. 2018;251:8-13.
21. Konst RE, Elias-Smale SE, Lier A, Bode C, Maas AHEM. Different cardiovascular risk factors and psychosocial burden in symptomatic women with and without obstructive coronary artery disease. Eur J Prev Cardiol. 2019;26:657-659.
22. Gomez MA, Merz NB, Eastwood JA, et al. Psychological stress, cardiac symptoms, and cardiovascular risk in women with suspected ischaemia but no obstructive coronary disease. Stress Health. 2020;36:264-273.
23. Bekendam MT, Vermeltfoort IAC, Kop WJ, Widdershoven JW, Mommersteeg PMC. Psychological factors of suspect coronary microvascular dysfunction in patients undergoing SPECT imaging. J Nucl Cardiol. 2022;29:768-778.
24. Hammadah M, Kim JH, Al Mheid I, et al. Coronary and Peripheral Vasomotor Responses to Mental Stress. J Am Heart Assoc. 2018;7:e008532.
25. Shah A, Chen C, Campanella C, et al. Brain correlates of stress-induced peripheral vasoconstriction in patients with cardiovascular disease. Psychophysiology. 2019;56:e13291.
26. Hung MY, Mao CT, Hung MJ, et al. Coronary Artery Spasm as Related to Anxiety and Depression:A Nationwide Population-Based Study. Psychosom Med. 2019;81:237-245.
27. Crea F, Montone RA, Rinaldi R. Pathophysiology of Coronary Microvascular Dysfunction. Circ J. 2022;86:1319-1328.
28. Probst S, Seitz A, Martínez Pereyra V, et al. Safety assessment and results of coronary spasm provocation testing in patients with myocardial infarction with unobstructed coronary arteries compared with patients with stable angina and unobstructed coronary arteries. Eur Heart J Acute Cardiovasc Care.2020:2048∖20932422.
29. Montone RA, Rinaldi R, Del Buono MG, et al. Safety and prognostic relevance of acetylcholine testing in patients with stable myocardial ischaemia or myocardial infarction and nonobstructive coronary arteries. EuroIntervention 2022;18:e666-e676.
30. Rinaldi R, Salzillo C, CaffèA, Montone RA. Invasive Functional Coronary Assessment in Myocardial Ischemia with Non-Obstructive Coronary Arteries:from Pathophysiological Mechanisms to Clinical Implications. Rev Cardiovasc Med. 2022;23:371.
31. EuroQol--a new facility for the measurement of health-related quality of life. Health Policy. 1990;16:199-208.