RESUMEN
Introducción y objetivos: El tratamiento óptimo de las lesiones angiográficas intermedias (diámetro de estenosis 40-69%) no culpables en pacientes con infarto agudo de miocardio con elevación del segmento ST (IAMCEST) está por determinar. La reserva fraccional de flujo (RFF) permite diagnosticar lesiones causantes de isquemia (RFF ≤ 0,80) que se benefician de una revascularización. No obstante, las lesiones con RFF > 0,80 y criterios de vulnerabilidad por tomografía de coherencia óptica (OCT) también se ha hipotetizado que pueden causar eventos adversos en el seguimiento. El objetivo es comparar la eficacia del tratamiento preventivo con implantación de stent más tratamiento médico óptimo de lesiones intermedias no culpables con RFF > 0,80 y características de placa vulnerable frente a solo tratamiento médico óptimo en pacientes con IAMCEST a 4 años de seguimiento.
Métodos: Estudio de grupos paralelos, multicéntrico, controlado, aleatorizado 1:1 y simple ciego. Se incluirán 600 pacientes con IAMCEST y al menos una lesión intermedia no culpable que presenten RFF > 0,80 y características de placa vulnerable por OCT. El objetivo primario se define como fallo del vaso diana, compuesto de muerte cardiaca, infarto del vaso diana y necesidad de revascularización del vaso diana. El estudio incluye un registro paralelo para pacientes con RFF > 0,80 sin características de placa vulnerable. Se define placa vulnerable como fibroateromas lipídicos con carga de placa ≥ 70% y capa fibrosa fina (≤ 80 µm).
Resultados: El estudio VULNERABLE permitirá conocer el papel del tratamiento preventivo con stent de placas vulnerables no culpables funcionalmente no significativas en pacientes con IAMCEST.
Conclusiones: Se trata del primer estudio aleatorizado para el tratamiento de placas vulnerables guiado por OCT. Registrado en ClinicalTrials.gov (NCT05599061).
Palabras clave: Reserva fraccional de flujo. Tomografía de coherencia óptica. Infarto agudo de miocardio con elevación del segmento ST. Placa vulnerable.
ABSTRACT
Introduction and objectives: The optimal treatment of nonculprit angiographic intermediate lesions (diameter stenosis 40%-69%) in patients with ST-segment elevation myocardial infarction (STEMI) is still unknown. Lesions with fractional flow reserve (FFR) ≤ 0.80 are indicative of ischemia and benefit from revascularization. However, lesions with FFR > 0.80 and optical coherence tomography (OCT) findings of vulnerability have been hypothesized to cause adverse events during follow-up. The study aims to compare the efficacy of a preventive treatment with stent implantation plus optimal medical therapy vs optimal medical therapy alone for nonculprit intermediate lesions with FFR > 0.80 and OCT findings of plaque vulnerability in STEMI patients at 4 years of follow-up.
Methods: This parallel-group, multicenter, controlled, single-blind, and 1:1 randomized trial will enroll a total of 600 STEMI patients with ≥ 1 intermediate nonculprit lesions with FFR > 0.80 and OCT findings of plaque vulnerability. The primary endpoint is target vessel failure, defined as the composite of cardiac death, target vessel myocardial infarction, or target vessel revascularization. The study will include a parallel registry of patients with FFR > 0.80 but without OCT findings of vulnerability. Vulnerable plaques are defined as lipid-rich fibroathermas with plaque burden ≥ 70% and a thin fibrous cap (≤ 80 mm).
Results: The VULNERABLE trial will reveal the role of preventive treatment with stent implantation for nonculprit and functionally nonsignificant vulnerable plaques in STEMI patients.
Conclusions: This is the first randomized trial of OCT-guided treatment of vulnerables plaques. Registered at ClinicalTrials.gov (NCT05599061).
Keywords: Fractional flow reserve. Optical coherence tomography. ST-segment elevation myocardial infarction. Vulnerable plaque.
Abreviaturas ALM: área luminal mínima. DE: diámetro de estenosis. IAMCEST: infarto agudo de miocardio con elevación del segmento ST. OCT: tomografía de coherencia óptica. RFF: reserva fraccional de flujo. TMO: tratamiento médico óptimo.
INTRODUCCIÓN
La presencia de enfermedad multivaso, definida como lesiones angiográficas con un diámetro de estenosis (DE) visual ≥ 50%, en pacientes con infarto agudo de miocardio con elevación del segmento ST (IAMCEST) se estima alrededor del 50%1. El estudio COMPLETE comparó la revascularización preventiva con stent añadido al tratamiento médico óptimo (TMO) de lesiones no culpables de infarto con un DE ≥ 70% guiada por angiografía frente a TMO2. En este estudio, la revascularización preventiva guiada por angiografía demostró una disminución significativa de los eventos cardiacos adversos a 3 años de seguimiento2. Aunque el ensayo COMPLETE requería la valoración fisiológica mediante la reserva fraccional de flujo (RFF) de las lesiones entre el 50% y el 69% para decidir la revascularización, en la práctica solo se determinó en un porcentaje muy pequeño de pacientes.
Los estudios FLOWER-MI y FRAME-AMI3,4 investigaron el tratamiento preventivo con implantación de stent en lesiones no culpables guiado por RFF, obtenido mediante guía de presión intracoronaria, comparado con la revascularización completa guiada por angiografía (estimación visual). Ambos estudios incluyeron mayoritariamente lesiones intermedias y demostraron que una revascularización preventiva guiada por guía de presión permite una disminución importante de la necesidad de revascularización, con una eficacia similar o superior a la de la revascularización completa guiada por angiografía3,4. A pesar de esto, basándose en el estudio COMPLETE, las guías de práctica clínica recomiendan el tratamiento preventivo mediante implante de stent en lesiones no culpables de infarto guiado solo por angiografía5,6.
Cabe destacar que la RFF es considerada la prueba de referencia para la detección de isquemia miocárdica (RFF ≤ 0,80). No obstante, diferir el tratamiento de lesiones no culpables de infarto que no generan isquemia (RFF > 0,80) mediante TMO genera dudas en casos seleccionados en los que las características anatómicas de la lesión sugieren signos de vulnerabilidad. En el estudio FLOWER-MI, el grupo de pacientes aleatorizados a revascularización guiada por guía de presión que presentaron una RFF > 0,80 (derivados a TMO) tuvieron más eventos adversos que los del mismo grupo que presentaron una RFF ≤ 0,80 (derivados a revascularización percutánea)7. Varios estudios basados en técnicas de imagen intravascular también han demostrado una asociación entre la presencia de placas fibrolipídicas con alto contenido lipídico y capa fibrosa fina, denominadas placas vulnerables, y el desarrollo de futuros eventos adversos causados por rotura de estas placas8-11.
El estudio VULNERABLE pretende valorar la eficacia de una estrategia combinada basada en técnicas de fisiología intracoronaria e imagen intravascular para guiar el tratamiento de las lesiones intermedias no culpables de infarto en pacientes con IAMCEST. La hipótesis del estudio es que un tratamiento preventivo con implantación de stent (añadido al TMO) en lesiones intermedias no culpables de infarto que presentan una RFF > 0,80 y características de placa vulnerable es superior al TMO solo. El presente artículo incluye la justificación y el diseño de este estudio.
MÉTODOS
Diseño
El estudio VULNERABLE (NCT05599061) contempla 3 grupos dependiendo de los resultados obtenidos durante la valoración combinada funcional y anatómica con guía de presión y tomografía de coherencia óptica (OCT). La figura 1 muestra el diagrama de flujo del estudio, donde se ilustran los 3 grupos: pacientes con RFF ≤ 0,80 tratados con stent (fallos de búsqueda), pacientes con RFF > 0,80 sin características de placa vulnerable (incluidos en el grupo de registro) y pacientes con RFF > 0,80 y características de placa vulnerable (incluidos en el ensayo clínico aleatorizado).
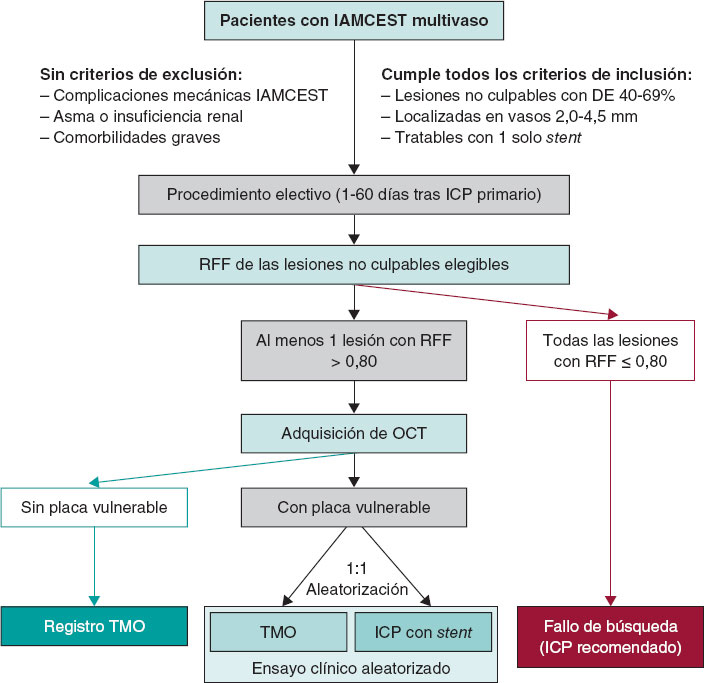
Figura 1. Diagrama del estudio. IAMCEST: infarto agudo de miocardio con elevación del segmento ST; ICP: intervencionismo coronario percutáneo; OCT: tomografía de coherencia óptica; RFF: reserva fraccional de flujo; TMO: tratamiento médico óptimo.
Se trata de un estudio multicéntrico, controlado, prospectivo, aleatorizado, de grupos paralelos y simple ciego para los pacientes incluidos en el grupo de ensayo clínico. El estudio se lleva a cabo siguiendo las recomendaciones recogidas en la Declaración de Helsinki sobre investigación clínica y ha sido aprobado por el comité de ética de referencia (Hospital Universitari de Bellvitge), y refrendado por el resto de los comités de ética de los centros participantes. En la tabla 1 del material adicional se detallan los centros y los investigadores principales participantes en el estudio.
Tabla 1. Objetivos del estudio VULNERABLE
| Objetivo primario |
|---|
| Comparar el porcentaje de FVD entre los dos grupos de pacientes asignados al ensayo clínico aleatorizado (RFF > 0,80 con características de placa vulnerable por OCT): revascularización preventiva con stent + TMO frente a solo TMO |
| Objetivo secundario clave |
| Comparar el porcentaje de FVD entre los pacientes asignados al grupo de registro (RFF > 0,80 sin características de placa vulnerable por OCT y tratados con TMO) y los pacientes asignados al grupo aleatorizado de TMO (RFF > 0,80 con características de placa vulnerable) |
| Otros objetivos secundarios |
| Comparar el porcentaje de muertes por todas las causas entre los 2 subgrupos de pacientes aleatorizados |
| Comparar el porcentaje de muertes de causa cardiaca entre los 2 subgrupos de pacientes aleatorizados |
| Comparar el porcentaje de todos los infartos entre los 2 subgrupos de pacientes aleatorizados |
| Comparar el porcentaje de infartos del vaso diana entre los 2 subgrupos de pacientes aleatorizados |
| Comparar el porcentaje de necesidad de revascularización del vaso diana entre los 2 subgrupos de pacientes aleatorizados |
| Valorar el porcentaje de restenosis y trombosis de stent en el grupo con revascularización preventiva con stent + TMO del ensayo clínico aleatorizado |
* Todos los objetivos están marcados con un seguimiento de 4 años completos, aunque se realizará un estudio intermedio planeado a 2 años. |
El estudio ha sido íntegramente diseñado e iniciado por investigadores y está auspiciado por el Grupo de Trabajo de Diagnóstico Intracoronario de la Asociación de Cardiología Intervencionista de la Sociedad Española de Cardiología. Dispone de un comité directivo, un comité de seguridad de los datos y un comité de adjudicación de eventos independiente. La tabla 2 del material adicional recoge los integrantes de los distintos comités. El comité directivo y todos los investigadores del estudio se comprometen a una correcta cumplimentación de los datos y al seguimiento del protocolo. La entidad financiadora (Abbott Vascular, Estados Unidos) no tiene ningún papel en el diseño del estudio, en la cumplimentación y el análisis de los datos, ni en la redacción de los resultados. El promotor del estudio (Fundación para Educación en Procedimientos de Intervencionismo en Cardiología [EPIC]) se hace responsable, junto con los investigadores principales, de la gestión de los datos y su confidencialidad.
Tabla 2. Criterios de inclusión y exclusión del estudio VULNERABLE
| Criterios de inclusión |
|---|
| Pacientes mayores de 18 años |
| Con IAMCEST (elevación > 1 mm del segmento ST en al menos 2 derivaciones contiguas o elevación verdadera del segmento ST posterior con infradesnivelación > 2 mm en derivaciones anteriores o bloqueo de rama izquierda de nueva aparición) tratados con revascularización exitosa de la lesión culpable dentro de las 72 horas desde el inicio de los síntomas |
| Que presenten enfermedad multivaso con al menos una lesión angiográficamente intermedia (DE visual 40-69%) en un vaso nativo distinto del de la lesión culpable del infarto |
| Que se plantee la revascularización percutánea con un solo stent de 2,0-4,5 mm guiada por RFF |
| Entre 1 y 60 días tras el procedimiento índice (revascularización del vaso culpable del IAMCEST) |
| Criterios de exclusión |
| Esperanza de vida menor de 4 años |
| Mujeres en edad fértil que deseen quedarse embarazadas |
| Intolerancia conocida al ácido acetilsalicílico, la heparina, el everolimus o el contraste iodado |
| Complicaciones mecánicas o shock cardiogénico relacionado con el infarto no resuelto |
| Lesiones elegibles para el estudio localizadas en el tronco común coronario izquierdo, en vasos con revascularización previa, en bifurcaciones con rama lateral > 2,5 mm, en grandes angulaciones o en segmentos con calcificación grave |
| Historia de asma grave |
| Insuficiencia renal crónica con filtrado glomerular < 45 ml/min |
DE: diámetro de estenosis; IAMCEST: infarto agudo de miocardio con elevación del segmento ST; RFF: reserva fraccional de flujo. |
Objetivos
El objetivo primario es comparar la eficacia del tratamiento preventivo con implantación de stent añadido al TMO de lesiones intermedias en arterias no culpables de infarto que presentan una RFF > 0,80 y muestran características de placa vulnerable por OCT, frente al TMO, a 4 años de seguimiento. El porcentaje de fallo del vaso diana (FVD) es el objetivo principal del estudio y se define como un combinado de muerte de causa cardiaca, infarto del vaso diana o necesidad de revascularización del vaso diana.
El estudio pretende comparar varios objetivos secundarios, resumidos en la tabla 1. Dentro de estos cabe destacar la comparación del porcentaje de FVD en el grupo de registro (pacientes con RFF > 0,80 sin características de placa vulnerable y tratados con TMO) y el grupo aleatorizado a TMO del ensayo clínico (RFF > 0,80 con características de placa vulnerable). En la tabla 3 del material adicional se encuentra la definición de los objetivos del estudio12,13.
Criterios de inclusión y exclusión de pacientes
La tabla 2 muestra los criterios de inclusión y exclusión del estudio. En resumen, son elegibles para el estudio todos los pacientes con IAMCEST con revascularización exitosa de la lesión culpable que presentan al menos una lesión intermedia (definida visualmente con un DE del 40-69%) en un vaso distinto del causante del infarto y se plantea realizarles una revascularización percutánea con un solo stent guiada por RFF. El procedimiento del estudio debe realizarse entre 1 y 60 días tras la revascularización de la lesión culpable del infarto. Se requiere la aceptación y la firma del consentimiento informado antes de la realización del procedimiento electivo para el estudio de la lesión no culpable.
Protocolo de estudio de las lesiones no culpables y aleatorización
Las lesiones elegibles son estudiadas inicialmente con guía de presión de acuerdo con el procedimiento estándar de cada laboratorio. Las lesiones con RFF ≤ 0,80 serán consideradas como fallos de búsqueda y se recomienda su revascularización por indicación clínica5,6.
Las lesiones con RFF > 0,80 deberán ser estudiadas con OCT según el método de adquisición habitual en cada centro con el objetivo de detectar placas vulnerables. La valoración y la decisión sobre si la lesión estudiada cumple criterios de placa vulnerable estarán a cargo del investigador local acreditado en el mismo acto del procedimiento del estudio.
Los pacientes que presenten al menos una lesión con RFF > 0,80 sin criterios de placa vulnerable por OCT serán incluidos en el grupo de registro del estudio. Por protocolo, se recomienda el TMO para todas las lesiones con RFF > 0,80 sin criterios de placa vulnerable. Los pacientes asignados al grupo de registro recibirán el mismo seguimiento clínico que los que se incluyan en el grupo de ensayo clínico aleatorizado.
Los pacientes que presenten al menos una lesión con RFF > 0,80 y criterios de placa vulnerable por OCT se incluirán en el grupo de ensayo clínico y serán aleatorizados 1:1 para recibir un tratamiento preventivo con implantación de stent añadido al TMO o solo TMO (figura 1). El proceso de aleatorización se realiza sin estratos por centro ni por condición clínica, aplicando algoritmos de aleatorización telemáticos; la aleatorización se realiza online en la misma web de recogida de datos habilitada por pInvestiga (Pontevedra, España).
En el material adicional se explica la metodología para la valoración de la RFF, así como también aquellas situaciones especiales en las que no se ha podido valorar por completo la lesión en estudio, cuando se observa una placa no culpable inestabilizada, complicaciones relacionadas con las técnicas diagnósticas o pacientes con más de una lesión no culpable.
Dispositivo en estudio y procedimiento de implante
Los pacientes con RFF > 0,80 y características de placa vulnerable por OCT asignados al grupo de intervencionismo coronario percutáneo con implantación de stent serán tratados con un stent farmacoactivo recubierto de everolimus (Xience, Abbott, Estados Unidos). Por protocolo, se requiere la implantación del stent guiada por OCT. La tabla 4 del material adicional recoge los criterios de implantación de stent guiada por OCT.
Tratamiento médico óptimo
Todos los pacientes incluidos en el ensayo clínico aleatorizado y en el registro deben ser tratados siguiendo las guías de práctica clínica de la Sociedad Europea de Cardiología para los síndromes coronarios agudos5. En el protocolo del estudio se hace hincapié en la gestión de los factores de riesgo modificables (dieta, tabaquismo, obesidad, ejercicio y estado psicológico), la gestión de los factores de riesgo no modificables con objetivos de presión arterial preestablecidos (sistólica < 130 y diastólica < 80 mmHg), colesterol unido a lipoproteínas de baja densidad < 55 mg/dl y hemoglobina glucosilada < 7%, y el tratamiento médico farmacológico basado en bloqueadores beta e inhibidores del sistema renina-angiotensina. Se recomienda también el uso de doble antiagregación, a criterio de cada centro, solo durante el primer año tras el procedimiento índice. Por protocolo, se informará anualmente del tratamiento recibido por el paciente y se realizarán 2 analíticas de control con perfil lipídico.
Criterios de placa vulnerable por tomografía de coherencia óptica y formación de los investigadores
Según datos anatomopatológicos, se define una placa como vulnerable cuando es causada por un fibroateroma con un gran núcleo necrótico formado por detritos celulares y gran cantidad de células inflamatorias con una capa fibrosa fina (≤ 65 μm)14. Los criterios de placa vulnerable del estudio se adaptan a la definición anatomopatológica clásica, pero adaptada a la valoración por OCT (figura 2).
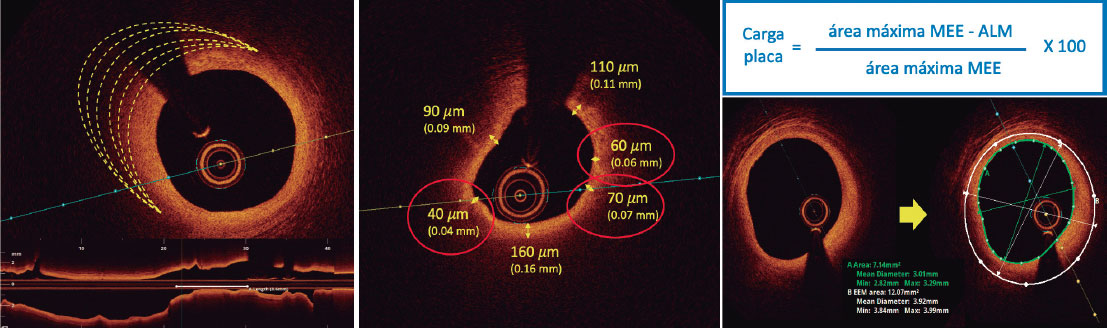
Figura 2. Criterios de placa vulnerable por tomografía de coherencia óptica. ALM: área luminal mínima; MEE: membrana elástica externa.
Según el protocolo, se requieren 3 criterios simultáneos para definir una placa vulnerable por OCT:
1) Presencia de una placa fibrolipídica con un núcleo necrótico > 90° de perímetro del vaso en más de 5 mm de longitud. Se define un núcleo necrótico como una imagen hipointensa de bordes mal definidos y que atenúa el paso del haz de luz de la sonda de OCT impidiendo la visualización de la arteria por detrás del núcleo.
2) Presencia de una capa fibrosa fina, definida como ≤ 80 μm (65 + 15 μm de resolución axial) en al menos 3 imágenes consecutivas. Se define la capa fibrosa como el tejido que separa el núcleo necrótico de la luz del vaso. Se entrena a los investigadores para poder diferenciar otros hallazgos que pueden confundirse con una capa fina por OCT. La figura 3 muestra ejemplos de imágenes análogas de OCT que pueden simular una capa fibrosa fina, pero que no corresponden a placas vulnerables.
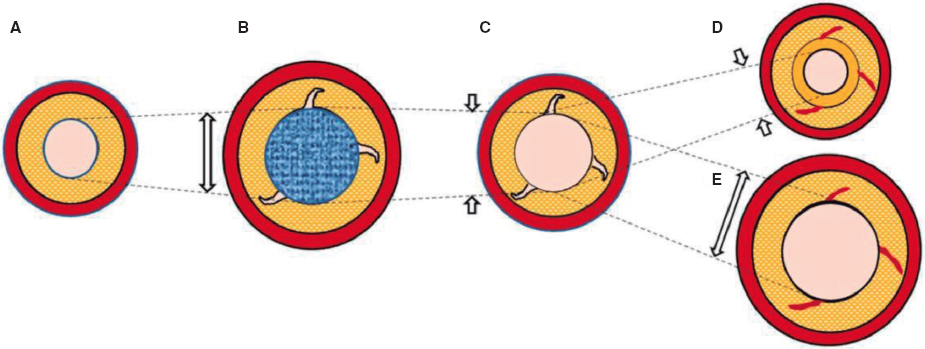
3) Se pide a los investigadores la medición de una carga de placa ≥ 70% en la sección transversal que corresponde con el área luminal mínima (ALM) dentro de la lesión. Para realizar esta valoración es necesario medir el perímetro del vaso delimitando la membrana elástica externa (MEE). Debido a la dificultad de valorar el perímetro del vaso en placas fibrolipídicas, especialmente en el lugar del ALM, se entrena a los investigadores para escoger una sección lo más cerca posible del ALM, en caso de imposibilidad en el mismo punto, donde se permita una visualización > 60% del perímetro del vaso. De esta ma- nera se puede calcular mediante la siguiente fórmula (figura 4):
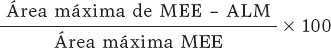
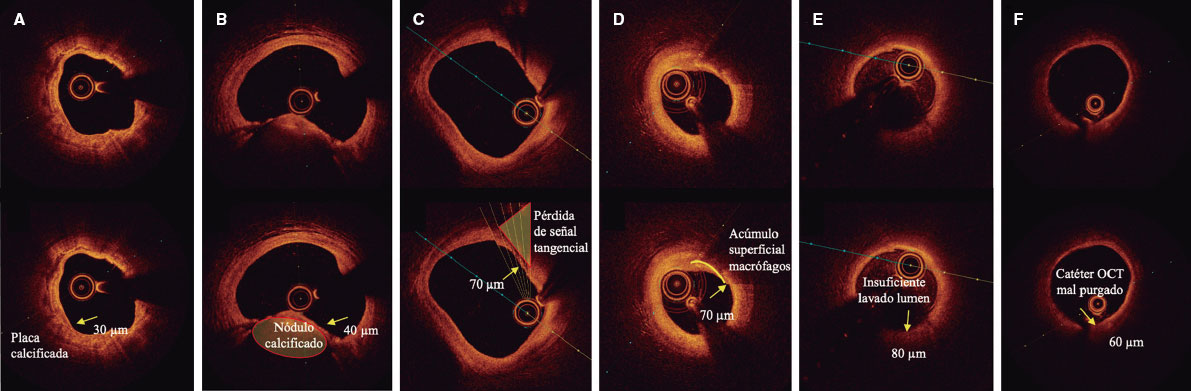
Figura 3. Diferenciación entre placas vulnerables y otros hallazgos por tomografía de coherencia óptica (OCT). A: placa con calcio superficial (núcleo hipointenso de bordes bien definidos que no atenúa el paso de luz; flecha) con una capa fibrosa fina. B: nódulo calcificado (flecha) con protrusión dentro del lumen y atenuación de la señal a pesar de tratarse de calcio. C: pérdida de señal tangencial (flecha) por falta de haces de luz por una posición periférica, no central, de la sonda de OCT. D: acúmulo superficial de macrófagos (flecha) con imagen hiperintensa, respecto a la íntima adyacente, con atenuación de la señal detrás. E: presencia de sangre en el lumen debido a un mal lavado (flecha) durante la adquisición que distorsiona la imagen de la pared arterial simulando regiones hipointensas. F: presencia de sangre entre la sonda y el catéter de OCT (flecha) debido a un mal purgado que distorsiona la imagen de la pared arterial simulando regiones hipointensas.
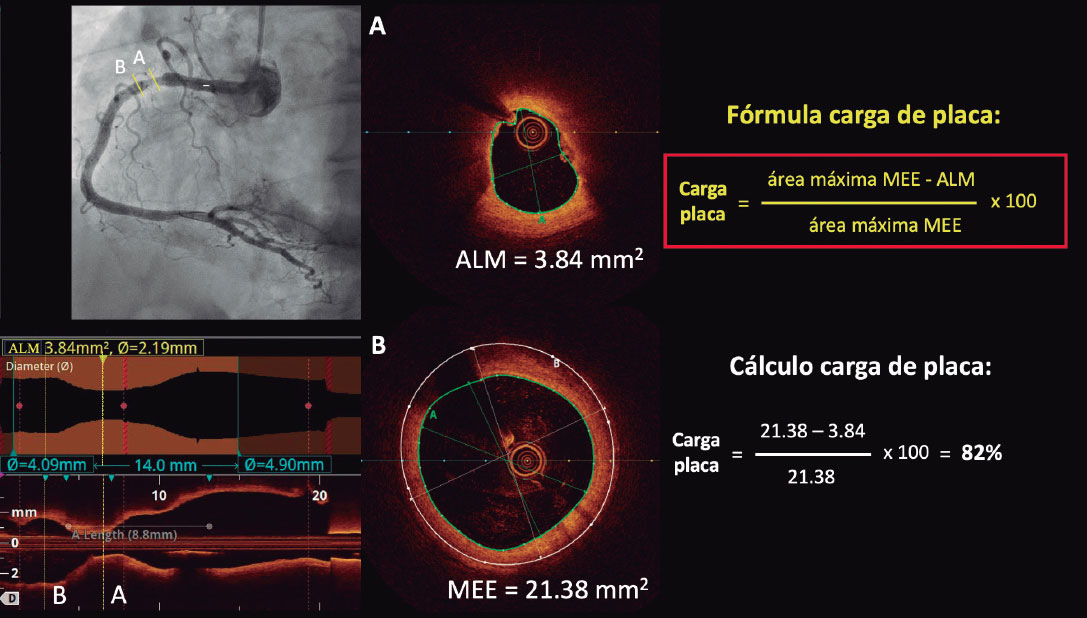
Figura 4. Valoración de la carga de placa por tomografía de coherencia óptica. A: sección del área luminal mínima (ALM). B: sección donde se ha medido la membrana elástica externa (MEE). Dado que la MEE no se puede valorar habitualmente en la sección transversal correspondiente al ALM, se hace una estimación aproximada midiendo la MEE dentro de los 10 mm proximales o distales al ALM (preferiblemente distales en ausencia de ramas laterales). Se valorará la MEE en la primera sección transversal donde se pueda evaluar un 60% del perímetro de la MEE.
Por protocolo, al menos un investigador local de cada centro participante debe haber realizado un curso de formación telemático para la detección y la valoración de placas vulnerables por OCT siguiendo los criterios del estudio. Tras la realización de este curso y la superación de un cuestionario específico, se acredita al investigador y se aprueba su participación en el estudio.
Análisis angiográfico y de tomografía de coherencia óptica
Para el estudio se dispone de un laboratorio de imágenes independiente que realizará el análisis de la cuantificación angiográfica y de OCT (Barcelona Cardiac Imaging Core-Laboratory [BARCICORE-Lab]), para monitorizar el cumplimiento de los criterios del estudio relativos al diagnóstico de placa vulnerable. Se hará un análisis ciego de los resultados del estudio y se adjudicarán los pacientes según el protocolo para llevar a cabo un análisis exploratorio. En el material adicional se explica con detalle el análisis angiográfico y de OCT por parte de dicho laboratorio.
Seguimiento clínico y cegado
Los pacientes incluidos en el grupo de registro y en el de ensayo clínico aleatorizado recibirán un seguimiento clínico durante 4 años. Se realizará un seguimiento telefónico a 1 y 3 años, y un seguimiento presencial a 2 y 4 años. El seguimiento clínico requerirá un electrocardiograma y análisis sanguíneos con determinación del colesterol.
Los pacientes incluidos en el ensayo clínico aleatorizado están cegados al grupo de tratamiento asignado (simple ciego). El cegado y la monitorización del ciego se especifican en el material adicional.
Cálculo del tamaño muestral
El tamaño de la muestra se ha calculado para el grupo de ensayo clínico aleatorizado. Los fallos de búsqueda y el número de pacientes incluidos en el registro dependerán del total de pacientes necesarios para alcanzar el tamaño muestral estimado para el ensayo clínico aleatorizado.
De acuerdo con estudios previos en pacientes con síndrome coronario agudo, el porcentaje de FVD de lesiones no culpables que presentan criterios de placa vulnerable tratadas con TMO se estima alrededor del 8-10% a 4 años de seguimiento, y en lesiones similares tratadas con stent se sitúa en torno al 4%2,7,9. En la tabla 5 del material adicional se resumen los estudios valorados para el cálculo del tamaño muestral. Considerando la hipótesis del estudio, el tratamiento preventivo con implantación de stent de lesiones no culpables con RFF > 0,80 y características de placa vulnerable, supondría una reducción del 60% en el objetivo primario. Se estima un 10% de eventos relativos al objetivo primario del estudio (FVD) en el grupo con TMO a 4 años. Asumiendo unas pérdidas anuales del 1,5% (6% en total), un total de 600 sujetos aleatorizados 1:1 a implantación preventiva de stent más TMO frente a TMO solo proporcionan un poder estadístico del 80% para demostrar superioridad del tratamiento preventivo con stent con un error alfa bilateral de 0,05.
Plan de análisis estadístico
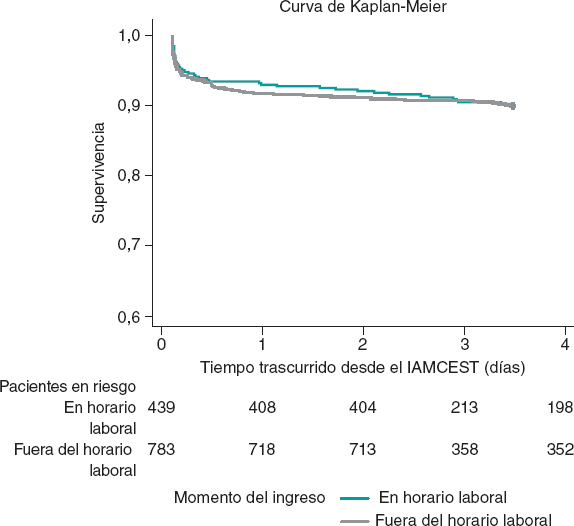
El análisis del objetivo principal y de los objetivos secundarios se realizará por intención de tratar a los 4 años de seguimiento completo. Las comparaciones estimarán proporciones de eventos entre grupos mediante regresión de Cox y los resultados serán presentados como cocientes de riesgo con intervalos de confianza del 95%. Solo se contará un evento del compuesto del objetivo primario por paciente. Se considerará estadísticamente significativo un valor p < 0,05 para el objetivo primario. Se utilizarán figuras de Kaplan Meier para la visualización del tiempo transcurrido hasta el primer evento entre grupos.
Con respecto a los compuestos del objetivo primario que presenten datos perdidos, se especificará un plan de monitorización específico que determine si los datos perdidos se deben al azar. En los casos con datos perdidos adjudicados al azar se utilizarán métodos de imputación, y en los casos no debidos al azar se realizarán análisis de sensibilidad con métodos de peor escenario y última observación.
Se planea realizar análisis de subgrupos para el objetivo primario del estudio y para el objetivo secundario consistente en la comparación del porcentaje de FVD entre los pacientes del registro y los pacientes aleatorizados a TMO en el ensayo clínico aleatorizado. Se preespecifican los siguientes subgrupos: edad > 75 años, sexo, diabetes mellitus, fracción de eyección del ventrículo izquierdo ≤ 35% en el procedimiento del estudio, lesiones localizadas en la descendente anterior proximal o media, y lesiones en vasos ≤ 2,75 mm de diámetro de referencia.
Finalmente, como generador de hipótesis, también se realizará un análisis paralelo de los datos de acuerdo con el protocolo del estudio. Se incluirán en el análisis aquellos pacientes en los que el laboratorio de imágenes del estudio concluya que existe concordancia entre el grupo asignado por parte del investigador local y la presencia de placa vulnerable por OCT definida por el laboratorio, y se excluirán aquellos con discordancia entre operador y laboratorio.
Análisis provisional
Tras 2 años de seguimiento hay planificado un análisis provisional de los datos para monitorizar el objetivo primario en el grupo de ensayo clínico aleatorizado. Se planea prolongar el seguimiento clínico en caso de que los eventos observados en el grupo de TMO del ensayo clínico aleatorizado sean < 4%.
DISCUSIÓN
El estudio VULNERABLE pretende investigar el uso combinado de fisiología e imagen intracoronaria para guiar el tratamiento de las lesiones intermedias no culpables en pacientes con IAMCEST.
Numerosos fármacos hipolipemiantes y antiinflamatorios han demostrado una reducción de los eventos trombóticos en los pacientes con IAMCEST que probablemente son causados por la estabilización de placas vulnerables funcionalmente no significativas15-17. En el estudio PACMAN-AMI, el tratamiento con alirocumab añadido a estatinas demostró una reducción significativa en el porcentaje de ateroma, una disminución en la cantidad de lípido y un engrosamiento de la capa fibrosa, frente al tratamiento con placebo en regiones coronarias con arteriosclerosis angiográfica no obstructiva (DE 20-50%)18. No obstante, es destacable que en este estudio solo un 31% de los pacientes presentaron estos 3 hallazgos indicativos de reducción de la arteriosclerosis y no se especifican datos relativos a placas de mayor entidad (por ejemplo, estenosis del 40-69% de obstrucción con criterios de vulnerabilidad)19.
La implantación de un stent en placas vulnerables espera que la cicatrización neointimal de los struts engrose la capa fibrosa y estabilice la placa. El estudio aleatorizado PREVENT investigó el tratamien- to preventivo con stent de lesiones vulnerables funcionalmente no significativas en pacientes con síndrome coronario crónico en comparación con TMO. Se definió la placa vulnerable por distintos métodos de imagen intravascular, aunque en la mayoría de los casos fue guiado solo por ecografía intravascular. En este estudio, el tratamiento preventivo con stent demostró una reducción estadísticamente significativa de la tasa de FVD a 2 años de seguimiento (0,4 frente a 3,4%; p = 0,0003)11.
Finalmente, varios estudios observacionales han demostrado que la OCT es un método eficaz para la detección de placas vulnerables y para monitorizar la respuesta a tratamientos intensivos dirigidos a estabilizar dichas placas mediante el engrosamiento de la capa fibrosa18,20. El estudio PECTUS-obs incluyó 438 pacientes con síndrome coronario agudo que presentaban lesiones no culpables con RFF > 0,80 y que fueron tratados solo con TMO10. Todas la lesiones se estudiaron con OCT y se siguieron criterios parecidos a los del estudio VULNERABLE para definir una placa vulnerable. En este estudio, un 34% de los pacientes presentaron al menos una lesión vulnerable, lo que se asoció a un mayor riesgo de eventos adversos (15,4% frente a 8,2% del compuesto de muerte, infarto o revascularización en los grupos con y sin placa vulnerable, respectivamente). El estudio VULNERABLE es el primero que utiliza la OCT para guiar el tratamiento de placas vulnerables en lesiones funcionalmente no significativas.
CONCLUSIONES
El estudio VULNERABLE está dirigido a valorar la eficacia del tratamiento preventivo con implantación de stent más TMO frente a solo TMO en placas vulnerables, definidas mediante OCT, en lesiones intermedias funcionalmente no significativas, en vasos no culpables de pacientes con IAMCEST. Además, aportará información acerca de la relevancia clínica de la presencia de placas vulnerables en lesiones no culpables de infarto.
FINANCIACIÓN
El presente estudio ha sido financiado por Abbott Vascular.
CONSIDERACIONES ÉTICAS
El estudio se lleva a cabo siguiendo las recomendaciones recogidas en la Declaración de Helsinki sobre investigación clínica y ha sido aprobado por el comité de ética de referencia (Hospital Universitari de Bellvitge) y refrendado por el resto de los comités de ética de los centros participantes. Es necesaria la aceptación y la firma del consentimiento informado previamente a la realización del procedimiento electivo para el estudio de la lesión no culpable. Se tienen en cuenta los posibles sesgos de sexo y género.
DECLARACIÓN SOBRE EL USO DE INTELIGENCIA ARTIFICIAL
No se ha utilizado inteligencia artificial para la redacción de este manuscrito.
CONTRIBUCIÓN DE LOS AUTORES
J. Gómez-Lara y E. Gutiérrez-Ibañes han redactado el borrador del documento. El resto de las personas firmantes han revisado el documento, realizado cambios a criterio propio y aprobado el texto final.
CONFLICTO DE INTERESES
J. Gómez-Lara y E. Gutiérrez-Ibañes han recibido una beca de Abbott Vascular para la realización de este estudio. A. Jurado- Román ha recibido honorarios de Abbott, Boston y Shockwave. E. Fernández ha recibido honorarios de Abbott y Hexacath. C. Cortés ha recibido un Contrato Río Hortega del Instituto de Salud Carlos III. S. Brugaletta ha recibido honorarios de Abbott, Microport y General Electric. T. García-Camarero ha recibido honorarios de Medtronic y Boston. J.A. Linares Vicente ha recibido honorarios de Abbott Vascular, Braun, AstraZeneca, Bayer y IZASA. O. Rodríguez-Leor ha recibido honorarios de Shockwave, WorlsMedica y Medtronic. S. Ojeda ha recibido honorarios de Abbott, Boston, WorldMedica y Biosensors. A. Pérez de Prado ha recibido becas y honorarios de Abbot, Boston, iVascular y Terumo. H.M. García-García ha recibido honorarios de ACIST, Boston Scientific, Medis, Biotronik, InfraRedx/Nipro, Chiesi y Cordis. S. Ojeda y A. Pérez de Prado son editores asociados de REC: Interventional Cardiology; se ha seguido el procedimiento editorial establecido en la revista para garantizar la gestión imparcial del manuscrito. El resto de los autores no presentan conflictos de intereses.
¿QUÉ SE SABE DEL TEMA?
- Las placas fibrolipídicas de capa fina, conocidas como vulnerables, son las causantes de la mayoría de los síndromes coronarios agudos. Aproximadamente un 50% de los pacientes con IAMCEST presentan otras lesiones angiográficas, además de la causante del infarto, que se asocian a un número relevante de eventos adversos isquémicos. Se ha demostrado que el tratamiento preventivo con stent de las lesiones no culpables graves (DE ≥ 70%) basado en angiografía disminuye el número de eventos adversos. No obstante, el tratamiento preventivo de lesiones no culpables angiográficamente intermedias (DE 40-69%) y que presentan características de placa vulnerable está por determinar.
¿QUÉ APORTA DE NUEVO?
- El estudio VULNERABLE es el primer estudio aleatorizado sobre el tratamiento preventivo de lesiones angiográficamente intermedias y no culpables que presentan características de vulnerabilidad por OCT en pacientes con IAMCEST.
BIBLIOGRAFÍA
1. Park DW, Clare RM, Schulte PJ, et al. Extent, location, and clinical significance of non-infarct-related coronary artery disease among patients with ST-elevation myocardial infarction. JAMA 2014;312:2019-2027.
2. Mehta SR, Wood DA, Storey RF, et al. Complete Revascularization with Multivessel PCI for Myocardial Infarction. N Engl J Med. 2019;381:1411-1421.
3. Lee JM, Kim HK, Park KH, et al. Fractional flow reserve versus angiography-guided strategy in acute myocardial infarction with multivessel disease:a randomized trial. Eur Heart J. 2023;44:473-484.
4. Puymirat E, Cayla G, Simon T, et al. Multivessel PCI Guided by FFR or Angiography for Myocardial Infarction. N Engl J Med. 2021;385:297-308.
5. Byrne RA, Rossello X, Coughlan JJ, et al. 2023 ESC Guidelines for the management of acute coronary syndromes. Eur Heart J. 2023;44:3720-3826.
6. Lawton JS, Tamis-Holland JE, Bangalore S, et al. 2021 ACC/AHA/SCAI Guideline for Coronary Artery Revascularization:Executive Summary:A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation. 2022;145:4-17.
7. Denormandie P, Simon T, Cayla G, et al. Compared Outcomes of ST-Elevation Myocardial Infarction Patients with Multivessel Disease Treated with Primary Percutaneous Coronary Intervention and Preserved Fractional Flow Reserve of Non-Culprit Lesions Treated Conservatively and of Those with Low Fractional Flow Reserve Managed Invasively:Insights from the FLOWER MI trial. Circ Cardiovasc Interv. 2021;14:011314.
8. Stone GW, Maehara A, Lansky AJ, et al. A prospective natural-history study of coronary atherosclerosis. N Engl J Med. 2011;364:226-235.
9. Erlinge D, Maehara A, Ben-Yehuda O, et al. Identification of vulnerable plaques and patients by intracoronary near-infrared spectroscopy and ultrasound (PROSPECT II):a prospective natural history study. Lancet. 2021;397:985-995.
10. Mol JQ, Volleberg R, Belkacemi A, et al. Fractional Flow Reserve-Negative High-Risk Plaques and Clinical Outcomes After Myocardial Infarction. JAMA Cardiol. 2023;8:1013-1021.
11. Park SJ, Ahn JM, Kang DY, et al. Preventive percutaneous coronary intervention versus optimal medical therapy alone for the treatment of vulnerable atherosclerotic coronary plaques (PREVENT):a multicentre, open-label, randomised controlled trial. Lancet. 2024;403:1753-1765.
12. Cutlip DE, Windecker S, Mehran R, et al. Clinical end points in coronary stent trials:a case for standardized definitions. Circulation. 2007;115:2344-2351.
13. Thygesen K, Alpert JS, Jaffe AS, et al. Fourth universal definition of myocardial infarction (2018). Eur Heart J. 2019;40:237-269.
14. Virmani R. Pathology of the vulnerable plaque. J Am Coll Cardiol. 2006;47:C13-8.
15. Cannon CP, Braunwald E, McCabe CH, et al. Intensive versus moderate lipid lowering with statins after acute coronary syndromes. N Engl J Med. 2004;350:1495-1504.
16. Schwartz GG, Steg PG, Szarek M, et al. Alirocumab and Cardiovascular Outcomes after Acute Coronary Syndrome. N Engl J Med. 2018;379:2097-2107.
17. Tardif JC, Kouz S, Waters DD, et al. Efficacy and Safety of Low-Dose Colchicine after Myocardial Infarction. N Engl J Med. 2019;381:2497-2505.
18. Raber L, Ueki Y, Otsuka T, et al. Effect of Alirocumab Added to High-Intensity Statin Therapy on Coronary Atherosclerosis in Patients With Acute Myocardial Infarction:The PACMAN-AMI Randomized Clinical Trial. JAMA. 2022;327:1771-1781.
19. Biccire FG, Haner J, Losdat S, et al. Concomitant Coronary Atheroma Regression and Stabilization in Response to Lipid-Lowering Therapy. J Am Coll Cardiol. 2023;82:1737-1747.
20. Kedhi E, Berta B, Roleder T, et al. Thin-cap fibroatheroma predicts clinical events in diabetic patients with normal fractional flow reserve:the COMBINE OCT-FFR trial. Eur Heart J. 2021;42:4671-4679.
* Autor para correspondencia.
Correo electrónico: gomezjosep@hotmail.com (J. Gómez-Lara).