RESUMEN
Introducción y objetivos: Se ha evidenciado en diversos estudios que la fracción de eyección del ventrículo izquierdo (FEVI) reducida (< 50%) es un factor de riesgo independiente de eventos y mortalidad en pacientes con estenosis aórtica (EA) grave tratados con recambio valvular. A pesar de que aquellos con FEVI conservada (> 50%) muestran mejor pronóstico, existe un grupo con FEVI supranormal (≥ 70%) que parece tener un pronóstico diferente por sus características particulares. El objetivo de este estudio fue evaluar los resultados del implante percutáneo de válvula aórtica (TAVI) en pacientes con EA grave y FEVI supranormal.
Métodos: Estudio de cohorte retrospectiva que incluyó 1.160 pacientes tratados con TAVI en 2007-2021 en el Hospital Clínico San Carlos (Madrid, España). Se clasificaron según su FEVI preoperatoria en reducida (< 50%), normal (50-69%) y supranormal (≥ 70%). Se compararon variables clínicas y ecocardiográficas, y los siguientes desenlaces: mortalidad por cualquier causa a los 30 días y al año, muerte por causa cardiovascular al año y rehospitalización por causa cardiovascular al año.
Resultados: De los 1.160 pacientes con EA grave que recibieron un TAVI durante el periodo del estudio, 276 (23,8%) se registraron con FEVI reducida, 702 (60,5%) con FEVI normal y 182 (15,7%) con FEVI supranormal. Los pacientes con FEVI supranormal eran predominantemente varones (82,9 ± 5,3 años), tenían menores volúmenes ventriculares, mayor grosor parietal relativo y geometría concéntrica. No hubo diferencias en la mortalidad a 30 días ni al año; sin embargo, la rehospitalización por causa cardiovascular al año fue significativamente superior en el grupo de FEVI supranormal (FEVI < 50%, 9,2%; FEVI 50-69%, 27,4%; FEVI ≥ 70%, 34,4%; p < 0,043).
Conclusiones: Los pacientes con EA grave tratados con TAVI que presentaban FEVI supranormal (≥ 70%) preprocedimiento tuvieron una mayor tasa de rehospitalización por causa cardiovascular al año, sin diferencias en la mortalidad.
Palabras clave: Fracción de eyección supranormal. Estenosis aórtica grave. TAVI. Rehospitalización.
ABSTRACT
Introduction and objectives: Several studies have shown that reduced (< 50%) left ventricular ejection fraction (LVEF) is an independent risk factor for cardiovascular events and mortality in patients with severe aortic stenosis (AS) undergoing valve replacement. Although patients with preserved LVEF (> 50%) have a better prognosis, there is a group with supranormal LVEF (≥ 70%) whose prognosis seems to differ due to their characteristics. The aim of this study was to evaluate outcomes after transcatheter aortic valve implantation (TAVI) in patients with severe AS and supranormal LVEF.
Methods: We performed a retrospective cohort study that included 1160 patients undergoing TAVI between 2007 and 2021 at Hospital Clínico San Carlos (Madrid, Spain). The patients were classified according to preoperative LVEF into reduced (< 50%), normal (50% to 69%), and supranormal (≥ 70%). Clinical, echocardiographic variables, and the following outcomes were compared: death from any cause at 30 days and at 1 year, death from cardiovascular causes at 1 year, and rehospitalization due to cardiovascular causes at 1 year.
Results: Of the 1160 patients with severe AS who underwent TAVI during the study period, 276 (23.8%) had reduced LVEF, 702 (60.5%) had normal LVEF, and 182 (15.7%) had supranormal LVEF. Patients with supranormal LVEF were predominantly men (82.9 ± 5.3 years) and had lower ventricular volumes, higher relative wall thickness, and concentric geometry. There were no differences in 30-day or 1-year mortality. However, rehospitalization for cardiovascular causes at 1 year was significantly higher in the supranormal LVEF group (LVEF < 50%: 29.2%; LVEF 50% to 69%: 27.4%; LVEF ≥ 70%: 34.4%; P < .043).
Conclusions: Patients with severe AS and supranormal preprocedural LVEF (≥ 70%) who underwent TAVI had a higher rate of cardiovascular rehospitalization at 1 year, with no differences in mortality.
Keywords: Supranormal ejection fraction. Severe aortic stenosis. TAVI. Rehospitalization.
Abreviaturas EA: estenosis aórtica. FEVI: fracción de eyección del ventrículo izquierdo. GPR: grosor parietal relativo. ITV: integral tiempo-velocidad. TAVI: implante percutáneo de válvula aórtica. TSVI: tracto de salida del ventrículo izquierdo.
INTRODUCCIÓN
La estenosis aórtica (EA) es la segunda valvulopatía más frecuente; se encuentra en el 12% de la población mayor de 75 años1,2. La EA grave sintomática presenta una supervivencia inferior a 3 años si no es intervenida3. El implante percutáneo de válvula aórtica (TAVI) está indicado en pacientes sintomáticos y en asintomáticos con fracción de eyección del ventrículo izquierdo (FEVI) reducida (< 50%)4.
La FEVI reducida se reconoce como un factor de riesgo independiente de eventos y mortalidad en los pacientes con EA grave5. Sin embargo, existen muchos interrogantes sobre el pronóstico de la EA grave en los pacientes con FEVI conservada (> 50%), ya que se ha demostrado la presencia de marcadores de daño miocárdico subclínico, como hipertrofia y fibrosis6. Dentro de ellos, el subgrupo de los pacientes con FEVI supranormal (≥ 70%) puede tener peor pronóstico después del TAVI, debido a sus características particulares de geometría y funcionalidad ventricular7.
El objetivo de este estudio fue evaluar el pronóstico de los pacientes con FEVI supranormal (≥ 70%) tratados con TAVI, así como estudiar sus características ecocardiográficas y clínicas.
MÉTODOS
Estudio de cohorte retrospectivo que incluyó pacientes con EA grave tratados con TAVI en el Hospital Clínico San Carlos (Madrid, España) entre junio de 2007 y diciembre de 2021. La EA grave se definió según los criterios de las guías vigentes (gradiente medio > 40 mmHg, velocidad pico > 4 m/s, área valvular aórtica < 1 cm2 o área valvular aórtica indexada < 0,6 cm2/m2). La decisión de intervención fue consensuada y definida por el equipo médico-quirúrgico. Los pacientes se clasificaron en 3 grupos según la FEVI preprocedimiento evaluada por ecocardiograma: reducida (< 50%), normal (50-69%) y supranormal (≥ 70%). Los datos clínicos se recogieron de la historia clínica de los pacientes. Se excluyeron los que fallecieron durante procedimiento y aquellos con cirugías cardiacas valvulares previas, con presencia de miocardiopatía no relacionada con la enfermedad valvular, con expectativa de vida menor de 1 año o con falta de datos en el estudio ecocardiográfico preprocedimiento o en el seguimiento clínico.
El objetivo del estudio fue determinar la mortalidad por cualquier causa a los 30 días y al año, la mortalidad por causa cardiovascular al año y la rehospitalización por causa cardiovascular al año, así como su correlación con las características ecocardiográficas y clínicas.
El estudio cumplió la Declaración de Helsinki de la Asociación Médica Mundial y contó con la aprobación del comité de ética del Hospital Clínico San Carlos (Madrid, España). El estudio no supuso ningún tipo de riesgo para los pacientes. No se requirió consentimiento informado por tratarse de datos retrospectivos y toda la información obtenida se manejó con la más estricta confidencialidad por parte de los investigadores.
Ecocardiografía
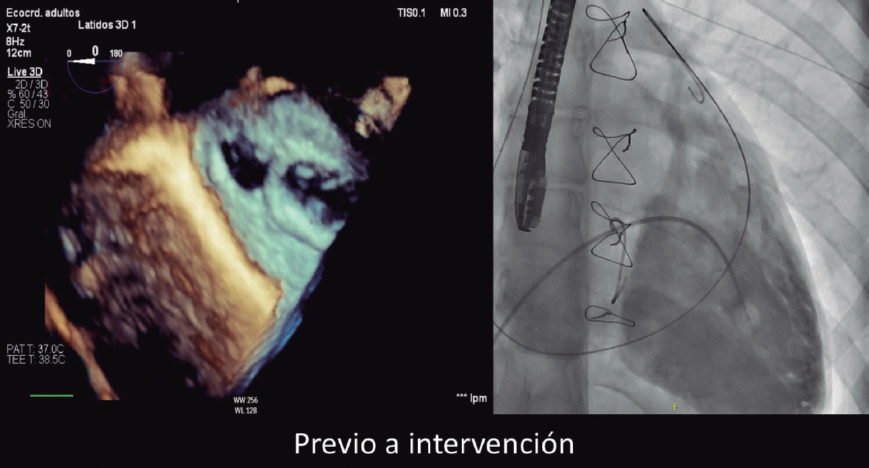
La evaluación con ecocardiograma bidimensional y Doppler se llevó a cabo con los equipos disponibles y acorde con las recomendaciones de las guías de práctica clínica8. El grosor del septo, la pared posterior, el diámetro de fin de diástole y el tracto de salida del ventrículo izquierdo (TSVI) se midieron en proyección paraesternal en el eje largo. Los gradientes pico y medio valvulares se midieron usando el Doppler continuo en diferentes ventanas hasta obtener la velocidad más alta. La integral tiempo-velocidad (ITV) se midió con Doppler pulsado, localizando el volumen de muestra justo antes del anillo valvular aórtico. El área valvular aórtica se calculó por medio de la ecuación de continuidad:
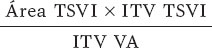
Los volúmenes ventriculares y la FEVI se calcularon por el método de Simpson biplano. La masa del ventrículo izquierdo (VI) se calculó con la fórmula de Devereux e indexada por superficie corporal (SC). El grosor parietal relativo (GPR) se calculó por la siguiente fórmula:
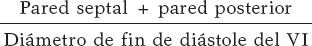
El volumen sistólico indexado se obtuvo mediante la siguiente fórmula:
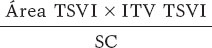
Análisis estadístico
El análisis estadístico se llevó a cabo con el software comercial disponible (IBM SPSS 28.0). Las variables continuas con distribución normal se expresaron como media y desviación estándar, con un intervalo de confianza del 95% (IC95%). Las variables categóricas se expresaron como números absolutos y su respectivo porcentaje. Para comparar variables normales se usó la prueba t de Student. El análisis de varianza y la prueba de Tukey post hoc se usaron para comparar las medias, y la prueba χ2 se usó para comparar las prevalencias entre los 3 grupos. Se aplicó un análisis de regresión logística univariable para evaluar los parámetros predictores de hospitalización y mortalidad. Se definió la significación estadística como un valor de p < 0,05.
RESULTADOS
De los 1.228 pacientes que recibieron un TAVI durante el periodo de estudio se incluyeron 1.160, de los cuales 276 (23,8%) tenían FEVI reducida (< 50%), 702 (60,5%) FEVI normal (50-69%) y 182 (15,7%) FEVI supranormal (≥ 70%). Se excluyeron 68 pacientes por cumplir criterios de exclusión: 23 por fallecimiento en el procedimiento, 15 por cirugías cardiacas valvulares previas, 6 por presencia de miocardiopatía no relacionada con la enfermedad valvular, 18 por expectativa de vida menor de 1 año y 6 por falta de datos en el estudio ecocardiográfico preprocedimiento o en el seguimiento clínico (figura 1).
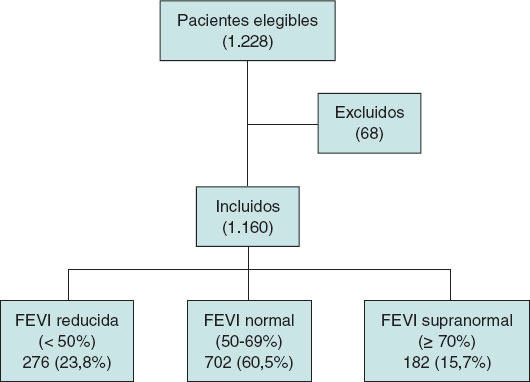
Figura 1. Flow chart indicando los pacientes incluidos y excluidos en el estudio, así como la muestra final analizada y su distribución en los 3 grupos de estudio. FEVI: fracción de eyección del ventrículo izquierdo.
Las características basales de la población se detallan en la tabla 1. El promedio de edad fue de 82,2 ± 5,8 años, siendo ligeramente me- nor en el grupo de pacientes con FEVI reducida que en los otros 2 grupos. El sexo masculino fue más frecuente en el grupo de FEVI ≥ 70% (p < 0,005). El grupo con FEVI < 50% presentó con más frecuencia infarto previo, enfermedad coronaria y revascularización, con una mayor puntuación en el EuroSCORE II (22,5 [14,7-32,0]; p < 0,001); además, estos pacientes requirieron en mayor proporción la intervención como procedimiento de urgencia (p < 0,001).
Tabla 1. Características basales de los pacientes
| Características | FEVI < 50% (n = 276) | FEVI 50-69% (n = 702) | ≥ 70% (n = 182) | p |
|---|---|---|---|---|
| Edad | 81,6 ± 6,3 | 82,2 ± 5,9 | 82,9 ± 5,3 | < 0,050 |
| Sexo, varón | 38,1% | 58,2% | 68,3% | < 0,001 |
| Hipertensión arterial | 80,7% | 82,9% | 86,0% | 0,363 |
| Diabetes mellitus | 41,7% | 35,6% | 33,9% | 0,182 |
| Índice de masa corporal | 27,1 ± 4,4 | 28,4 ± 5,2 | 27,7 ± 5,1 | < 0,002 |
| Hiperlipidemia | 56,9% | 59,8% | 56,0% | 0,254 |
| ACTP previa | 30,6% | 19,4% | 16,8% | < 0,001 |
| CABG previa | 9,6% | 4,5% | 3,3% | < 0,002 |
| Infarto previo | 20,6% | 9,1% | 7,6% | < 0,001 |
| Enfermedad coronaria | 45,6% | 32,7% | 34,7% | < 0,002 |
| Enfermedad de tronco coronario izquierdo | 5,6% | 3,4% | 1,8% | 0,222 |
| Revascularización incompleta | 20,7% | 30,4% | 35,3% | 0,174 |
| EPOC | 16,7% | 15,1% | 14,5% | 0,714 |
| Tabaquismo | 37,2% | 41,7% | 14,4% | 0,034 |
| Fibrilación auricular | 38,6% | 37,8% | 42,1% | 0,570 |
| Filtrado glomerular | 61,2 (46,0-77,9) | 63,1 (46,8-79,4) | 60,9 (45,5-75,2) | 0,311 |
| Cáncer | 16,0% | 15,5% | 18,7% | 0,725 |
| EuroSCORE II | 22,5 (14,7-32,0) | 14,3 (7,4-18,0) | 11,8 (8,9-18,9) | < 0,001 |
| Disnea | 87,5% | 87,5% | 91,7% | 0,289 |
| Procedimiento de urgencia | 33,9% | 17,5% | 14,1% | < 0,001 |
| Valve-in-valve | 3,6% | 3,3% | 2,7% | 0,881 |
| Resultado (post-TAVI) | ||||
| Gradiente pico, mmHg | 18,3 ± 7,3 | 19,3 ± 8,9 | 19,4 ± 8,7 | 0,223 |
| Gradiente medio, mmHg | 9,3 ± 3,8 | 9,9 ± 4,8 | 10,0 ± 5,7 | 0,229 |
ACTP: angioplastia coronaria transluminal percutánea; CABG: cirugía de revascularización coronaria; EPOC: enfermedad pulmonar obstructiva crónica; FEVI: fracción de eyección del ventrículo izquierdo; TAVI: implante percutáneo de válvula aórtica. | ||||
Datos ecocardiográficos
Los pacientes con FEVI ≥ 70% presentaron volúmenes del VI de fin de diástole y de fin de sístole menores, y grosor de la pared septal y GPR mayores que los otros 2 grupos. El índice de masa del ventrículo izquierdo (IMVI) en este grupo fue de 126,3 ± 32,8 g/m2, lo que constituye un fenotipo predominante de hipertrofia y remodelación concéntrica. Algo similar ocurrió en el grupo de FEVI normal (50-60%), pero en este con un volumen de fin de diástole del VI mayor (tabla 2). Los pacientes con FEVI < 50% presentaron mayor masa, con un IMVI de 147,6 ± 40,2 g/m2 (p < 0,001), un GPR bajo (< 0,42) y un volumen de fin de diástole elevado, mostrando un fenotipo predominante de hipertrofia excéntrica. Además, en este grupo el volumen sistólico indexado era menor (32,5 ± 11,8; p < 0,001).
Tabla 2. Características basales de los pacientes
| Características | FEVI < 50 % | FEVI 50-69% | ≥ 70% | p |
|---|---|---|---|---|
| GPR | 0,48 (0,41-0,58) | 0,57 (0,50-0,65) | 0,60 (0,52-0,69) | < 0,001 |
| VFSVI indexado, ml/m2 | 31 (25-39) | 38 (31-45) | 39 (31-49) | < 0,001 |
| VFDVI indexado, ml/m2 | 63 (48-80) | 48 (38-59) | 45 (35-56) | < 0,001 |
| IMVI, g/m2 | 147,6 ± 40,2 | 128,8 ± 34,2 | 126,3 ± 32,8 | < 0,001 |
| SIV, mm | 12,1 ± 2,6 | 13,6 ± 2,4 | 14,1 ± 2,7 | < 0,001 |
| Volumen sistólico indexado, ml/m2 | 32,5 ± 11,8 | 38 ± 11,5 | 40 ± 11,6 | < 0,001 |
FEVI: fracción de eyección del ventrículo izquierdo; GPR: grosor parietal relativo; IMVI: índice de masa ventricular izquierda; SIV: septo interventricular; VFDVI: volumen de fin de diástole del ventrículo izquierdo; VFSVI: volumen de fin de sístole del ventrículo izquierdo. | ||||
Resultados clínicos periprocedimiento
No se encontraron diferencias significativas entre los 3 grupos en cuanto a mortalidad intra- y posprocedimiento.
Resultados clínicos en el seguimiento
Durante el seguimiento de 1 año la mortalidad fue de 164 pacientes (14,13%) y no hubo diferencias significativas entre los 3 grupos (FEVI < 50%, 14,6%; FEVI 50-69%, 12,6%; FEVI ≥ 70%, 12,7%; p < 0,736). Sin embargo, sí se encontraron diferencias significativas en la rehospitalización por causa cardiovascular al año, siendo mayor en el grupo de FEVI supranormal (FEVI ≥ 70%, 34,4%; FEVI < 50%, 29,2%; FEVI 50-69%, 27,4%; p < 0,043). Los resultados clínicos se recogen en la tabla 3.
Tabla 3. Resultados clínicos
| Variables | FEVI < 50 % (n = 276) | FEVI 50-69% (n = 702) | ≥ 70% (n = 182) | p |
|---|---|---|---|---|
| Periprocedimiento | ||||
| Muerte intraprocedimiento | 0,4% | 1,4% | 0,6% | 0,345 |
| Muerte posprocedimiento | 2,8% | 3,7% | 4,3% | 0,676 |
| Seguimiento | ||||
| Muerte por cualquier causa a 30 días | 2,4% | 3,9% | 5,0% | 0,359 |
| Muerte por causa cardiovascular al año | 12,8% | 9,6% | 15,2% | 0,370 |
| Muerte por cualquier causa al año | 14,6% | 12,6% | 12,7% | 0,736 |
| Rehospitalización por causa cardiovascular al año | 29,2% | 27,4% | 34,4% | < 0,043 |
FEVI: fracción de eyección del ventrículo izquierdo. | ||||
Análisis de regresión univariable
En los pacientes con FEVI supranormal, la presencia de enfermedad coronaria y un grosor del septo interventricular aumentado fueron predictores de hospitalización por causa cardiovascular en el primer año (tabla 4). En este grupo, el volumen de fin de diástole del VI indexado y el antecedente de enfermedad coronaria fueron predictores de mortalidad por cualquier causa al año (tabla 5). En la población general, con excepción de la edad, no hubo predictores de mortalidad a 1 año (tabla 6).
Tabla 4. Fracción de eyección del ventrículo izquierdo supranormal y predictores de hospitalización por causa cardiovascular al año
| Características | HR | IC95% | p | HR |
|---|---|---|---|---|
| Edad | 1,077 | 0,991-1,169 | 0,080 | 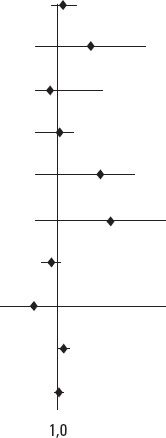 |
| Hipertensión arterial | 1,687 | 0,546-5,213 | 0,364 | |
| Diabetes mellitus | 1,846 | 0,767-4,440 | 0,171 | |
| Índice de masa corporal | 1,012 | 0,933-1,099 | 0,770 | |
| Enfermedad coronaria | 0,327 | 0,137-0,780 | 0,012 | |
| Tabaquismo | 1,796 | 0,650-4,965 | 0,259 | |
| EuroSCORE II | 1,046 | 0,998-1,096 | 0,060 | |
| GPR | 1,004 | 0,041-24,392 | 0,998 | |
| VFDVI indexado | 0,979 | 0,949-1,010 | 0,188 | |
| SIV | 0,965 | 0,933-0,998 | 0,036 | |
GPR: grosor parietal relativo; HR: hazard ratio; IC95%: intervalo de confianza del 95%; SIV: septo interventricular; VFDVI: volumen de fin de diástole del ventrículo izquierdo. | ||||
Tabla 5. Fracción de eyección del ventrículo izquierdo supranormal y predictores de mortalidad al año
| Características | HR | IC95% | p | HR |
|---|---|---|---|---|
| Edad | 1,180 | 0,976-1,426 | 0,087 | 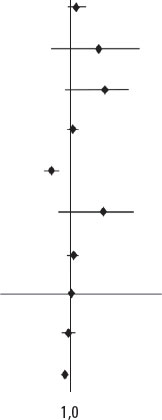 |
| Hipertensión arterial | 2,181 | 0,167-28,575 | 0,552 | |
| Diabetes mellitus | 0,875 | 0,154-4,968 | 0,154 | |
| Índice de masa corporal | 1,004 | 0,796-1,265 | 0,976 | |
| Enfermedad coronaria | 3,372 | 0,612-18,575 | 0,012 | |
| Tabaquismo | 7,453 | 0,691-61,024 | 0,259 | |
| EuroSCORE II | 0,921 | 0,831-1,022 | 0,12 | |
| GPR | 0,011 | 0,00-154,979 | 0,998 | |
| VFDVI indexado | 1,094 | 1,018-1,177 | 0,015 | |
| SIV | 1,004 | 0,943-1,068 | 0,912 | |
GPR: grosor parietal relativo; HR: hazard ratio; IC95%: intervalo de confianza del 95%; SIV: septo interventricular; VFDVI: volumen de fin de diástole del ventrículo izquierdo. | ||||
Tabla 6. Predictores de mortalidad a 1 año en población general
| Características | HR | IC95% | p | HR |
|---|---|---|---|---|
| Edad | 1,070 | 1,002-1,143 | 0,043 | 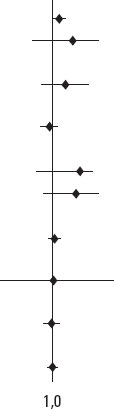 |
| Hipertensión arterial | 1,268 | 0,545-2,947 | 0,582 | |
| Diabetes mellitus | 1,458 | 0,764-2,784 | 0,253 | |
| Índice de masa corporal | 0,949 | 0,882-1,020 | 0,152 | |
| Enfermedad coronaria | 1,593 | 0,867-2,929 | 0,134 | |
| Tabaquismo | 1,794 | 0,899-3,581 | 0,097 | |
| EuroSCORE II | 1,046 | 0,973-1,033 | 0,868 | |
| GPR | 0,252 | 0,022-2,836 | 0,264 | |
| VFDVI indexado | 0,986 | 0,967-1,006 | 0,188 | |
| SIV | 1,000 | 0,974-1,027 | 0,036 | |
GPR: grosor parietal relativo; HR: hazard ratio; IC95%: intervalo de confianza del 95%; SIV: septo interventricular; VFDVI: volumen de fin de diástole del ventrículo izquierdo. | ||||
DISCUSIÓN
El estudio muestra que la FEVI es un importante factor pronóstico en los pacientes con EA grave tratados con TAVI. Si bien no se encontraron diferencias en la mortalidad a 1 mes y a 1 año, se demostró que los pacientes con FEVI supranormal (≥ 70%) presentan una mayor tasa de rehospitalización al año que aquellos con FEVI reducida (< 50%) o normal (50-69%).
La FEVI ha sido ampliamente reconocida en la literatura como un factor pronóstico en cualquier contexto clínico. En el estudio de Wehner et al.9 se encontró que una FEVI del 60-65% tiene el mejor pronóstico, y que los pacientes con FEVI ≥ 70% presentan una tasa de mortalidad a 5 años similar a la de los pacientes con FEVI reducida. En el estudio de Gu et al.10 también se hallaron mayores tasas de mortalidad y de hospitalización a 5 años en los pacientes hospitalizados por insuficiencia cardiaca y con FEVI > 65% en comparación con los pacientes con FEVI normal.
En cuanto a los pacientes con EA tratados con TAVI, el registro OCEAN-TAVI mostró que la FEVI > 65% era un predictor independiente de muerte y de rehospitalización en el seguimiento a 3 años (hazard ratio [HR] = 1,16; IC95%, 1,02-1,31; p = 0,023)11. No se encontraron diferencias significativas en cuanto a mortalidad entre los grupos de estudio, salvo en la tasa de rehospitalización. Queda por determinar si un seguimiento a más largo plazo detectaría también diferencias en la mortalidad.
En los pacientes con EA intervenidos quirúrgicamente, la FEVI es un reconocido marcador pronóstico. En el estudio realizado por Dahl et al.12 se halló que la FEVI reducida (< 50%) es un claro predictor de riesgo a 5 años. Se detectó que los pacientes con FEVI supranormal presentaron mayores tiempos de hospitalización, ventilación mecánica e incidencia de hemodiálisis, así como también una mayor tasa de rehospitalización. Este último hallazgo es similar a lo observado en nuestro estudio. Al no existir una explicación exacta para estos resultados, se sugiere que pueden tener relación con que la hipertrofia miocárdica o la disfunción diastólica no regresen después de la intervención13.
Según estudios previos, los volúmenes ventriculares tanto aumentados (> 80 ml/m2) como reducidos (< 55 ml/m2) son otra condición de riesgo que hay que tener en cuenta en los pacientes con EA grave14,15. En este análisis, en el subgrupo de pacientes con FEVI supranormal, el volumen de fin de diástole del VI fue predictor de la mortalidad al año (HR = 1,094; IC95%, 1,018-1,177; p < 0,015). Un volumen sistólico indexado bajo también se ha asociado con peor pronóstico en los pacientes con EA, tanto con FEVI reducida como con FEVI conservada16. Los pacientes con FEVI conservada pueden presentar un volumen sistólico bajo cuando la cavidad ventricular es pequeña y presentan fisiología restrictiva limitando el volumen sistólico, incluso con una fracción de eyección supranormal17. En la mayoría de los estudios, estos pacientes han mostrado tener un peor pronóstico, con mayor riesgo de mortalidad y menos tiempo libre de eventos18,19.
La FEVI supranormal se presenta como un nuevo fenotipo dentro de los pacientes con FEVI conservada (> 50%), con características clínicas y hemodinámicas distintivas. No hay un consenso definitivo sobre qué valor de FEVI es considerado supranormal; según el American College of Cardiology, es supranormal una FEVI ≥ 70%20, y otros grupos la definen como una FEVI ≥ 65%. Para el objetivo de este estudio se tomó como referencia una FEVI ≥ 70% con la finalidad de destacar más las diferencias clínicas y ecocardiográficas entre los grupos de estudio, lo que probablemente condicionó la prevalencia encontrada en la población estudiada.
En el estudio de Wehner et al.9 se revisaron 403.977 ecocardiogramas de 203.135 pacientes sin diagnóstico preespecificado, y se encontró una FEVI ≥ 70% en el 3% (13.553) de ellos. En el presente estudio en pacientes con EA grave, el 15% presentaron FEVI ≥ 70%. En otros estudios, como el registro OCEAN-TAVI11 antes mencionado, los pacientes con FEVI supranormal y EA supusieron un porcentaje más alto (47%), debido probablemente a que el punto de corte de la FEVI supranormal fue menor (≥ 65%). Estos datos reflejan que la EA grave se asocia a una FEVI mayor de lo normal, debido probablemente a la remodelación y la hipertrofia concéntrica del VI por el efecto de la elevada poscarga21-24. En este estudio, el IMVI fue elevado en la mayoría de los pacientes sin importar la FEVI, destacando que los pacientes con FEVI normal y supranormal presentaron predominantemente una geometría concéntrica con una cavidad ventricular izquierda reducida y mayor grosor septal. En los pacientes con FEVI reducida, en cambio, la geometría fue predominantemente excéntrica con el VI dilatado.
Por último, nuestros resultados señalan que, aunque las escalas de riesgo muy usadas (como el EuroSCORE II) siguen siendo válidas, podrían tenerse en cuenta factores ecocardiográficos al elegir el momento adecuado y el tipo de intervención25.
Limitaciones
Se trata de un estudio retrospectivo, observacional y realizado en un solo centro. Todos los pacientes habían recibido un TAVI y no se compararon con otros tratados con recambio valvular quirúrgico. No se especificó el tratamiento médico-farmacológico empleado; detalle importante, teniendo en cuenta los avances que ha habido en los últimos tiempos en el tratamiento de la insuficiencia cardiaca. El seguimiento a 1 año puede ser demasiado corto para obtener diferencias en cuanto a mortalidad entre los grupos; un seguimiento a largo plazo podría mostrar diferencias.
CONCLUSIONES
La FEVI es aún un importante factor pronóstico para la toma de decisiones en los pacientes con EA grave. En este estudio, los pacientes con FEVI preprocedimiento reducida (< 50%), normal (50-69%) o supranormal (≥ 70%) que recibieron un TAVI no presentaron diferencias en cuanto a mortalidad a 1 año de seguimiento. Sin embargo, aquellos con FEVI supranormal (≥ 70%) tuvieron una mayor tasa de rehospitalización por causa cardiovascular al año, lo que sugiere que este subgrupo presenta factores desfavorables, como la presencia de disfunción diastólica significativa. Son necesarios más estudios que investiguen y confirmen estos hallazgos.
FINANCIACIÓN
No hubo financiación externa.
CONSIDERACIONES ÉTICAS
El presente estudio se adhirió a la Declaración de Helsinki de la Asociación Médica Mundial y contó con la aprobación del comité de ética del Hospital Clínico San Carlos (Madrid, España). El estudio no supuso ningún tipo de riesgo para los pacientes. No se requirió consentimiento informado por tratarse de datos retrospectivos y toda la información obtenida se manejó con la más estricta confidencialidad por parte de los investigadores. Se reclutaron pacientes consecutivos durante los años definidos para el estudio, sin realizar muestreo ni aleatorización, por lo que no se han tenido en cuenta sesgos de sexo o género en el análisis.
DECLARACIÓN SOBRE EL USO DE INTELIGENCIA ARTIFICIAL
No se usaron herramientas de inteligencia artificial durante el desarrollo del estudio.
CONTRIBUCIÓN DE LOS AUTORES
E. Martínez Gómez, X. Solar, D. Faria, L. Nombela Franco y J.A. de Agustín contribuyeron en la concepción y el diseño, la adquisición de datos, su análisis e interpretación. E. Martínez Gómez, X. Solar, D. Faria, L. Nombela Franco, P. Jiménez Quevedo, G. Tirado, E. Pozo Osinalde, C. Olmos Blanco, P. Mahía Casado, P. Marcos Alberca, M. Luaces, J.J. Gómez de Diego, L. Collado Yurrita, A. Fernández-Ortiz, J. Pérez-Villacastín y J.A. de Agustín contribuyeron en la redacción del artículo o en su revisión crítica. Todos los autores han dado su aprobación a la versión final del artículo.
CONFLICTO DE INTERESES
No hay conflicto de intereses.
¿QUÉ SE SABE DEL TEMA?
- La FEVI es un parámetro pronóstico con gran importancia en cardiología. Paradójicamente, los estudios han mostrado que los pacientes con FEVI supranormal presentan un peor pronóstico en algunos escenarios, como la EA.
¿QUÉ APORTA DE NUEVO?
- El estudio muestra que los pacientes tratados con TAVI que presentan una FEVI supranormal (≥ 70%) tienen una mayor tasa de rehospitalización al año que aquellos con FEVI reducida (< 50%) o normal (50-69%).
BIBLIOGRAFÍA
1. Osnabrugge RL, Mylotte D, Head SJ, et al. Aortic stenosis in the elderly:disease prevalence and number of candidates for transcatheter aortic valve replacement:a meta-analysis and modeling study. J Am Coll Cardiol. 2013;62:1002-1012.
2. D'Arcy JL, Coffey S, Loudon MA, et al. Large-scale community echocardiographic screening reveals a major burden of undiagnosed valvular heart disease in older people:the OxVALVE Population Cohort Study. Eur Heart J. 2016;37:3515-3522.
3. Ross J, Braunwald E. Aortic stenosis. Circulation. 1968;38(1 Suppl):61-67.
4. Vahanian A, Beyersdorf F, Praz F, et al. ESC/EACTS Scientific Document Group. 2021 ESC/EACTS Guidelines for the management of valvular heart disease. Eur Heart J. 2022;43:561-632.
5. Dahl JS, Eleid MF, Michelena HI, et al. Effect of left ventricular ejection fraction on postoperative outcome in patients with severe aortic stenosis undergoing aortic valve replacement. Circ Cardiovasc Imaging. 2015;8:002917.
6. Bing R, Cavalcante JL, Everett RJ, et al. Imaging and Impact of Myocardial Fibrosis in Aortic Stenosis. JACC Cardiovasc Imaging. 2019;12:283-296.
7. Shah S, Segar MW, Kondamudi N, et al. Supranormal Left Ventricular Ejection Fraction, Stroke Volume, and Cardiovascular Risk:Findings From Population-Based Cohort Studies. JACC Heart Fail. 2022;10:583-594.
8. Lang RM, Badano LP, Mor-Avi V, et al. Recommendations for cardiac chamber quantification by echocardiography in adults:an update from the American Society of Echocardiography and the European Association of Cardiovascular Imaging. J Am Soc Echocardiogr. 2015;28:1-39.14.
9. Wehner GJ, Jing L, Haggerty CM, et al. Routinely reported ejection fraction and mortality in clinical practice:where does the nadir of risk lie?Eur Heart J. 2020;41:1249-1257.
10. Gu J, Ke JH, Wang Y, Wang CQ, Zhang JF. Characteristics, prognosis, and treatment response in HFpEF patients with high vs. ejection fraction. Front Cardiovasc Med. 2022;9:944441.
11. Imamura T, Hida Y, Ueno H, et al. Clinical Implication of Supra-Normal Left Ventricular Ejection Fraction in Patients Undergoing Transcatheter Aortic Valve replacement. J Clin Med. 2023;12:7429.
12. Dahl JS, Eleid MF, Michelena HI, et al. Effect of left ventricular ejection fraction on postoperative outcome in patients with severe aortic stenosis undergoing aortic valve replacement. Circ Cardiovasc Imaging. 2015;8:002917.
13. Mariage JL, Bulpa P, Michaux I, et al. Impact of myocardial hypertrophy and preoperative left ventricular ejection fraction on post operative complications after aortic valve replacement for aortic stenosis. Chest. 2005;128:268S.
14. Cohn JN, Ferrari R, Sharpe N. Cardiac remodeling concepts and clinical implications:a consensus paper from an international forum on cardiac remodeling. Behalf of an International Forum on Cardiac Remodeling. J Am Coll Cardiol. 2000;35:569-582.
15. Hein S, Arnon E, Kostin S, et al. Progression from compensated hypertrophy to failure in the pressure overloaded human heart:structural deterioration and compensatory mechanisms. Circulation. 2003;107:984-991.
16. Kwak S, Everett RJ, Treibel TA, et al. Markers of Myocardial Damage Predict Mortality in Patients With Aortic Stenosis. J Am Coll Cardiol. 2021;78:545-558.
17. Severino P, Maestrini V, Mariani MV, et al. Structural and myocardial dysfunction in heart failure beyond ejection fraction. Heart Fail Rev. 2020;25:9-17.
18. Ito S, Nkomo VT, Orsinelli DA, et al. Impact of Stroke Volume Index and Left Ventricular Ejection Fraction on Mortality After Aortic Valve Replacement. Mayo Clin Proc. 2020;95:69-76.
19. Dumesnil JG, Pibarot P, Carabello B. Paradoxical low flow and/or low gradient severe aortic stenosis despite preserved left ventricular ejection fraction:implications for diagnosis and treatment. Eur Heart J. 2010;31:281-289.
20. Lang RM, Badano LP, Mor-Avi V, et al. Recommendations for cardiac chamber quantification by echocardiography in adults:an update from the American Society of Echocardiography and the European Association of Cardiovascular Imaging. J Am Soc Echocardiogr. 2015;28:1-39.14.
21. Forrest L, Rocheleau G, Bafna S, et al. Genetic and phenotypic profiling of supranormal ejection fraction reveals decreased survival and underdiagnosed heart failure. Eur J Heart Fail. 2022;24:2118-2127.
22. Dumesnil JG, Shoucri RM. Effect of the geometry of the left ventricle on the calculation of ejection fraction. Circulation. 1982;65:91-98.
23. González Gómez A, Fernández Golfín C, Monteagudo JM, et al. Severe aortic stenosis patients with preserved ejection fraction according to flow and gradient classification:Prevalence and outcomes. Int J Cardiol. 2017;248:211-215.
24. Hachicha Z, Dumesnil JG, Bogaty P, et al. Paradoxical low-flow, low-gradient severe aortic stenosis despite preserved ejection fraction is associated with higher afterload and reduced survival. Circulation. 2007;115:2856-2864.
25. Strachinaru M, Van Mieghem NM. Low-gradient severe aortic stenosis with preserved ejection fraction:how fast should we act?Int J Cardiovasc Imaging. 2021;37:3177-3180.
* Autor para correspondencia.
Correo electrónico: eimartin1980@gmail.com (E. Martínez Gómez).