RESUMEN
Introducción y objetivos: La seguridad de la revascularización fisiológica en pacientes diabéticos ha sido poco investigada. El objetivo fue determinar la seguridad de diferir la revascularización basándose en la reserva fraccional de flujo (FFR) o en el índice instantáneo libre de ondas (iFR) en pacientes con diabetes mellitus.
Métodos: Análisis retrospectivo, unicéntrico, de pacientes con estenosis coronarias intermedias en quienes se había diferido la revascularización en función de unos valores de FFR > 0,80 o de iFR > 0,89. Se analizó la incidencia a largo plazo de eventos cardiovasculares adversos mayores, una combinación de muerte por cualquier causa, infarto miocárdico y revascularización del vaso diana (RVD) en pacientes con y sin diabetes. También se evaluó la incidencia de RVD según el tipo de índice fisiológico utilizado para diferir la revascularización.
Resultados: Se evaluaron 164 pacientes diabéticos (214 vasos) y 280 pacientes no diabéticos (379 vasos), con una mediana de seguimiento de 43 meses. No se observaron diferencias significativas en los eventos cardiovasculares adversos mayores entre pacientes con y sin diabetes mellitus (20,1 frente a 13,2%; p = 0,245). La mortalidad por cualquier causa y de causa cardiaca no fue estadísticamente diferente entre ambos grupos en el análisis ajustado (p > 0,05). Se observó una tendencia a una mayor incidencia de infarto de miocardio en los pacientes con diabetes mellitus (6,7 frente a 2,9%; p = 0,063), pero el infarto relacionado con el vaso diana fue similar en ambos grupos (p = 0,906). En general, la RVD fue similar en diabéticos y no diabéticos (4,7 frente a 4,2%; p = 0,787); sin embargo, cuando se analizó según el índice fisiológico, los diabéticos tuvieron una mayor tasa numérica de RVD cuando se utilizó la FFR en la toma de decisiones en comparación con el iFR (6,4 frente a 0,0%; p = 0,064).
Conclusiones: Diferir la revascularización de estenosis intermedias en pacientes con diabetes mellitus según la FFR o el iFR es seguro en términos de RVD e infarto relacionado con el vaso diana, con una tasa de eventos en el seguimiento a largo plazo similar a la observada en pacientes sin diabetes mellitus.
Palabras clave: Reserva fraccional de flujo. Índice instantáneo libre de ondas. iFR. Diabetes mellitus.
ABSTRACT
Introduction and objectives: The safety of physiology-based revascularization in patients with diabetes mellitus has been scarcely investigated. Our objective was to determine the safety of deferring revascularization based on the fractional flow reserve (FFR) or the instantaneous wave-free ratio (iFR) in diabetic patients.
Methods: Single-center, retrospective analysis of patients with intermediate coronary stenoses in whom revascularization was deferred based on FFR > 0.80 or iFR > 0.89 values. The long-term rate of major adverse cardiovascular events, a composite of all-cause mortality, myocardial infarction, and target vessel revascularization (TVR), was assessed in diabetic and non-diabetic patients at the follow-up. The rate of TVR based on the type of physiological index used to defer the lesion was also evaluated.
Results: We evaluated 164 diabetic (214 vessels) and 280 non-diabetic patients (379 vessels). No significant differences in the rate of major adverse cardiovascular events was seen between diabetic and non-diabetic patients (20.1% vs 13.2%; P = .245) at a median follow-up of 43 months. All-cause mortality and cardiac death were not statistically different between both groups in the adjusted analysis (P > .05). A trend towards a higher rate of myocardial infarction was seen in diabetic patients (6.7% vs 2.9%; P = .063). However, the rate of target vessel myocardial infarction was similar in both groups (P = .874). Overall, TVR was similar in diabetics and non-diabetics (4.7% vs 4.2%; P = .814); however, when analyzed based on the physiological index, numerically, diabetics had a higher rate of TVR when the FFR was used in the decision-making process compared to when the iFR was used (6.4% vs 0.0%; P = .064).
Conclusions: Deferring the revascularization of intermediate stenoses in patients with DM based on the FFR or the iFR is safe regarding the risk of TVR or target vessel myocardial infarction, with a rate of events at the long-term follow-up similar to that seen in non-diabetic patients.
Keywords: Fractional flow reserve. Instantaneous wave-free ratio. iFR. Diabetes mellitus.
Abreviaturas DM: diabetes mellitus. FFR: reserva fraccional de flujo. iFR: índice instantáneo libre de ondas. MACE: eventos cardiovasculares adversos mayores. RVD: revascularización del vaso diana.
INTRODUCCIÓN
La valoración fisiológica para guiar la revascularización coronaria tiene una recomendación clase IA en las guías actuales de práctica clínica1. Tanto la reserva fraccional de flujo (FFR) como el índice instantáneo libre de ondas (iFR) han demostrado ser herramientas seguras para guiar el tratamiento de revascularización en diferentes escenarios clínicos2-4.
Los resultados del estudio DEFER tras 15 años de seguimiento confirmaron la seguridad a largo plazo de la FFR para diferir el tratamiento de estenosis no significativas a nivel funcional5. Después, los estudios DEFINE-FLAIR y iFR-SWEDEHEART demostraron, tras 1 año de seguimiento, la no inferioridad del iFR frente a la FFR para guiar la revascularización de estenosis moderadas3,6. La utilidad del estudio fisiológico para guiar la revascularización durante el tratamiento de la enfermedad multivaso ha sido confirmada por los estudios FAME y SYNTAX II7,8.
No obstante, el valor pronóstico de la valoración funcional en ciertos grupos de alto riesgo todavía no ha podido establecerse de un modo concluyente. Un análisis conjunto de los estudios DEFINE-FLAIR y iFR-SWEDEHEART demostró que los paciente con síndrome coronario agudo tuvieron una tasa más alta de eventos al diferir la revascularización de los vasos no culpables mediante FFR e iFR en comparación con los pacientes con agina estable3,6. Los pacientes con diabetes mellitus (DM) son un grupo de alto riesgo que tienen una conocida carga de enfermedad cardiovascular más alta y un peor pronóstico, incluida una aterosclerosis coronaria más extensa, una mayor prevalencia de enfermedad multivaso y un avance más rápido de la enfermedad que los pacientes no diabéticos9-11. Las características especiales asociadas al grado y extensión de la aterosclerosis en pacientes con DM plantean dudas de seguridad a la hora de decidir si diferir, o no, la revascularización en esta población de pacientes. Nuestro objetivo fue evaluar la seguridad a largo plazo del diferimiento de la revascularización de las estenosis intermedias en función de la valoración fisiológica con guía de presión en pacientes diabéticos.
MÉTODOS
Población del estudio
Se trata de un estudio retrospectivo, abierto y de un único centro. La población del estudio fue reclutada de un total de 1.321 pacientes consecutivos con enfermedad coronaria cuyos índices iFR o FFR se usaron para determinar la necesidad de revascularización coronaria entre enero de 2012 y diciembre de 2016. Se pospuso la revascularización de una o más estenosis en 444 pacientes (34%) tras observarse valores de FFR > 0,80 o iFR > 0,89. El estudio incluyó a pacientes con angina estable y síndrome coronario agudo (con estenosis no culpables valoradas fisiológicamente mediante guía de presión). La población general fue dividida en 2 grupos para poder realizar los análisis pertinentes: pacientes con y sin DM. El primer grupo se definió según los antecedentes médicos incluidos en la historia clínica. El flujograma del estudio con la selección de pacientes se muestra en la figura 1.
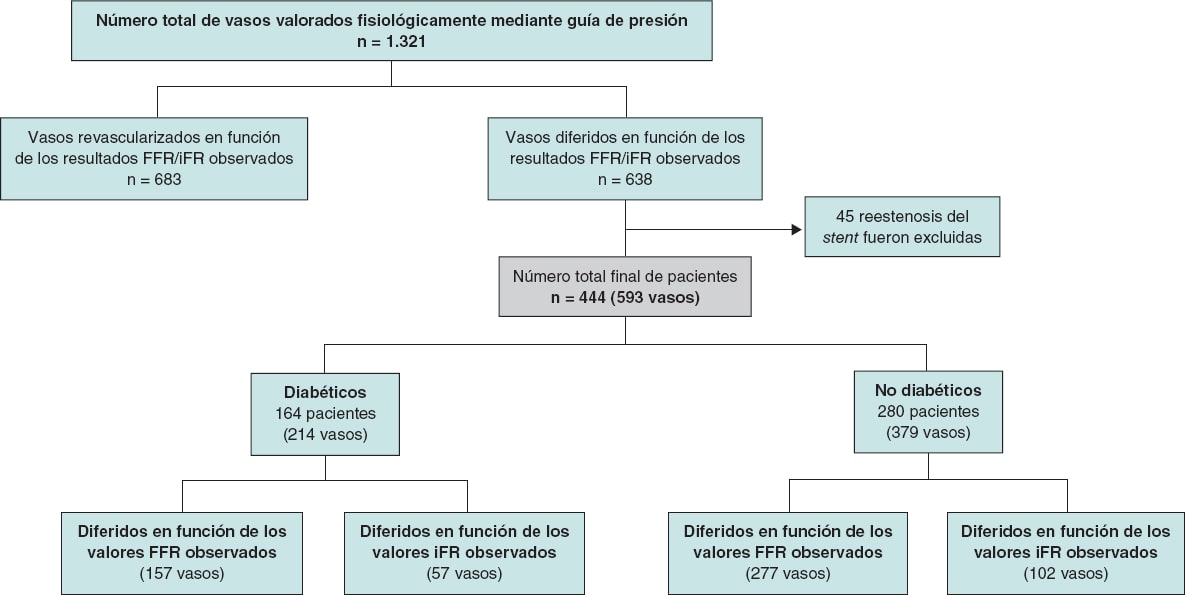
Figura 1. Flujograma del estudio. FFR: reserva fraccional de flujo; iFR: índice instantáneo libre de ondas.
Este estudio retrospectivo de cohorte se llevó a cabo según los principios establecidos por la Declaración de Helsinki. No se solicitó el consentimiento informado de los pacientes ni fue necesaria la valoración del comité de investigación debido a la naturaleza del estudio; todos los pacientes incluidos en la base de datos fueron encriptados y su identidad protegida a fin de salvaguardar la privacidad de todos ellos.
Valoración fisiológica
La valoración fisiológica se realizó con las guías de presión disponibles en el mercado (Verrata, Philips Healthcare, Estados Unidos; PressureWire [Certus. Aeris, X] St. Jude Medical, Estados Unidos) siguiendo la técnica estándar descrita con anterioridad3,12. Como práctica de rutina, se administró un bolo intracoronario de nitratos (200 mcg) antes de observar los valores de FFR o iFR. Los casos remitidos para valoración FFR recibieron adenosina IV a razón de 140 µg/kg/min. Los valores de corte para diferir la revascularización fueron FFR > 0,80 o iFR > 0,89. Para descartar la presencia de drift se colocó el sensor de la guía de presión en la punta del catéter guía tras la obtención de las mediciones fisiológicas.
En pacientes con angina estable, la valoración fisiológica se realizó dentro de la misma intervención valorándose todas las estenosis intermedias. En pacientes con síndrome coronario agudo, la valoración fisiológica con guía de presión se realizó en una intervención por etapas solo en los vasos no culpables.
Definición de eventos adversos
El criterio de valoración principal del estudio fue el riesgo de eventos cardiovascular adversos mayores (MACE) a los 4 años definido como un evento compuesto de mortalidad por cualquier causa, infarto de miocardio o revascularización del vaso diana (RVD) no programada. Los eventos secundarios fueron: a) todos y cada uno de los ECAM, b) la tasa de infarto de miocardio del vaso diana y c) la tasa de RVD no programada según el índice fisiológico empleado (FFR o iFR).
Análisis estadístico
Las variables continuas se expresaron como media ± desviación estándar (DE). Las discretas como frecuencias (porcentajes). Las comparativas entre los 2 grupos se realizaronempleando las pruebas t de Student o U Mann Whittney para las variables continuas y la prueba de la χ2 para las variables discretas.
Para analizar el tiempo transcurrido hasta el evento se emplearon el método de Kaplan-Meier y una comparativa de grupos mediante la prueba de Mantel-Cox (prueba de log-rank). Para la comparativa de los objetivos primario y secundarios entre diabéticos y no diabéticos se usó el modelo de riesgos proporcionales de Cox para así poder calcular el hazard ratio (HR). El análisis ajustado se realizó en función de la edad, sexo, hipertensión, dislipemia, hábito tabáquico, insuficiencia renal crónica y antecedentes de accidente cerebrovascular, intervención coronaria percutánea y cirugía de revascularización coronaria.
Todos los valores de probabilidad fueron bilaterales con intervalos de confianza el 95% (IC95%). Los valores p < 0,05 se consideraron significativos a nivel estadístico. Se emplearon los paquetes estadísticos SPSS versión 23.0 (IBM Corp, Armonk, NY, Estados Unidos) y STATA versión 15 (Stata Corp, College Station, TX, Estados Unidos) para realizar todos los cálculos.
RESULTADOS
Características clínicas y angiográficas basales
Las características clínicas basales se muestran en la tabla 1. La media de edad de la población del estudio fue de 68,4 años. El 39,6% eran pacientes con DM (164 pacientes). Como cabía esperar, los pacientes con DM tenían más factores de riesgo cardiovascular y comorbilidades que sus homólogos sin DM. No se observaron diferencias significativas en los síntomas de presentación entre los 2 grupos a estudio (p > 0,05). La mayoría de los pacientes recibieron tratamiento médico óptimo tras el alta hospitalaria y no se observaron diferencias significativas entre pacientes con y sin DM (p > 0,05).
Tabla 1. Características basales
| Total (N = 444) | Diabéticos (N = 164) | No diabéticos (N = 280) | p | |
|---|---|---|---|---|
| Características clínicas, n (%) | ||||
| Sexo | 0,026 | |||
| Varón | 340 (76,5) | 116 (70,7) | 224 (80,0) | |
| Mujer | 104 (23,4) | 48 (29,3) | 56 (20,0) | |
| Edad (año) | 68,41 | 70,02 | 67,46 | 0,003 |
| Hipertensión arterial | 321 (72,3) | 138 (84,1) | 183 (65,4) | < 0,001 |
| Hiperlipemia | 287 (64,6) | 124 (75,6) | 163 (58,2) | < 0,001 |
| >Hábito tabáquico en la actualidad | 253 (57,0) | 85 (51,8) | 168 (60,0) | 0,093 |
| Insuficiencia renal crónica | 41 (9,2) | 29 (17,7) | 12 (4,3) | 0,000 |
| EPOC | 30 (6,8) | 9 (5,5) | 21 (7,5) | 0,415 |
| Enfermedad cerebrovascular previa | 21 (4,7) | 12 (7,3) | 9 (3,2) | 0,049 |
| Enfermedad vascular periférica | 38 (8,6) | 18 (11,0) | 20 (7,1) | 0,164 |
| IAM previo | 47 (10,6) | 17 (10,4) | 30 (10,7) | 0,908 |
| ICP previa | 220 (49,5) | 70 (42,7) | 150 (53,6) | 0,027 |
| CABG previa | 13 (2,9) | 9 (5,5) | 4 (1,4) | 0,019 |
| Síntomas de presentación, N (%) | ||||
| Infarto de miocardio | 148 (33,3) | 46 (28,0) | 102 (36,4) | 0,302 |
| Angina inestable | 89 (20,0) | 33 (20,1) | 56 (20,0) | |
| Angina estable | 112 (25,2) | 44 (26,8) | 68 (24,3) | |
| Isquemia silente | 46 (10,4) | 22 (13,4) | 24 (8,6) | |
| Otros | 49 (11,0) | 19 (11,6) | 30 (10,7) | |
| Tratamiento al alta, N (%) | ||||
| Ácido acetilsalicílicoa | 408 (93,8) | 150 (94,3) | 258 (93,5) | 0,720 |
| Clopidogrela | 165 (37,9) | 53 (33,3) | 112 (40,6) | 0,134 |
| Prasugrela | 22 (5,1) | 9 (5,7) | 13 (4,7) | 0,663 |
| Ticagrelora | 78 (17,9) | 30 (18,9) | 48 (17,4) | 0,699 |
| TAPD | 332 (56,3) | 111 (52,6) | 221 (58,3) | 0,181 |
| Estatinasb | 396 (93,2) | 148 (93,1) | 248 (93,2) | 0,952 |
| Bloqueadores betab | 334 (78,6) | 121 (76,1) | 213 (80,1) | 0,334 |
| IECAb | 324 (76,2) | 126 (79,2) | 198 (74,4) | 0,260 |
| Acenocoumarola | 41 (9,4) | 18 (11,3) | 23 (8,3) | 0,304 |
| Insulina | 53 (8,9) | 53 (24,8) | ||
CABG: cirugía de revascularización coronaria; EPOC: enfermedad pulmonar obstructiva crónica; IAM: infarto agudo de miocardio; ICP: intervención coronaria percutánea; IECA: inhibidores de la enzima de conversión de la angiotensina. a n = 435. b n = 425. | ||||
Características de los vasos con diferimiento de la revascularización
De manera general se difirió la revascularización en vasos con estenosis de gravedad intermedia (porcentaje de estenosis por diámetro, 59,73 ± 9,2%). La arteria más estudiada fue la descendente anterior (43,2%). En la mayoría de los pacientes se procedió a diferir la revascularización de 1 solo vaso (72,7%). No obstante, en aproximadamente el 4% de los pacientes, esta se difirió en 3 vasos dentro de la misma intervención.
En la población de nuestro estudio, el diferimiento de la revascularización se basó principalmente en la FFR (434 vasos, 73,2%) y, después, en iFR (159 vasos, 26,8%). Esta misma proporción se aplicó a pacientes con DM: se procedió a diferir la revascularización en 157 vasos (73,4%) tras observar los valores de FFR frente a 57 vasos (26,6%) tras observar los valores de iFR. Los valores medios de la población general, tanto de FFR como de iFR, fueron 0,87 ± 0,46 y 0,94 ± 0,41, respectivamente, y no se observaron diferencias significativas entre pacientes diabéticos y no diabéticos (tabla 2).
Tabla 2. Características de las arterias diferidas
| Total (N = 593) | Diabéticos (N = 214) | No diabéticos (N = 379) | p | |
|---|---|---|---|---|
| Vaso diferido | ||||
| TCI | 25 (4,2) | 8 (3,7) | 17 (4,5) | 0,664 |
| DA | 256 (43,2) | 90 (42,1) | 166 (43,8) | 0,681 |
| CXI | 173 (29,2) | 59 (27,6) | 114 (30,1) | 0,519 |
| CD | 138 (23,3) | 57 (26,6) | 81 (21,4) | 0,145 |
| Número de vasos diferidos por paciente* | ||||
| 1 vaso | 323 (72,7) | 122 (74,4) | 201 (71,8) | 0,475 |
| 2 vasos | 98 (22,1) | 35 (21,3) | 63 (22,5) | |
| 3 vasos | 19 (4,3) | 7 (4,3) | 12 (4,3) | |
| 4 vasos | 4 (0,9) | 4 (1,4) | 0 (0,0) | |
| Parámetros fisiológicos coronarios | ||||
| Valores medios de la FFR | 0,87 ± 0,46 | 0,86 ± 0,41 | 0,87 ± 0,48 | 0,387 |
| Valores medios del iFR | 0,94 ± 0,41 | 0,94 ± 0,43 | 0,95 ± 0,40 | 0,091 |
| Diferimiento en función de los valores de FFR observados | 434 (73,2) | 157 (73,4) | 277 (73,1) | 0,942 |
| Diferimiento en función de los valores de iFR observados | 159 (26,8) | 57 (26,6) | 102 (26,9) | 0,942 |
CD, coronaria derecha; CXI: circunfleja izquierda; DA: descendente anterior; FFR: reserva fraccional de flujo; iFR: índice instantáneo libre de ondas; TCI, tronco común izquierdo. * n = 444. | ||||
Resultados clínicos en el seguimiento a largo plazo según la presencia o no, de diabetes
La mediana de seguimiento fue de 43 meses [rango intercuartílico, 31,1-55,8], no observándose ninguna diferencia entre pacientes con y sin DM. Los resultados clínicos se muestran en la tabla 3. Los diabéticos presentaron tasas más altas de MACE (33 pacientes [20,1%] frente a 37 pacientes [13,2%] en pacientes sin DM), aunque se trató de una diferencia sin significación estadística en el análisis ajustado (HR = 0,98; IC95%, 0,46-2,11; p = 0,964). La tasa de mortalidad por cualquier causa fue mayor entre los diabéticos (18 pacientes [10,8%] frente a 15 pacientes [5,3%]) que entre los no diabéticos, pero las tasas de muerte cardiovascular no fueron estadísticamente diferentes en ninguno de los 2 grupos (3,1 frente al 2,1%). Se observó una tendencia hacia una tasa más alta de infarto de miocardio entre pacientes con DM (6,7 frente al 2,9%; p = 0,063), sin embargo la tasa de infarto de miocardio del vaso diana fue parecido en ambos grupos (HR = 0,87; IC95%, 0,15-4,89; p = 0,906). Se observaron tasassimilares de revascularización y RVD no programadas entre diabéticos y no diabéticos (figura 2 y tabla 3).
Tabla 3. Eventos clínicos tras 4 años de seguimiento en función de la presencia o ausencia de diabetes
| Diabéticos (N = 164) | No diabéticos (N = 280) | Análisis no ajustado | Análisis completamente ajustado* | |||
|---|---|---|---|---|---|---|
| HR (IC95%) | p | HR (IC95%) | p | |||
| MACE | 33 (20,1) | 37 (13,2) | 1,58 (0,99-2,53) | 0,058 | 0,98 (0,46-2,11) | 0,964 |
| Mortalidad por cualquier causa | 18 (10,8) | 15 (5,3) | 2,10 (1,06-4,17) | 0,034 | 2,01 (0,92-4,40) | 0,079 |
| Muerte cardiovascular | 5 (3,1) | 6 (2,1) | 1,45 (0,44-4,74) | 0,543 | 0,72 (0,19- 2,76) | 0,641 |
| Infarto de miocardio | 11 (6,7) | 8 (2,9) | 2,54 (1,02-6,32) | 0,045 | 2,56 (0,95- 6,91) | 0,063 |
| Revascularización no programada | 17 (10,4) | 20 (7,1) | 1,53 (0,80-2,93) | 0,195 | 1,55 (0,77- 3,10 | 0,219 |
| Diabéticos (N = 214) | No diabéticos (N = 379) | Análisis no ajustado | Análisis completamente ajustado* | |||
| HR (IC95%) | p | HR (IC95%) | p | |||
| Infarto de miocardio del vaso diana | 2 (0,9) | 4 (1,1) | 0,96 (0,18-5,23) | 0,971 | 0,87 (0,15- 4,89) | 0,874 |
| Revascularización del vaso diana | 10 (4,7) | 16 (4,2) | 1,15 (0,52-2,54) | 0,767 | 1,14 (0,38- 3,42) | 0,814 |
HR: hazard ratio; IC95%: intervalo de confianza del 95%; MACE: eventos cardiovasculares adversos mayores (mortalidad por cualquier causa, infarto de miocardio, revascularización del vaso diana). * Tanto el HR como los valores p se obtuvieron tras ajustar el modelo con diferentes variables basales (edad, hipertensión, dislipemia, hábito tabáquico, insuficiencia renal crónica y antecedentes de intervención coronaria percutánea y cirugía de revascularización coronaria). | ||||||
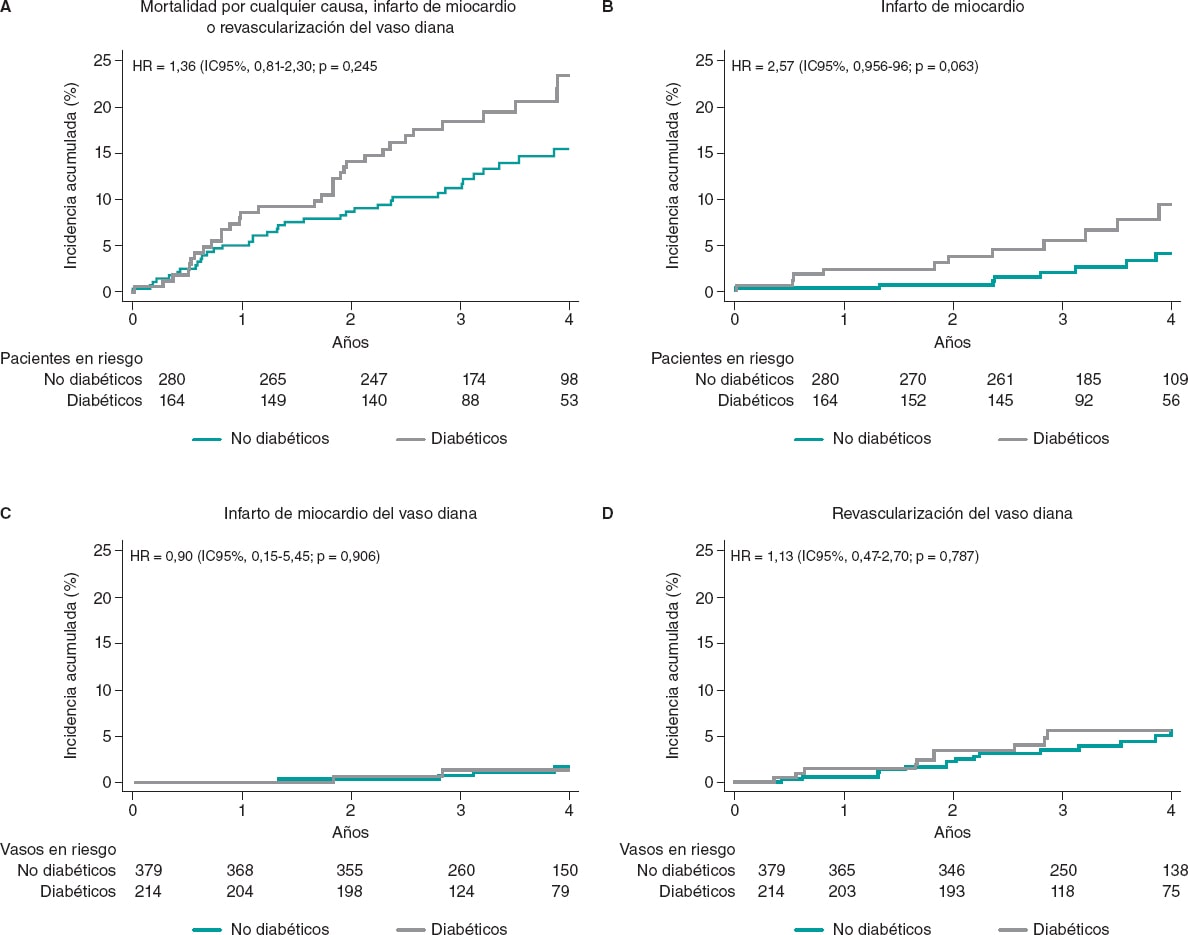
Figura 2. Resultados clínicos en pacientes diabéticos y no diabéticos tras 4 años de seguimiento. HR: hazard ratio; IC95%: intervalo de confianza del 95%.
Resultados clínicos a largo plazo según el índice fisiológico utilizado para diferir la revascularización
En pacientes con DM el índice fisiológico empleado (FFR o iFR) para el diferimiento de la revascularización no se asoció a diferencias estadísticamente significativas en las tasas de MACE (p = 0,688) ni a diferencias importantes de mortalidad por cualquier causa, muerte cardiovascular, infarto de miocardio o revascularización no programada. Se observaron tasas similares de infarto de miocardio del vaso diana en pacientes diferidos con ambas técnicas (con independencia de si tenían DM o no (tabla 4).
Tabla 4. Resultados clínicos tras 4 años de seguimiento según la técnica empleada para diferir la revascularización
| Pacientes diferidos en función de los valores FFR observados (N = 347) | Pacientes diferidos en función de los valores iFR observados (N = 97) | p (log-rank) | |
|---|---|---|---|
| MACE | 59 (17,0) | 11 (11,3) | 0,288 |
| Diabéticos | 27 (21,1) | 6 (16,7) | 0,688 |
| No diabéticos | 32 (14,6) | 5 (8,2) | 0,277 |
| Mortalidad por cualquier causa | 25 (7,2) | 8 (8,3) | 0,574 |
| Diabéticos | 13 (10,2) | 5 (13,9) | 0,417 |
| No diabéticos | 12 (5,5) | 3 (4,9) | 0,972 |
| Mortalidad cardiovascular | 8 (2,3) | 3 (3,1) | 0,593 |
| Diabéticos | 4 (3,1) | 1 (2,8) | 0,964 |
| No diabéticos | 4 (1,8) | 2 (3,3) | 0,436 |
| Infarto de miocardio | 16 (4,6) | 3 (3,1) | 0,762 |
| Diabéticos | 10 (7,8) | 1 (2,8) | 0,396 |
| No diabéticos | 6 (2,7) | 2 (3,3) | 0,596 |
| Revascularización no programada | 33 (9,5) | 4 (4,1) | 0,133 |
| Diabéticos | 16 (12,5) | 1 (2,8) | 0,112 |
| No diabéticos | 17 (7,8) | 3 (4,9) | 0,542 |
| Pacientes diferidos en función de los valores FFR observados (N = 434) | Pacientes diferidos en función de los valores iFR observados (N = 159) | p (log-rank) | |
| Infarto de miocardio del vaso diana | 4 (0,9) | 2 (1,3) | 0,527 |
| Diabéticos | 2 (1,3) | 0 (0,0) | 0,433 |
| No diabéticos | 2 (0,7) | 2 (2,0) | 0,172 |
| Revascularización del vaso diana | 24 (5,5) | 2 (1,3) | 0,037 |
| Diabéticos | 10 (6,4) | 0 (0,0) | 0,064 |
| No diabéticos | 14 (5,1) | 2 (2,0) | 0,244 |
FFR: reserva fraccional de flujo; iFR: índice instantáneo libre de ondas; MACE: eventos cardiovasculares adversos mayores (mortalidad por cualquier causa, infarto de miocardio, revascularización del vaso diana). | |||
La tasa de RVD fue mucho más alta en pacientes diferidos según los valores de FFR que según los valores de iFR (24 [5,5%] frente a 2 [1,3%]; p = 0,037). Este resultado se debió, principalmente, a una tendencia significativa hacia una tasa más alta de RVD en pacientes con DM diferidos según los valores de FFR que en pacientes diabéticos diferidos según los valores de iFR (10 [6.4%] frente a 0 [0%]), lo cual no tuvo significación estadística (p = 0,065). Esta tendencia hacia un índice más bajo de RVD en vasos diferidos según los valores del iFR no se observó en pacientes sin DM (14 [5,1%] frente a 2 [2,0%]; p = 0,244) (figura 3).
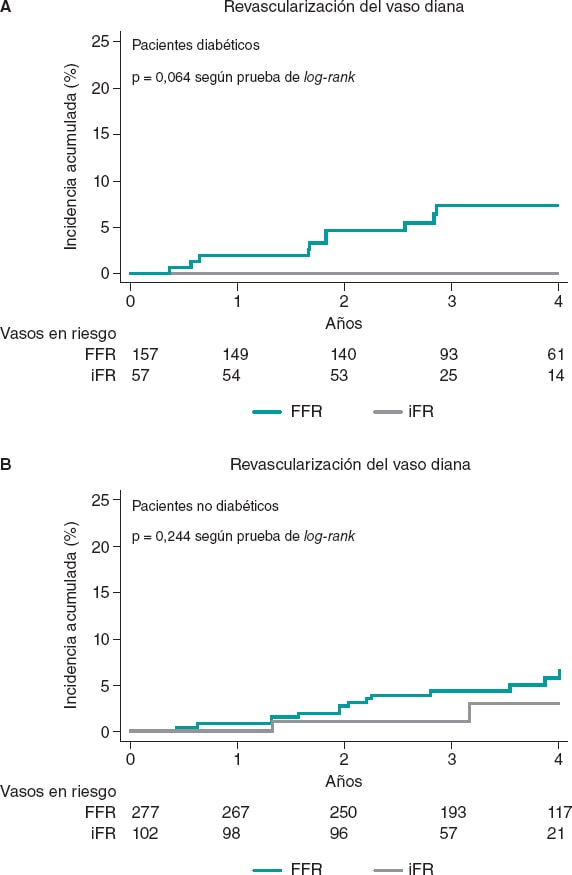
Figura 3. Revascularización del vaso diana según la técnica utilizada para diferir la revascularización tras 4 años de seguimiento. FFR: reserva fraccional de flujo; iFR: índice instantáneo libre de ondas.
DISCUSIÓN
Estos fueron los principales hallazgos del estudio: a) los pacientes con DM presentaban índices altos de MACE. No obstante, diferir la revascularización de estenosis intermedias en pacientes con DM en función de los resultados obtenidos en una valoración fisiológica realizada mediante guía de presión es seguro en lo que respecta al riesgo de RVD o infarto de miocardio del vaso diana con una tasa de eventos a largo plazo similar a la descrita en pacientes no diabéticos; b) ambos índices, FFR e iFR, se pueden usar de manera segura para diferir la revascularización de estenosis intermedias en pacientes diabéticos; c) se observó una tendencia hacia una tas más alta de RVD en pacientes diabéticos diferidos según los valores de FFR.
Resultados clínicos en función de la presencia o no de diabetes mellitus
Comparado con la valoración angiográfica, usar la fisiología coronaria para guiar la revascularización mejora los resultados de los pacientes3,6,7,13. En la actualidad, las guías de práctica clínica dan a los índices fisiológicos FFR e iFR una recomendación clase IA, en materia de valoración funcional de las estenosis coronarias para guiar la revascularización1.
Los diabéticos son una población de alto riesgo, con una carga aterosclerótica más agresiva y acelerada que los no diabéticos. En el estudio PARADIGM ((Progression of atherosclerotic plaque determined by computed tomographic angiography imaging), la presencia de DM fue un factor de riesgo independiente para el avance de la placa14. En un análisis conjunto de 5 estudios sobre ecografías intravasculares, Nicholls SJ et al. confirmaron que los pacientes con DM presentaban un volumen porcentual de placa de ateroma mayor y un avance más rápido de dicha placa15.
Aproximadamente el 25% de los pacientes de importantes estudios que demostraron la efectividad de la FFR y el iFR tenían DM3,4,6,16,17. Si es, o no, seguro diferir la revascularización según los índices fisiológicos observados en el contexto de la DM no ha sido objeto de estudio como tal en ensayos clínicos aleatorizados. Por otro lado, los resultados de los pocos estudios no aleatorizados realizados hasta la fecha que han analizado el tratamiento guiado mediante valoración fisiológica en pacientes diabéticos ofrecen resultados contradictorios18,19.
Domínguez-Franco et al. analizaron la seguridad pronóstica del índice FFR en diabéticos. Aunque sus resultados coinciden con los nuestros en el sentido de que no se observaron diferencias en la RVD en el seguimiento a largo plazo tras diferir la revascularización en pacientes con o sin DM, la aplicabilidad y fortaleza de su estudio son limitadas por el pequeño tamaño de la muestra (136 pacientes, 144 lesiones). Además, el valor de corte de la FFR empleado en el proceso de toma de decisiones fue de 0,75 mientras que, en la práctica contemporánea, suelen usarse valores de corte de 0,8018.
Recientemente, Kennedy et al. analizaron a 250 pacientes (128 y 122 pacientes con y sin DM, respectivamente) y descubrieron que la DM se asoció a un índice más alto de estenosis diferidas fracasadas (18,1 frente al 7,5%; p ≤ 0,01, ajuste según el modelo de regresión de Cox (HR = 3,65; IC95%, 1,40-9,53; p < 0,01) y revascularización de la lesión diana de la lesión diferida (17,2 frente al 7,5%; HR = 3,52; IC95%, 1,34-9,30; p = 0,01). No obstante, igual que ocurrió en nuestros resultados, no se observaron diferencias significativas en la tasa de infarto de miocardio del vaso diana (6,1 frente al 2,0%; HR = 3,34; IC95%, 0,64-17,30; p = 0,15)19. La tasa de RLD descrita en el anterior estudio es mucho más alta que el de nuestra población y el de anteriores estudios (por ejemplo, en el FAME, el índice de RLD a los 2 años fue del 3,2% en lesiones FFR negativas)2. Estas diferencias podrían estar asociadas a las características del tratamiento médico concomitante que no se especificó pero que podría haber jugado un papel crítico en la evolución de los pacientes con DM. En la población de nuestro estudio la mayoría de los pacientes recibieron tratamiento médico óptimo y más del 93% recibió estatinas. El anterior estudio, no obstante, no especificó el tratamiento médico empleado. Otro factor importante es el porcentaje de pacientes insulinodependientes con DM (el 42% en el anterior estudio frente al 24% en nuestra población). En otro estudio los mismos autores comunicaron que el tratamiento con insulina fue un factor predictivo del fracaso de la lesión diferida en pacientes con valores FFR observados > 0,8020. Por lo tanto, el perfil de riesgo tan desigual de las distintas poblaciones explicaría la variabilidad de los resultados obtenidos. Nuestro estudio, con una muestra de mayor tamaño, demuestra que, comparado con los no diabéticos, diferir la revascularización de estenosis intermedias en pacientes diabéticos es seguro hasta el punto de que no se observan diferencias en la RVD durante el seguimiento. Otro estudio con resultados parecidos fue el de Van Belle et al. que comprobaron que la FFR es una herramienta importante para redefinir la gravedad de la estenosis en pacientes con DM, con buenos resultados al cabo de 1 año en pacientes diferidos (HR = 0,77; IC95%, 0,47-1,25; p = 0,29; pacientes con DM reclasificados frente a no reclasificados)21.
Resultados clínicos según el índice fisiológico empleado para diferir la revascularización
Nuestros resultados sugieren que tanto la FFR como el iFR se pueden utilizar de forma segura para diferir la revascularización de estenosis intermedias en pacientes con DM. Nuestros hallazgos con tasas bajas de MACE durante el seguimiento coinciden con el subanálisis de pacientes con DM del estudio DEFINE-FLAIR comparado con el seguimiento a 1 año22. No deja de ser interesante que observáramos una tendencia hacia una tasa más alto de RVD en pacientes diabéticos diferidos con la FFR que con el iFR. Esto podría deberse a la presencia de disfunción microvascular en pacientes diabéticos y a una mejor correlación del iFR con índices que se usan para valorar la microcirculación como la reserva de flujo coronario (RFC). Un estudio comparó el rendimiento de los índices fisiológicos, iFR y FFR, frente a la RFC invasiva en 216 estenosis, encontró una correlación mucho más sólida y un mayor rendimiento diagnóstico para el iFR (área bajo la curva ROC del iFR, 0,82 frente a área bajo la curva ROC de la FFR, 0,72; p < 0,001, para una reserva de velocidad del flujo coronario = 2)23. Cook et al. analizaron 567 vasos con guías de presión equipadas con sensor en la punta y guías intracoronarias Doppler. Descubrieron que en presencia de FFR–/iFR+ discrepantes tanto la velocidad del flujo hiperémico como la RFC eran parecidas a las del grupo FFR+/iFR+ (p > 0,05). No obstante, en presencia de FFR+/iFR– discrepantes, la velocidad del flujo hiperémico y la RFC eran parecidas tanto a los índices FFR–/iFR– como a los grupos coronarios no obstruidos (p > 0,05)24. Estos hallazgos explicarían el peor rendimiento de la FFR en presencia de disfunción microvascular, así como la tendencia observada hacia una mayor RVD en pacientes diabéticos diferidos tras observar los valores FFR. Resulta interesante que esta tendencia no se observó en pacientes sin DM, lo cual avalaría la hipótesis del compromiso microvascular como una de las posibles causas para las diferencias descritas entre los 2 índices.
Limitaciones
Este estudio tiene varias limitaciones. En primer lugar, se trata de un estudio no aleatorizado, retrospectivo, observacional y de un único centro. Los resultados deben analizarse con cautela e interpretarse, solo, como generadores de hipótesis dado el pequeño tamaño de la muestra que limita el poder estadístico del estudio. Se valoró fisiológicamente a más pacientes con el índice FFR que con el iFR, lo cual podría haber influido en los resultados obtenidos. Ni los médicos ni los pacientes se mantuvieron ciegos a los resultados fisiológicos, lo cual podrían haber influido en futuras decisiones de revascularización. En la mayoría de los pacientes la revascularización solo se difirió en 1 vaso, lo cual quiere decir que es complejo extrapolar estos datos a pacientes con enfermedad multivaso. Por último, en esta población de pacientes, no se valoró la disfunción microvascular, razón por la cual no se pudo determinar el verdadero impacto que esto tuvo en los resultados.
CONCLUSIONES
Diferir la revascularización de estenosis intermedias en pacientes con DM según los índices FFR o iFR observados es seguro en lo que respecta al riesgo de RVD o infarto de miocardio del vaso diana con un índice similar de estos eventos en el seguimiento a largo plazo comparado con el índice descrito en pacientes no diabéticos.
FINANCIACIÓN
Ninguna.
CONTRIBUCIÓN DE LOS AUTORES
A.F. Castro-Mejía y A. Travieso-González contribuyeron a la idea y diseño del estudio, a la adquisición, análisis e interpretación de los datos, así como a la redacción del artículo, M.J. Pérez-Vizcayno contribuyó tanto al análisis como a la interpretación de los datos, H. Mejía-Rentería, I.J. Núñez-Gil, P. Salinas, L. Nombela-Franco, P. Jiménez-Quevedo, A. Fernández-Ortiz y C. Macaya contribuyeron tanto a la redacción del artículo como a la revisión crítica de su contenido intelectual. J. Escaned y N. Gonzalo contribuyeron a la redacción del artículo, llevaron a cabo la revisión crítica de su contenido intelectual y dieron su aprobación a la versión final.
CONFLICTO DE INTERESES
I.J Núñez-Gil es consultor de Aztrazeneca. P. Salinas declaró haber recibido honorarios por su labor como conferenciante para Boston Scientific, Terumo, Alvinedica y Biomenco. L. Nombela-Franco ha declarado ser proctor de Abbott y haber recibido honorarios por su labor como conferenciante para Edwards Lifesciences Inc. A. Fernández-Ortiz es conferenciante en eventos de formación para Medtronic, Biotronik, Biosensor y Bayer. J. Escaned es conferenciante y consultor de Abbott, Boston Scientific y Philips y declaró haber recibido honorarios de Philips Volcano, Boston Scientific y Abbott/St. Jude Medical fuera del ámbito del presente estudio. N. Gonzalo es conferenciante en eventos de formación para Abbott y Boston Scientific. Los demás autores no han declarado ningún conflicto de intereses.
¿QUÉ SE SABE DEL TEMA?
- Tanto la FFR como el iFR han demostrado ser herramientas seguras para guiar el tratamiento de revascularización en diferentes escenarios clínicos en el seguimiento a largo plazo. No obstante, la seguridad de las revascularizaciones basadas en índices fisiológicos en pacientes diabéticos en riesgo alto de sufrir eventos cardiovasculares apenas se ha estudiado.
¿QUÉ APORTA DE NUEVO?
- Diferir la revascularización de estenosis intermedias en pacientes diabéticos en función de los resultados obtenidos en una valoración fisiológica realizada mediante guía de presión es seguro y tiene una tasa baja de ocurrencia de eventos secundarios, en el vaso diferido, similar a las tasas descritas en pacientes no diabéticos durante el seguimiento a largo plazo.
BIBLIOGRAFÍA
1. Neumann F-J, Sousa-Uva M, Ahlsson A, et al. 2018 ESC/EACTS Guidelines on myocardial revascularization. Eur Heart J. 2018;40:87-165.
2. Pijls NH, Fearon WF, Tonino PA, et al. Fractional flow reserve versus angiography for guiding percutaneous coronary intervention in patients with multivessel coronary artery disease:2-year follow-up of the FAME (Fractional Flow Reserve Versus Angiography for Multivessel Evaluation) study. J Am Coll Cardiol. 2010;56:177-184.
3. Davies JE, Sen S, Dehbi HM, et al. Use of the Instantaneous Wave-free Ratio or Fractional Flow Reserve in PCI. New Engl J Med. 2017;376:1824-1834.
4. Escaned J, Ryan N, Mejia-Renteria H, et al. Safety of the Deferral of Coronary Revascularization on the Basis of Instantaneous Wave-Free Ratio and Fractional Flow Reserve Measurements in Stable Coronary Artery Disease and Acute Coronary Syndromes. JACC Cardiovasc Interv. 2018;11:1437-1449.
5. Zimmermann FM, Ferrara A, Johnson NP, et al. Deferral vs performance of percutaneous coronary intervention of functionally non-significant coronary stenosis:15-year follow-up of the DEFER trial. Eur Heart J. 2015;36:3182-3188.
6. Gotberg M, Christiansen EH, Gudmundsdottir IJ, et al. Instantaneous Wave-free Ratio versus Fractional Flow Reserve to Guide PCI. New Engl J Med. 2017;376:1813-1823.
7. Escaned J, Collet C, Ryan N, et al. Clinical outcomes of state-of-the-art percutaneous coronary revascularization in patients with de novo three vessel disease:1-year results of the SYNTAX II study. Eur Heart J. 2017;38:3124-3134.
8. van Nunen LX, Zimmermann FM, Tonino PA, et al. Fractional flow reserve versus angiography for guidance of PCI in patients with multivessel coronary artery disease (FAME):5-year follow-up of a randomised controlled trial. Lancet. 2015;386:853-1860.
9. Norhammar A, Malmberg K, Diderholm E, et al. Diabetes mellitus:the major risk factor in unstable coronary artery disease even after consideration of the extent of coronary artery disease and benefits of revascularization. J Am Coll Cardiol. 2004;43:585-591.
10. Castro Mejia A, Ortega Armas M, Lopez Ferreo L. Factores de riesgo en pacientes con cardiopatía isquémica angiográficamente severa:diferencias según sexo. Rev Cuba Cardiol Cir Cardiovasc. 2015;21:7p.
11. Esper RB, Farkouh ME, Ribeiro EE, et al. SYNTAX Score in Patients With Diabetes Undergoing Coronary Revascularization in the FREEDOM Trial. J Am Coll Cardiol. 2018;72:2826-2837.
12. Jeremias A, Kirtane AJ, Stone GW. A Test in Context. Fractional Flow Reserve:Accuracy, Prognostic Implications, and Limitations. J Am Coll Cardiol. 2017;69:2748-2758.
13. Tonino PA, De Bruyne B, Pijls NH, et al. Fractional flow reserve versus angiography for guiding percutaneous coronary intervention. New Engl J Med. 2009;360:213-224.
14. Kim U, Leipsic JA, Sellers SL, et al. Natural History of Diabetic Coronary Atherosclerosis by Quantitative Measurement of Serial Coronary Computed Tomographic Angiography. Results of the PARADIGM Study (Progression of Atherosclerotic Plaque Determined by Computed Tomographic Angiography Imaging). J Am Coll Cardiol Img. 2018:11:1461-1471.
15. Nicholls SJ, Tuzcu EM, Kalidindi S, et al. Effect of Diabetes on Progression of Coronary Atherosclerosis and Arterial Remodeling:A Pooled Analysis of 5 Intravascular Ultrasound Trials. J Am Coll Cardiol. 2008;52:255-262.
16. Xaplanteris P, Fournier S, Pijls NHJ, et al. Five-Year Outcomes with PCI Guided by Fractional Flow Reserve. New Engl J Med. 2018;379:250-259.
17. De Bruyne B, Fearon WF, Pijls NH, et al. Fractional flow reserve-guided PCI for stable coronary artery disease. New Engl J Med. 2014;371:1208-1217.
18. Domínguez-Franco AJ, Jiménez-Navarro MF, Muñoz-García AJ, et al. Pronóstico a largo plazo de diferir la intervención coronaria en diabéticos sobre la base de la reserva fraccional de flujo. Rev Esp Cardiol. 2008;61:352-359.
19. Kennedy MW, Kaplan E, Hermanides RS, et al. Clinical outcomes of deferred revascularisation using fractional flow reserve in patients with and without diabetes mellitus. Cardiovasc Diabetol. 2016;15:100.
20. Kennedy MW, Fabris E, Hermanides RS, et al. Factors associated with deferred lesion failure following fractional flow reserve assessment in patients with diabetes mellitus. Catheter Cardiovasc Interv. 2017;90:1077-1083.
21. Van Belle E, Cosenza A, Baptista SB, et al. Usefulness of Routine Fractional Flow Reserve for Clinical Management of Coronary Artery Disease in Patients With Diabetes. JAMA Cardiol. 2020;5:272-281.
22. Lee JM, Choi KH, Koo BK, et al. Comparison of Major Adverse Cardiac Events Between Instantaneous Wave-Free Ratio and Fractional Flow Reserve-Guided Strategy in Patients With or Without Type 2 Diabetes:A Secondary Analysis of a Randomized Clinical Trial. JAMA Cardiol. 2019;4:857-864.
23. Petraco R, van de Hoef TP, Nijjer S, et al. Baseline instantaneous wave-free ratio as a pressure-only estimation of underlying coronary flow reserve:results of the JUSTIFY-CFR Study (Joined Coronary Pressure and Flow Analysis to Determine Diagnostic Characteristics of Basal and Hyperemic Indices of Functional Lesion Severity-Coronary Flow Reserve). Circ Cardiovasc Interv. 2014;7:492-502.
24. Cook CM, Jeremias A, Petraco R, et al. Fractional Flow Reserve/Instantaneous Wave-Free Ratio Discordance in Angiographically Intermediate Coronary Stenoses:An Analysis Using Doppler-Derived Coronary Flow Measurements. JACC Cardiovasc Interv. 2017;10:2514-2524.
* Autor para correspondencia: Departamento de Cardiología Intervencionista, Instituto Cardiovascular, Hospital Universitario Clínico San Carlos, IdISSC, Universidad Complutense, Prof. Martín Lagos s/n, 28040 Madrid, España.
Correo electrónico: nieves_gonzalo@yahoo.es (N. Gonzalo).