RESUMEN
Introducción y objetivos: El implante percutáneo de válvula aórtica (TAVI) ha demostrado ser seguro y eficaz en pacientes tanto de bajo como de alto riesgo, pero los procedimientos emergentes se han excluido en los principales estudios. El objetivo fue determinar los resultados actuales y los condicionantes del pronóstico durante el TAVI emergente.
Métodos: Se realizó una búsqueda sistemática en PubMed y Google Scholar de cualquier estudio que comparara el TAVI electivo frente al emergente. Los términos empleados fueron «emergent» y/o «urgent», «elective», y «transcatheter valve replacement» y/o «heart failure» y/o «cardiogenic shock». Se consideró TAVI emergente todo procedimiento no programado realizado para tratar la insuficiencia cardiaca refractaria o el shock cardiogénico. Se utilizó un modelo de efectos aleatorios.
Resultados: Se incluyeron 7 estudios (84.427 pacientes) tratados con TAVI (14.241 emergentes y 70.186 electivos). Los casos electivos presentaron una mayor puntuación de riesgo (EuroSCORE logístico 65,9 ± 21 frente a 29,4 ± 18%, p < 0,001; Society of Thoracic Surgeons Risk Score 29,4 ± 27,4 frente a 13,7 ± 11,6%, p < 0,001). Presentaron una enfermedad cardiaca más avanzada, con peor función ventricular izquierda (39,5 ± 17,8 frente a 52,5 ± 12,8%; p < 0,001) y mayor diámetro telediastólico del ventrículo izquierdo (55 ± 9 frente a 48 ± 7 mm; p < 0,001), pese a tener similar área valvular aórtica y gradientes. El TAVI electivo tuvo mayor tasa de éxito (93,6 frente a 92,5%; odds ratio [OR] = 0,84; IC95%, 0,74-0,95; p = 0,005), con menor tasa de fallo renal agudo y menos necesidad de diálisis y de soporte circulatorio mecánico. En conjunto, los casos no emergentes tuvieron menor mortalidad intrahospitalaria (3,3 frente a 5,7%; p < 0,001), a 30 días (4,4 frente a 8,8%; p < 0,001) y a 1 año (19,7 frente a 34,75%; p = 0,0001). Los principales determinantes de mortalidad fueron la nueva necesidad de diálisis (OR = 2.26; IC95%, 1,84-2,76; p < 0,001) o requerir soporte circulatorio mecánico (OR = 2,55; IC95%, 1,14-5,67; p < 0,001).
Conclusiones: Los receptores de TAVI emergente presentaron peor riesgo basal y enfermedad cardiaca más avanzada, que determinaron una mayor mortalidad intrahospitalaria, a 30 días y a 1 año. La identificación precoz del riesgo de precisar soporte circulatorio mecánico o diálisis podría ayudar a una optimización de la indicación de TAVI emergente.
Palabras clave: Shock cardiogénico. Insuficiencia cardiaca. Implante percutáneo de válvula aórtica. Estenosis aórtica.
ABSTRACT
Introduction and objectives: Transcatheter aortic valve implantation (TAVI) has proven safe and effective in low-to-high risk patients, but emergency procedures have been excluded from the landmark trials. We aimed to assess the current outcomes and main factors conditioning the prognosis during emergency TAVI.
Methods: A systematic search in PubMed and Google Scholar was conducted for all studies comparing elective vs emergency TAVI. Searched terms were “emergency” and/or “urgent”, “elective”, and “transcatheter valve replacement” and/or “heart failure” and/or “cardiogenic shock”. Emergency TAVI was considered as any unscheduled TAVI performed to treat refractory heart failure or cardiogenic shock. A random-effects model was used.
Results: A total of 7 studies with 84 427 TAVI patients were included (14 241 emergency procedures; 70 186 elective TAVIs). Emergency cases presented higher risk scores (logistic EuroSCORE 65.9% ± 21% vs 29.4% ± 18%, P < .001; Society of Thoracic Surgeons Risk Score 29.4% ± 27.4% vs 13.7% ± 11.6%, P < .001). More advanced heart disease was observed with deterioration of left ventricular (LV) function (39.5% ± 17.8% vs 52.5% ± 12.8%; P < .001) and larger LV end-diastolic diameters (55 ± 9 mm vs 48 ± 7 mm; P < .001) despite similar aortic valve areas and gradients. Elective TAVIs presented a greater success rate (93.6% vs 92.5%; odds ratio [OR] = 0.84; 95%CI, 0.74-0.95; P = .005), less acute kidney injury, and a lower need for dialysis and mechanical circulatory support. Overall, non-emergency cases had lower in-hospital (3.3% vs 5.7%; P < .001), 30-day (4.4% vs 8.8%; P < .001) and 1-year mortality rates (19.7% vs 34.75%; P = .0001). The main determinants of mortality were need for new dialysis (OR = 2.26; 95%CI, 1.84-2.76; P < .001) or mechanical circulatory support (OR = 2.55; 95%CI, 1.14-5.67; P < .001).
Conclusions: Emergency TAVI recipients presented worse baseline risk and more advanced cardiac disease that determined greater in-hospital, 30-day, and 1-year mortality rates. The early identification of patients at risk for requiring mechanical circulatory support or dialysis may contribute to a better indication of TAVI in emergency scenarios.
Keywords: Cardiogenic shock. Heart failure. Transcatheter aortic valve replacement. Aortic stenosis.
Abreviaturas:
EA: estenosis aórtica. IRC: insuficiencia renal crónica. SC: shock cardiogénico. IC: insuficiencia cardiaca. RVAQ: reemplazo valvular aórtico quirúrgico. TAVI: implante percutáneo de válvula aórtica.
INTRODUCCIÓN
La estenosis aórtica (EA) es la valvulopatía más tratada en los países occidentales1. En un porcentaje relativamente pequeño pero creciente de pacientes (de entre el 3,5 y el 12%), la EA puede presentarse como shock cardiogénico (SC) con un índice de mortalidad estimado a corto plazo de hasta el 70% si no se trata, de forma definitiva, bien quirúrgica o percutáneamente2. El SC se caracteriza por una inadecuada perfusión tisular que es resultado de una enfermedad cardiaca descompensada y que se traduce en un estado de bajo gasto cardiaco. El tratamiento inicial consiste en mantener un perfil hemodinámico estable y garantizar la oxigenación de los tejidos mediante medicación y soporte avanzado3. No obstante, se necesitan tratamientos específicos si se quiere garantizar una resolución completa, si bien el reemplazo valvular aórtico quirúrgico (RVAQ) convencional suele asociarse a un riesgo muy alto de mortalidad2.
Varios estudios han demostrado que el implante percutáneo de válvula aórtica (TAVI) resulta una alternativa segura al RVAQ en pacientes de riesgo entre bajo y alto y en situaciones estables. En la actualidad, se considera la opción de elección en pacientes con un elevado riesgo quirúrgico4-7. En cualquier caso, se calcularon las escalas de riesgo para los principales estudios que fijaron las evidencias para el TAVI tras excluir a pacientes con SC. Como consecuencia, los principales resultados en esta situación tan desafiante no se han comparados aleatoriamente a los de la cirugía. Esta comparativa quizás nunca llegue a realizarse debido al perfil basal tan variable y la desigual disponibilidad de recursos, como los dispositivos de asistencia mecánica circulatoria. Además, los diferentes resultados del TAVI de urgencia y electivos tampoco se han estudiado mucho; aun así, son clave para mejorar los resultados del peor escenario clínico posible. Nuestro objetivo fue valorar los resultados actuales del TAVI en condiciones de emergencia/urgencia, así como los principales factores condicionantes de su pronóstico a través de una revisión sistemática y un metanálisis.
MÉTODOS
Estrategia de búsqueda en la literatura científica
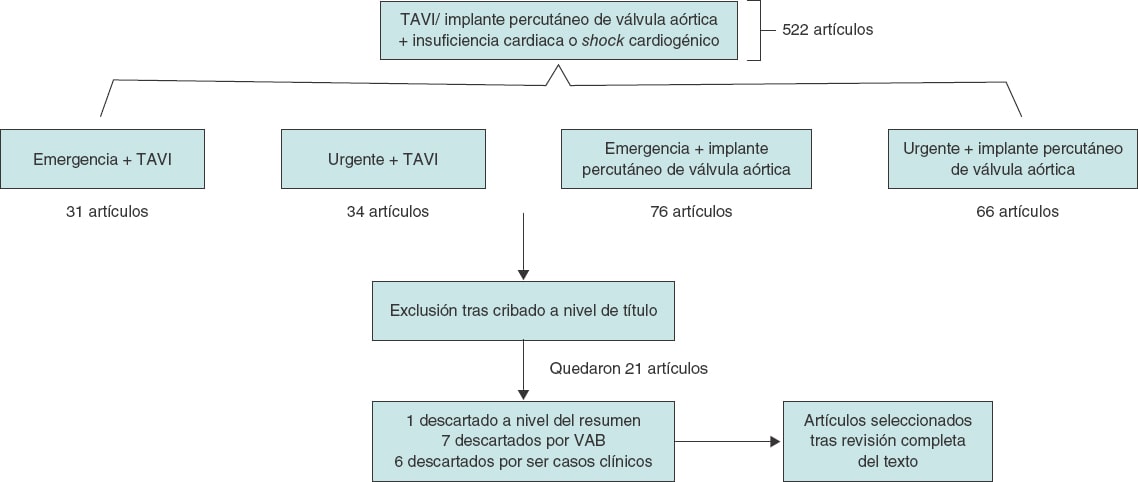
Entre enero de 2014 y enero de 2020, 2 autores independientes (AA y MCM) llevaron a cabo una revisión sistemática de todos los artículos publicados en las bases de datos de PubMed y Google Scholar sobre TAVI en condiciones de emergencia/urgencia frente a TAVI electivo para el tratamiento de la EA grave. Los términos objeto de la búsqueda fueron: «Emergente», «urgent», «elective» y «transcatheter valve replacement», «TAVR», «heart failure» o «cardiogenic shock». La definición de intervención en condiciones de emergencia/urgencia fue variable, si bien el consenso que se alcanzó para este artículo fue la inclusión de pacientes que necesitaron un TAVI no programado para tratar su insuficiencia cardiaca o SC refractarios y corregir esta patología durante las 72 horas siguientes a la hospitalización. Se escogió un total de 7 estudios8-14 y los criterios de inclusión establecidos por nuestro grupo fueron: a) la población del estudio incluyó a pacientes con estenosis aórtica que recibieron TAVI; b) solo se incluyeron estudios que hubieran comparado TAVI realizados en condiciones de emergencia o urgencia frente a procedimientos electivos; c) solo se escogieron artículos escritos completamente en inglés revisados por pares de los que se tenían suficientes datos. Los criterios de exclusión seleccionados fueron: a) resúmenes; b) casos clínicos; c) editoriales; d) opiniones de expertos y e) estudios repetitivos. Las discrepancias entre los revisores se resolvieron mediante discusión y consenso. La figura 1 muestra un diagrama de flujo y la tabla 1 del material adicional, las características principales de los estudios incluidos.
Figura 1. Diagrama de flujo con los resultados y selección de los estudios incluidos en el metanálisis.
Tabla 1. Características clínicas y ecocardiográficas basales de pacientes tratados con TAVI electivo o emergente
| Variable | Nº de pacientes | Población TAVI global n = 84.427 | TAVI electivo n = 70.186 (83,1%) | TAVI emergente/urgente n = 14.241 (16,9%) | p |
|---|---|---|---|---|---|
| Características clínicas | |||||
| Sexo (varón) (%) | 84.427 | 43.735/84.427 (51,8%) | 36.576/70.186 (52,11%) | 7.159/14.241 (50,27%) | < 0,001 |
| Edad (años) | 44.385 | 81,12 ± 8,47 | 81,16 ± 8,27 | 80,96 ± 9,08 | 0,041 |
| EuroSCORE (%) | 1.387 | 31,24 ± 18,15 | 29,42 ± 17,99 | 68,88 ± 20,97 | < 0,001 |
| Escala STS (%) | 985 | 14,76 ± 13,34 | 13,66 ± 11,61 | 29,39 ± 27,39 | < 0,001 |
| Anemia (%) | 42.524 | 11.415/42.524 (26,84%) | 8.004/32.382 (24,71%) | 3.411/10.142 (33,63%) | < 0,001 |
| Fibrilación auricular (%) | 41.185 | 17.373/41.885 (41,47%) | 15.304/37.780 (40,51%) | 2.069/4.105 (50,40%) | < 0,001 |
| EC (%) | 41.329 | 25.723/41.329 (62,24%) | 23.178/37.308 (62,13%) | 2.545/4.021 (63,29%) | 0,147 |
| ERC (%) | 83.308 | 17.948 /83.308 (21,54%) | 13.368/69.187 (19,32%) | 4.580/14.121 (32,43%) | < 0,001 |
| EPOC (%) | 84.398 | 25.081/84.398 (29,72%) | 20.315/70.157 (28,96%) | 4.766/14.241 (33,47%) | < 0,001 |
| Diabetes (%) | 84.040 | 29.670/84.040 (35,30%) | 24.571/69.820 (35,19%) | 5.099/14.220 (35,86%) | 0,130 |
| Hipertensión (%) | 83.308 | 70.608/83.308 (84,75%) | 59.117/69.187 (85,44%) | 11.491/14.121 (81,38%) | < 0,001 |
| NYHA III-IV (%) | 41.143 | 33.056/41.143 (80,34%) | 29.297/37.065 (79,04%) | 3.759/4.078 (92,17%) | < 0,001 |
| EAP (%) | 84.069 | 25.236/84.069 (30,02%) | 20.933/69.849 (29,96%) | 4.303/14.220 (30,26%) | 0,490 |
| Aorta de porcelana (%) | 40.669 | 2.158/40.669 (5,3%) | 1.914/36.669 (5,22%) | 244/4.000 (6,1%) | 0,018 |
| RVA previo (%) | 40.658 | 1.599/40.658 (3,93%) | 1.292/36.664 (3,53%) | 307/3.994 (7,69%) | < 0,001 |
| CABG previo (%) | 83.656 | 20.924/83.656 (25,01%) | 18.000/69.442 (25,92%) | 2.924/14.214 (20,57%) | < 0,001 |
| IM previo (%) | 83.040 | 15.173/83.040 (18,27%) | 12.597/68.868 (18,29%) | 2.576/14.172 (18,18%) | 0,747 |
| ICP previa (%) | 83.029 | 22.118/83.029 (26,64%) | 18.979/68.863 (27,56%) | 3.139/14.166 (22,16%) | < 0,001 |
| MP/DCI previo | 40.774 | 8.304/40.774 (20,36%) | 7.401/36.723 (20,15%) | 903/4.051 (22,29%) | 0,001 |
| ACV/AIT previo (%) | 42.244 | 8.815/42.244 (20,87%) | 7.884/38.118 (20,68%) | 931/4.126 (22,57%) | 0,005 |
| Características ecocardiográficas | |||||
| Área valvular aórtica (cm²) | 2.230 | 0,7 ± 0,23 | 0,7 ± 0,23 | 0,66 ± 0,21 | 0,308 |
| DTDVI (mm) | 616 | 48,98 ± 7,34 | 48,53 ± 7,20 | 55,05 ± 9,03 | < 0,001 |
| FEVI (%) | 1.861 | 51,51 ± 13,24 | 52,23 ± 12,71 | 29,58 ± 14,89 | < 0,001 |
| Gradiente medio (mmHg) | 1.398 | 43,71 ± 16,42 | 43,91 ± 16,31 | 40,26 ± 18,29 | 0,061 |
| IA III-IV (%) | 41.032 | 8.156/41.032 (19,88%) | 7.159/37.033 (19,33%) | 997/3.999 (24,93%) | < 0,001 |
| HTP (%) | 43.251 | 2.003/43.251 (4,63%) | 1.536/33.088 (4,64%) | 467/10.163 (4,6%) | 0,843 |
|
DCI: desfibrilador-cardioversor implantable; DTDVI: diámetro telediastólico del ventrículo izquierdo; EAP: enfermedad arterial periférica; EC: enfermedad coronaria; EPOC: enfermedad pulmonar obstructiva crónica; FEVI: fracción de eyección del ventrículo izquierdo; IA: insuficiencia aórtica; HTP: hipertensión pulmonar; ICP: intervención coronaria percutánea; IM: infarto de miocardio; ERC: enfermedad renal crónica; MP: marcapasos; NYHA: New York Heart Association; RVA: reemplazo valvular aórtico; STS: Society of Thoracic Surgeons score; TAVI: implante percutáneo de válvula aórtica. |
|||||
Objetivos primarios
Los objetivos primarios fueron la mortalidad a corto plazo y el éxito de la intervención. Los objetivos secundarios fueron las complicaciones perioperatorias. Las complicaciones se reportaron utilizando, principalmente, las definiciones establecidas por el Valve Academic Research Consortium-215.
Análisis estadístico
Las variables cualitativas se expresaron como frecuencia absoluta y porcentaje; las continuas, como media ± desviación estándar salvo que se especificara de otro modo. Para comparar las variables demográficas y los factores de riesgo entre ambos grupos se emplearon la prueba de la X2 o la prueba exacta de Fisher para el estudio de las variables categóricas. La prueba t de Student se empleó para comparar las variables continuas, si así fuese necesario.
Como medida del efecto combinado, los estudios incorporaron el odds ratio (OR), un intervalo de confianza del 95% y significación estadística. La homogeneidad entre los distintos estudios se comparó utilizando la estadística QH. Con respecto a la baja sensibilidad de esta prueba, valores p < 0,10 se consideraron significativos. Para superar, de alguna forma, esta limitación se calculó también el índice estadístico I2, que mide el porcentaje de variación global de los estudios explicado por la heterogeneidad y por su IC95%. Se empleó un modelo de efectos aleatorios para casos con índices estadísticos I2 > 50%y un modelo de efectos fijos para los casos contrarios. El posible seso de publicación se valoró mediante un gráfico de embudo y empleando la prueba de Egger y la de correlación de rango ajustado de Begg y Mazumdar. En presencia de sesgo de publicación, se empleó el método de recorte y relleno para volver a valorar el OR combinado. También se realizaron análisis de sensibilidad para eliminar secuencialmente estudios distintos.
Todos los valores de p fueron bilaterales. Los análisis estadísticos se realizaron utilizando el software R, versión 3.6.1 (proyecto R para estadística computacional) y Review Manager 5.3.
RESULTADOS
Distribución de los pacientes y características basales
Se seleccionaron 7 estudios con un total de 84.427 pacientes tratados con TAVI [70.186 procedimientos electivos (83,1%) y 14.241 emergentes (16,9%)]. Las principales características basales según el carácter electivo o emergente del procedimiento se muestran en la tabla 1 y los análisis de sensibilidad y asimetría en la tabla 2 del material adicional y figura 1 del material adicional. Se detectó asimetría en el daño renal agudo, por lo que hubo que emplear el método de recorte y relleno para volver a valorar el odds ratio. El porcentaje de varones que recibieron procedimientos electivos (52,1%) fue mayor que el de aquellos que recibieron procedimientos de emergencia (50,27%, p < 0,01). En líneas generales, los pacientes tratados en condiciones de emergencia/urgencia tuvieron más comorbilidades tal y como revelaron la escala EuroSCORE logistic (65,9% ± 21% frente al 29,4% ± 18%, p < 0,001) y el modelo de riesgo de la escala de riesgo de la Society of Thoracic Surgeons (STS) (29,4 ± 27,4 frente a 13,7 ± 11,6, p < 0,001). No obstante, los factores tradicionales de riesgo cardiovascular no variaron entre los distintos grupos (hipertensión y diabetes mellitus) y los índices de infarto de miocardio e intervención coronaria percutánea fueron similares. Por el contrario, los pacientes más propensos a ser tratados en condiciones de urgencia ya habían sido tratados mediante reemplazo valvular aórtico quirúrgico previo. En lo que a las principales características ecocardiográficas se refiere, los procedimientos emergentes se realizaron en pacientes con deterioro de la función del ventrículo izquierdo (VI) (39,5% ± 17,8% frente al 52,5% ± 12,8%; p < 0,001), diámetros telediastólicos VI más grandes (55 ± 9 frente a 48 ± 7; p < 0,001), pero áreas valvulares aórticas (0,66 ± 0,21 frente a 0,70 ± 0,23; p < 0,308) y gradientes medios transaórticos similares (40,3 ± 18,3 frente a 43,9 ± 16,3; p < 0,061).
Tabla 2. Características de la intervención de pacientes tratados con TAVI electivo o emergente/urgente
| Variable | Nº de pacientes | Población TAVI global | TAVI electivo | TAVI emergente/urgente | p |
|---|---|---|---|---|---|
| Índice de éxito (%) | 41.140 | 38.765/41.440 (93,54%) | 35.038/37.413 (93,65%) | 3.727/4.027 (92,55%) | 0,007 |
| Migración del dispositivo (%) | 40.042 | 105/40.042 (0,26%) | 90/36.090 (0,25%) | 15/3.952 (0,38%) | 0,129 |
| Anestesia general (%) | 40.669 | 34.419/40.669 (84,6%) | 31.004/36.669 (84,55%) | 3.415/4.000 (85,37%) | 0,170 |
| Transapical (%) | 83.953 | 14.742/83.953 (17,56%) | 12.194/69.790 (17,47%) | 2.548/14.163 (18%) | 0,139 |
| Transfemoral (%) | 83.811 | 66.526/83.811 (79,38%) | 55.196/69.612 (79,29%) | 11.330/14.199 (79,79%) | 0,177 |
| Transubclavio (%) | 40.813 | 643/40.813 (1,57%) | 573/36.834 (1,55%) | 70/3.979 (1,76%) | 0,327 |
| Soporte circulatorio mecánico (%) | 83.326 | 1.858/83.326 (2,29%) | 1.355/69.211 (1,96%) | 503/14.115 (3,56%) | < 0,001 |
|
TAVI: implante percutáneo de válvula aórtica. |
|||||
Características perioperatorias
Los resultados de la intervención en los estudios incluidos se muestran en la tabla 2. El abordaje transfemoral (79,3% frente al 76.8%; p = 0,177) y el uso de anestesia general (84.5% frente a 85.4%; p = 0,17) fueron los abordajes preferidos en los 2 grupos. El índice de éxito quirúrgico de los procedimientos electivos fue mayor (93,6% frente al 92,5%; p = 0,007) y la necesidad de soporte circulatorio mecánico menor (1,96% frente al 3,56 %; p < 0,001). Otros resultados de la intervención fueron comparables entre ambas cohortes.
Resultados posoperatorios
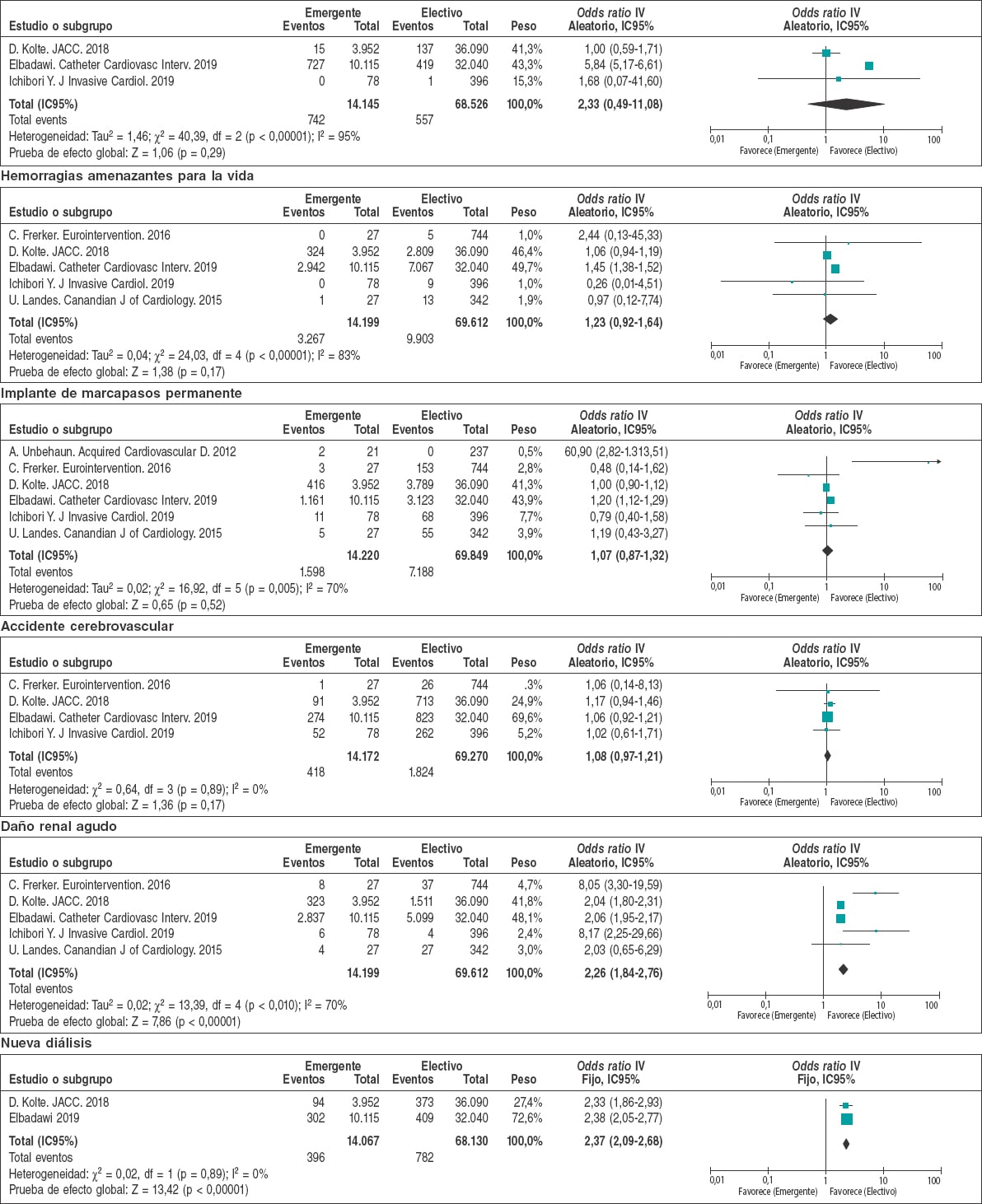
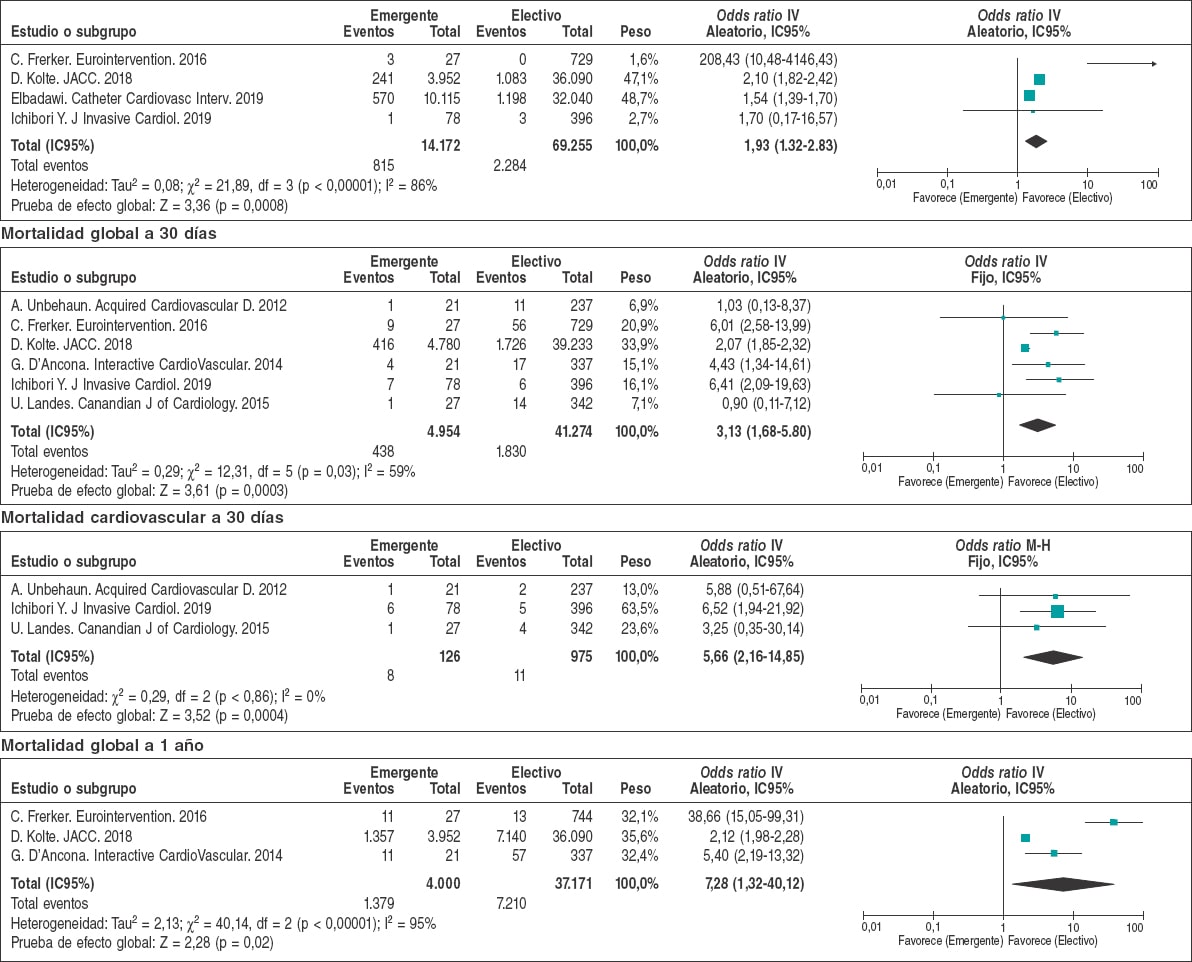
Los principales resultados posoperatorios se muestran en la tabla 3 y en la figura 2. Los OR para el infarto de miocardio, hemorragias amenazantes para la vida, necesidad de implantar un marcapasos permanente y accidentes cerebrovasculares perioperatorios fueron similares con independencia de que el procedimiento fuera programado o emergente. Por el contrario, la cohorte electiva tuvo índices más bajos de daño renal agudo (9,6% frente al 22,4%; OR = 2,26; IC95%, 1,84-2,76; p < 0,001) y necesidad de diálisis (1,1% frente al 2,8%; OR = 2,37; IC95%, 2,09-2,68; p < 0,001). En líneas generales, esto se tradujo en estancias hospitalarias más cortas para los casos electivos y en índices, también más bajos, de mortalidad intrahospitalaria (3,3% frente al 5,75%; OR = 1,32; IC95%, 1,32-2,83; p < 0,001), a los 30 días (4,43% frente al 8,84%; OR = 3,13; IC95%, 1,68-5,80; p < 0,001) y a 1 año (19,7% frente al 34,47%; OR = 2,87; IC95%, 1,67-4,94; p = 0,0001) para los procedimientos electivos (figura 3).
Tabla 3. Principales resultados posoperatorios de pacientes tratados con TAVI electivo o emergente/urgente
| Variable | Nº de pacientes | Población TAVI global | TAVI electivo | TAVI emergente/urgente | p |
|---|---|---|---|---|---|
| Resultados clínicos | |||||
| Hemorragias amenazantes para la vida (%) | 83.811 | 13.170/83.811 (15,71%) | 9.903/69.612 (14,22%) | 3.267/14.199 (23,01%) | < 0,001 |
| Hemorragias mayores (%) | 43.400 | 14.725/43.400 (33,93%) | 11.065/33.180 (33,35%) | 3.660/10.220 (35,81%) | < 0,001 |
| Complicaciones vasculares mayores (%) | 41.656 | 513/41.656 (1,23%) | 460/37.572 (1,22%) | 53/4.084 (1,29%) | 0,686 |
| Infarto de miocardio (%) | 82.671 | 1.299/82.671 (1,57%) | 557/68.526 (0,81%) | 742/14.145 (5,24%) | < 0,001 |
| Daño renal agudo (%) | 83.811 | 9.856/83.811 (11,75%) | 6.678/69.612 (9,59%) | 3.178/14.199 (22,38%) | < 0,001 |
| Necesidad de diálisis (%) | 82.197 | 1.178/82.197 (1,43%) | 782/68.130 (1,15%) | 396/14.067 (2,81%) | < 0,001 |
| IMP (%) | 84.069 | 8.786/84.069 (10,45%) | 7.188/69.849 (10,29%) | 1.598/14.220 (11,24%) | < 0,001 |
| ACV (%) | 83.442 | 2.242/83.442 (2,69%) | 1.824/69.270 (2,63%) | 418/14.172 (2,94%) | 0,034 |
| Índice de mortalidad intrahospitalaria | 83.427 | 3.099/83.427 (3,71%) | 2.284/69.255 (3,3%) | 815/14.172 (5,75%) | < 0,001 |
| Índice de mortalidad a 30 días | 46.228 | 2.268/46.228 (4,9%) | 1.830/41.274 (4,43%) | 430/4.954 (8,84%) | < 0,001 |
| Índice de mortalidad a 1 año | 41.156 | 8.706/41.156 (21 15%) | 7.327/37.156 (19,72%) | 1.379/4.000 (34,75%) | < 0,001 |
| Resultados ecocardiográficos | |||||
| Gradiente medio (mmHg) | 369 | 7,75 ± 4,15 | 7,82 ± 4,22 | 6,9 ± 3,2 | 0,269 |
| IA III-IV (%) | 17.977 | 1.465/17.977 (8,15%) | 1.299/16.125 (8,05%) | 166/1.852 (8,96%) | 0,176 |
|
ACV: accidente cerebrovascular; IA: insuficiencia aórtica; IMP: implante de marcapasos permanente; TAVI: implante percutáneo de válvula aórtica. |
|||||
Figura 2. Diagrama de bosque con las principales complicaciones posoperatorias de pacientes incluidos en el metanálisis.* * La línea vertical representa un punto «sin diferencia» entre los grupos de TAVI emergente o electivo. Las líneas horizontales representan el IC95%. Los cuadrados representan el OR para cada estudio (el tamaño de cada cuadrado es la cantidad de información proporcionada por cada estudio). Los rombos representan los OR combinados de todos los estudios.
Figura 3. Diagrama de bosque con los índices de mortalidad intrahospitalaria y a 1 año de pacientes incluidos en el metanálisis.* * La línea vertical representa un punto «sin diferencia» entre los grupos de TAVI emergente o electivo. Las líneas horizontales representan el IC95%. Los cuadrados representan el OR para cada estudio (el tamaño de cada cuadrado es la cantidad de información proporcionada por cada estudio). Los rombos representan los OR combinados de todos los estudios.
DISCUSIÓN
Cuando pacientes con EA presentan insuficiencia cardiaca (IC) aguda grave o SC, la mortalidad por cualquier causa al cabo de 5 años está por encima del 60% a pesar de la implementación de terapias para tratar la valvulopatía, un índice que no resiste la comparación en pacientes sin IC (~20%) ni síntomas de IC crónica (~30%) en este marco (16). Determinar qué factores condicionan un índice de mortalidad tan alto es clave para mejorar el manejo de este grupo de pacientes que va en aumento. Los principales hallazgos de este estudio son: a) los pacientes que precisaron TAVI emergentes presentaban un riesgo basal más alto que los que precisaron procedimientos programados, no solo por la situación de emergencia sino también por la alta carga de comorbilidades y deterioro de la función VI; b) aunque el índice de éxito de la intervención fue mucho mayor en los casos programados, la diferencia fue poca (93,6% frente al 92,5%; p = 0,007). Esto sugiere que los índices más altos de mortalidad a corto y medio plazo de los casos emergentes se debieron, principalmente, a las complicaciones posoperatorias y no al procedimiento propiamente dicho; c) la necesidad de soporte circulatorio mecánico y diálisis fue mayor después de los casos emergentes. Identificar precozmente qué pacientes de riesgo podrían requerir estos tratamientos es útil para una mejor indicación de TAVI en situaciones de emergencia.
Características basales y mortalidad estimada
En nuestro estudio, los pacientes con TAVI emergente/urgente presentaban muchas más comorbilidades que los que recibieron el procedimiento electivo. Se debe mencionar que la escala de STS se viene empleando para valorar el riesgo de mortalidad en pacientes con RVAQ17. En cualquier caso, es posible que la escala desarrollada por el grupo de trabajo Transcatheter Valve Therapy (TVT) para evaluar los índices de mortalidad intrahospitalaria y al cabo de 30 días18 sea más precisa. Según esa escala, el pronóstico tiene mucho que ver con la presencia de enfermedad renal crónica (ERC), enfermedad pulmonar obstructiva crónica y necesidad de TAVI emergente. Cabe destacar que la EA con ERC concomitante se asocia a índices de mortalidad por cualquier causa y cardiovascular más altos que la EA sin dicha patología; de hecho, esta mayor mortalidad por cualquier causa se correlaciona exponencialmente con un descenso de la tasa de filtración glomerular19. Además, tanto el índice más alto de anemia20 como el mayor riesgo hemorrágico de pacientes con ERC son bien conocidos, lo cual condiciona una mayor necesidad de transfusión de glóbulos rojos21 y, paralelamente, el deterioro de la función renal y del índice de supervivencia.
La función del VI es un factor pronóstico bien conocido de la valvulopatía y su deterioro condiciona el tratamiento quirúrgico o percutáneo de la válvula aórtica, incluso en pacientes asintomáticos22. Se debe mencionar que el similar gradiente transaórtico, a pesar de una función VI reducida en los casos basales emergentes, y el mayor índice de insuficiencia aórtica de esta cohorte sugieren la presencia de una valvulopatía más grave y de probables válvulas nativas más calcificadas y degeneradas. Por esta razón, un abordaje multidisciplinario y con múltiples imágenes podría ser especialmente útil a efectos de programar la intervención y con vistas a mejorar los resultados23.
Mortalidad y complicaciones asociadas a la intervención
La mayoría de las complicaciones asociadas a la intervención fueron similares tanto en los procedimientos electivos como en los emergentes. Aunque esto podría explicarse, en parte, por la mayor experiencia de los operadores, a nivel internacional, y por la falta de diferencias en el índice de abordaje transfemoral24, el mayor uso de dispositivos de soporte circulatorio mecánico podría haber sido especialmente relevante en cohortes emergentes/urgentes. De hecho, la reserva contráctil del VI más limitada de este grupo de pacientes puede condicionar un rápido deterioro en presencia de complicaciones tales como shunt perianular, insuficiencia aórtica severa u obstrucción coronaria. Por lo tanto, la presencia de factores de riesgo para estas complicaciones sugiere la necesidad de implantar dispositivos de soporte circulatorio en determinados casos antes implantar la prótesis valvular como posible estrategia para evitar los pronósticos nefastos que pueden llegar a darse en los procedimientos emergentes25-27. Anteriores experiencias con el dispositivo Impella y el oxigenador extracorpóreo de membrana (ECMO) se pueden consultar en la tabla 3 del material adicional; no obstante, si hay diferencias de mortalidad entre pacientes con y sin soporte mecánico es algo que se debe seguir investigando. Como el éxito de la intervención fue similar al que se obtiene en el ámbito estándar, la traducción clínica que se puede hacer de esto es que, aunque estos casos pueden resolverse con éxito en todos los centros que realizan TAVI, este perfil de pacientes solo debería tratarse en centros que dispongan de dispositivos de soporte circulatorio mecánico, sobre todo ECMO. Los centros de bajo volumen o los no quirúrgicos quedarían excluidos.
El presente metanálisis no incluyó ningún caso tratado exclusivamente mediante valvuloplastia aórtica. Esta estrategia tiene un nivel de evidencia clase IIb-C en la última versión de las guías clínicas, pero se suele emplear como terapia puente hasta el TAVI definitivo en pacientes hemodinámicamente inestables28,29. Un estudio retrospectivo de un único centro halló que el procedimiento de TAVI podría ser superior solo a la valvuloplastia aórtica y al tratamiento médico en pacientes con EA y SC graves, ya que la valvuloplastia aórtica aislada no está exenta de complicaciones (~25%) y presenta índices de mortalidad más altos30. A pesar de esto, se echan en falta extensos estudios controlados y aleatorizados que exploren este escenario con TAVI.
Complicaciones posoperatorias asociadas a un índice más alto de mortalidad
En esta revisión sistemática y metanálisis, se descubrió que los procedimientos TAVI realizados en condiciones de emergencia/urgencia tenían un índice mucho más alto de daño renal agudo (DRA), hemodiálisis y mortalidad. Esto coincide con lo descrito en casos anteriores que confirmaron que los pacientes con DRA post-TAVI eran más propensos a fallecer. El DRA es, además, un predictor de la sepsis, que es, a su vez, un predictor independiente de la mortalidad. Los principales factores que aumentan el riesgo de DRA son la ERC, enfermedad arterial periférica, la diabetes mellitus y el deterioro de la función VI31,32. La estrategia profiláctica va desde la simple hidratación con una solución salina normal hasta diuresis forzada con medidas de soporte precoz33; de hecho, se ha explorado el uso de diálisis profiláctica en pacientes tratados con TAVI y alto riesgo de DRA que podría ser especialmente útil en el ámbito de la emergencia.
Limitaciones del estudio
Son varias las limitaciones asociadas a esta revisión sistemática y metanálisis. En primer lugar, los estudios incluidos fueron observacionales porque no se pudo encontrar ningún estudio aleatorizado multicéntrico que abordara específicamente esta cuestión. En segundo lugar, la definición de procedimiento emergente/urgente fue variable en los diferentes estudios, si bien el equipo del estudio logró elaborar una definición inclusiva. Por último, los resultados podrían no ser extrapolables por lo que deberían interpretarse con cautela debido a la alta heterogeneidad descrita, lo cual estaría asociado a la variabilidad de las muestras y diseños de los estudios.
CONCLUSIONES
La relación entre TAVI en condiciones de emergencia/urgencia y un índice más alto de mortalidad a corto/medio plazo se debe, principalmente, a un perfil basal de riesgo alto, a la fase avanzada de la enfermedad cardiaca y a un índice más alto de daño renal agudo. La identificación y derivación precoces de pacientes de alto riesgo de colapso circulatorio o DRA se debe llevar a cabo convenientemente para reducir el índice de mortalidad asociado a TAVI. Se necesitan seguir investigando para determinar el papel del TAVI en escenarios emergentes o urgentes.
FINANCIACIÓN
Ninguna.
CONFLICTO DE INTERESES
I.J. Amat-Santos es proctor de Boston Scientific.
¿QUÉ SE SABE DEL TEMA?
- El TAVI se realiza, principalmente, en pacientes estables a nivel hemodinámico. De lo contrario, la valvuloplastia aórtica es el tratamiento empírico preferido como terapia puente hasta poder realizar el TAVI. No obstante, son pocos los estudios que han analizado el TAVI en escenarios amenazantes para la vida e inexistentes los estudios controlados aleatorizados y multicéntricos realizados a este respecto.
¿QUÉ APORTA DE NUEVO?
- En este extenso metanálisis combinado (n = 84.427) los TAVI emergentes no fueron algo excepcional sino que se asociaron a índices más altos de mortalidad intrahospitalaria, a 30 días y 1 año comparados con los TAVI electivos. La necesidad de diálisis o soporte circulatorio mecánico condicionó el índice de mortalidad post-TAVI emergente. La identificación precoz de pacientes en riesgo de colapso circulatorio o daño renal agudo podría ayudar a determinar si el TAVI es fútil en este ámbito.
BIBLIOGRAFÍA
1. Thaden JJ., Nkomo VT., Enriquez-Sarano M. The Global Burden of Aortic Stenosis. Prog Cardiovasc Dis. 2014;56:565-571.
2. Akodad M., Schurtz G., Adda J., Leclercq F., Roubille F. Management of valvulopathies with acute severe heart failure and cardiogenic shock. Arch Cardiovasc Dis. 2019;112:773-780.
3. Castrodeza J, Serrador Frutos AM, Amat-Santos IJ, et al. Prophylactic percutaneous circulatory support in high risk transcatheter aortic valve implantation. Cardiol J. 2019;26:424-426.
4. Smith CR., Leon MB., Mack MJ., et al. Transcatheter versus Surgical Aortic-Valve Replacement in High-Risk Patients. New Engl J Med. 2011;364:2187-2198.
5. Leon MB., Smith CR., Mack MJ., et al. Transcatheter or Surgical Aortic-Valve Replacement in Intermediate-Risk Patients. New Engl J Medicine. 2016;374:1609-1620.
6. Reardon MJ., Mieghem NMV., Popma JJ., et al. Surgical or Transcatheter Aortic-Valve Replacement in Intermediate-Risk Patients. New Engl J Medicine 2017;376:1321-1331.
7. Waksman R., Rogers T., Torguson R., et al. Transcatheter Aortic Valve Replacement in Low-Risk Patients with Symptomatic Severe Aortic Stenosis. J Am Coll Cardiol. 2018;72:2095-2105.
8. D'Ancona G., Pasic M., Buz S., et al. Transapical transcatheter aortic valve replacement in patients with cardiogenic shock. Interact Cardiov Th. 2012;14:426-430.
9. Unbehaun A., Pasic M., Buz S., et al. Transapical aortic valve implantation in patients with severely depressed left ventricular function. J Thorac Cardiovasc Surg. 2012;143:1356-1363.
10. Landes U., Orvin K., Codner P., et al. Urgent Transcatheter Aortic Valve Implantation in Patients With Severe Aortic Stenosis and Acute Heart Failure:Procedural and 30-Day Outcomes. Can J Cardiol. 2016;32:726-31.
11. Frerker C., Schewel J., Schlüter M., et al. Emergente transcatheter aortic valve replacement in patients with cardiogenic shock due to acutely decompensated aortic stenosis. Eurointervention. 2016;11:1530-1536.
12. Kolte D., Khera S., Vemulapalli S., et al. Outcomes Following Urgent/Emergency Transcatheter Aortic Valve Replacement:Insights from the STS/ACC TVT Registry. Jacc Cardiovasc Interventions 2018;11:1175-1185.
13. Elbadawi A., Elgendy IY., Mentias A., et al. Outcomes of urgent versus nonurgent transcatheter aortic valve replacement. Catheter Cardiovasc Interv. 2020 Jul;96:189-195.
14. Ichibori Y., Li J., Patel T., et al. Short-Term and Long-Term Outcomes of Patients Undergoing Urgent Transcatheter Aortic Valve Replacement Under a Minimalist Strategy. J Invasive Cardiol. 2019:E30-E36.
15. Kappetein AP., Head SJ., Généreux P., et al. Updated standardized endpoint definitions for transcatheter aortic valve implantation:the Valve Academic Research Consortium-2 consensus document. Eur Heart J. 2012;33:2403-2418.
16. Nagao K., Taniguchi T., Morimoto T., et al. Acute Heart Failure in Patients With Severe Aortic Stenosis- Insights From the CURRENT AS Registry. Circ J. 2018;82:874-885.
17. Yakubov SJ., Adams DH., Watson DR., et al. 2-Year Outcomes After Iliofemoral Self-Expanding Transcatheter Aortic Valve Replacement in Patients With Severe Aortic Stenosis Deemed Extreme Risk for Surgery. J Am Coll Cardiol. 2015;66:1327-1334.
18. Arnold SV., O'Brien SM., Vemulapalli S., et al. Inclusion of Functional Status Measures in the Risk Adjustment of 30-Day Mortality After Transcatheter Aortic Valve Replacement A Report From the Society of Thoracic Surgeons/American College of Cardiology TVT Registry. JACC Cardiovasc Interv. 2018;11:581-589.
19. Patel KK., Shah SY., Arrigain S., et al. Characteristics and Outcomes of Patients With Aortic Stenosis and Chronic Kidney Disease. J Am Heart Assoc. 2019 Feb 5;8:e009980.
20. DeLarochellière H., Urena M., Amat-Santos IJ., et al. Effect on Outcomes and Exercise Performance of Anemia in Patients With Aortic Stenosis Who Underwent Transcatheter Aortic Valve Replacement. Am J Cardiol. 2015;115:472-479.
21. Kanjanahattakij N., Rattanawong P., Krishnamoorthy P., et al. Anaemia and mortality in patients with transcatheter aortic valve replacement:a systematic review and meta-analysis. Acta Cardiol. 2018;74:1-7.
22. Baumgartner H, Falk V, Bax JJ, et al. 2017 ESC/EACTS Guidelines for the management of valvular heart disease. Eur Heart J. 2017;38:2739-2791.
23. Fassa A-A., Himbert D., Vahanian A. Mechanisms and management of TAVR-related complications. Nat Rev Cardiol. 2013;10:685-695.
24. TerréJA., George I., Smith CR. Pros and cons of transcatheter aortic valve implantation (TAVI). Ann Cardiothorac Surg. 2017;6:444-452.
25. Chieffo A., Ancona MB., Burzotta F., et al. Observational multicentre registry of patients treated with IMPella mechanical circulatory support device in ITaly:the IMP-IT registry. EuroIntervention. 2020 Feb 7;15:e1343-e1350.
26. Singh V., Damluji AA., Mendirichaga R., et al. Elective or Emergency Use of Mechanical Circulatory Support Devices During Transcatheter Aortic Valve Replacement. J Interv Cardiol. 2016;29:513-522.
27. Shreenivas SS., Lilly SM., Szeto WY., et al. Cardiopulmonary bypass and intra?aortic balloon pump use is associated with higher short and long term mortality after transcatheter aortic valve replacement:A PARTNER trial substudy. Catheter Cardiovasc Interv. 2015:316-322.
28. Singh V, Damluji AA, Mendirichaga R, et al. Elective or Emergency Use of Mechanical Circulatory Support Devices During Transcatheter Aortic Valve Replacement. J Interv Cardiol. 2016;29:513-522.
29. Baumgartner H., Falk V., Bax JJ., et al. 2017 ESC/EACTS Guidelines for the management of valvular heart disease. Eur Heart J. 2017;38:2739-2791.
30. Saia F., Marrozzini C., Ciuca C., et al. Emerging indications, in-hospital and long-term outcome of balloon aortic valvuloplasty in the transcatheter aortic valve implantation era. Eurointervention. 2013;8:1388-1397.
31. Ram P., Mezue K., Pressman G., Rangaswami J. Acute kidney injury post-transcatheter aortic valve replacement. Clin Cardiol. 2017;40:1357-1362.
32. Wang J., Yu W., Zhou Y., et al. Independent Risk Factors Contributing to Acute Kidney Injury According to Updated Valve Academic Research Consortium-2 Criteria After Transcatheter Aortic Valve Implantation:A Meta-analysis and Meta-regression of 13 Studies. J Cardiothor Vasc An. 2017;31:816-826.
33. Putzu A, Berto MB, Belletti A, et al. Prevention of contrast-induced acute kidney injury by furosemide with matched hydration in patients undergoing interventional procedures:a systematic review and meta-analysis of randomized trials. JACC Cardiovasc Interv. 2017;10:355-363.