Sr. Editor:
El implante percutáneo de válvula aórtica (TAVI) es una técnica consolidada para el tratamiento de la estenosis aórtica grave sintomática.
La fragilidad es un síndrome clínico multidimensional que indica una vulnerabilidad del paciente ante eventos adversos. Su evaluación es compleja, con múltiples escalas disponibles para su valoración: Fried scale con parámetros como la pérdida de peso o la fuerza de agarre; Short Physical Performance Battery (SPPB), que evalúa el equilibrio, la velocidad de la marcha y levantarse de una silla; y otras como Essential Frailty Toolset, Clinical Frailty Scale, etc.1. Además de las características clásicas, como la edad y la comorbilidad, es clave valorar la fragilidad antes de indicar la intervención sobre la válvula, ya que esta se correlaciona con el pronóstico posterior al TAVI2.
En los pacientes con fragilidad leve o grave, la toma de decisión sobre la intervención es más clara. Sin embargo, los pacientes con fragilidad moderada –definida como la presencia de uno o dos criterios de fragilidad– representan un grupo intermedio entre la robustez y la fragilidad avanzada. Estos pacientes presentan un riesgo moderado de caídas, discapacidad, hospitalización y mortalidad, así como una mayor probabilidad de progresar hacia una fragilidad grave en los siguientes años3.
Nos propusimos evaluar las características y el pronóstico de los pacientes con fragilidad moderada tratados con TAVI, para lo cual llevamos a cabo un estudio retrospectivo unicéntrico de pacientes con estenosis aórtica grave sintomática y fragilidad moderada, a quienes se realizó un TAVI entre 2016 y 2023. Los eventos analizados fueron la mortalidad global, los reingresos por cualquier causa y la descompensación de insuficiencia cardiaca (IC). El estudio fue aprobado por el comité de ética de nuestro hospital (n.º 2019/8735/I).
El servicio de geriatría hace una evaluación integral, clasificando la fragilidad en leve, moderada o grave. Para valorar la fragilidad en pacientes con estenosis aórtica grave candidatos a TAVI utilizamos la escala SPPB4 por su alta capacidad para discriminar entre pacientes robustos y frágiles de forma rápida y objetiva, permitiendo identificar la fragilidad no reversible. La SPPB ofrece más precisión que otras escalas para predecir eventos adversos y reingresos, y es sencilla de aplicar en la práctica clínica. Se definió fragilidad moderada como una puntuación < 10 en la SPPB, así como dependencia para las actividades instrumentales y dependencia leve para las actividades básicas de la vida diaria, deterioro cognitivo leve-moderado y riesgo de desnutrición.
De los 306 pacientes evaluados, se excluyeron aquellos con fragilidad grave, comorbilidad mayor o rechazo del procedimiento, y recibieron un tratamiento conservador. Se incluyeron 236 pacientes que recibieron un TAVI; de estos, 54 presentaban fragilidad moderada y constituyeron la cohorte de estudio.
Se recogieron datos clínicos, funcionales y analíticos en el momento del procedimiento. Las variables se analizaron con las pruebas χ2 o Fisher para las variables categóricas, y con las pruebas t de Student o no paramétricas para las variables continuas. Se empleó el método de Kaplan-Meier para analizar la relación entre la IC previa y los eventos de mortalidad, descompensación de la IC y reingreso hospitalario. Las curvas de supervivencia se compararon mediante log-rank. La IC previa se analizó como posible factor independien- te de pronóstico mediante un modelo de regresión de Cox, ajustado por variables clínicamente relevantes: diabetes mellitus, fracción de eyección del ventrículo izquierdo previa al TAVI, enfermedad renal crónica y cardiopatía isquémica.
La edad media fue de 83,4 ± 4 años, con predominio del sexo femenino (81,5%) y un índice de Barthel medio de 89. La comorbilidad más frecuente consistió en hipertensión arterial (94,5%), enfermedad renal crónica en estadio ≥ 3 (50%), diabetes mellitus (22,2%), fibrilación auricular (44,4%) y cardiopatía isquémica (31,5%). La fracción de eyección del ventrículo izquierdo media fue del 60 ± 10%. Un 59,3% tenían diagnóstico previo de IC congestiva y había requerido tratamiento diurético intravenoso.
Respecto a la clínica que motivó la indicación de TAVI, el 48,2% presentaron IC congestiva, el 40,7% disnea sin congestión, el 7,4% angina de pecho y el 3,7% síncope.
Durante un seguimiento medio de 25,5 meses se documentaron 26 fallecimientos (48,1%), con causa cardiovascular como la más frecuente (51,9%). La mediana de tiempo hasta el fallecimiento fue de 24 meses [10,5-41,5]. Un 57,4% de los pacientes reingresaron, siendo el principal motivo la infección (24,1%); un 42,6% presentaron descompensación de la IC y requirieron diurético intravenoso.
En el análisis de variables, solo el antecedente de IC se asoció de manera significativa con mayor mortalidad global, reingresos por cualquier causa y mayor riesgo de descompensación de la IC durante el seguimiento (tabla 1). La curva de Kaplan-Meier mostró una mayor proporción de descompensaciones en pacientes con IC previa al seguimiento (figura 1). No se alcanzó significación estadística para la mortalidad ni para el reingreso. En el análisis multivariado, la IC previa fue la única variable asociada de manera significativa con el evento de descompensación de la IC (razón de riesgos ajustada, 5,4; intervalo de confianza del 95%, 1,2-24,1; p < 0,026).
Tabla 1. Características clínicas asociadas a eventos tras un TAVI en pacientes con fragilidad moderada (n = 54)
| Variable | Evento combinado |
Sin evento combinado (n = 15) | p |
|---|---|---|---|
| Sexo femenino, n (%) | 32 (82,1) | 12 (80) | 1 |
| Comorbilidad cardiovascular, n (%) | |||
| Hipertensión arterial | 37 (94,9) | 14 (93,3) | 1 |
| Diabetes mellitus | 11 (28,2) | 1 (6,7) | 0,145 |
| Dislipemia | 19 (48,7) | 11 (73,3) | 0,133 |
| Cardiopatía isquémica | 12 (70,6) | 6 (29,4) | 1 |
| Fibrilación auricular | 19 (48,7) | 5 (33,3) | 0,28 |
| Insuficiencia cardiaca previa | 28 (71,8) | 4 (26,7) | 0,003 |
| Valvuloplastia previa | 9 (23,1) | 6 (40) | 0,309 |
| Otra comorbilidad, n (%) | |||
| EPOC | 8 (20,5) | 3 (20) | 1 |
| SAHS | 4 (10,3) | 1 (6,7) | 1 |
| ERC (FG < 60) | 19 (48,7) | 8 (53,3) | 0,761 |
| ACV | 6 (15,4) | 2 (13,3) | 1 |
| Vasculopatía periférica | 4 (10,3) | 1 (6,7) | 1 |
| Neoplasia | 3 (7,7) | 3 (20) | 0,331 |
| Aspectos funcionales y cognitivos, n (%) | |||
| Vive solo/a | 14 (35,9) | 2 (13,3) | 0,182 |
| Deterioro cognitivo | 5 (12,8) | 6 (40) | 0,054 |
| Procedimiento TAVI, n (%) | |||
| Complicaciones intraprocedimiento | 21 (53,8) | 6 (40) | 0,362 |
| Implante de marcapasos tras TAVI | 7 (17,9) | 2 (13,3) | 1 |
|
ACV: accidente cerebrovascular; EPOC: enfermedad pulmonar obstructiva crónica; ERC: enfermedad renal crónica (filtrado glomerular < 60 ml/min/1,73 m²); SAHS: síndrome de apnea-hipopnea del sueño; TAVI: implante percutáneo de válvula aórtica. * Evento combinado: ingreso, descompensación de insuficiencia cardiaca o fallecimiento. |
|||
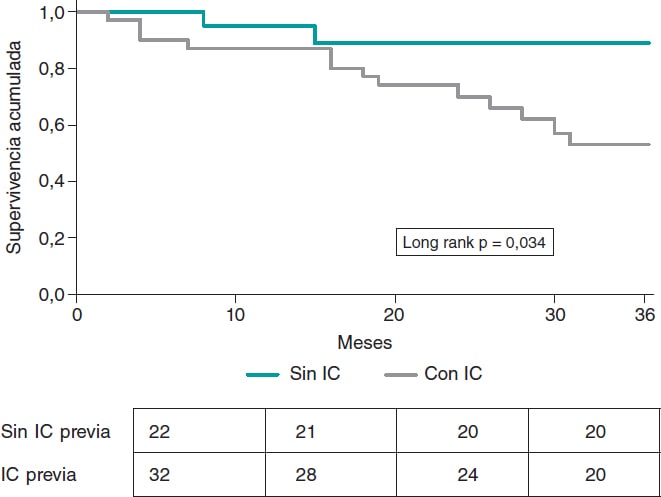
Figura 1. Curva de Kaplan-Meier para el evento de descompensación de la insuficiencia cardiaca (IC) durante el seguimiento, según la presencia de IC previa.
La IC se asocia a mayores mortalidad y tasa de reingresos tras el TAVI5. Las puntuaciones de riesgo propuestas por las guías de la Sociedad Europea de Cardiología para la valoración antes del TAVI (FRANCE-2 Risk Score y Partner Risk Score) no incluyen la IC previa como factor de riesgo, aunque FRANCE-2 considera la clase funcional IV de la New York Heart Association como un factor de futilidad tras un TAVI. Incluso el CAPRI risk score6, que predice el riesgo de IC tras un TAVI según la comorbilidad y los parámetros ecocardiográficos, tampoco la contempla.
En el grupo de pacientes con fragilidad moderada, en los que la toma de decisiones clínicas resulta compleja, es fundamental identificar factores que predigan una evolución desfavorable tras el TAVI. No obstante, la evidencia disponible sobre este aspecto es limitada. Nuestros resultados coinciden con estudios previos al mostrar que el antecedente de IC congestiva se asocia de manera significativa con un mayor riesgo de reingreso por IC durante el seguimiento tras el TAVI.
La identificación de este subgrupo con alto riesgo de nuevas descompensaciones permitiría individualizar el seguimiento y optimizar la conducta en el posoperatorio, con el objetivo de prevenir eventos adversos y mejorar el pronóstico. Son necesarios estudios con mayor tamaño muestral y diseño prospectivo para confirmar estos hallazgos y fortalecer la evidencia. A pesar de estas limitaciones, nuestro estudio subraya la importancia del antecedente de IC congestiva como predictor clave del desarrollo de IC tras un TAVI en los pacientes frágiles.
FINANCIACIÓN
No se ha recibido financiación por la redacción de este artículo.
CONSIDERACIONES ÉTICAS
Este estudio cumple con las consideraciones éticas pertinentes, y fue evaluado y aprobado por el Comité de Ética del Hospital del Mar (Barcelona) en diciembre de 2019 (Proyecto de investigación 2019/8735/I). Confirmamos que se obtuvo, y está archivado, el consentimiento informado de los pacientes para la publicación de su caso. Asimismo, confirmamos que se han seguido las directrices SAGER adecuadamente. Se ha considerado el sexo/género de los participantes como una variable potencialmente relevante, y se ha comunicado dicha información de manera transparente. También se ha analizado si existían diferencias significativas según sexo/género, y se ha informado cuando ha sido pertinente.
DECLARACIÓN SOBRE EL USO DE INTELIGENCIA ARTIFICIAL
No se han empleado herramientas de inteligencia artificial para la redacción del texto.
CONTRIBUCIÓN DE LOS AUTORES
C. Belmonte Herrera: recopilación y gestión de datos, redacción de artículo. D.M. Rojas Aguirre: recopilación y gestión de datos. L.C. Belarte Tornero: análisis estadístico. S. Ruiz Bustillo: validación y revisión. B. Vaquerizo Montilla: validación y revisión. S. Valdivielso Moré: definición del estudio, validación y revisión.
CONFLICTO DE INTERESES
No existen conflictos de intereses.
AGRADECIMIENTOS
A todo el equipo de cardiología del Hospital del Mar, en especial a la unidad de insuficiencia cardiaca del servicio de cardiología.
BIBLIOGRAFÍA
1. Chung KJNC, Wilkinson C, Veerasamy M, Kunadian V. Frailty Scores and Their Utility in Older Patients with Cardiovascular Disease. Interv Cardiol. 2021;16:e05.
2. Li Z, Dawson E, Moodie J, et al. Measurement and prognosis of frail patients undergoing transcatheter aortic valve implantation:a systematic review and meta-analysis. BMJ Open. 2021;11:e040459.
3. Fried LP, Tangen CM, Walston J, et al. Frailty in older adults:evidence for a phenotype. J Gerontol A Biol Sci Med Sci. 2001;56:M146-56.
4. Guralnik JM, Simonsick EM, Ferrucci L, et al. A short physical performance battery assessing lower extremity function:association with self-reported disability and prediction of mortality and nursing home admission. J Gerontol. 1994;49:M85-M94.
5. Nilsson K, Buccheri S, Christersson C, et al. Causes, pattern, predictors, and prognostic implications of new hospitalizations after transcatheter aortic valve implantation:a long-term nationwide observational study. Eur Heart J Qual Care Clin Outcomes. 2022;8:150-160.
6. Harbaoui B, Durand E, DupréM, et al. Significance of the CAPRI risk score to predict heart failure aahospitalization post-TAVI:The CAPRI-HF study. Int J Cardiol. 2019;296:98-102.

