Sr. Editor:
Las fístulas entre la aorta y las aurículas son una patología extremadamente rara en la que se establece una conexión anómala entre las estructuras aórticas y las aurículas cardiacas. En concreto, las fístulas entre la aorta y la aurícula izquierda (Ao-AI) son particularmente poco comunes y están asociadas, principalmente, a complicaciones tales como endocarditis infecciosas, abscesos periprotésicos, disecciones aórticas y cirugías cardiacas con, a menudo, afectación de la válvula o la raíz aórtica1. Presentamos el caso de un paciente con una fístula Ao-AI iatrogénica tratada con éxito con un dispositivo percutáneo Amplatzer.
Se trata de un hombre de 82 años hospitalizado con un cuadro de insuficiencia cardiaca aguda. Tres semanas antes, había sido intervenido por cirugía cardiaca con reparación de las válvulas mitral y tricúspide mediante doble anuloplastia y revascularización mediante un puente de arteria mamaria interna a la descendente anterior.
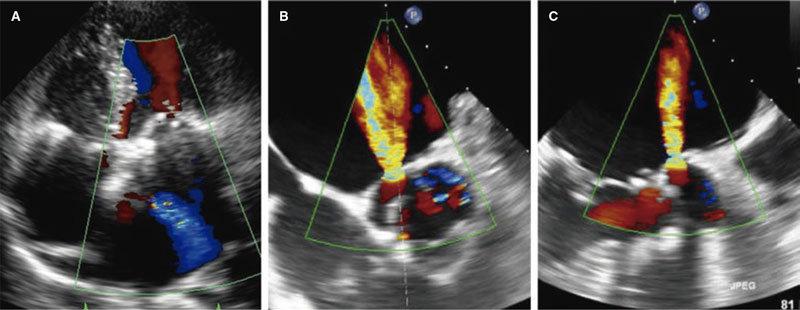
El ecocardiograma transtorácico reveló la presencia de una función biventricular y valvular conservada, pero también un flujo anomalo sistólico y diastólico en la aurícula izquierda (figura 1A y vídeo 1 del material adicional). En el ecocardiograma transesofágico, este flujo se debía a una fístula Ao-AI a través del seno aórtico no coronario con un shunt significativo a su través (figura 1B-C y vídeo 2 del material adicional). No se apreciaban imágenes sugestivas de endocarditis infecciosa. Los hemocultivos repetidos fueron negativos para cualquier tipo de crecimiento bacteriano. La tomografía computarizada vino a confirmar estos hallazgos, aunque los artefactos metálicos derivados de la anuloplastia mitral impidieron la reconstrucción en 3D. El paciente fue considerado de alto riesgo para reintervención quirúrgica por el equipo multidisciplinar, y fue tratado inicialmente con fármacos. No obstante, a pesar de tratamiento médico óptimo, reingresó 2 veces durante los siguientes 3 meses. Fue, entonces, cuando se optó por el manejo intervencionista de la fístula. El paciente dió su consentimiento informado por escrito.
Figura 1. Imagen del ecocardiograma transtorácico (A) y transesofágico (B, C) que muestra un flujo de alta velocidad procedente del seno no coronario de Valsalva en dirección a la aurícula izquierda.
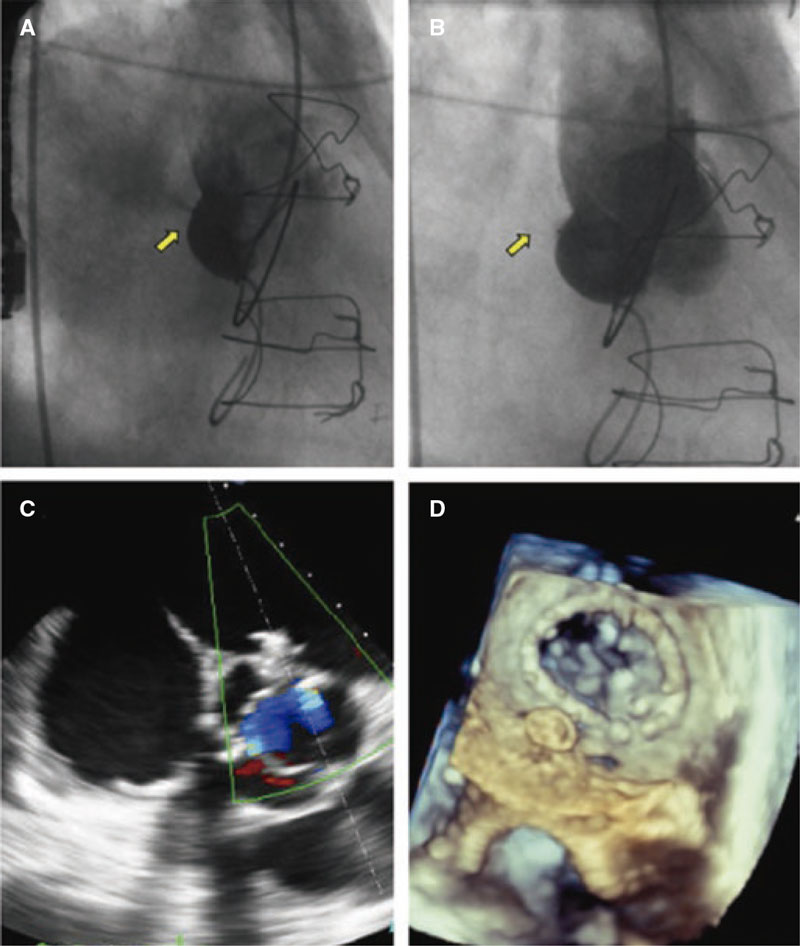
Se intentó el abordaje percutáneo bajo anestesia general empleando un acceso retrógrado a través de la arteria femoral derecha. La angiografía inicial realizada con un catéter guía Judkins derecho de 6 Fr (Medtronic, Estados Unidos) reveló la presencia de abundante paso de contraste desde el seno no coronario a la aurícula izquierda (figura 2A y vídeo 3 del material adicional). A continuación, se cruzó una guía Sion Blue (Asahi Intecc, Tailandia) a la aurícula izquierda y sobre esta se avanzó el catéter guía Judkins derecho hacia el interior de la aurícula para usarlo a modo de sistema de liberación. Se implantó con éxito un dispositivo de cierre Amplatzer Duct Occluder II de 6 mm (Abbott, Estados Unidos) con confirmación mediante angiografía (figura 2B y vídeo 4 del material adicional) y ecocardiografía transesofágica (figura 2C-D y vídeos 5 y 6 del material adicional) del cierre casi completo de la fístula. Aunque el paciente ya estaba crónicamente anticoagulado por presentar fibrilación auricular permanente, se decidió tratamiento combinado empírico añadiendo 100 mg de ácido acetilsalicílico durante 6 meses. No hubo ninguna complicación a los 6 meses y el paciente permaneció en clase funcional I sin shunt residual en el ecocardiograma 2D realizado al mes de la intervención.
Figura 2. A: aortografía basal con llenado de la aurícula izquierda a través de la fístula (flecha). D: ausencia de paso de contraste tras colocación del dispositivo Amplatzer Duct Occluder II (flecha). E, F: dispositivo Amplatzer colocado sin presencia de shunt en los planos que ofrece la ecografía Doppler color y la ecocardiografía transesofágica 3D.
Las fístulas que se localizan entre la aorta y las aurículas son una patología rara, siendo la cirugía cardiaca una causa reconocida1. En particular, las fístulas entre la aorta y la aurícula izquierda son sumamente raras y sobrevienen con mayor frecuencia tras cirugías aórticas que tras cirugías de revascularización coronaria. Hasta la fecha, jamás se han descrito casos asociados a reparaciones de la válvula mitral1. El flujo anómalo entre la aorta y la aurícula izquierda a menudo conduce a una sobrecarga de volumen y al desarrollo de signos y síntomas de insuficiencia cardiaca2. La detección y diagnóstico precocesde esta grave patología dependen de su caracterización ecocardiográfica, siendo el ecocardiograma transesofágico la técnica de imágen por excelencia para su diagnóstico. La combinación con técnicas de imágen en 3D, ya sea la ecocardiografía transesofágica o la tomografía computarizada, es altamente recomendable siempre que sea posible, ya que ofrecen orientación espacial y una alta definición anatómica a efectos de planificar la intervención3. La evaluación también puede incluir la resonancia magnética cardiaca o el cateterismo cardíaco para cuantificar el shunt de manera adicional4.
Debido a la baja incidencia de las fístulas entre la aorta y las aurículas, las estrategias de tratamiento dependen de la enfermedad de base, y las intervenciones se basan en las opiniones de los expertos y en el consenso entre los médicos tratantes. No obstante, se recomienda el cierre de la fístula en pacientes sintomáticos5. Aunque la cirugía es el tratamiento estándar, el cierre percutáneo es una opción que considerar en pacientes de alto riesgo con características angiográficas favorables como la localización en el seno no coronario o en fístulas de pequeño diámetro1. En ausencia de material percutáneo específico, el fuera de ficha técnica de un dispositivo Amplatzer Duct Occluder II bajo guia ecocardiográfica y fluoroscópica simultánea es una opción viable tal y como ilustra nuestro caso y otros casos aislados descritos en la literatura6,7. Tras implantar el dispositivo se recomienda el uso de terapia antiagregante /anticoagulante, aunque la evidencia en torno al régimen antitrombótico óptimo y la duración del mismo sigue siendo empírica.
En conclusión, aunque raras, las fístulas entre la aorta y las aurículas son una complicación grave capaz de provocar insuficiencia cardiaca refractaria. Es necesario con frecuencia, cerrar el trayecto fistuloso. La evidencia disponible a este respecto es escasa y se basa, únicamente, en casos clínicos o series de casos2,6. Se necesita más información para definir mejor las estrategias terapéuticas óptimas en este escenario.
FINANCIACIÓN
M. Tamargo declaró haber recibido financiación parcial de subvenciones concedidas por la Fundación para la Investigación Biomédica Gregorio Marañón (Madrid) y CM20/00054 del Instituto de Salud Carlos III (Madrid).
CONTRIBUCIÓN DE LOS AUTORES
Todos los autores han contribuido por igual al artículo.
CONFLICTO DE INTERESES
Ninguno.
MATERIAL ADICIONAL
Vídeo 1. Tamargo M. DOI: 10.24875/RECIC.M23000387
Vídeo 2. Tamargo M. DOI: 10.24875/RECIC.M23000387
Vídeo 3. Tamargo M. DOI: 10.24875/RECIC.M23000387
Vídeo 4. Tamargo M. DOI: 10.24875/RECIC.M23000387
Vídeo 5. Tamargo M. DOI: 10.24875/RECIC.M23000387
Vídeo 6. Tamargo M. DOI: 10.24875/RECIC.M23000387
BIBLIOGRAFÍA
1. Fierro EA, Sikachi RR, Agrawal A, Verma I, Ojrzanowski M, Sahni S. Aorto-Atrial Fistulas: A Contemporary Review. Cardiol Rev. 2018;26:137-144.
2. Foster TJ, Amin AH, Busu T, et al. Aorto-cardiac fistula etiology, presentation, and management: A systematic review. Heart Lung. 2020;49:317-323.
3. Patel V, Fountain A, Guglin M, Nanda NC. Three-Dimensional Transthoracic Echocardiography in Identification of Aorto-Right Atrial Fistula and Aorto-Right Ventricular Fistulas. Echocardiography. 2010;27:E105-E108.
4. Valsangiacomo Buechel ER, Grosse-Wortmann L, Fratz S, et al. Indications for cardiovascular magnetic resonance in children with congenital and acquired heart disease: an expert consensus paper of the Imaging Working Group of the AEPC and the Cardiovascular Magnetic Resonance Section of the EACVI. Eur Heart J Cardiovasc Imaging. 2015;16:281-297.
5. Jainandunsing JS, Linnemann R, Maessen J, et al. Aorto-atrial fistula formation and therapy. J Thorac Dis. 2019;11:1016-1021.
6. Alkhouli M, Almustafa A, Kawsara A, et al. Transcatheter closure of an aortoatrial fistula following a surgical aortic valve replacement. J Card Surg. 2017;32:186-189.
7. Hernández García JM, Alonso-Briales JH, Jiménez-Navarro MF, Cabrera-Bueno F, González-Cocina E, Such-Martínez M. Transcatheter Closure of Aorto-Left Atrial Fistula Using an Amplatzer Device. Rev Esp Cardiol. 2005;58:1121-1123.