RESUMEN
Introducción y objetivos: Valorar el impacto del sangrado en la relación riesgo-beneficio de la revascularización coronaria previa al implante percutáneo de válvula aórtica por vía transfemoral (TAVI-TF).
Métodos: Se realizó un análisis retrospectivo de los pacientes tratados con TAVI-TF en nuestro centro entre los años 2008 y 2018, y se identificó la actuación sobre su enfermedad coronaria (revascularización percutánea frente a no revascularización). Posteriormente, se comparó entre ambos grupos la incidencia de sangrado mayor, definido por los criterios del Bleeding Academic Research Consortium (BARC) (tipos 3-5), y de eventos cardiovasculares adversos mayores (MACE) isquémicos durante un seguimiento medio de 60 meses.
Resultados: Se incluyeron 379 pacientes. La incidencia total de sangrado mayor fue del 21,4%, más alta en los pacientes con revascularización, pero sin alcanzar la significación estadística. La incidencia global de sangrado mayor entre la coronariografía diagnóstica y el TAVI fue del 5,5%, y resultó significativamente más alta en los pacientes revascularizados (12,0% frente a 3,5%; p = 0,07). Durante el ingreso para el TAVI-TF y el seguimiento posterior de 60 meses, la incidencia global de sangrado mayor fue del 6,1% y del 9,6%, respectivamente, sin diferencias significativas entre ambos grupos. Tampoco hubo diferencias en la incidencia de MACE a los 5 años de seguimiento.
Conclusiones: En nuestra cohorte de pacientes, la revascularización coronaria previa al TAVI-TF conlleva un aumento inicial del riesgo de sangrado, sin diferencias estadísticamente significativas en sangrado mayor ni en MACE en el seguimiento a 5 años. Estos hallazgos apoyan la necesidad de generar una evidencia clínica de calidad que demuestre un beneficio clínico neto de la revascularización en este contexto.
Palabras clave: Implante percutáneo de válvula aórtica. Revascularización coronaria. Sangrados.
ABSTRACT
Introduction and objectives: To evaluate the impact of bleeding on the risk-benefit balance of coronary revascularization prior to transfemoral transcatheter aortic valve implantation (TF-TAVI).
Methods: We conducted a retrospective analysis of the patients who underwent TF-TAVI at our center between 2008 and 2018 to evalute the management of coronary artery disease (percutaneous revascularization vs no revascularization). Subsequently, the rate of major bleeding —defined according to the Bleeding Academic Research Consortium (BARC) criteria (type 3-5)— and major adverse cardiovascular events (MACE) was compared between the 2 groups over a mean 60-month follow-up period.
Results: A total of 379 patients were included. The overall rate of major bleeding was 21.4%, higher in revascularized patients but without reaching statistical significance. The rate of major bleeding between coronary angiography and TF-TAVI implantation was 5.5% and significantly higher in revascularized patients (12.0% vs 3.5%; P = .07). During the hospitalization for TF-TAVI and throughout follow-up, the rate of major bleeding was 6.1% and 9.6%, respectively, with no significant inter-group differences. There were no significant differences either in the 5-year rate of MACE.
Conclusions: In our patient cohort, pre-TF-TAVI preoperative coronary revascularization was associated with an initially higher bleeding risk; however, no statistically significant differences were observed in major bleeding or MACE at the 5-year follow-up. These findings support the need to generate high-quality clinical evidence to demonstrate the net clinical benefit of coronary revascularization in this context.
Keywords: Transcatheter aortic valve implantation. Coronary revascularization. Bleeding.
Abreviaturas
MACE: eventos cardiovasculares adversos mayores. TAVI-TF: implante percutáneo de válvula aórtica por vía transfemoral.
INTRODUCCIÓN
En la actualidad, el implante percutáneo de válvula aórtica por vía transfemoral (TAVI-TF) es el tratamiento de elección para la mayoría de los pacientes con estenosis aórtica grave, especialmente para aquellos con riesgo quirúrgico alto o de edad avanzada1. Existen varios ensayos clínicos en los que se evidencian unos hallazgos clínicos similares entre el TAVI-TF y el recambio valvular aórtico quirúrgico2-4. El sangrado, tanto mayor como menor, sigue siendo una de las complicaciones más frecuentes del procedimiento, y además se asocia a mayores tasas de morbimortalidad5. En los últimos años, gracias a la mejora de los materiales (disminución del calibre necesario para realizar el implante) y a la creciente experiencia de los operadores, se ha conseguido disminuir de manera importante las tasas de sangrado periprocedimiento, pero siguen siendo altas. Entre los principales factores de riesgo de sangrado se encuentra la necesidad de uso de doble terapia antiagregante periprocedimiento6, cuyo principal escenario clínico es la revascularización coronaria percutánea asociada al procedimiento de TAVI.
Adicionalmente, la alta prevalencia de enfermedad arterial coronaria en los pacientes que van a recibir un TAVI-TF, que según las series publicadas puede llegar hasta el 80%, unida a la actual recomendación de las guías de práctica clínica de revascularizar todas las lesiones ≥ 70% en los segmentos coronarios proximales, conllevan una alta incidencia de revascularización1.
Nuestro grupo de trabajo ha publicado recientemente datos que evidencian que la revascularización sistemática completa en los pacientes a quienes se realiza un TAVI-TF no implica un beneficio pronóstico en términos de mortalidad ni de eventos cardiovasculares adversos mayores (MACE) (combinado de muerte, infarto, ictus y hospitalización por insuficiencia cardiaca)7. Dada la alta tasa de eventos hemorrágicos en dichos pacientes, consideramos de gran interés clínico evaluar si la revascularización puede conllevar un mayor riesgo de estos, así como su impacto clínico6.
MÉTODOS
Se llevó a cabo un estudio retrospectivo basado en la cohorte histórica de pacientes a quienes se realizó un procedimiento de TAVI-TF entre los años 2008 y 2018 en nuestro centro. La información para el estudio se extrajo de la base de datos local (Géminis) y se complementó con la revisión de las historias clínicas para los eventos durante el seguimiento. El estudio fue aprobado por el Comité de Ética en la Investigación Clínica de A Coruña-Ferrol. El objetivo fue comparar la incidencia de sangrado mayor, definido por los criterios del Bleeding Academic Research Consortium (BARC) (tipos 3-5), desde la coronariografía diagnóstica, durante el ingreso para el implante valvular y en el seguimiento posterior, así como la de MACE y la del evento combinado de MACE y sangrado mayor en el mismo periodo, en los pacientes a quienes se realizó revascularización coronaria percutánea en comparación con los tratados de forma conservadora.
Análisis estadístico
En el estudio, las variables continuas se presentan como media y desviación estándar, y las variables cualitativas como proporciones. En las variables continuas se aplicaron las pruebas t de Student y de análisis de la varianza (ANOVA) con contraste polinomial de primer orden. En las variables cualitativas, para la comparación de las características basales entre las diferentes categorías se emplearon la prueba χ2 de tendencia lineal y la prueba exacta de Fisher si correspondía.
Se realizó un análisis de la supervivencia mediante el modelo de riesgos proporcionales de Cox para determinar si existía asociación entre la revascularización coronaria y el pronóstico de los pacientes en términos de mortalidad, MACE, sangrado mayor (BARC 3-5) y evento combinado de MACE y sangrado mayor. Los resultados se representaron mediante gráficas ajustadas por edad y sexo.
El análisis estadístico se efectuó con SPSS 26.0 (IBM, EE.UU.) y R versión 4.1.3 (R Foundation for Statistical Computing, Austria). El nivel de significación estadística se fijó en p < 0,05 para todos los contrastes.
RESULTADOS
Se incluyeron 379 pacientes que recibieron un TAVI-TF entre 2008 y 2018. De ellos, se produjeron 4 pérdidas en el seguimiento, por lo que finalmente la muestra fue de 375 pacientes para el análisis estadístico. La tabla 1 muestra las características basales de los pacientes, con una edad media de 83,1 años, predominio del sexo femenino (58,0%) y riesgo quirúrgico intermedio (Society of Thoracic Surgeons score 4,3%). Si bien la mayoría de las características basales estaban bien balanceadas entre los pacientes con y sin revascularización, los no revascularizados tenían un riesgo quirúrgico ligeramente mayor (4,5% frente a 3,5%) y un porcentaje más alto de mujeres (61,3% frente a 47,8%).
Tabla 1. Características basales de los pacientes
| Variable | No revascularizados | Revascularizados | Total | p |
|---|---|---|---|---|
| Edad, años | 84 (5,5) | 82 (6,7) | 83,1 (5,9) | 0,015 |
| Sexo femenino | 176 (61,3%) | 44 (47,8%) | 220 (58,0%) | 0,022 |
| Diabetes | 83 (28,9%) | 36 (39,1%) | 119 (31,4%) | 0,066 |
| Hipertensión arterial | 219 (76,3%) | 73 (79,3%) | 292 (77,0%) | 0,546 |
| Hipercolesterolemia | 165 (57,5%) | 65 (70,7%) | 230 (60,6%) | 0,025 |
| Índice de masa corporal | 29,6 (5,2) | 28,3 (5,5) | 29,3 (5,3) | 0,032 |
| Hemoglobina basal (mg/dl) | 12,1 (1,6) | 11,8 (1,8) | 12,1 (1,7) | 0,160 |
| Aclaramiento creatinina (ml/min) | 55,7 (20,9) | 53,6 (21,4) | 55,2 (21,0) | 0,420 |
| STS score | 4,5% (2,5) | 3,5% (3,8) | 4,3% (2,9) | 0,002 |
| EuroSCORE I | 13,3% (7,8) | 8,6% (5,2) | 12,2% (7,5) | 0,001 |
| EuroSCORE II | 4,4% (3,4) | 2,6% (1,9) | 4,0% (3,2) | 0,001 |
| FEVI basal | 59,7% (13,2) | 56,9% (13,5) | 59,0% (13,3) | 0,083 |
| Gmáx basal (mmHg) | 80,6 (25,0) | 79,1 (22,2) | 80,3 (24,4) | 0,602 |
| Gmed basal (mmHg) | 47,1 (15,4) | 47,2 (14,0) | 47,1 (15,0) | 0,952 |
| Insuficiencia aórtica basal | 0,384 | |||
| 0 | 69 (24,2%) | 23 (25,6%) | 92 (24,3%) | |
| 1 | 151 (53,0%) | 54 (60,0%) | 205 (54,0%) | |
| 2 | 46 (16,1%) | 11 (12,2%) | 57 (15,0%) | |
| 3 | 15 (5,3%) | 1 (1,1%) | 16 (4,2%) | |
| 4 | 4 (1,4%) | 1 (1,1%) | 5 (1,3%) | |
| Síntomas de angina | 45 (15,7%) | 23 (25,0%) | 68 (17,9%) | 0,043 |
| Grado NYHA | 0,278 | |||
| 1 | 1 (0,3%) | 1 (1,1%) | 2 (0,5%) | |
| 2 | 41 (14,3%) | 19 (20,7%) | 60 (15,8%) | |
| 3 | 221 (77,0%) | 62 (67,4%) | 283 (74,7%) | |
| 4 | 24 (8,4%) | 10 (10,9%) | 34 (8,9%) | |
| IAM previo | 32 (11,3%) | 21 (23,1%) | 53 (14,0%) | 0,005 |
| CABG previa | 18 (6,3%) | 6 (6,6%) | 24 (6,3%) | 0,931 |
| ICP previa | 24 (8,5%) | 75 (82,4%) | 99 (26,1%) | 0,001 |
| ACV | 26 (9,2%) | 8 (8,9%) | 34 (9,0%) | 0,932 |
| Hepatopatía | 8 (2,8%) | 1 (1,1%) | 9 (2,4%) | 0,351 |
| EPOC | 39 (13,7%) | 7 (7,7%) | 46 (12,1%) | 0,126 |
| Arteriopatía periférica | 9 (3,1%) | 5 (5,4%) | 14 (3,7%) | 0,309 |
| Tratamiento AVK | 83 (29,2%) | 21 (23,1%) | 104 (27,4%) | 0,254 |
| Tratamiento ACOD | 11 (3,9%) | 3 (3,3%) | 14 (3,7%) | 0,801 |
|
ACOD: anticoagulantes de acción directa; ACV: accidente cerebrovascular; AVK: antagonista de la vitamina K; CABG: cirugía de revascularización coronaria; EPOC: enfermedad pulmonar obstructiva crónica; FEVI: fracción de eyección del ventrículo izquierdo; Gmáx: gradiente máximo; Gmed: gradiente medio; IAM: infarto agudo de miocardio; ICP: intervención coronaria percutánea; NYHA: New York Heart Association; STS: Society of Thoracic Surgeons. |
||||
Con respecto a los síntomas, la mayoría de los pacientes estaban en clase funcional III de la New York Heart Association (74,7%). De los pacientes revascularizados, el 25,0% presentaban síntomas de angina (23 pacientes), y de los no revascularizados, únicamente el 15,7% (41 pacientes). En cuanto al tratamiento anticoagulante, de los pacientes no revascularizados el 29,2% (83 pacientes) tomaban fármacos antagonista de la vitamina K y el 3,9% (11 pacientes) anticoagulantes orales directos. Estos porcentajes eran ligeramente menores en los pacientes con revascularización, con el 23,1% (21 pacientes) en tratamiento previo con fármacos antagonista de la vitamina K y el 3,3% (3 pacientes) con anticoagulantes orales directos (tabla 1).
Revascularización percutánea y sangrados
De los pacientes con TAVI-TF, 92 (24,3%) recibieron revascularización coronaria, que en nuestro centro se realizó siempre previamente a la sustitución valvular, con una mediana de 88 días (46-162) entre la revascularización y el TAVI, por lo que, en general, los pacientes mantenían tratamiento con terapia antiplaquetaria dual en el momento del procedimiento. La decisión con respecto a la revascularización se tomaba en sesión multidisciplinaria de acuerdo con las guías de práctica clínica del momento (entre 2008 y 2018). La tendencia era revascularizar la mayor parte de las lesiones coronarias, y el criterio clínico no cambió a lo largo del seguimiento.
Los resultados con respecto a los eventos clínicos en el seguimiento se muestran en la tabla 2. No se observaron diferencias estadísticamente significativas en el tiempo transcurrido entre el cateterismo y el TAVI entre ambos grupos (mediana de 118 días en los revascularizados frente a 123 días en los no revascularizados, p = 0,835). Como puede verse en la figura 1, la incidencia total de sangrado mayor fue del 21,4% (81/375), con una incidencia del 28,3% en los pacientes con revascularización (26/92) y del 19,0% en los no revascularizados (55/283), sin alcanzar la significación estadística (p = 0,074).
Tabla 2. Eventos clínicos durante el seguimiento según el estado de revascularización
| Evento clínico | No revascularizados, n (%) | Revascularizados n (%) | Total, n (%) | p |
|---|---|---|---|---|
| Sangrado mayor (BARC 3-5) | 55 (19,0%) | 26 (28,3%) | 81 (21,4%) | 0,074 |
| MACE 60 meses | 160 (55,7%) | 49 (53,2%) | 209 (55,1%) | 0,082 |
| MACE pre-TAVI | 58 (20,4%) | 25 (27,2%) | 83 (22,1%) | NS |
| Mortalidad a 60 meses | 125 (43,7%) | 36 (39,0%) | 161 (42,2%) | NS |
| IAM a 60 meses | 8 (2,8%) | 10 (11,5%) | 18 (4,8%) | 0,001 |
| Revascularización a 60 meses | 3 (1,0%) | 6 (6,5%) | 9 (2,4%) | 0,003 |
| Evento combinado | 174 (60,6%) | 61 (66,3%) | 235 (62,0%) | 0,139 |
|
BARC: Bleeding Academic Research Consortium; IAM: infarto agudo de miocardio; MACE: eventos cardiovasculares adversos mayores; NS: no significativo; TAVI: implante percutáneo de válvula aórtica. |
||||
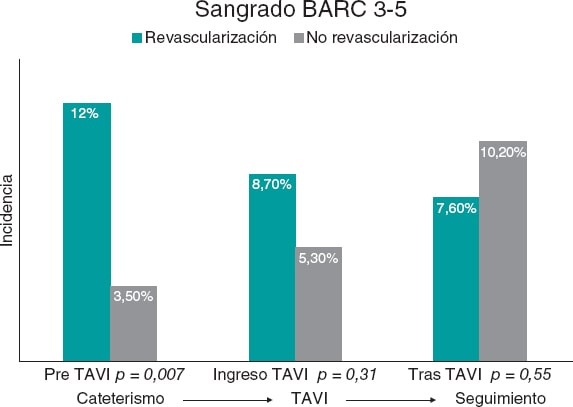
Figura 1. Figura central. Incidencia total de sangrado mayor en los distintos periodos de seguimiento. BARC: Bleeding Academic Research Consortium; TAVI: implante percutáneo de válvula aórtica.
En la tabla S1 se recogen los eventos de sangrado según la clasificación BARC y el estado de revascularización a lo largo de todo el seguimiento. La incidencia global de sangrado mayor (BARC 3-5) entre la coronariografía y el TAVI-TF fue del 5,5% (21/375), y resultó estadísticamente superior en los pacientes revascularizados (12,0% frente a 3,5%, p = 0,007). En cuanto a los sangrados durante el ingreso para el TAVI-TF, la incidencia global de sangrado mayor alcanzó el 6,1% (23/375), sin diferencias estadísticamente significativas entre ambos grupos (8,7% en los revascularizados frente a 5,3% en los no revascularizados, p = 0,31). En el seguimiento posterior al TAVI-TF, la incidencia global de sangrado alcanzó el 9,6% (36/375), sin diferencias significativas entre los grupos (7,6% en los revascularizados frente a 10,2% en los no revascularizados, p = 0,545) (figura 1).
Tras un seguimiento medio de 60 meses, el 55,1% (209/379) de los pacientes presentaron MACE; en concreto, el 55,7% en el grupo de no revascularizados (160 pacientes) y el 53,2% en el de revascularizados (49 pacientes), sin encontrar diferencias estadísticamente significativas entre ambos (p = 0,082) (figura 2). Con respecto a la mortalidad, la tasa total a los 60 meses fue del 42,2% (161/378); por grupos, en los pacientes no revascularizados fue del 43,7% (125 pacientes) y en los revascularizados fue del 39,0% (36 pacientes), sin diferencias estadísticamente significativas, p = 0,380 (figura 3).
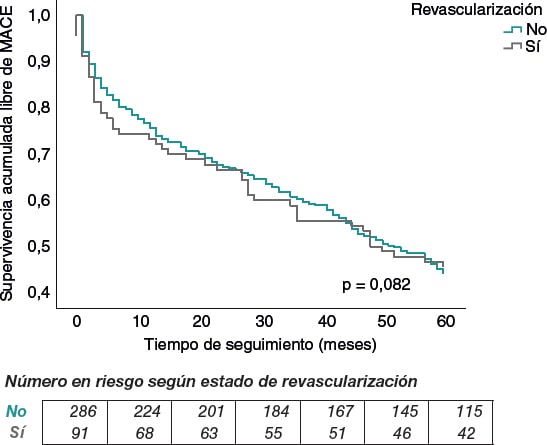
Figura 2. Curva de Kaplan-Meier para la supervivencia libre de eventos cardiovasculares adversos mayores (MACE) según el estado de revascularización.
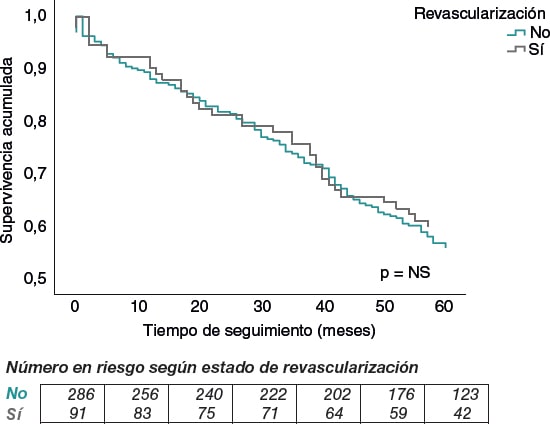
Figura 3. Curva de Kaplan-Meier para la supervivencia total según el estado de revascularización.
En el grupo de pacientes revascularizados se observaron tasas más altas de infarto agudo de miocardio (11,5% frente a 2,8%, p = 0,001) y de revascularización posteriores (6,5% frente a 1,0%, p = 0,003).
En cuanto al evento combinado (MACE o sangrado mayor), en un seguimiento medio de 60 meses, globalmente ocurrió en el 62,0% (235 pacientes) del total de la muestra, sin diferencias estadísticamente significativas entre los grupos (66,3% en no revascularizados frente a 60,6% en revascularizados, p = 0,139) (figura 4).
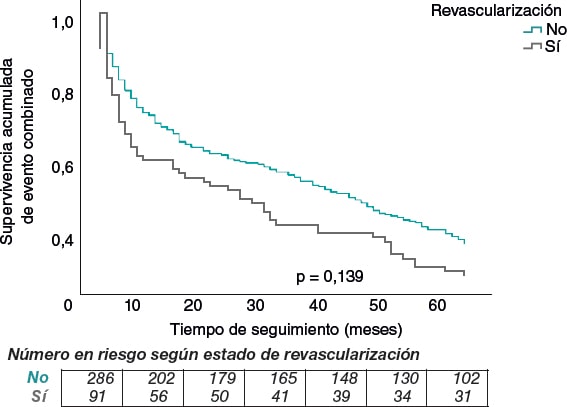
Figura 4. Curva de Kaplan-Meier para la supervivencia libre de evento combinado (isquémico o hemorrágico) según el estado de revascularización.
DISCUSIÓN
En la actualidad no existe evidencia clínica firme con respecto al tratamiento de la enfermedad arterial coronaria en pacientes que van a recibir un TAVI. Las guías de práctica clínica recomiendan revascularización percutánea en todos aquellos en los que se va a realizar TAVI-TF y que presentan una estenosis coronaria en los segmentos proximales ≥ 70% del diámetro del vaso, con un nivel de evidencia IIa. Sin embargo, hasta la fecha solo existen 2 ensayos clínicos que hayan evaluado los beneficios de la revascularización previa al TAVI, con resultados contradictorios8,9.
El sangrado mayor es una de las complicaciones más frecuentes y que más se asocia a morbimortalidad tras un TAVI-TF. De hecho, en el ensayo PARTNER 2, que incluía pacientes de riesgo intermedio, se reportó hasta un 15,2% de sangrados al año del implante3. Sin embargo, la evidencia con respecto a cómo influye en las tasas de sangrado la revascularización de las lesiones coronarias previa al TAVI es escasa.
En el ensayo ACTIVATION8 se aleatorizó a 235 pacientes que iban a ser tratados con TAVI-TF y que presentaban enfermedad coronaria significativa para recibir revascularización percutánea (119) o tratamiento médico (116). Se analizaron los resultados en ambos grupos con respecto a un objetivo primario compuesto de mortalidad por cualquier causa y hospitalización. Al año de seguimiento no se consiguió demostrar la no inferioridad de la estrategia de revascularización percutánea añadida al TAVI-TF en los pacientes sin revascularización, pero se observaron ta- sas más altas de sangrados en los pacientes del grupo de intervención.
Recientemente se han publicado los resultados del ensayo NOTION-39, en el cual 452 pacientes que iban a recibir un TAVI-TF y tenían enfermedad coronaria significativa fueron aleatorizados para realizar abordaje invasivo o no. En este caso, la decisión de revascularización, además, estaba guiada por la determinación de la gravedad de la estenosis según la reserva fraccional de flujo. Se analizaron los resultados con respecto a un objetivo primario compuesto de mortalidad por cualquier causa, infarto de miocardio y revascularización urgente. Se observó que, a los 2 años, los pacientes que habían sido revascularizados tenían una reducción significativa del riesgo de MACE en comparación con el grupo de abordaje conservador (26,0% frente a 36,0%), principalmente a expensas de una mayor tasa de revascularización no planificada y sin impacto en la mortalidad. Sin embargo, esta reducción del riesgo iba unida a una mayor incidencia de eventos hemorrágicos (28,0% frente a 20,0%). Una limitación significativa de este estudio es que se trata de un ensayo abierto y que no excluyó a pacientes con clínica de angina, lo que pudo conllevar un aumento de la tasa de revascularización no planificada.
En nuestro estudio no se observaron diferencias estadísticamente significativas en los MACE ni en los eventos hemorrágicos mayores a los 60 meses entre los pacientes con y sin revascularización. No obstante, sí hubo un porcentaje más alto de sangrados mayores en los pacientes que fueron revascularizados en el periodo entre el cateterismo diagnóstico y el TAVI, lo que es congruente con los datos de estudios previos que demuestran una mayor tasa de sangrados en pacientes con doble antiagregación8,9. En este grupo también se encontraron tasas mayores de infarto agudo de miocardio y revascularización posteriores. Aunque estos hallazgos eran esperables, deben interpretarse con cautela porque, si bien las diferencias son estadísticamente significativas, el reducido número de eventos limita la potencia del estudio para extraer conclusiones definitivas. Un abordaje posible sería una revascularización selectiva, destinada al control de los síntomas, principalmente en pacientes que presenten clínica de angina.
Nuestro estudio tiene una serie de limitaciones significativas, de las cuales la más importante es que se trata de un estudio unicéntrico, observacional, no aleatorizado y retrospectivo, por lo que los pacientes analizados presentan varios sesgos de selección. El primero de ellos es un sesgo de selección biológico, pues el estudio incluye pacientes que se han autoseleccionado al llegar a una edad media de 83 años con unas condiciones biológicas que les hace elegibles para el TAVI-TF. El segundo es un sesgo de selección médico con respecto a qué pacientes van a ser tratados con TAVI y cuáles no, ya que al tratarse de un estudio retrospectivo resulta imposible unificar el criterio con el que en su momento se seleccionó a los pacientes candidatos al implante. Por último, nuestra serie de pacientes corresponde a aquellos en los que finalmente se realizó el procedimiento (no los que iniciaron el estudio para realizarlo), por lo que es probable que haya un grupo de pacientes en quienes se hizo el cateterismo diagnóstico (con o sin revascularización) y finalmente no se llevó a cabo el TAVI, y no están incluidos en el análisis. Desconocemos el porcentaje de pacientes con indicación de intervención valvular a los que finalmente no se llegó a realizar el procedimiento, así como las causas de dicha situación. Aunque los motivos pueden ser múltiples, dados los riesgos inherentes al intervencionismo coronario y que estos pacientes suelen presentar una enfermedad coronaria compleja, es posible que parte de los pacientes candidatos a TAVI no llegasen al implante por complicaciones derivadas del procedimiento de revascularización, si bien esta afirmación no puede ser demostrada con nuestros datos y se trata únicamente de una hipótesis. Por otra parte, este es un estudio unicéntrico y con un número limitado de pacientes, lo que podría limitar tanto la validez externa de los hallazgos como la potencia estadística para encontrar diferencias entre los grupos.
CONCLUSIONES
En nuestra cohorte de pacientes, la revascularización sistemática de las lesiones coronarias previa al TAVI-TF conlleva un aumento del riesgo inicial de sangrado mayor (en concreto en el periodo entre el cateterismo previo al TAVI-TF y el implante valvular), sin observar diferencias estadísticamente significativas en el seguimiento a largo plazo en cuanto a sangrado mayor, MACE y el evento combinado de ambos entre los pacientes revascularizados y los no revascularizados. Nuestros datos, unidos a la reciente evidencia de que la revascularización de la enfermedad coronaria estable no mejora claramente el pronóstico10, refuerzan la necesidad de disponer de una evidencia clínica de calidad que aclare el impacto clínico de la revascularización coronaria sistemática previa al TAVI.
FINANCIACIÓN
No se ha recibido financiación para la realización de este estudio.
CONSIDERACIONES ÉTICAS
El estudio fue aprobado por el Comité de Ética en la Investigación Clínica de A Coruña-Ferrol. No se solicitó el consentimiento informado de los participantes por las características del estudio (retrospectivo, con pacientes de una base de datos recogida con anterioridad, destinado a mejorar y analizar resultados de la intervención). Se siguieron las directrices SAGER para minimizar posibles sesgos por diferencias según el sexo de los pacientes.
DECLARACIÓN SOBRE EL USO DE INTELIGENCIA ARTIFICIAL
No se ha utilizado inteligencia artificial en el desarrollo de este artículo.
CONTRIBUCIÓN DE LOS AUTORES
C. Vidau Getán se encargó de la recopilación de parte de los datos y de la redacción del texto. D. López Vázquez fue el principal revisor del texto y ayudó al perfeccionamiento del análisis estadístico. X. Flores Ríos concibió el trabajo y realizó el análisis estadístico inicial. M. González Montes y G. González Barbeito participaron en la recogida de datos. El resto de los autores firmantes revisaron la última versión del texto. Todos los autores otorgaron su aprobación final.
CONFLICTO DE INTERESES
Los autores no presentan ningún conflicto de intereses que de- clarar.
¿QUÉ SE SABE DEL TEMA?
- Las guías de práctica clínica recomiendan la revascularización percutánea en todos aquellos pacientes que van a recibir un TAVI-TF y que presentan una estenosis coronaria en los segmentos proximales ≥ 70% del diámetro del vaso.
- No existe evidencia clínica de calidad que demuestre el beneficio clínico de revascularizar sistemáticamente las lesiones coronarias antes de la realización del TAVI-TF.
- Existen dos ensayos clínicos en este tipo de población, con resultados discordantes en cuanto a los beneficios encontrados en términos de eventos isquémicos y con una tasa más alta de eventos hemorrágicos en los pa- cientes con revascularización.
¿QUÉ APORTA DE NUEVO?
- Los pacientes con revascularización presentaron unas tasas más altas de sangrado mayor precoz (entre el cateterismo diagnóstico y el TAVI), sin diferencias significativas en eventos isquémicos o hemorrágicos en el seguimiento a largo plazo.
- Los resultados de este estudio refuerzan la necesidad de disponer de una evidencia científica de calidad que aclare el impacto clínico de la revascularización coronaria sistemática previa al TAVI.
BIBLIOGRAFÍA
1. Vahanian A, Beyersdorf F, Praz F, et al. 2021 ESC/EACTS Guidelines for the management of valvular heart disease. Eur Heart J. 2022;43:561-632.
2. Smith CR, Leon MB, Mack MJ, et al. Transcatheter versus Surgical Aortic-Valve Replacement in High-Risk Patients. N Engl J Med. 2011;364: 2187-2198.
3. Leon MB, Smith CR, Mack MJ, et al. Transcatheter or Surgical Aortic-Valve Replacement in Intermediate-Risk Patients. N Engl J Med. 2016;374: 1609-1620.
4. Reardon MJ, Mieghem NMV, Popma JJ, et al. Surgical or Transcatheter Aortic-Valve Replacement in Intermediate-Risk Patients. N Engl J Med. 2017;376:1321-1331.
5. Moat N, Brecker S. Transfemoral TAVI is superior to SAVR in elderly high-risk patients with symptomatic severe aortic stenosis! Eur Heart J. 2016;37:3513-3514.
6. Avvedimento M, Nuche J, Farjat-Pasos JI, Rodés-Cabau J. Bleeding Events After Transcatheter Aortic Valve Replacement: JACC State-of-the-Art Review. J Am Coll Cardiol. 2023;81:684-702.
7. Vázquez DJL, López GA, Guzmán MQ, et al. Prognostic impact of coronary lesions and its revascularization in a 5-year follow-up after the TAVI procedure. Catheter Cardiovasc Interv. 2023;102:513-520.
8. Patterson T, Clayton T, Dodd M, et al. ACTIVATION (PercutAneous Coronary inTervention prIor to transcatheter aortic VAlve implantaTION): A Randomized Clinical Trial. JACC Cardiovasc Interv. 2021;14:1965- 1974.
9. Lønborg J, Jabbari R, Sabbah M, et al. PCI in Patients Undergoing Transcatheter Aortic-Valve Implantation. N Engl J Med. 2024;391:2189-2200.
10. Maron DJ, Hochman JS, Reynolds HR, et al. ISCHEMIA Research Group. Initial Invasive or Conservative Strategy for Stable Coronary Disease. N Engl J Med. 2020;382:1395-1407.

