RESUMEN
Introducción y objetivos: La desescalada desde prasugrel y ticagrelor a clopidogrel en pacientes tras intervencionismo coronario percutáneo por síndrome coronario agudo (SCA) constituye una de las estrategias para intentar disminuir las hemorragias. El objetivo de este estudio es averiguar si dicha desescalada guiada por la prueba de agregación plaquetaria VerifyNow (Werfen, España) tiene un efecto beneficioso en el tratamiento del SCA.
Métodos: Estudio multicéntrico, prospectivo y aleatorizado 1:1, en curso. Se incluirán 634 pacientes con SCA y revascularización con stent de sirolimus que sean dados de alta con doble terapia antiagregante con ticagrelor o prasugrel. Solo se incluirán aquellos con un nivel de reactividad plaquetaria muy bajo (unidades de reactividad plaquetaria ≤ 30) basado en VerifyNow al mes del alta. El objetivo primario es un combinado de muerte por causa cardiovascular, infarto agudo de miocardio no fatal, accidente cerebrovascular no fatal y sangrado en un seguimiento a 1 año.
Resultados: El estudio EPIC17-VERONICA (NCT04654052) permitirá averiguar la eficacia de la estrategia de desescalada basada en la prueba de agregación plaquetaria VerifyNow, además de conocer el papel de este dispositivo en la selección de los pacientes candidatos a beneficiarse de esta estrategia.
Conclusiones: Este estudio determinará si las pruebas de función plaquetaria aportan beneficio en el tratamiento tras el SCA.
Palabras clave: Síndrome coronario agudo. Terapia antiagregante. Prueba de función plaquetaria. Sangrado.
ABSTRACT
Introduction and objectives: De-escalation from prasugrel and ticagrelor to clopidogrel in patients undergoing percutaneous coronary intervention after acute coronary syndrome (ACS) is a strategy aimed at reducing bleeding. This study evaluates whether VerifyNow (Werfen, Spain)–guided de-escalation, based on platelet aggregation measurement, provides a therapeutic benefit in ACS management.
Methods: This ongoing multicenter, prospective, randomized 1:1 trial will enroll 634 patients with ACS who underwent revascularization with a sirolimus-eluting stent and were discharged on dual antiplatelet therapy with ticagrelor or prasugrel. Only those patients with a very low platelet reactivity level (platelet reactivity units ≤ 30) based on VerifyNow 1 month after discharge will be included. The primary endpoint is a composite of cardiovascular death, nonfatal acute myocardial infarction, nonfatal stroke, and bleeding at 1-year follow-up.
Results: The EPIC17-VERONICA study (NCT04654052) will reveal the efficacy profile of the de-escalation strategy, based on the VerifyNow platelet aggregation test, and determine the role of this device in the selection of patients who are eligible to benefit from this strategy.
Conclusions: This study will determine whether platelet function testing provide clinical benefit in the management of patients with ACS.
Keywords: Acute coronary syndrome. Antiplatelet therapy. Platelet function test. Bleeding.
Abreviaturas
ICP: intervencionismo coronario percutáneo. URP: unidades de reactividad plaquetaria. SCA: síndrome coronario agudo.
INTRODUCCIÓN
Tras el intervencionismo coronario percutáneo (ICP) en pacientes con síndrome coronario agudo (SCA) se recomienda doble terapia antiagregante con un inhibidor del receptor P2Y12 y ácido acetilsalicílico durante 12 meses, independientemente del tipo de stent implantado, excepto si existen contraindicaciones1. Aunque el prasugrel y el ticagrelor son preferibles al clopidogrel en este contexto, existe controversia sobre la potencia y la duración de la doble antiagregación. Esto se debe a que en la mayoría de los pacientes coexisten dos riesgos, el isquémico y el hemorrágico, que al ser opuestos y tener consecuencias fatales deben estar equilibrados en cada caso.
La introducción de stents con baja trombogenicidad, junto con el hecho de que el riesgo trombótico es mayor durante los primeros meses tras el ICP, mientras que el riesgo de hemorragia permanece estable a lo largo del tiempo, han impulsado investigaciones centradas en la reducción de las hemorragias. Estas estrategias incluyen el acortamiento de la doble terapia antiagregante, el uso en monoterapia de los inhibidores de P2Y12 y la desescalada2,3.
La desescalada consiste en el cambio de prasugrel o ticagrelor a clopidogrel, y puede hacerse de forma guiada (con pruebas genéticas o de función plaquetaria) o no guiada. Dado que esta estrategia puede aumentar los eventos isquémicos, no se recomienda durante el primer mes tras el ICP1.
En el ensayo clínico TOPIC4, la estrategia de desescalada no guiada 1 mes tras el SCA consiguió una reducción significativa de las hemorragias (escala Bleeding Academic Research Consortium [BARC] ≥ 2) al año sin un aumento de los eventos isquémicos. En el ensayo TROPICAL-ACS5, la desescalada de prasugrel a clopidogrel a las 2 semanas de la revascularización guiada por pruebas de función plaquetaria fue no inferior al tratamiento estándar, con una tendencia a la reducción de las hemorragias a los 12 meses y una tasa similar de episodios trombóticos1,2,6. En el ensayo clínico TALOS-AMI7 hubo una disminución de los eventos a 12 meses, fundamentalmente por disminución de las hemorragias en los pacientes con desescalada no guiada al mes tras el SCA. En la tabla 1 se ofrece un resumen de estos estudios.
Tabla 1. Ensayos clínicos de desescalada en pacientes con síndrome coronario agudo
| TOPIC (2017)4 | TROPICAL-ACS (2018)5 | TALOS-AMI (2021)12 | |
|---|---|---|---|
| Población | n = 645 | n = 2.610 | n = 2.697 |
| Diseño | Abierto, monocéntrico, aleatorizado, de superioridad | Abierto, multicéntrico, aleatorizado, de no inferioridad | Abierto, multicéntrico, aleatorizado, de no inferioridad |
| Estrategia | Tratamiento estándar frente a desescalada no guiada | Terapia estándar frente a terapia guiada por prueba de función plaquetaria (dispositivo Multiplate) | Tratamiento estándar frente a desescalada no guiada |
| Grupo control | Mantiene doble terapia con ácido acetilsalicílico y ticagrelor o prasugrel | Mantiene doble terapia con ácido acetilsalicílico y prasugrel | Mantiene doble terapia con ácido acetilsalicílico y ticagrelor |
| Grupo experimental | Desescalada a ácido acetilsalicílico y clopidogrel | 1 semana de prasugrel, seguida de 1 semana de clopidogrel y después prasugrel o clopidogrel desde el día 14, según el resultado de la prueba de función plaquetaria | Desescalada a ácido acetilsalicílico y clopidogrel |
| Tiempo desde la revascularización hasta la desescalada | 1 mes | 2 semanas | 1 mes |
| Seguimiento | 1 año | 1 año | 1 año |
| Objetivo primario | Muerte de causa cardiovascular, revascularización urgente, ictus o sangrado BARC ≥ 2 | Muerte de causa cardiovascular, infarto de miocardio, ictus o sangrado BARC ≥ 2 | Muerte de causa cardiovascular, infarto de miocardio, ictus o sangrado BARC ≥ 2 |
| Resultados | 13,4% en el grupo experimental frente a 26,3% en el grupo control (HR = 0,48; IC95%, 0,34-0,68; p < 0,01) | 7,3% en el grupo experimental frente a 9,0% en el grupo control (HR = 0,81; IC95%, 0,62-1,06; p = 0,0004) | 4,6% en el grupo experimental frente a 8,2% en el grupo control (HR = 0,55; IC95%, 0,42-0,76; p < 0,0001) |
|
BARC: Bleeding Academic Research Consortium; HR: hazard ratio; IC95%: intervalo de confianza del 95%. |
|||
Tras los resultados tan satisfactorios del TOPIC, el estudio VerifyNow to Optimise Platelet InhIbition in Coronary Acute Syndrome (EPIC17-VERONICA; ClinicalTrials.gov: NCT04654052) pretende dar un paso más en esta estrategia, aplicando la desescalada solo a los pacientes que presenten exceso de efecto del prasugrel y del ticagrelor al cabo del primer mes, y que por tanto estén en riesgo teórico de sangrado, mediante la prueba de agregación plaquetaria VerifyNow (Werfen, España). De esta forma, aquellos pacientes para los que estos fármacos tengan un efecto adecuado continuarán con ellos durante el primer año, mientras que aquellos con reactividad plaquetaria muy baja tras un primer mes de doble terapia antiagregante con prasugrel o ticagrelor son el objeto del estudio.
MÉTODOS
Diseño
Ensayo clínico abierto, multicéntrico, prospectivo y aleatorizado, en 16 centros españoles. Según los resultados de la prueba de agregación plaquetaria para los inhibidores de P2Y12 (unidades de reactividad plaquetaria [URP]) con el dispositivo VerifyNow se seleccionan los pacientes con un nivel muy bajo de reactividad plaquetaria (URP ≤ 30), que se aleatorizan 1:1 para mantener tratamiento con ticagrelor o prasugrel, o ser desescalados a clopidogrel; los pacientes con URP > 30 no son aleatorizados. La figura 1 muestra el diagrama de flujo del estudio.
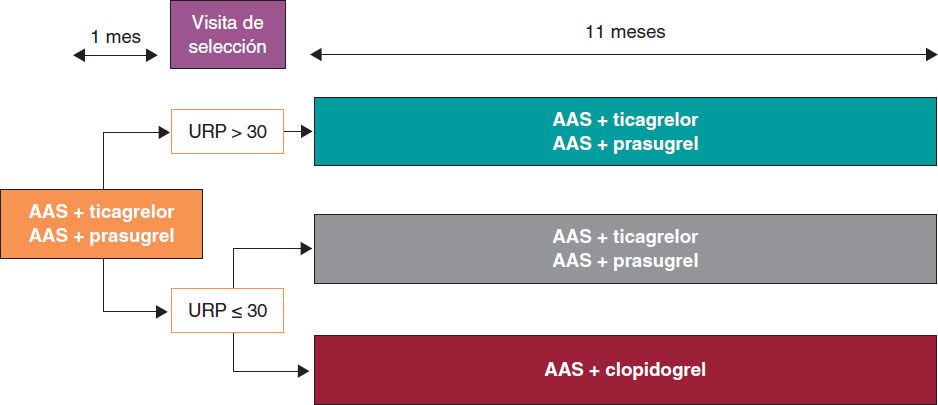
Figura 1. Diagrama de flujo del estudio. AAS: ácido acetilsalicílico; URP: unidades de reactividad plaquetaria.
El estudio se lleva a cabo siguiendo las recomendaciones recogidas en la Declaración de Helsinki sobre investigación clínica y ha sido aprobado por el comité de ética de referencia (Comité del Bierzo, León), y refrendado por el resto de los comités de ética de los centros participantes. En el anexo del material adicional se detallan los centros y los investigadores principales participantes en el estudio.
El promotor del estudio (Fundación para Educación en Procedimientos de Intervencionismo en Cardiología [EPIC]) se hace responsable, junto con los investigadores principales, de la gestión de los datos y su confidencialidad.
Población
Criterios de inclusión y exclusión
La tabla 2 muestra los criterios de inclusión y exclusión del estudio. En resumen, son elegibles todos los pacientes con SCA e ICP con stent de sirolimus y polímero reabsorbible durante el ingreso que son dados de alta con doble terapia antiagregante a base de ácido acetilsalicílico y ticagrelor o prasugrel.
Tabla 2. Criterios de inclusión y exclusión
| Criterios de inclusión |
|---|
| Pacientes con edad mayor de 18 años |
| Pacientes con síndrome coronario agudo sometidos a revascularización percutánea con stent de sirolimus y polímero reabsorbible, y que han sido dados de alta con doble terapia antiplaquetaria con ácido acetilsalicílico y ticagrelor o prasugrel |
| Firma del consentimiento informado |
| Criterios de exclusión |
| Antecedentes de hemorragia intracraneal |
| Contraindicación para el uso de ácido acetilsalicílico, clopidogrel, prasugrel o ticagrelor |
| Eventos isquémicos o hemorrágicos mayores durante el primer mes de tratamiento antiagregante |
| Trombocitopenia < 50.000/µl |
| Anticoagulación oral permanente |
| Embarazadas o en periodo de lactancia |
| Imposibilidad para completar 1 año de seguimiento |
| Esperanza de vida inferior a 24 meses |
Se requieren la aceptación y la firma del consentimiento informado antes de la realización del análisis de agregación plaquetaria.
Protocolo del estudio y aleatorización
Los pacientes potencialmente elegibles son citados para analizar su grado de inhibición del receptor P2Y12 con el dispositivo VerifyNow entre 30 y 40 días después del alta hospitalaria. La medición se realiza con una ventana de al menos 6 horas desde la última administración del inhibidor de P2Y12. Aquellos con URP ≤ 30 (muy baja reactividad plaquetaria) son aleatorizados 1:1, mediante un sistema informatizado, para continuar con el tratamiento previo o desescalar a 75 mg al día de clopidogrel, con una carga previa de 600 mg 24 h después de la última administración de ticagrelor o de 75 mg de clopidogrel 24 h después de la última dosis de prasugrel, tal como se recomienda en el documento de la Sociedad Europea de Cardiología de 20178.
Los pacientes restantes con un URP > 30 no son aleatorizados y, por tanto, su doble terapia antiagregante no se modifica respecto al alta.
Seguimiento clínico
A los pacientes de los dos grupos aleatorizados se les realiza un seguimiento telefónico para la monitorización de eventos a los 2, 5, 8 y 11 meses de la inclusión en el estudio, que corresponden al tercero, sexto, noveno y decimosegundo meses después del ingreso.
En los pacientes cuya prueba con VerifyNow al mes del alta dé URP > 30, y por tanto no sean aleatorizados, solo se recogerán sus características basales, sin realizar un seguimiento posterior.
Protocolo para la realización de la prueba VerifyNow
El dispositivo VerifyNow permite determinar la actividad plaquetaria midiendo el grado de agregación in vitro en una muestra de sangre expuesta a agonistas específicos. Se trata de un instrumento (figura 2) de detección óptica basado en turbidimetría que necesita kits de un solo uso. En este estudio se emplean kits específicos (PRUTest, Werfern, España) para conocer el grado de agregación plaquetaria bajo tratamiento con inhibidores del receptor P2Y12 plaquetario (ticagrelor, prasugrel y clopidogrel). El kit PRUTest contiene una preparación liofilizada de microesferas recubiertas con fibrinógenos, activadores de plaquetas y una solución amortiguadora. La prueba se basa en la capacidad de las plaquetas activadas de unirse a los fibrinógenos. La transmisión de la luz aumenta a medida que las plaquetas activadas se unen y agregan a las microesferas recubiertas con fibrinógenos. El instrumento mide este cambio en la señal óptica e informa los resultados en URP (figura 3).

Figura 2. Dispositivo VerifyNow. Reproducida con permiso de Werfen.
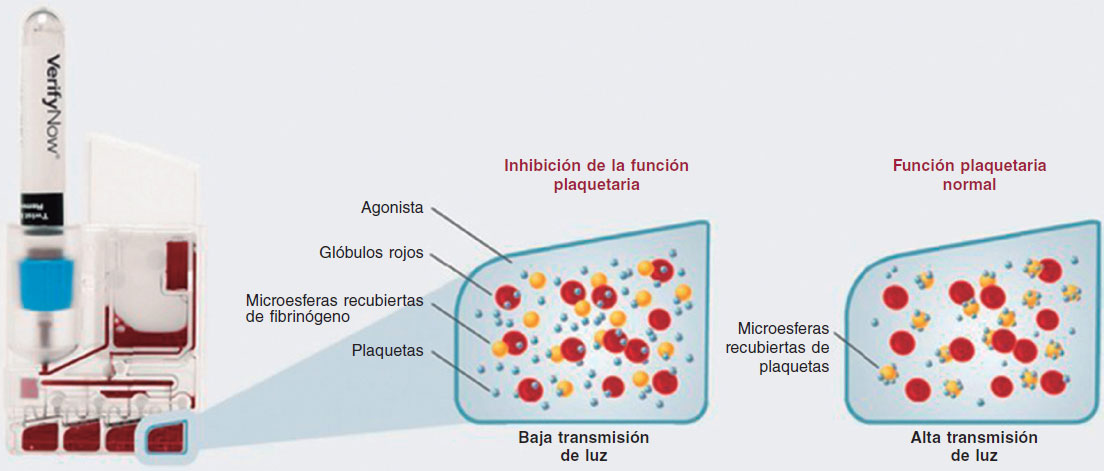
Figura 3. Funcionamiento del dispositivo VerifyNow basado en agregometría de transmisión de luz. La transmisión de la luz aumenta a medida que las plaquetas activadas se unen y agregan a las microesferas recubiertas con fibrinógenos del kit. Por tanto, una alta transmisión de luz (lo que se traduce en un valor de unidades de reactividad plaquetaria [URP] elevado) se correlaciona con una función plaquetaria normal. La baja transmisión de luz (valor de URP disminuido) se produce por la inhibición plaquetaria inducida por los fármacos probados.
Se considera que existe efecto antiagregante del fármaco con URP ≤ 180 (figura 4). Solo son aleatorizados los pacientes con URP ≤ 30, al considerarse aquellos con muy baja reactividad plaquetaria bajo tratamiento antiagregante.
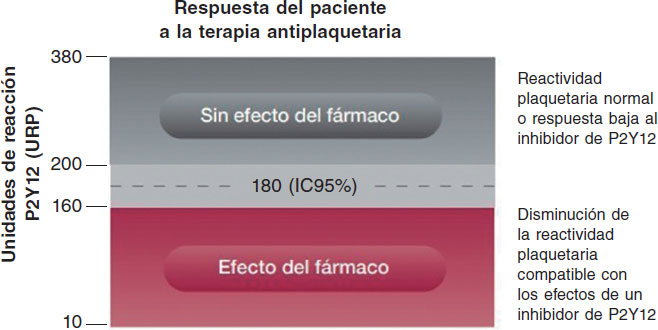
Figura 4. Niveles de referencia para unidades de reactividad plaquetaria (URP). IC95%: intervalo de confianza del 95%.
Objetivos
El objetivo primario es comparar la eficacia de la desescalada de ticagrelor o prasugrel a clopidogrel en pacientes tratados con ICP en el contexto de un SCA, basada en la prueba de antiagregación plaquetaria VerifyNow, frente a la doble terapia antiagregante estándar a 1 año de seguimiento. El porcentaje de eventos cardiovasculares adversos netos es el objetivo principal del estudio y se define como un combinado de muerte por causa cardiovascular, infarto agudo de miocardio no fatal, accidente cerebrovascular no fatal y sangrado (definido como criterios BARC ≥ 2). La escala BARC se detalla en la tabla S1.
El estudio también pretende comparar varios objetivos secundarios (tabla 3), como son la ocurrencia en el seguimiento de eventos isquémicos: muerte por causa cardiovascular y por cualquier causa, infarto agudo de miocardio, accidente cerebrovascular, trombosis del stent y necesidad de revascularización urgente. También se comparará la incidencia de sangrado (definido como criterios BARC ≥ 2). En la tabla S2 se encuentra la definición de los objetivos del estudio.
Tabla 3. Objetivos del estudio
| Objetivo primario |
|---|
| Comparar el porcentaje de eventos cardiovasculares adversos netos entre los dos subgrupos de pacientes con baja reactividad plaquetaria (URP ≤ 30) aleatorizados: con desescalada a clopidogrel frente a terapia estándar |
| Objetivos secundarios |
| Comparar el porcentaje de muertes de causa cardiovascular entre los dos subgrupos de pacientes aleatorizados |
| Comparar el porcentaje de muerte por cualquier causa entre los dos subgrupos de pacientes aleatorizados |
| Comparar el porcentaje de infarto agudo de miocardio entre los dos subgrupos de pacientes aleatorizados |
| Comparar el porcentaje de accidentes cerebrovasculares entre los dos subgrupos de pacientes aleatorizados |
| Comparar el porcentaje de trombosis del stent entre los dos subgrupos de pacientes aleatorizados |
| Comparar el porcentaje de necesidad de revascularización urgente entre los dos subgrupos de pacientes aleatorizados |
| Comparar el porcentaje de sangrado (definido como criterios BARC ≥ 2) entre los dos subgrupos de pacientes aleatorizados |
|
BARC: Bleeding Academic Research Consortium; URP: unidades de reactividad plaquetaria. |
Estadística
Cálculo del tamaño muestral
El tamaño de la muestra se ha calculado para el grupo del ensayo clínico aleatorizado. El número total de pacientes (incluidos los no aleatorizados por URP > 30) dependerá del total de pacientes necesarios para alcanzar el tamaño muestral estimado para el ensayo clínico aleatorizado.
Estimamos una diferencia de eventos entre ambos grupos menor que la observada en el estudio TOPIC4; en concreto, un 14% en el grupo con desescalada frente a un 22% en el grupo de terapia estándar. Para un nivel de significación de 0,05, una potencia del 80%, un valor p de 2 colas y un 10% de pérdidas en el seguimiento, se necesitarán en total 634 pacientes aleatorizados (317 por grupo).
Plan de análisis estadístico
Las variables cuantitativas se presentarán como media y desviación estándar si siguen una distribución normal, o como mediana y rango intercuartílico si no siguen una distribución normal. Las variables categóricas se presentarán como valor absoluto y porcentaje. Los datos obtenidos en el estudio serán analizados por análisis unilateral de varianza (ANOVA) para las variables continuas, y por la prueba exacta de Fisher o la prueba de χ2 para las variables categóricas, según proceda. Para las variables con distribución no normal, o cuando no sea posible la normalización, se usarán pruebas no paramétricas, según proceda. Para el análisis de la variable principal se presentarán curvas de supervivencia de Kaplan-Meier con estadístico log-rank para los criterios previamente especificados, y se realizará regresión de Cox multivariable para corregir el riesgo conocido y las potenciales variables de confusión. Se presentarán los coeficientes de probabilidad y los intervalos de confianza del 95% para todas las variables estadísticas significativas.
Se realizará un análisis por intención de tratar (según la asignación en el momento de la aleatorización) y también por protocolo (en caso de necesidad de cambio de grupo). El análisis por intención de tratar será el análisis primario del estudio.
DISCUSIÓN
El estudio EPIC17-VERONICA pretende demostrar la eficacia de la estrategia de desescalada, basada en la prueba de agregación plaquetaria VerifyNow, en la disminución de los eventos hemorrágicos sin incremento en los isquémicos en pacientes con SCA tras una revascularización percutánea con reactividad plaquetaria muy baja después de un primer mes con prasugrel o ticagrelor.
La ausencia inicial de los resultados esperados de las pruebas de función plaquetaria en la detección de los pacientes en riesgo de eventos trombóticos bajo tratamiento con clopidogrel en los estudios GRAVITAS9, TRIGGER-PCI10 y ARCTIC11 relegó su uso a una recomendación de clase IIb en las guías de antiagregación de la Sociedad Europea de Cardiología para guiar el momento más adecuado de la cirugía cardiaca después de un SCA8. Sin embargo, los resultados a 1 año del estudio multicéntrico a gran escala ADAPT-DES12 mostraron, en 8.500 pacientes con ICP, que la reactividad plaquetaria evaluada mediante la prueba de agregación plaquetaria VerifyNow es un factor predictivo independiente de presentar hemorragias.
En los ensayos clínicos TOPIC4 y TALOS-AMI7, la estrategia de desescalada no guiada consiguió una reducción significativa de las hemorragias sin un aumento de los eventos isquémicos. En el estudio TROPICAL-ACS5, esta estrategia de desescalada guiada por la prueba de antiagregación plaquetaria mostró una tendencia a la reducción de los sangrados, también con una tasa similar de complicaciones trombóticas.
El estudio EPIC17-VERONICA persigue, además, mejorar la aplicación de esta estrategia de desescalada al seleccionar, con el empleo de la prueba de agregación plaquetaria VerifyNow, a los pacientes con reactividad plaquetaria muy baja (URP ≤ 30) como aquellos que podrían beneficiarse de la estrategia.
CONCLUSIONES
El estudio EPIC17-VERONICA está dirigido a investigar la eficacia de la desescalada de los antiagregantes más potentes (ticagrelor y prasugrel) al clopidogrel tras el primer mes de tratamiento en pacientes con SCA y reactividad plaquetaria muy baja, consiguiendo una disminución de los eventos hemorrágicos sin aumentar las complicaciones isquémicas. Además, aportará información sobre la utilidad de la prueba de agregación plaquetaria VerifyNow para la selección de los pacientes candidatos.
FINANCIACIÓN
El presente estudio no ha sido financiado.
CONSIDERACIONES ÉTICAS
El estudio se lleva a cabo siguiendo las recomendaciones recogidas en la Declaración de Helsinki sobre investigación clínica y ha sido aprobado por el comité de ética de referencia (Comité del Bierzo, León), y refrendado por el resto de los comités de ética de los centros participantes. Se requieren la aceptación y la firma del consentimiento informado antes de la realización del análisis de agregación plaquetaria. Se tienen en cuenta los posibles sesgos de sexo y género.
DECLARACIÓN SOBRE EL USO DE INTELIGENCIA ARTIFICIAL
No se ha utilizado inteligencia artificial para la redacción de este artículo.
CONTRIBUCIÓN DE LOS AUTORES
C. Garilleti Cámara e I. Lozano Martínez-Luengas redactaron el borrador del documento, el resto de los autores lo revisaron y todos los firmantes han aprobado el texto final.
CONFLICTO DE INTERESES
J.M. de la Torre-Hernández es editor jefe de REC: Interventional Cardiology; A. Pérez de Prado es editor asociado de REC: Interventional Cardiology. En ambos casos se ha seguido el procedimiento editorial establecido en la revista para garantizar la gestión imparcial del manuscrito. Los demás autores no declaran conflictos de intereses.
¿QUÉ SE SABE DEL TEMA?
- La desescalada de los antiagregantes más potentes a clopidogrel constituye una de las estrategias para la disminución de los sangrados tras la revascularización percutánea en el síndrome coronario agudo. Esta desescalada puede realizarse de forma no guiada u orientada por test genéticos o pruebas de función plaquetaria.
¿QUÉ APORTA DE NUEVO?
- El estudio EPIC17-VERONICA es el primer estudio que emplea la prueba de agregación plaquetaria VerifyNow para la selección de los pacientes candidatos a la desescalada.
BIBLIOGRAFÍA
1. Byrne RA, Rossello X, Coughlan JJ, et al. 2023 ESC Guidelines for the management of acute coronary syndromes. Eur Heart J. 2023;44:3720-3826.
2. Angiolillo DA, Galli M, Collet JP, Kastrati A, O'Donoghue MO. Antiplatelet therapy after percutaneous coronary intervention. EuroIntervention. 2022;17:e1371-e1396.
3. Angiolillo DJ. The Evolution of Antiplatelet Therapy in the Treatment of Acute Coronary Syndromes. Drugs. 2012;72:2087-2116.
4. Cuisset T, Deharo P, Quilici J, et al. Benefit of switching dual antiplatelet therapy after acute coronary syndrome:the TOPIC (timing of platelet inhibition after acute coronary syndrome) randomized study. Eur Heart J. 2017;38:3070-3078.
5. Sibbing D, Aradi D, Jacobshagen C, et al. Guided de-escalation of antiplatelet treatment in patients with acute coronary syndrome undergoing percutaneous coronary intervention (TROPICAL-ACS):a randomised, open-label, multicentre trial. Lancet. 2017;390:1747-1757.
6. Gorog DA, Ferreiro JL, Ahrens I, et al. De-escalation or abbreviation of dual antiplatelet therapy in acute coronary syndromes and percutaneous coronary intervention:a Consensus Statement from an international expert panel on coronary thrombosis. Nat Rev Cardiol. 2023;20:830-844.
7. Kim CJ, Park MW, Kim MC, et al. Unguided de-escalation from ticagrelor to clopidogrel in stabilised patients with acute myocardial infarction undergoing percutaneous coronary intervention (TALOS-AMI):an investigator-initiated, open-label, multicentre, non-inferiority, randomised trial. Lancet. 2021;398:1305-1316.
8. Valgimigli A del G de TM, Bueno H, Byrne RA, et al. Actualización ESC 2017 sobre el tratamiento antiagregante plaquetario doble en la enfermedad coronaria, desarrollada en colaboración con la EACTS. Rev Esp Cardiol. 2018;71:42.e1-42.e58.
9. Price MJ, Berger PB, Teirstein PS, et al. Standard- vs high-dose clopidogrel based on platelet function testing after percutaneous coronary intervention:the GRAVITAS randomized trial. JAMA. 2011;305:1097-105. Erratum in: JAMA. 2011;305;2174. Stillablower, Michael E [corrected to Stillabower, Michael E]. PMID:21406646.
10. Trenk D, Stone GW, Gawaz M, et al. A Randomized Trial of Prasugrel Versus Clopidogrel in Patients With High Platelet Reactivity on Clopidogrel After Elective Percutaneous Coronary Intervention With Implantation of Drug-Eluting Stents. J Am Coll Cardiol. 2012;59:2159-2164.
11. Collet JP, Cuisset T, RangéG, et al. Bedside Monitoring to Adjust Antiplatelet Therapy for Coronary Stenting. N Engl J Med. 2012;367:2100-2109.
12. Sibbing D, Schulz S, Braun S, et al. Antiplatelet effects of clopidogrel and bleeding in patients undergoing coronary stent placement. J Thromb Haemost. 2010;8:250-256.

