RESUMEN
Introducción y objetivos: Existen resultados contradictorios sobre la eficacia del poscondicionamiento isquémico local (iPost) como intervención para reducir el tamaño del infarto (TI). Pretendemos evaluar si el efecto del iPost se ve alterado por el tiempo de isquemia en un modelo porcino de infarto de miocardio.
Métodos: Se sometió a 38 cerdos Large-White a isquemia-reperfusión coronaria con balón de angioplastia. Se realizaron dos series de experimentos: isquemia de intermedia (30 minutos) y larga (40 minutos) duración. Los animales se asignaron 1:1 a iPost (4 ciclos de 1 minuto inflado/1 minuto desinflado, comenzando 1 minuto tras la reperfusión) o control. Se realizó una resonancia magnética 7 días después. El objetivo primario fue el TI medido por resonancia magnética (porcentaje de masa ventricular izquierda con realce tardío de gadolinio). La interacción de la asignación al tratamiento y la duración de la isquemia se evaluó mediante un análisis de varianza de dos vías.
Resultados: El iPost no se asoció con un menor TI en ninguno de los grupos de duración de la isquemia (duración intermedia: 0,3 [0,0-3,9] frente a 0,9% [0,0-2,6] en iPost y control, respectivamente, p = 0,378; larga duración: 31,1 [27,3-32,8] frente a 27,3% [25,1-27,5] en iPost y control, respectivamente; p = 0,248). Al analizar conjuntamente todos los animales, el iPost tampoco se asoció con un TI más pequeño (3,9% [0,0-30,9] frente a 4,6% [0,2-25,1] en iPost y control, respectivamente; p = 0,672). Los tiempos de relajación en T1 fueron más largos en los animales sometidos a iPost (1.306,2 [1.190,7-1.492,7] ms frente a 1.240,7 [1.167,1–1.304,5] ms; p = 0,024).
Conclusiones: El iPost no logró reducir el TI en ninguna duración de la isquemia. Los tiempos de relajación T1 fueron más largos en los animales sometidos a iPost, lo que sugiere un daño potencial de esta intervención.
Palabras clave: Daño por reperfusión. Condicionamiento isquémico. Cardioprotección. Infarto de miocardio.
ABSTRACT
Introduction and objectives: Ischemic postconditioning (iPost, coronary intermittent re-occlusion maneuvers immediately after PCI mediated reperfusion) has been proposed to limit infarct size (IS). However, a few experimental and clinical contradictory results have been reported. We hypothesized that iPost cardioprotection is affected by the duration of ischemia. Our objective was to assess IS in the presence/absence of iPost in a pig model of myocardial infarction of variable ischemia duration.
Methods: Large white pigs (n = 38) underwent angioplasty balloon-induced coronary ischemia followed by reperfusion. Two set of experiments were carried out: intermediate (30 min) and prolonged (40 min) ischemia. In both, pigs were allocated on a 1:1 ratio to receive iPost (4 cycles of “1 min balloon inflation followed by 1 min deflation” upon reperfusion) or control. Animals underwent contrast-enhanced multiparametric cardiac magnetic resonance scan on day 7. Primary outcome measure was cardiac magnetic resonance based IS (% of left ventricular mass). The interaction between treatment allocation and ischemia duration was assessed using a 2-way ANOVA test.
Results: iPost was not associated with smaller IS in any of the ischemia duration protocols (intermediate ischemia: 0.3% [0.0 – 3.9] vs 0.9% [0.0 – 2.6] in iPost and control, respectively; P = .378; long ischemia: 31.1% [27.3 – 32.8] vs 27.3% [25.1 – 27.5]; P = .248). When both ischemia-duration protocols were combined, iPost was not associated with smaller IS (3.9% [0.0 – 30.9] vs 4.6% [0.2 – 25.1]; P = .672). T1 relaxation times were longer in animals undergoing iPost compared to controls (1306.2 ms [1190.7 – 1492.7] vs 1240.7 ms [1167.1 – 1304.5]; P = .024).
Conclusions: In a pig model of reperfused myocardial infarction of variable ischemia duration, iPost failed to reduce IS. T1 relaxation times were longer in animals undergoing iPost indicative of the potential harm involved in this procedure.
Keywords: Reperfusion injury. Ischemic postconditioning. Cardioprotection. Myocardial infarction.
Abreviaturas
IC: insuficiencia cardiaca. IM: infarto de miocardio. iPost: poscondicionamiento isquémico local. LIR: lesión por isquemia-reperfusión. RTG: realce tardío de gadolinio. TI: tamaño del infarto.
INTRODUCCIÓN
El infarto agudo de miocardio con elevación del segmento ST (IAMCEST) es una patología amenazante para la vida que afecta a más de 7 millones de personas en el mundo cada año1. A pesar de que la intervención coronaria percutánea (ICP) ha mejorado la supervivencia a corto plazo y reducido la necesidad de nuevas revascularizaciones, la supervivencia a largo plazo y la incidencia de insuficiencia cardiaca (IC) apenas han mejorado durante los últimos años2.
El tamaño del infarto (TI) (grado de irreversibilidad de la lesión tras el IM) es uno de los principales factores que contribuyen tanto a la mortalidad a largo plazo como al desarrollo de IC en los supervivientes de un IAMCEST3-5. Así pues, es necesario identificar qué estrategias intervencionistas (invasivas) o farmacológicas son capaces de reducir el tamaño de IM. En las oclusiones coronarias se observa una mayor irreversibilidad de la lesión en función del tiempo de isquemia6. En consecuencia, restaurar el flujo sanguíneo (reperfusión) en la zona isquémica es de vital importancia para reducir el TI y mejorar la fracción de eyección del ventrículo izquierdo (FEVI)7. No obstante, la reperfusión per se provoca otros daños en el miocardio y en la microcirculación que contribuyen al TI final8, la llamada lesión por isquemia-reperfusión (LIR)9.
El poscondicionamiento isquémico (iPost) es un procedimiento intervencionista cuya efectividad se ha evaluado en ensayos experimentales10 y clínicos11-14. La inducción de isquemia transitoria y controlada tras las reperfusión podría conducir a un menor daño por reperfusión que una terapia de reperfusión directa14. La ventaja de esta intervención es que es fácil de implementar durante una intervención coronaria percutánea (ICP). Se trata de episodios cortos e intermitentes de 1 minuto de reoclusión del flujo coronario (por ejemplo, reinflado del balón de angioplastia).
No obstante, éste sigue siendo un campo controvertido ya que hay estudios que avalan la fuerte cardioprotección que ofrece el iPost11 mientras que otros muestran resultados opuestos12. Una posible explicación de estos resultados tan dispares es que iPost podría tener un efecto protector sólo en aquellos casos en los que el tiempo isquémico previo no hubiese sido muy prolongado.
Para saber si el iPost tiene efectos cardioprotectores que varían en función del tiempo isquémico, llevamos a cabo un estudio experimental controlado en el que sometimos a varios cerdos a diferentes tiempos de isquemia coronaria y les asignamos a un grupo iPost o a uno de control. Empleamos tecnología de última generación (resonancia magnética cardiaca, [RMC]) para valorar el efecto cardioprotector de esta intervención.
MÉTODOS
Los estudios fueron aprobados por los Comités de Experimentación Animal competentes a nivel institucional y regional.
Diseño del estudio
El efecto cardioprotector iPost se puso a prueba en 2 grupos experimentales distintos: duración intermedia (30) y prolongada (40) de la isquemia seguida de reperfusión en ambos casos. Se sometió a todos los animales a una RMC multiparamétrica 1 semana después de la inducción del IM. Se optó por la ventana de 7 días para valorar el efecto de la intervención por ser este tiempo el que se recomienda en un consensos previos5. La definición de isquemia intermedia o prolongada se basó en anteriores experimentos en los que se observó que duraciones de isquemia < 30 minutos generaban TI muy pequeños (< 20% del área miocárdica en riesgo [AER]) lo cual impide la existencia de una ventana de cardioprotección en intervenciones farmacológicas bien establecidas (por ejemplo, metoprolol)15. Asimismo, en nuestro contexto experimental, duraciones de isquemia > 40 minutos se asociaron a TI muy grandes (> 80% del AER) con la correspondiente reducción de la ventana de cardioprotección15.
Según el principio de las 3 «R» sobre un menor uso de animales, los datos referidos al grupo experimental de duración prolongada de la isquemia (40 minutos) con/sin iPost, corresponde a experimentos cuyos resultados ya se habían publicado en un artículo con un objetivo distinto.16 Para este estudio, se realizaron experimentos ad hoc para evaluar el efecto cardioprotector del iPost en animales con isquemia de duración intermedia (30 min) (n = 28).
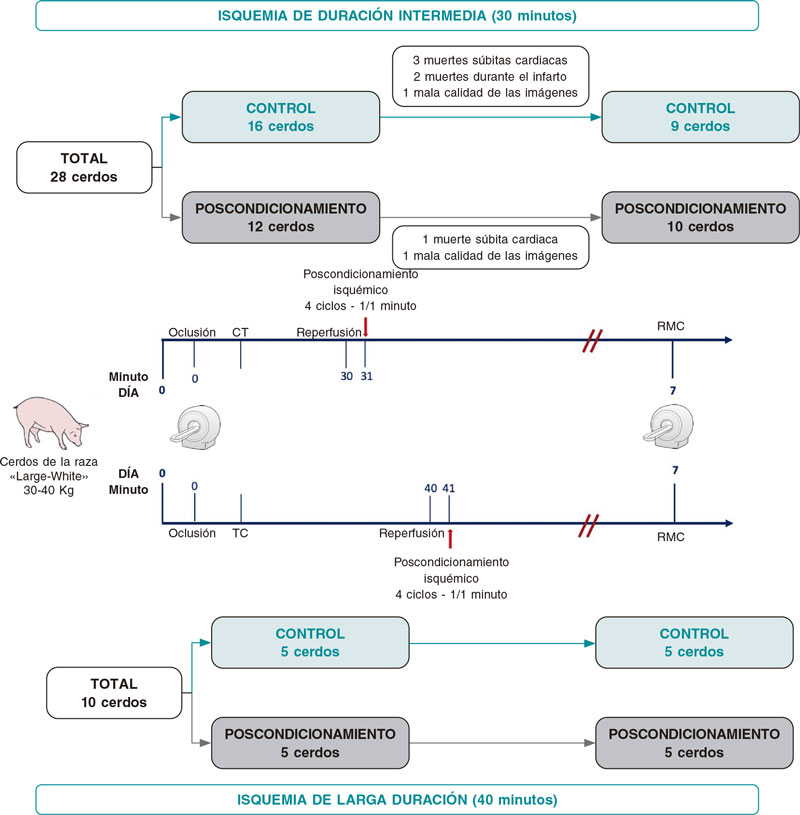
El protocolo del estudio fue el mismo para los 2 grupos de isquemia de diferente duración. En estos experimentos se emplearon cerdos macho castrados de la raza White-Large de 3 meses de edad con un peso de entre 30 y 40 kilos. Fueron asignados al grupo iPost o al de control antes de inducir el IM. El AER se estudió a partir de una tomografía computarizada multidetector realizada inmediatamente después de la oclusión coronaria siguiendo una metodología ya publicada.16 Siete días después de inducirles el IM, todos los animales fueron sometidos a una RMC multiparamétrica para poder estudiar el TI (objetivo primario), la FEVI y los tiempos de relajación T1 y T2 tanto en el AER como en el área remota (figura 1).
Figura 1. Figura central. Diseño del estudio y diagrama de flujo. RMC: resonancia magnética cardiaca; TC: tomografía computarizada.
Protocolo para la administración de anestesia y cuidado animal
Cada prueba o experimento se llevó a cabo bajo sedación profunda que se indujo mediante una inyección intramuscular de ketamina (20 mg/Kg), xilacina (2 mg/Kg) y midazolam (0,5 mg/Kg) y se mantuvo mediante la infusión continua de ketamina (2 mg/Kg/h), xilacina (0,2 mg/Kg/h) y midazolam (0,2 mg/Kg/h), Se administró buprenorfina intramsucular (0,03 mg/Kg) inmediatamente antes del experimento de inducción de IM.
Los animales fueron intubados y ventilados mecánicamente mediante ventilación obligatoria intermitente sincronizada con control de volumen (fracción de oxígeno inspirado del 28%).
Para evitar la aparición de trombosis coronaria tras el IM inducido por balón, los animales recibieron 150 mg de clopidogrel por vía oral el mismo día de la intervención y 75 mg 24 y 48 horas después. Todos los animales fueron sacrificados inmediatamente después de la RMC que se hizo el 7.o día.
Protocolo sobre el manejo del infarto de miocardio y poscondicionamiento
Se empleó el mismo protocolo de isquemia-reperfusión a tórax cerrado en todos los animales16 consistente en una oclusión de la descendente anterior (inmediatamente distal a la primera rama diagonal) de 30 o 40 minutos con un balón de angioplastia monorraíl insertado percutáneamente a través de la arteria femoral. La posición del balón y el estado del inflado del mismo se monitorizó con angiografía. Se administró 1 único bolo intraarterial de 300 UI/kg de heparina no fraccionada inmediatamente antes de la oclusión coronaria. Además, para reducir la incidencia de arritmias ventriculares, se optó por una infusión continua de amiodarona (300 mg/h, sin bolo) inmediatamente después de la oclusión coronaria, que se mantuvo hasta la retirada de los catéteres.
Los cerdos fueron distribuidos en proporción 1:1 al grupo iPost o al grupo de control previo a la inducción del IM. Tras completar el tiempo de isquemia (30 o 40 minutos según protocolo), los animales asignados al grupo de control recibieron reperfusión directa (desinflado del balón) y los del iPost 4 ciclos de inflado/desinflado de balón de 1 minuto de duración cada uno, iniciados 1 minuto después de la reperfusión. La permeabilidad de la arteria se valoró después de cada ciclo de inflado/desinflado mediante angiografía.
Protocolo para la realización de tomografía computarizada multidetector potenciada arterial y análisis
Tras la oclusión coronaria se realizó una tomografía computarizada multidetector (TCMD) empleando un escáner de tomografía computarizada de 64 cortes (Brilliance CT 64; Philips Healthcare, Estados Unidos) tras la administración IV de un medio de contraste yodado. Al realizarse durante la isquemia (con el balón inflado), las regiones no potenciadas representan con precisión la región isquémica (el AER). Las imágenes de TCMD se analizaron empleando un software dedicado (Extended MR Workspace 2,6; Philips Healthcare, Países Bajos) y fueron obtenidas por 2 observadores ciegos a la asignación de los grupos. La orientación de los ejes cortos se obtuvo de las imágenes obtenidas mediante tomografía computarizada volumétrica con reconstrucción multiplanar. Tanto el AER como el área remota se pudieron identificar visualmente gracias a las diferencias potenciadas por contraste y se delinearon manualmente expresándose como porcentaje del área del ventrículo izquierdo (VI)15,16.
Protocolo para la realización de la resonancia magnética cardiaca
Las RMC se realizaron 7 días después del IM con un escáner de cuerpo entero Philips 3-Tesla Achieva Tx (Philips Healthcare, Países Bajos) equipado con una bobina de matriz de fase de 32 elementos. El protocolo de imágenes incluyó una imagen cine segmentada estándar con secuencia de cine SSFP (steady-state free precession) que proporcionó referencias anatómicas de alta calidad y permitió valorar la masa del ventrículo izquierdo, el grosor de la pared y la FEVI, una secuencia de mapeo de T1 (secuencia de inversión-recuperación look-locker modificada) para valorar el tiempo de relajación T1 nativo, otra secuencia de mapeo de T2 a partir de imágenes obtenidas mediante secuencia de spin-echo para obtener el tiempo de relajación T2 del tejido miocárdico17 y una secuencia de pulsos de inversión-relajación en turbo spin-echo ponderada en T1 adquirida entre 10 y 15 minutos después de la administración de contraste con gadolinio (realce tardío de gadolinio, RTG) para valorar el TI. Las imágenes de RMC se analizaron empleando un software dedicado (MR Extended Workspace 2,6; QMassMR 7,6; Medis, Países Bajos e IntelliSpace Portal, Philips Healthcare, Países Bajos) y fueron obtenidas por 2 observadores experimentados en análisis RMC ciegos a la asignación de los grupos.
Análisis estadístico
La distribución normal de los datos se valoró empleando la prueba de Shapiro-Wilk. Las variables cuantitativas se expresaron como mediana (rango intercuartil). Las categóricas como números y porcentajes con redondeo al número entero más próximo. Se realizó una prueba ANOVA de 2 vías en toda la muestra con los datos obtenidos de las RMC realizadas el 7.o día (29 cerdos) para determinar el efecto del tiempo de isquemia e iPost sobre los objetivos primarios y secundarios (TI, % de la masa del VI), TI indexado al AER, FEVI, tiempo de relajación T2 y tiempo de relajación T1 nativo). En las variables con una interacción significativa entre la duración de la isquemia y el iPost, se hizo un análisis post hoc (método de Tukey) para confirmar las diferencias observadas. Se estimó el tamaño de la muestra en base a nuestros experimentos anteriores sobre cardioprotección con metoprolol.15 Los animales que se perdieron fueron reemplazados para mantener el tamaño de la muestra requerido.
RESULTADOS
Grupos del estudio
Protocolo de isquemia intermedia (30 min)
Tal y como se muestra en la figura 1, se indujo un IM a un total de 28 animales tras reemplazar a los ejemplares perdidos. Fallecieron 3 (19%) de los 16 cerdos asignados al grupo control, 3 (19%) murieron durante el IM y otros 3 (19%) de muerte súbita antes de la RMC. Uno (10%) de los 10 animales que completaron el protocolo de RMC al 7º día fue excluido del análisis por la mala calidad de las imágenes.
Ninguno de los 12 cerdos asignados al grupo iPost falleció durante la inducción del IM (0%) pero 1 (8%) sí falleció súbitamente antes de poder hacer la RMC. Uno (9%) de los 11 animales que completaron el protocolo de RMC al 7º fue excluido del análisis por la mala calidad de las imágenes.
En consecuencia, la población final disponible para poder valorar los resultados fue de 19 cerdos (9 controles y 10 sometidos a iPost, figura 1).
Protocolo de isquemia prolongada (40 min)
Tal y como se muestra en la figura 1, se incluyó a 10 animales que ya habían completado el protocolo en otro estudio publicado.
Características basales
El grupo de control y el iPost fueron similares tanto en el peso como en las características basadas en la RMC basales salvo en la masa del ventrículo izquierdo indexada que fue mayor en el grupo de control de animales con tiempos de isquemia de 40 minutos (tabla 1). Se observó una tendencia no significativa hacia un mayor AER según la TCMD (% de la masa del ventrículo izquierdo) en el grupo iPost (tabla 1).
Tabla 1. Características basales
| Variable | Muestra global (n = 29) |
Isquemia intermedia (30 min) (n = 19) |
Isquemia prolongada (40 min) (n = 10) |
|||
|---|---|---|---|---|---|---|
| Control (n = 14) |
iPost (n = 15) |
Control (n = 9) |
iPost (n = 10) |
Control (n = 5) |
iPost (n = 5) |
|
| Peso, kg | 36,2 (34,0-38,5) |
33,5 (31,0-40,0) |
36,0 (34,5-38,5) |
37,5 (31,0-41-0) |
36,5 (30,5-38) |
32,5 (32,5-33,5) |
| FEVI, % | 57,6 (55,2-63,0) |
55,9 (52,3-59,5) |
57,7 (55,9-61,3) |
55,8 (52,3-65,4) |
57,4 (55,2-63,0) |
56,0 (55,8-59,3) |
| VTDVII, ml/m2 | 104,2 (93,5-105,8) |
105,9 (96,1-123,6) |
95,8 (87,5-105,3) |
97,7 (94,5-105,9) |
112,8 (105,8-123,5) |
127,4 (123,6-128,4) |
| VTSVII, ml/m2 | 43,0 (37,0-46,8) |
45,6 (38,0-54,5) |
40,7 (35,8-46,6) |
42,8 (37,3-45,7) |
46,1 (44,3-48,8) |
54,4 (51,7-61,4) |
| Área miocárdica en riesgo (% VI) | 27,8 (26,2-27,2) |
31,7 (29,2-32,3) |
24,6 (23,3-27,6) |
27,3 (26,0-29,2) |
27,8 (26,2-27,8) |
31,7 (29,2-32,3) |
|
FEVI: fracción de eyección del ventrículo izquierdo; iPost: poscondicionamiento isquémico; VI: ventrículo izquierdo; VTDVII: volumen telediastólico del ventrículo izquierdo indexado; VTSVII: volumen telesistólico del ventrículo izquierdo indexado. |
||||||
Resultados de la resonancia magnética cardiaca
Efecto del iPost en un modelo de protocolo de isquemia intermedia
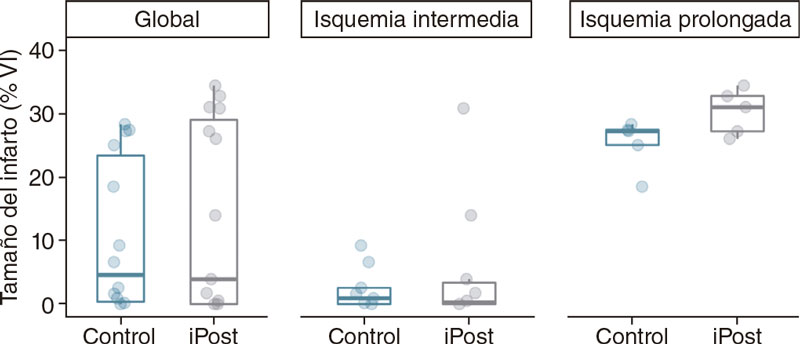
En el grupo de isquemia de duración intermedia, iPost no tuvo ningún efecto sobre ninguna de las variables evaluadas mediante RMC (tabla 2; figura 2, figura 3 y figura 4). Tanto el grupo de animales asignados a recibir iPost como el grupo de control presentan un TI pequeño no observándose ninguna diferencia entre los distintos grupos de intervención (0,3% de la masa del VI [0,0 – 3,9] frente al 0,9% [0,0 – 2,6] % del VI en el grupo iPost y de control, respectivamente; p = 0,378). Tampoco se observó ninguna diferencia en el TI indexado (TI/AER) (tabla 2).
Tabla 2. Parámetros de RMC para el grupo de isquemia intermedia
| Variable | Isquemia de duración intermedia (n = 19) | ||
|---|---|---|---|
| Control (n = 9) | iPost (n = 10) | p (análisis post hoc) | |
| TI, % masa del VI | 0,9 (0,0-2,6) | 0,3 (0,0-3,9) | 0,378 |
| TI indexado, TI/AER (%) | 3,8 (0,0-8,5) | 0,9 (0,0-15,1) | 0,474 |
| FEVI, % | 54,0 (50,2-55,9) | 52,9 (47,1-56,0) | 0,521 |
| VTDVII, ml/m2 | 98,7 (92,3-104,1) | 107,3 (90,0-118,6) | 0,438 |
| VTSVII, ml/m2 | 45,9 (40,4-52,4) | 48,5 (41,0-55,2) | 0,355 |
| Tiempo de relajación T2 en el AER, ms | 51,3 (49,3-54,8) | 57,0 (53,2-58,5) | 0,583 |
| Tiempo de relajación T2 en el AR, ms | 45,6 (42,2-46,1) | 44,7 (43,7-47,4) | 0,881 |
| Tiempo de relajación T1 nativo en el AER, ms | 1.179,2 (1.167,1-1.266,4) | 1.225,9 (1.170,2-1.306,2) | 0,584 |
| Tiempo de relajación T1 nativo en el AR, ms | 1.087,8 (1.075,1-1.109,7) | 1.078,4 (1.051,2-1.134,8) | 0,925 |
|
AER: área miocárdica en riesgo; AR: área remota; FEVI: fracción de eyección del ventrículo izquierdo; iPost: poscondicionamiento isquémico; TI: tamaño del infarto; VI: ventrículo izquierdo; VTDVII: volumen telediastólico del ventrículo izquierdo indexado; VTSVII: volumen telesistólico del ventrículo izquierdo indexado. |
|||
Figura 2. Diferencias en el tamaño del infarto según las imágenes obtenidas por resonancia magnética cardiaca (% de la masa del ventrículo izquierdo) entre los grupos de control e iPost, en la población general y según la duración de la isquemia.
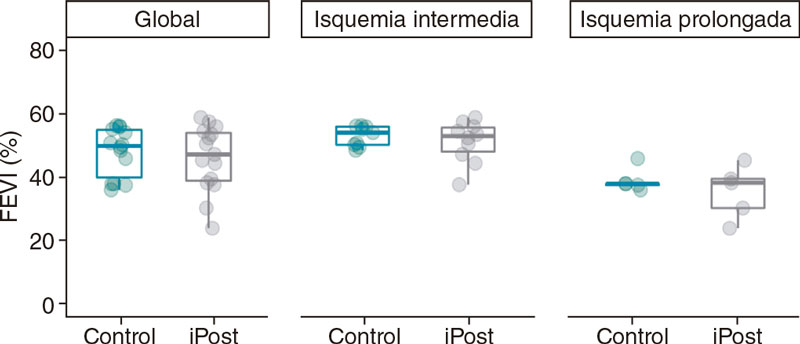
Figura 3. Diferencias en la FEVI según las imágenes obtenidas por resonancia magnética cardiaca (%) entre los grupos de control e iPost, en la población general y según la duración de la isquemia.
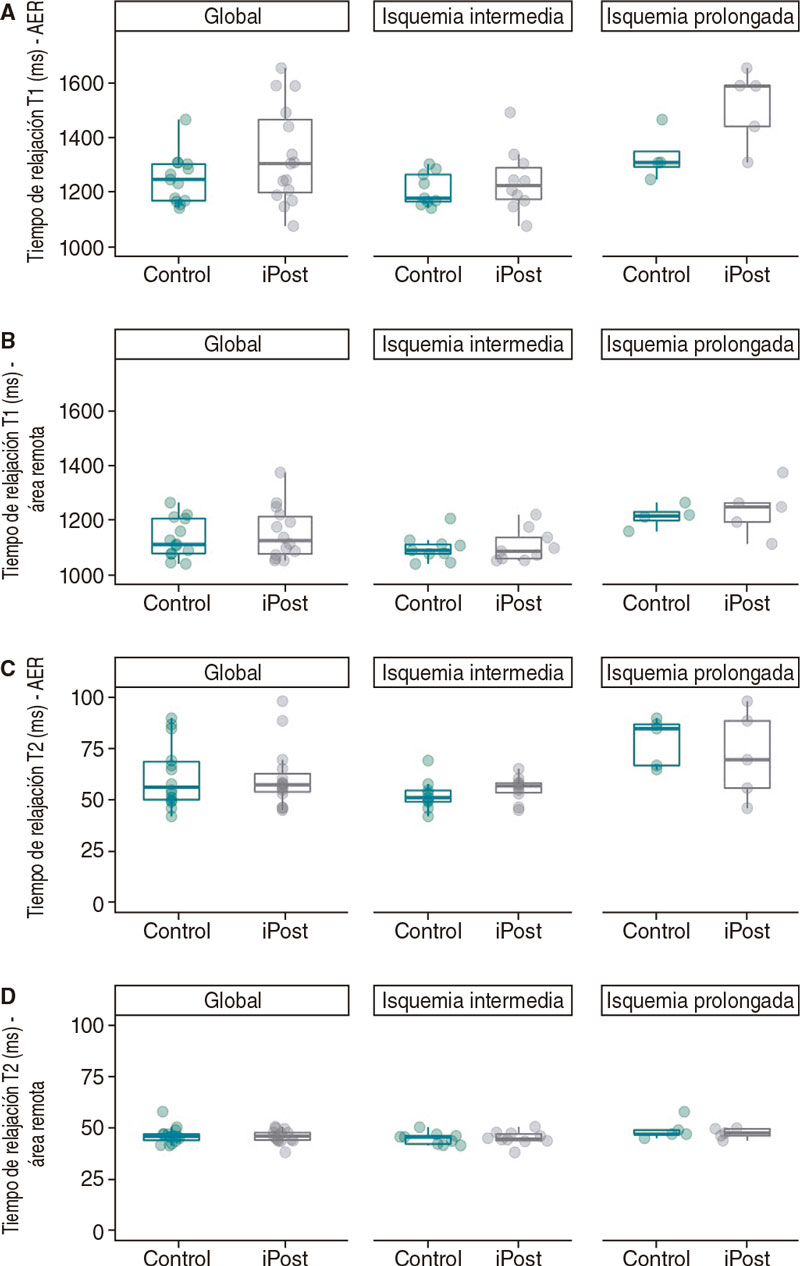
Figura 4. Diferencias en las imágenes obtenidas por resonancia magnética cardiaca en los tiempos de relajación T1 y T2 nativos (ms) entre los grupos de control e iPost, en la población general y según la duración de la isquemia. A: tiempo de relajación T1 nativo en el área miocárdica en riesgo. B: tiempo de relajación T1 nativo en el área remota. C: tiempo de relajación T2 nativo en el área miocárdica en riesgo. D: tiempo de relajación T2 nativo en el área remota. AER: área miocárdica en riesgo.
Efecto del iPost en un modelo de protocolo de isquemia prolongada
Los resultados de este experimento fueron publicados previamente16. El iPost no tuvo ningún efecto cardioprotector a la hora de reducir el TI (31,1% de la masa del VI [27,3–32,8] LV frente al 27,3% [25,1– 27,5] en los grupos iPost y de control, respectivamente; p = 0,248). Tampoco se halló ninguna diferencia en el TI indexado (TI/AER), ni diferencias en otros parámetros basados en la RMC, salvo un tiempo de relajación T1 más largo en el AER (1.590,3 ms [1.441,6 – 1.591,4] frente a 1.309,7 ms [1.248,1–1.310,8] en los grupos iPost y de control, respectivamente; p = 0,002) (tabla 3 y figura 2, figura 3 y figura 4).
Tabla 3. Parámetros de RMC para el grupo de isquemia prolongada
| Variable | Isquemia de larga duración (n = 10) | ||
|---|---|---|---|
| Control (n = 5) | iPost (n = 5) | p (análisis post hoc) | |
| TI, % de la masa del VI | 27,3 (25,1-27,5) | 31,1 (27,3-32,8) | 0,248 |
| TI indexado, TI/AER (%) | 98,2 (70,7-98,8) | 96,2 (93,4-100) | 0,640 |
| FEVI, % | 37,9 (37,4-38,0) | 38,2 (30,2-39,4) | 0,323 |
| VTDVII, ml/m2 | 150,8 (150,4-153,1) | 150,9 (148,3-159,8) | 0,644 |
| VTSVII, ml/m2 | 95,1 (94,1-96,6) | 105,4 (88,8-109,8) | 0,234 |
| Tiempo de relajación T2 en el AER, ms | 85,0 (67,0-87,0) | 69,8 (55,9-88,7) | 0,342 |
| Tiempo de relajación T2 en el AR, ms | 47,0 (47,0-49,0) | 47,6 (46,2-49,6) | 0,420 |
| Tiempo de relajación T1 nativo en el AER, ms | 1.309,7 (1.248,1-1.310,8) | 1.590,3 (1.441,6-1.591,4) | 0,002 |
| Tiempo de relajación T1 nativo en el AR, ms | 1.209,7 (1.156,8-1.217,3) | 1.246,8 (1.191,2-1.260,9) | 0,101 |
|
AER: área miocárdica en riesgo; AR: área remota; FEVI: fracción de eyección del ventrículo izquierdo; iPost: poscondicionamiento isquémico; TI: tamaño del infarto; VI: ventrículo izquierdo; VTDVII: volumen telediastólico del ventrículo izquierdo indexado; VTSVII: volumen telesistólico del ventrículo izquierdo indexado. |
|||
Interacción entre la duración de la isquemia y los beneficios del iPost
No se observó ninguna interacción significativa entre la duración de la isquemia y el efecto del iPost ni en el TI evaluados mediante RMC (3,9% de la masa del VI [0,0–30,9] frente al 4,6% [0,2 – 25,1]) en los grupos iPost y de control, respectivamente, F [1,25] = 0,18; p = 0,672). En consecuencia, el iPost no se asoció a un menor TI con independencia de la duración de la isquemia (tabla 4 y figura 2). Tampoco se observó ninguna diferencia en el TI indexado (TI/AER), la FEVI ni en los volúmenes telediastólicos ni telesistólicos del VI (tabla 4 y figura 3).
Tabla 4. Parámetros de RMC para la población general incluidos tiempos de isquemia intermedios y prolongados
| Variable | Población general (n = 29) | ||
|---|---|---|---|
| Control (n = 14) | iPost (n = 15) | p (ANOVA de 2 vías) | |
| TI, % de la masa del VI | 4,6 (0,2-25,1) | 3,9 (0,0-30,9) | 0,672 |
| TI indexado, TI/AER (%) | 15,7 (0,7-70,7) | 15,1 (0,0-96,2) | 0,965 |
| FEVI, % | 49,8 (37,9-55,1) | 47,1 (38,2-54,4) | 0,738 |
| VTDVII, ml/m2 | 104,9 (98,1-150,4) | 118,6 (90,3-148,3) | 0,751 |
| VTSVII, ml/m2 | 53,5 (45,4-94,1) | 55,2 (43,8-88,8) | 0,628 |
| Tiempo de relajación T2 en el AER, ms | 56,4 (49,9-69,4) | 57,5 (53,2-65,4) | 0,531 |
| Tiempo de relajación T2 en el AR, ms | 45,9 (43,6-47,0) | 46,0 (43,8-47,8) | 0,892 |
| Tiempo de relajación T1 nativo en el AER, ms | 1.240,7 (1.167,1-1.304,5) | 1.306,2 (1.190,7-1.492,7) | 0,024 |
| Tiempo de relajación T1 nativo en el AR, ms | 1.107,5 (1.075,1-1.203,9) | 1.111,4 (1.057,8-1.218,2) | 0,164 |
|
AER: área miocárdica en riesgo; AR: área remota; FEVI: fracción de eyección del ventrículo izquierdo; iPost: poscondicionamiento isquémico; TI: tamaño del infarto; VI: ventrículo izquierdo; VTDVII: volumen telediastólico del ventrículo izquierdo indexado; VTSVII: volumen telesistólico del ventrículo izquierdo indexado. |
|||
Por el contrario, los animales que recibieron iPost presentaron tiempos de relajación T1 nativo más largos en el AER (1.306,2 [1.190,7–1.492,7] frente a 1.240,7 ms [1.167,1–1.304,5] en los grupos iPost y de control, respectivamente (F [1,25] = 5,79; p = 0,024) no observándose ninguna diferencia en el área remota ni en el tiempo de relajación T2 (figura 4).
DISCUSIÓN
En este estudio, se puso a prueba el posible efecto cardioprotector del iPost en un gran modelo animal de isquemia/reperfusión con tiempos de isquemia de duración intermedia (30 min) y prolongada (40 min)15. En nuestro modelo porcino de isquemia/reperfusión, iPost no redujo el TI en ninguno de los protocolos de duración de la isquemia tal y como confirmó la RMC realizada 7 días después de inducir el IM. Se observaron signos no significativos de daño (tendencia hacia un mayor TI, una menor FEVI y tiempos de relajación T1 más largos en la región isquémica) asociados al iPost en aquellos animales en los que se empleó el protocolo de isquemia de duración prolongada. Nuestros datos no avalan el uso de iPost como una intervención capaz de mejorar los resultados en el contexto de una LIR.
iPost es una intervención muy atractiva para reducir la LIR ya que puede aplicarse en la sala de hemodinámica en el momento de la reperfusión2. Técnicamente, es una intervención directa que no requiere de ningún otro material al ya empleado habitualmente durante la realización de una ICP.
El precondicionamiento isquémico local (ciclos repetitivos de breve oclusión coronaria/restauración del flujo sanguíneo previo a isquemia prolongada) ha demostrado sistemáticamente ser una intervención cardioprotectora muy potente18 para reducir la LIR. En la mayoría (si no en todos) de los contextos experimentales esta estrategia se asocia, de un modo consistente, a un descenso importante del TI. No obstante, este procedimiento no es aplicable en pacientes reales. Para superar esta limitación, el grupo de Vinten-Johansen estudió si la misma maniobra de condicionamiento isquémico iniciada justo después de la reperfusión (iPost) podría también estar asociada a un menor TI10. Este grupo mostró en un modelo canino de LIR (60 min de isquemia seguidos de restauración del flujo sanguíneo), que 3 ciclos de «30 segundos de reoclusión seguidos de 30 segundos de reperfusión» aplicados 1 minuto después de la reperfusión se asociaron a un descenso significativo del TI10. Debido a su fácil implementación, el iPost se evaluó en un estudio clínico piloto. El grupo de Ovize confirmó en un pequeño grupo de pacientes con IAMCEST que el iPost (en este caso, 4 ciclos de 1 min oclusión seguidos de 1 min reperfusión) iniciado justo después de reperfusión mediada por ICP se asoció a un menor TI11. En otro pequeño estudio de 79 pacientes con IAMCEST, Freixa et al. aseguraron que el iPost no solo no redujo el TI sino que el miocardio salvado también fue significativamente menor19. Otros 2 estudios clínicos más extensos, el POST20 (n = 700) y el DANAMI-3–iPOST12 (n = 1.234) tampoco lograron demostrar los beneficios del iPost.
Puede darse alguna explicación a los dispares resultados obtenidos. Se ha especulado con la posibilidad de que la cardioprotección que proporciona el iPost interactúe, de algún modo, con la duración de la isquemia precedente21. No obstante, no se ha podido demostrar en un estudio diseñado ad hoc. Teniendo esto en cuenta, realizamos este estudio en el que el iPost no proporcionó ninguna cardioprotección con independencia de la duración de la isquemia.
Aunque parece que no hay mucha diferencia entre 30 y 40 minutos de isquemia, sí se ha descrito con anterioridad que, en modelos porcinos, tiempos de oclusión < 30 min se asocian a TI muy pequeños mientras que oclusiones > 40 min están asociadas a infartos transmurales15,22,23. En líneas generales, en nuestro estudio, 4 ciclos de iPost (1 minuto de oclusión seguido de 1 minuto de reperfusión) no tuvieron ningún efecto cadioprotector asociado a un menor TI, % de la masa del VI o % del AER (tabla 2). Este fue el caso en ambos protocolos de duración de la isquemia. Aunque no se ha observado una interacción formal entre la duración de la isquemia y los efectos del iPost sobre el TI, algunos hallazgos sugieren un posible efecto deletéreo del iPost en el protocolo de isquemia de duración más prolongada (tendencia hacia un mayor TI, una menor FEVI y, especialmente, un tiempo de relajación T1 mucho más largo en el AER). Además, aunque no se observaron diferencias significativas en el grupo sometido a isquemia intermedia, cuando se analizaron los datos por separado (figura 2), se observó una cierta asimetría hacia mayores TI en el grupo iPost incluidos los 2 ejemplares con los mayores TI de toda la cohorte con oclusiones de 30 minutos. Además, las diferencias observadas en los resultados de la RMC sugieren un posible efecto deletéreo del iPost en nuestro modelo de isquemia-reperfusión: los cerdos del grupo iPost tuvieron tiempos de relajación T1 nativos mucho más largos, lo cual es un marcador indirecto de una mayor fibrosis intersticial.5 También descubrimos una tendencia no significativa hacia una menor FEVI en animales sometidos a iPost tanto en el grupo de isquemia intermedia como prolongada. En cualquier caso, este hallazgo podría deberse a una tendencia no significativa hacia un mayor AER en el grupo sometido a iPost (tabla 1).
Una posible explicación de estos resultados es el inicio tardío del protocolo iPost puesto que los experimentos en animales han venido a confirmar que el efecto cardioprotector del iPost se circunscribe únicamente al primer minuto después de la reperfusión, efecto que no se observa si se demora la maniobra durante otros 60 segundos24,25. De hecho, en estudios clínicos en los que el iPost resultó ser efectivo, el protocolo de inflado/desinflado se inició inmediatamente después de la reperfusión11.
Limitaciones del estudio
Este estudio presenta algunas limitaciones que no deben obviarse. A pesar de ser uno de los más extrapolables, el presente modelo porcino presenta diferencias con respecto a las LIR humanas: la tolerancia a la isquemia es distinta según la especie y, además, la duración de la isquemia en cerdos no es igual que en humanos. Asimismo, el avance a lo largo del tiempo de las lesiones irreversibles es mucho más rápido en cerdos que en humanos tal y como confirma el avance transmural del infarto en isquemias con duraciones de entre 30 y 40 minutos. Otra limitación del estudio es que la asignación de los animales a los grupos iPost y de control no fue aleatoria, sino alternativa. En cualquier caso, la persona responsable de validar el análisis de la RMC desconocía la asignación de ejemplares a cada grupo. Además, como ya se ha expuesto, los datos del grupo sometido a isquemia prolongada coinciden con los experimentos ya realizados en nuestro centro por otro operador y publicados en otros medios. El uso de animales de diferentes colonias, diferentes protocolos de anestesia, diferentes materiales o de cualquier otro factor medioambiental explicaría, en parte al menos, las enormes diferencias observadas en el TI entre los grupos sometidos a isquemia intermedia y prolongada. No obstante, la decisión de usar estos datos ya publicados se basó en el principio de reducir el uso de animales en las investigaciones26,27.
CONCLUSIONES
En un modelo porcino de isquemia/reperfusión, el iPost (4 ciclos de 1 minuto de inflado/desinflado de balón) iniciado inmediatamente después de la reperfusión no redujo, de un modo efectivo, el TI. Esta ausencia de beneficios coincidió con los diferentes protocolos establecidos sobre duración de la isquemia que descartaron cualquier posible correlación entre la duración de la oclusión coronaria y los beneficios del iPost. En líneas generales, se observaron señales de daño secundario al iPost (tiempos de relajación T1 mucho más largos) debido, principalmente, a un efecto en el protocolo de isquemia prolongada.
FINANCIACIÓN
Este estudio está financiado por el Ministerio de Ciencia e Innovación («RETOS 2019», beca nº PID2019-107332RB-I00 a B.I). B.I ha recibido financiación de la Comisión Europea (becas ERC-CoG nº 819775 y H2020-HEALTH nº 945118). J.N. es receptor de una beca predoctoral (Jordi Soler Soler) concedida a través de CIBERCV. El CNIC está financiado por el Instituto de Salud Carlos III (ISCIII), el Ministerio de Ciencia e Innovación, la Fundación Pro CNIC y el Centro de Excelencia Severo Ochoa (CEX2020-001041-S).
CONTRIBUCIÓN DE LOS AUTORES
J. Nuche: experimentos y análisis de las imágenes por RMC, así como el análisis de datos y la redacción del manuscrito. C. Galán-Arriola: análisis ciego de las imágenes por RMC, apoyo al análisis estadístico y al diseño de las figuras. R. Fernández-Jiménez: experimentos y análisis del grupo de isquemia prolongada. M. I. Higuero Verdejo, R. Vazirani, M. Anguita-Gámez y A. Lanaspa: apoyo y colaboraron con los experimentos. G. J. López Martín: responsable de la obtención de las imágenes por TC y RMC. J. Sánchez-González: diseño del protocolo de obtención de imágenes por RMC. B. Ibáñez: diseño del proyecto, supervisión de resultados y aprobación de la versión final del manuscrito previo a su publicación.
CONFLICTO DE INTERESES
J. Sánchez-González trabaja para Philips Healthcare. Los autores no han declarado ningún conflicto de intereses. Todos los coautores han leído y están de acuerdo con los contenidos del manuscrito y aseguran no tener ningún conflicto de interés económico.
AGRADECIMIENTOS
Deseamos expresar nuestro agradecimiento a Eugenio Fernández, Tamara Córdoba, Inés Sanz, Nuria Valladares, Antonio Benítez, Santiago Rodríguez-Colilla y Rubén Mota por el apoyo técnico y veterinario prestado tanto en el centro de animales como en la granja del CNIC.
¿QUÉ SE SABE DEL TEMA?
- Es de suma importancia identificar aquellos procedimientos intervencionistas o farmacológicos capaces de reducir el TI, un factor que contribuye enormemente a la insuficiencia cardiaca a largo plazo en supervivientes de IAMCEST.
- La cardioprotección en torno al iPost local es un asunto controvertido tanto en modelos experimentales como en estudios clínicos.
- La posible relación entre duración de la isquemia y beneficios del iPost podría explicar esta controversia.
¿QUÉ APORTA DE NUEVO?
- Confirma que el iPost no reduce el TI.
- La ausencia de beneficios coincide con lo que apuntan diferentes protocolos de duración de la isquemia que descartan cualquier posible interacción entre la duración de la oclusión coronaria y los beneficios del iPost.
- El iPost se asocia a daños, sobre todo si se aplica tras una isquemia de larga duración.
BIBLIOGRAFÍA
1. Reed GW, Rossi JE, Cannon CP. Acute myocardial infarction. Lancet 2017;389:197-210.
2. De Maria GL, Garcia-Garcia HM, Scarsini R, et al. Novel device-based therapies to improve outcome in ST-segment elevation myocardial infarction. Eur Heart J Acute Cardiovasc Care 2021.
3. Stone GW, Selker HP, Thiele H, et al. Relationship Between Infarct Size and Outcomes Following Primary PCI: Patient-Level Analysis From 10 Randomized Trials. J Am Coll Cardiol 2016;67:1674-1683.
4. Ibáñez B, Heusch G, Ovize M, Van de Werf F. Evolving therapies for myocardial ischemia/reperfusion injury. J Am Coll Cardiol 2015;65:1454-1471.
5. Ibanez B, Aletras AH, Arai AE, et al. Cardiac MRI Endpoints in Myocardial Infarction Experimental and Clinical Trials: JACC Scientific Expert Panel. J Am Coll Cardiol 2019;74:238-256.
6. Lorca R, Jiménez-Blanco M, García-Ruiz JM, et al. Coexistence of transmural and lateral wavefront progression of myocardial infarction in the human heart. Rev Esp Cardiol. 2021;74:870-877.
7. Ibanez B, James S, Agewall S, et al. 2017 ESC Guidelines for the management of acute myocardial infarction in patients presenting with ST-segment elevation: The Task Force for the management of acute myocardial infarction in patients presenting with ST-segment elevation of the European Society of Cardiology (ESC). Eur Heart J 2018;39:119-177.
8. Heusch G, Gersh BJ. The pathophysiology of acute myocardial infarction and strategies of protection beyond reperfusion: a continual challenge. Eur Heart J 2017;38:774-784.
9. Hausenloy DJ, Botker HE, Engstrom T, et al. Targeting reperfusion injury in patients with ST-segment elevation myocardial infarction: trials and tribulations. Eur Heart J 2017;38:935-941.
10. Zhao ZQ, Corvera JS, Halkos ME, et al. Inhibition of myocardial injury by ischemic postconditioning during reperfusion: comparison with ischemic preconditioning. Am J Physiol Heart Circ Physiol 2003;285:H579-588.
11. Staat P, Rioufol G, Piot C, et al. Postconditioning the human heart. Circulation 2005;112:2143-2148.
12. Engstrøm T, Kelbæk H, Helqvist S, et al. Effect of Ischemic Postconditioning During Primary Percutaneous Coronary Intervention for Patients With ST-Segment Elevation Myocardial Infarction: A Randomized Clinical Trial. JAMA Cardiol 2017;2:490-497.
13. Eitel I, Stiermaier T, Rommel KP, et al. Cardioprotection by combined intrahospital remote ischaemic perconditioning and postconditioning in ST-elevation myocardial infarction: the randomized LIPSIA CONDITIONING trial. Eur Heart J 2015;36:3049-3057.
14. Heusch G, Rassaf T. Time to Give Up on Cardioprotection? A Critical Appraisal of Clinical Studies on Ischemic Pre-, Post-, and Remote Conditioning. Circ Res 2016;119:676-695.
15. Lobo-Gonzalez M, Galán-Arriola C, Rossello X, et al. Metoprolol blunts the time-dependent progression of infarct size. Basic Res Cardiol 2020;115:55.
16. Fernández-Jiménez R, Galán-Arriola C, Sánchez-González J, et al. Effect of Ischemia Duration and Protective Interventions on the Temporal Dynamics of Tissue Composition After Myocardial Infarction. Circ Res 2017;121:439-450.
17. Fernández-Jiménez R, Sánchez-González J, Aguero J, et al. Fast T2 gradient-spin-echo (T2-GraSE) mapping for myocardial edema quantification: first in vivo validation in a porcine model of ischemia/reperfusion. J Cardiovasc Magn Reson 2015;17:92.
18. Hausenloy DJ, Barrabes JA, Bøtker HE, et al. Ischaemic conditioning and targeting reperfusion injury: a 30 year voyage of discovery. Basic Res Cardiol 2016;111:70.
19. Freixa X, Bellera N, Ortiz-Pérez JT, et al. Ischaemic postconditioning revisited: lack of effects on infarct size following primary percutaneous coronary intervention. Eur Heart J. 2012;33:103-112.
20. Hahn JY, Song YB, Kim EK, et al. Ischemic postconditioning during primary percutaneous coronary intervention: the effects of postconditioning on myocardial reperfusion in patients with ST-segment elevation myocardial infarction (POST) randomized trial. Circulation. 2013;128:1889-1896.
21. Manintveld OC, Te Lintel Hekkert M, van den Bos EJ, et al Cardiac effects of postconditioning depend critically on the duration of index ischemia. Am J Physiol Heart Circ Physiol. 2007;292:H1551-1560.
22. Fernández-Jiménez R, García-Prieto J, Sánchez-González J, et al. Pathophysiology Underlying the Bimodal Edema Phenomenon After Myocardial Ischemia/Reperfusion. J Am Coll Cardiol. 2015;66:816-828.
23. García-Ruiz JM, Fernández-Jiménez R, García-Alvarez A, et al. Impact of the Timing of Metoprolol Administration During STEMI on Infarct Size and Ventricular Function. J Am Coll Cardiol. 2016;67:2093-2104.
24. Kin H, Zhao ZQ, Sun HY, et al. Postconditioning attenuates myocardial ischemia-reperfusion injury by inhibiting events in the early minutes of reperfusion. Cardiovasc Res. 2004;62:74-85.
25. Yang XM, Proctor JB, Cui L, Krieg T, Downey JM, Cohen MV. Multiple, brief coronary occlusions during early reperfusion protect rabbit hearts by targeting cell signaling pathways. J Am Coll Cardiol. 2004;44:1103-1110.
26. MacArthur Clark J. The 3Rs in research: a contemporary approach to replacement, reduction and refinement. Br J Nutr. 2018;120:S1-S7.
27. Bøtker HE, Hausenloy D, Andreadou I, et al. Practical guidelines for rigor and reproducibility in preclinical and clinical studies on cardioprotection. Basic Res Cardiol. 2018;113:39.