RESUMEN
Introducción y objetivos: La fuga paravalvular (FPV) moderada o grave tras el implante percutáneo de válvula aórtica (TAVI) se ha asociado a peores resultados. La calcificación de la válvula aórtica constituye un importante factor predictivo de FPV. ACURATE neo (Boston Scientific Corporation, Estados Unidos) es una válvula cardiaca transcatéter autoexpandible para el tratamiento de la estenosis aórtica degenerativa. Se evaluó la presencia de FPV tras el implante de ACURATE neo y neo2, así como el papel de la calcificación de la válvula aórtica.
Métodos: Se analizaron pacientes intervenidos de TAVI con ACURATE neo y neo2 de un hospital terciario de alto volumen. Todas las tomografías computarizadas cardiacas se analizaron con el software 3Mensio Structural Heart (Pie Medical Imaging, Países Bajos). El volumen de calcio aórtico se cuantificó mediante tomografía computarizada cardiaca con contraste. Se registró prospectivamente la evolución clínica y ecocardiográfica a 30 días.
Resultados: Se incluyeron 165 pacientes intervenidos de TAVI con ACURATE (neo = 87; neo2 = 78). La mediana de edad fue de 82 años, el 65% eran mujeres y la mediana de EuroSCORE II fue de 4,7 [rango intercuartílico, 2,4-6,1]. Los pacientes del grupo con neo presentaban una mayor cantidad de calcio total aórtico (320 frente a 200 mm3; p = 0,0305). No se hallaron diferencias significativas entre los grupos en cuanto a los resultados clínicos tanto durante el ingreso como a los 30 días. A los 30 días, la tasa de FPV ≥ leve (61 frente a 34%; p < 0,001) y de FPV ≥ moderada (15,9 frente a 5,4%, p = 0,0365) fue más alta en el grupo con neo. Tras el emparejamiento por puntuación de propensión ajustado por la cantidad total de calcio aórtico, neo2 se relacionó con un menor riesgo de FPV ≥ leve (odds ratio [OR] = 0,35; intervalo de confianza del 95% [IC95%], 0,18-0,69; p = 0,003) y de FPV ≥ moderada (OR = 0,16; IC95%, 0,03-0,74; p = 0,019).
Conclusiones: El TAVI con ACURATE neo2, en comparación con neo, se asocia a un menor riesgo de cualquier grado de FPV y a un menor riesgo de FPV ≥ moderada. Tras el ajuste por volumen de calcio aórtico, ACURATE neo2 se asocia a un menor riesgo de FPV.
Palabras clave: Implante percutáneo de válvula aórtica. Válvula cardiaca transcatéter. Fuga paravalvular.
Abstract
Introduction and objectives: Moderate or severe paravalvular leak (PVL) following transcatheter aortic valve implantation (TAVI) has been associated with worse outcomes. Aortic valve (AV) calcification is a strong predictor of PVL. ACURATE neo (Boston Scientific Corporation, United States) is a self-expanding transcatheter heart valve to treat degenerative aortic stenosis. We evaluated PVL after ACURATE neo and neo2 implantation, and the role of AV calcification.
Methods: We analyzed patients referred for TAVI with ACURATE neo and neo2 from a large volume tertiary center. All cardiac computed tomography scans were analyzed using 3Mensio Structural Heart software (Pie Medical Imaging, The Netherlands). The volume of AV calcium was quantified using contrast-enhanced cardiac computed tomography series. The 30-day clinical and echocardiographic data were prospectively recorded.
Results: We included 165 patients referred for TAVI with ACURATE (neo = 87; neo2 = 78). Median age was 82 years-old, 65% were women with a median EuroSCORE II of 4.7 [IQR, 2.4-6.1]. Patients in the neo group showed a larger amount of total AV calcium (320 mm3 vs 200 mm3; P = .0305). We found no significant inter-group differences regarding clinical outcomes both in-hospital or at 30-days. At 30-days, the rate of PVL ≥ mild (61% vs 34%; P < .001) and ≥ moderate (15.9% vs 5.4%; P = .0365) were higher in the neo group. After propensity score matching adjusted by the total amount of AV calcium, neo2 was associated with a lower risk of PVL ≥ mild (OR, 0.35, 95%CI, 0.18-0.69; P = .003), and ≥ moderate (OR, 0.16; 95%CI, 0.03-0.74; P = .019).
Conclusions: TAVI with ACURATE neo2 vs neo is associated with a lower risk of any degree of PVL and a reduced risk of PVL ≥ moderate. After adjusting for AV calcium volume, ACURATE neo2 was still associated with a lower risk of PVL.
Keywords: Transcatheter aortic valve implantation. Transcatheter heart valve. Paravalvular leak.
Abreviaturas
FPP: fuga periprotésica. TAVI: implante percutáneo de válvula aórtica. TCC: tomografía computarizada cardiaca. TSVI: tracto de salida del ventrículo izquierdo. VA: válvula aórtica. VCP: válvula cardiaca percutánea.
INTRODUCCIÓN
El implante percutáneo de válvula aórtica (TAVI) se ha convertido en una opción terapéutica cada vez más frecuente en pacientes con estenosis aórtica grave degenerativa en todo el espectro de riesgos estimados asociados a esta intervención1,2. Comparado con el reemplazo quirúrgico de válvula aórtica, las válvulas cardiacas percutáneas (VCP) se asocian a un mayor riesgo de fuga periprotésica (FPP), una cuestión especialmente preocupante en pacientes más jóvenes de bajo riesgo derivados para ser tratados de reemplazo de la válvula aórtica3. Además, la presencia de FPP residual moderada o grave tras el TAVI se ha asociado un mayor riesgo de mortalidad a corto y largo plazo4,5. El papel pronóstico de la FPP leve sigue siendo controvertido. Aun así, algunos estudios ofrecen peores resultados en pacientes con FPP leve frente a aquellos sin FPP o con una FPP mínima5. Estudios publicados han identificado la presencia y distribución del calcio en la válvula aórtica (VA) como predictor de la FPP residual tras el TAVI6,7. La calcificación del tracto de salida del ventrículo izquierdo (TSVI) también se asocia a un mayor riesgo de FPP residual8. ACURATE neo (Boston Scientific Corporation, Estados Unidos) es una VCP autoexpandible indicada para el tratamiento de la estenosis aórtica. No obstante, los primeros datos de la ACURATE neo revelaron una incidencia más alta de FPP moderada o grave frente a otras VCP autoexpandibles9. En su última versión, la ACURATE neo2 incorpora una falda doble interna y externa de pericardio, diseñada para reducir la incidencia de FPP.
El objetivo de este estudio fue comparar la incidencia de FPP 30 días después del implantar las válvulas ACURATE neo y neo2 y analizar el papel que juega el volumen de calcio aórtico en el desarrollo de FPP significativa tras el implante de las válvulas ACURATE neo y neo2.
MÉTODOS
Se seleccionó a pacientes de nuestro registro prospectivo TAVI derivados para recibir el TAVI con las válvulas ACURATE neo y neo2 en nuestro centro, un hospital terciario de alto volumen y centro de referencia en intervencionismo en cardiopatía estructural. En todos los casos, la decisión de realizar el TAVI frente a reemplazo quirúrgico fue acordada por el equipo multidisciplinar basándose en las características de los pacientes, sus comorbilidades y puntuaciones estimadas del riesgo. Según el protocolo del centro, se programaron visitas de seguimiento a los 30 días y ecocardiogramas transtorácicos de seguimiento en todos los pacientes. Debido al brote de la COVID-19 declarado en Países Bajos en marzo de 2020, algunas de las consultas de seguimiento a 30 días fueron telefónicas. Todos los ecocardiogramas transtorácicos los realizó un cardiólogo especializado en imágenes cardiacas que valoró las VCP según los criterios establecidos por las actuales guías de práctica clínica sobre el abordaje de la FPP tras el TAVI10. En consecuencia, la FPP se clasificó como inexistente/mínima, leve, moderada y grave según las recomendaciones incluidas en las definiciones estandarizadas VARC-3 (Valve Academic Research Consortium) en materia de investigación clínica sobre VA10. Los datos sobre los ingresos hospitalarios, las características demográficas, clínicas y de la intervención, los eventos intrahospitalarios y el seguimiento a 30 días se recopilaron prospectivamente y se gestionaron con el REDCap (Research Electronic Data Capture), una plataforma de software segura, basada en la web, para la captura y gestión de datos de investigaciones. El estudio ha recibido la aprobación del comité de ética de la investigación del St. Antonius Hospital (Nieuwegein, Países bajos). El consentimiento informado de los pacientes no fue necesario por el diseño retrospectivo y observacional del estudio.
Definiciones de los eventos
Tanto para estudiar los eventos adversos intrahospitalarios como a los 30 días, se emplearon las definiciones estandarizadas VARC-3 en materia de investigación clínica sobre VA10.
Análisis del calcio coronario por tomografía computarizada cardiaca
Se empleó el software 3Mensio Structural Heart versión 10.3 (Pie Medical Imaging, Bilthoven, Países Bajos) para evaluar todas las tomografías computarizadas cardiacas (TCC). Todas las TCC se analizaron, de forma independiente, por 1 operador experimentado en dimensionamiento de VCP y con formación específica en el software 3Mensio. En los primeros casos, nuestro protocolo TCC para la evaluación del TAVI no incluyó series de imágenes no potenciadas con contraste. Como consecuencia, las series de imágenes no potenciadas con contraste no estuvieron disponibles para muchos de estos pacientes. Por eso, se decidió evaluar el volumen de calcio coronario empleando series de imágenes potenciadas con contraste. Se siguió el método descrito recientemente por Angelillis et al. que demostró que existe una buena correlación con la puntuación obtenida en la escala Agatston mediante secuencias de TCC no potenciadas con contraste11. En resumen, este método para calcular el volumen de calcio coronario modifica el umbral de unidades Hounsfield en función de la media hallada en el TSVI. En TSVI altamente contrastados (> 300 UH) el umbral empleado fueron 850 UH. En TSVI poco contrastados, sin embargo, (< 300 UH), el umbral empleado fue de 450 UH. Tras identificar el anillo aórtico (plano basal), se empleó la ´herramienta de puntuación del volumen de calcio coronario´ incluida en el software para calcular el volumen aórtico. El cajetín aórtico tenía una longitud de 15 mm desde el plano basal hasta la raíz aórtica. Todo el calcio de la pared aórtica o coronarias se identificó meticulosamente y se excluyó del volumen estimado. También se calculó el volumen de calcio en el TSVI. A tal efecto, se incluyó un cajetín de 10 mm de longitud desde el plano basal hasta el TSVI. Se identificó todo el calcio asociado a la valva anterior de la válvula mitral y se excluyó del volumen estimado. Para analizar el impacto del tamaño de la VCP y de la relación entre el tamaño de la VCP y el tamaño del anillo aórtico, se calculó el índice de cobertura (100 x [diámetro de la válvula – diámetro del anillo derivado del perímetro TCC en sístole]/diámetro de la válvula) según la descripción establecida por Kim et al.12.
Análisis estadístico
Las variables cuantitativas se expresaron como media ± desviación estándar o mediana (rango intercuartil). Se empleó la prueba Kolmogorov-Smirnov para evaluar el ajuste a la normalidad. Las variables categóricas se expresaron como números (porcentaje). Las pruebas t de Student o U de Mann–Whitney se emplearon para comparar las variables continuas. Se empleó la prueba de la χ2 para las variables categóricas. Los predictores de FPP binaria se analizaron empleando la regresión logística. La prueba para buscar una tendencia por una variable categórica se realizó con el comando nptrend (STATA). Se emplearon 2 modelos de emparejamiento por puntuación de propensión (proporción 1:1), el primero, ajustado por la cantidad total de calcio VA según la TCC y el segundo, por la cantidad total de calcio en el TSVI, también según la TCC. Valores de p bilateral < 0,05 se consideraron significativos a nivel estadístico. Todas las pruebas se realizaron con el paquete de software estadístico STATA 12 (StataCorp LLC, Estados Unidos).
RESULTADOS
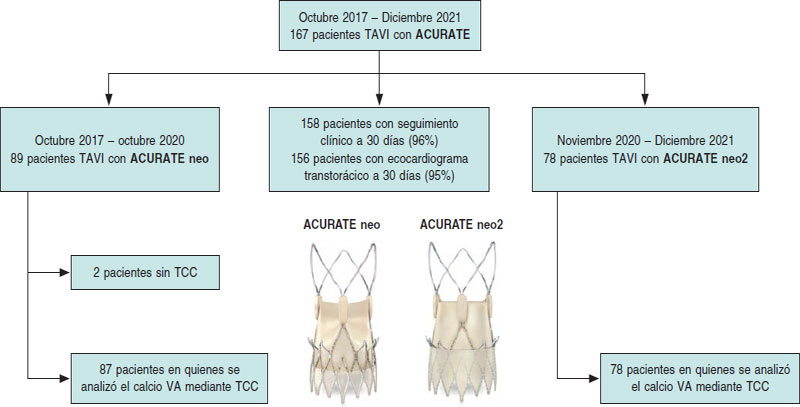
Se derivó a 167 pacientes para recibir el TAVI con la válvula ACURATE en nuestro centro entre octubre de 2017 y diciembre 2021. De estos, se derivó a 89 pacientes para el TAVI con una válvula ACURATE neo entre octubre de 2017 y octubre de 2020. Se derivó a 78 pacientes para recibir el TAVI con la válvula ACURATE neo2 entre noviembre de 2020 y diciembre de 2021. No se pudo obtenerse información TCC preoperatoria en 2 pacientes del grupo ACURATE neo y se los excluyó a ambos del análisis. Pudo hacerse un seguimiento a 30 días en 158 pacientes (96%). La información sobre la presencia de FPP a los 30 días mediante ecocardiograma transtorácico estuvo disponible en 156 pacientes (95%). El diagrama de flujo del estudio se muestra en la figura 1.
Las características basales de la cohorte se muestran en la tabla 1. No se observó ninguna diferencia en función de la edad, el sexo y los factores de riesgo cardiovascular entre los 2 grupos (mediana de edad, 82 años; el 65%, mujeres). Tampoco se observó ninguna diferencia entre los 2 grupos en lo referente al cálculo del riesgo según la escala EuroSCORE II (4,2 frente a 4,8; p = 0,5371). La tercera parte de los pacientes presentaban fibrilación auricular, la cuarta parte habían sido tratados de intervención coronaria percutánea y el 9% de cirugía de revascularización coronaria, sin que se observara ninguna diferencia entre los grupos. Casi 2 terceras partes de los pacientes presentaban una clase funcional NYHA III-IV antes de la intervención y el 17% presentaba disfunción sistólica (fracción de eyección del ventrículo izquierdo < 50%) según el ecocardiograma transtorácico.
Figura 1. Diagrama de flujo del estudio. TAVI: implante percutáneo de válvula aórtica; TCC: tomografía computarizada cardiaca; VA: válvula aórtica; Imágenes cortesía de Boston Scientific. Imágenes reproducidas con permiso de Boston Scientific Corporation o sus filiales.
Tabla 1. Características basales
| Cohorte global (n = 165) | ACURATE neo (n = 87) | ACURATE neo2 (n = 78) | p | |
|---|---|---|---|---|
| Edad, años | 82 [79-85] | 82 [79-85] | 82 [79-85] | 0,7536 |
| Sexo (mujer) | 107 (65) | 57 (66) | 50 (64) | 0,8493 |
| Hipertensión | 107 (65) | 61 (70) | 46 (59) | 0,1345 |
| Diabetes mellitus | 43 (26) | 20 (23) | 23 (30) | 0,3173 |
| EPOC | 43 (26) | 13 (15) | 11 (14) | 0,8786 |
| ERC | 47 (28) | 26 (30) | 21 (27) | 0,6739 |
| Enfermedad arterial periférica | 20 (12) | 9 (10) | 11 (14) | 0,4603 |
| Aorta en porcelana | 5 (3) | 1 (1) | 4 (5) | 0,1402 |
| Puntuación escala EuroSCORE II | 4,7 [2,4-6,1] | 4,2 [2,2-6,1] | 4,8 [2,7-6,5] | 0,5371 |
| FA previa | 60 (36) | 33 (38) | 27 (35) | 0,6585 |
| AIT/accidente cerebrovascular previo | 10 (6) | 4 (5) | 6 (8) | 0,4056 |
| ICP previa | 45 (27) | 25 (29) | 20 (26) | 0,6559 |
| CABG previa | 15 (9) | 7 (8) | 8 (10) | 0,6219 |
| Altura, cm | 167 ± 9 | 167 ± 9 | 167 ± 9 | 0,6656 |
| Peso, kg | 76 ± 13 | 75 ± 14 | 77 ± 13 | 0,3275 |
| IMC | 27 ± 5 | 27 ± 5 | 27 ± 5 | 0,4786 |
| Angina | 19 (12) | 9 (10) | 10 (13) | 0,6189 |
| Clase funcional III-IV según la NYHA | 105 (64) | 56 (64) | 49 (63) | 0,8366 |
| Disfunción sistólica (FEVI < 50%) | 28 (17) | 15 (17) | 13 (17) | 0,9218 |
|
AIT: accidente isquémico transitorio; CABG: cirugía de revascularización coronaria; EPOC: enfermedad pulmonar obstructiva crónica; ERC: enfermedad renal crónica; FA: fibrilación auricular; ICP: intervención coronaria percutánea; IMC: índice de masa corporal; NYHA: New York Heart Association. |
||||
Los datos principales sobre el análisis de la TCC se muestran en la tabla 2. No se observó ninguna diferencia en el diámetro medio, área o perímetro del anillo aórtico entre uno y otro grupo. En lo que respecta al análisis del calcio coronario, los pacientes del grupo neo presentaban una mayor cantidad total de calcio en la VA (320 frente a 200 mm3; p = 0,0305) condicionada por diferencias en la cantidad de calcio presente en las cúspides no coronaria y coronaria izquierda (154 frente a 98 mm3; p = 0,0149; 86 frente a 37 mm3; p = 0,0335, respectivamente). No se observaron diferencias entre grupos en la cuantificación del calcio coronario en el TSVI. No obstante, la presencia de cualquier cantidad de calcio en el TSVI fue más habitual en el grupo neo (61 frente al 41%; p = 0,0107). No se comunicaron diferencias en el índice de cobertura entre ambos grupos, con una mediana de sobredimensionado del 6.8% [RIQ, 4,4-8,5] en toda la cohorte.
Los datos sobre las características de la intervención y la evolución intrahospitalaria se muestran en la tabla 3. Todos los casos se realizaron mediante abordaje transfemoral. Los primeros 8 casos del grupo neo se realizaron con anestesia general y los restantes casos de los 2 grupos con anestesia local. Se observó una tendencia no significativa hacia un menor uso de la válvula ACURATE de 23 mm en la cohorte neo2 (p = 0,0523). La predilatación fue más habitual en el grupo neo2 (99 frente al 92%; p = 0,0434) y la posdilatación en el neo (43 frente al 22%; p = 0,0046). No se encontró ninguna diferencia en la presencia de FPP residual ≥ moderada en la angiografía inmediatamente después del implante (7 frente al 5%; p = 0,6346). En lo referente a los resultados intrahospitalarios, solo 1 paciente falleció en el ingreso índice por un cuadro de sepsis 59 días después del TAVI. Tres pacientes sufrieron un accidente cerebrovascular sin que se observara ninguna diferencia entre los grupos. Sí se observó, no obstante, una tendencia no significativa hacia un mayor riesgo hemorrágico en el grupo neo (18 frente al 12%; p = 0,2203), pero ninguna diferencia en la incidencia de hemorragias graves o amenazantes para la vida. El índice de implante de marcapasos definitivo fue del 7,3% sin observarse ninguna diferencia entre los distintos grupos. La duración media de la estancia hospitalaria fue de 2 días [RIQ, 2-4]. Se dio de alta a la mitad de los pacientes en tratamiento con ácido acetilsalicílico y los pacientes del grupo neo recibieron, con mayor frecuencia, tratamiento con doble antiagregación plaquetaria al alta (41 frente al 10%; p < 0,001). Se dio de alta al 40% de la cohorte bajo tratamiento con anticoagulación oral.
Tabla 2. Análisis mediante tomografía computarizada
| Cohorte global (n = 165) | ACURATE neo (n = 87) | ACURATE neo2 (n = 78) | p | |
|---|---|---|---|---|
| Dimensionamiento anular según TCC | ||||
| Diámetro mínimo del anillo aórtico | 21 ± 2 | 20 ± 2 | 21 ± 2 | 0,0757 |
| Diámetro máximo del anillo aórtico | 26 ± 2 | 26 ± 2 | 27 ± 2 | 0,7989 |
| Diámetro medio del anillo aórtico | 24 ± 1 | 23 ± 1 | 24 ± 1 | 0,2337 |
| Área del anillo aórtico | 427 ± 51 | 421 ± 50 | 434 ± 51 | 0,1134 |
| Perímetro del anillo aórtico | 74 ± 4 | 74 ± 4 | 75 ± 4 | 0,1159 |
| Cuantificación del calcio coronario | ||||
| Volumen total de calcio en la VA, mm3 | 266 [100-566] | 320 [123-696] | 200 [90-377] | 0,0305 |
| Volumen de calcio en la CNC-VA, mm3 | 125 [50-275] | 154 [68-305] | 98 [32-203] | 0,0149 |
| Volumen de calcio en la CCD-VA, mm3 | 62 [19-150] | 81 [25-193] | 51 [12-126] | 0,2122 |
| Volumen de calcio en la CCI-VA, mm3 | 56 [20-148] | 86 [24-194] | 37 [14-96] | 0,0335 |
| Volumen total de calcio en el TSVI, mm3 | 1 [0-29] | 4 [0-34] | 0 [0-22] | 0,2897 |
| Volumen de calcio en CNC-TSVI, mm3 | 0 [0-5] | 0 [0-6] | 0 [0-0] | 0,5474 |
| Volumen de calcio en la CCD-VA, mm3 | 0 [0-0] | 0 [0-0] | 0 [0-0] | 0,8615 |
| Volumen de calcio en la CCI-VA, mm3 | 0 [0-3] | 0 [0-7] | 0 [0-0] | 0,3521 |
| Cualquier volumen de calcio en el TSVI | 85 (52) | 53 (61) | 32 (41) | 0,0107 |
| Índice de cobertura (sobredimensionamiento) % | 6,8 [4,4-8,5] | 6,8 [3,7-8,4] | 6,9 [5,2-9] | 0,1769 |
|
CCD: cúspide coronaria derecha; CCI: cúspide coronaria izquierda; CNC: cúspide no coronaria; TSVI: tracto de salida del ventrículo izquierdo; VA: válvula aórtica. |
||||
Tabla 3. Característica de la intervención, evolución intrahospitalaria y seguimiento a 30 días
| Cohorte global (n = 165) | ACURATE neo (n = 87) | ACURATE neo2 (n = 78) | p | |
|---|---|---|---|---|
| Tipo de anestesia | 0,0060 | |||
| General | 8 (5) | 8 (9) | 0 | |
| Local | 157 (95) | 79 (91) | 78 (100) | |
| Tamaño de la válvula ACURATE | 0,0523 | |||
| 23 mm (pequeña) | 35 (21) | 24 (28) | 11 (14) | |
| 25 mm (mediana) | 78 (47) | 39 (44) | 39 (50) | |
| 27 mm (grande) | 52 (32) | 24 (28) | 28 (36) | |
| Predilatación | 157 (95) | 80 (92) | 77 (99) | 0,0434 |
| Posdilatación | 54 (33) | 37 (43) | 17 (22) | 0,0046 |
| FPP residual (angio) ≥ moderada | 10 (6) | 6 (7) | 4 (5) | 0,6346 |
| Resultados intrahospitalarios | ||||
| Mortalidad | 1 (0,6) | 0 | 1 (1,3) | 0,2894 |
| Infarto de miocardio | 0 | 0 | 0 | |
| Accidente cerebrovascular | 3 (1,8) | 1 (1,2) | 2 (2,6) | 0,4971 |
| Cualquier sangrado | 25 (15) | 16 (18) | 9 (12) | 0,2203 |
| Hemorragia mayor o amenazante para la vida | 4 (2,4) | 2 (2,3) | 2 (2,6) | 0,8634 |
| Nuevo BRI | 23 (14) | 13 (15) | 10 (13) | 0,2172 |
| Nuevo IMD | 12 (7,3) | 6 (6,9) | 6 (7,7) | 0,8442 |
| Estancia hospitalaria, días | 2 [2-4] | 2 [2-4] | 2 [2-3] | 0,5119 |
| Tratamiento al alta | ||||
| Ácido acetilsalicílico | 87 (53) | 46 (53) | 41 (53) | 0,9683 |
| Inhibidores del receptor plaquetario P2Y12 | 73 (44) | 55 (63) | 18 (23) | < 0,001 |
| DAPT | 44 (27) | 36 (41) | 8 (10) | < 0,001 |
| Anticoagulación oral | 66 (40) | 36 (41) | 30 (38) | 0,7025 |
| Seguimiento a 30 días (n = 158) | ||||
| Mortalidad | 4 (2,5) | 1 (1,2) | 3 (4) | 0,2700 |
| Infarto de miocardio | 0 | 0 | 0 | |
| Accidente cerebrovascular | 7 (4,4) | 2 (2,4) | 5 (6,7) | 0,1941 |
| Cualquier hemorragia | 27 (17) | 18 (22) | 9 (12) | 0,0986 |
| Gradiente VA medio | 8 ± 3 | 7 ± 3 | 8 ± 4 | 0,3160 |
| Gradiente VA medio ≥ 20 mmHg | 1 (0,6) | 0 | 1 (1,4) | 0,2909 |
| Gradiente VA máximo | 15 ± 7 | 14 ± 6 | 15 ± 7 | 0,3365 |
| Velocidad VA máxima ≥ 3 m/s | 3 (2) | 1 (1,2) | 2 (2,7) | 0,5006 |
| FPP ≥ leve | 75/156 (48) | 50 (61) | 25 (34) | 0,0007 |
| FPP ≥ moderada | 17/156 (10,9) | 13 (15,9) | 4 (5,4) | 0,0365 |
|
BRI: bloqueo de rama izquierda; DAPT: doble antiagregación plaquetaria; FPP: fuga periprotésica; IMD: implante de marcapasos definitivo; VA: válvula aórtica. |
||||
La información del seguimiento a 30 días se muestra en la tabla 3. La información de seguimiento clínico a 1 mes estuvo disponible en 158 pacientes. No se observó ninguna diferencia en la incidencia de muerte, infarto de miocardio y accidente cerebrovascular entre los 2 grupos. No obstante, sí se observó una tendencia hacia un mayor riesgo hemorrágico en los pacientes del grupo neo (22 frente al 12%; p = .0986). En el ecocardiograma de control, no se observó ninguna diferencia en los gradientes transvalvulares aórticos medio ni máximo entre los dos grupos (gradiente medio, 7 ± 3 frente a 8 ± 4 mmHg; p = 0,3160; gradiente máximo 14 ± 6 frente a 15 ± 7 mmHg; p = 0,3365). La incidencia de FPP ≥ leve a los 30 días fue mayor en el grupo neo frente al neo2 (61 frente al 34%; p < 0,001). La incidencia de FPP ≥ moderada también fue mayor en el grupo neo (15,9 frente al 5,4%; p = 0,0365) comparada con la última generación de esta VCP.
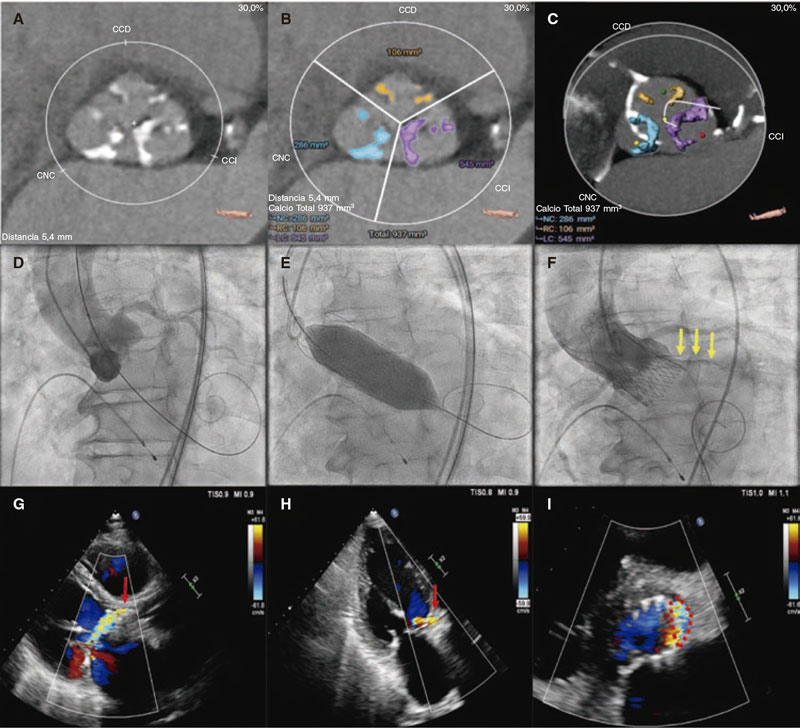
Un análisis crudo reveló una relación univariada significativa entre la ACURATE neo2 con una incidencia más baja de FPP ≥ leve (OR, 0,33; IC95%, 0,17-0,63; p = 0,001) y ≥ moderada (OR, 0,30; IC95%, 0,10-0,98; P = 0,045) en el seguimiento a 30 días. Un análisis de tendencias confirmó la existencia de una correlación significativa entre el cuartil de calcio en la VA y la presencia de FPP ≥ leve (Q1, 37%; Q2, 38%; Q3, 54%; Q4, 63%; valor p para la tendencia = 0,012). Este análisis no mostró correlaciones significativas entre el cuartil de calcio en la VA y la FPP ≥ moderada (P = 0,125), No obstante, el Q4 sí mostró una incidencia mucho mayor de FPP ≥ moderada en la comparativa binaria (Q4 frente a Q1-3; del 20 frente al 7,8%; p = 0,0322). Un análisis de tendencias no mostró correlación alguna entre el índice de cobertura y la presencia de FPP ≥ leve (p = 0,961) o ≥ moderada (p = 0,596). La figura 2 ilustra un caso de FPP moderada tras el implante de ACURATE neo en una VA intensamente calcificada.
Figura 2. A: varón de 79 años con estenosis aórtica grave y clase funcional NYHA III. La tomografía computarizada cardiaca (TCC) muestra la calcificación de las valvas de la válvula aórtica (VA) (con compromiso, sobre todo, de las cúspides coronaria izquierda y no coronaria). B-C: el calcio coronario de la VA calculado mediante TCC empleando el software 3Mensio arrojó un volumen total de calcio de 937 mm3 (Q4). D: proyección convencional coplanar de 3 cúspides del implante. Tras predilatación con un balón no distensible de 24 mm (no registrado) se implantó, con éxito, una válvula ACURATE neo de 27 mm. E: la válvula cardiaca percutánea se posdilató con un balón no distensible de 25 mm. F: no obstante, el angiograma final confirmó la presencia de fuga periprotésica (FPP) de leve a moderada asociada a la cúspide coronaria izquierda (flechas amarrillas). G-I: el ecocardiograma transtorácico a los 30 días confirmó la presencia de FPP moderada con un chorro procedente del área de la cúspide coronaria izquierda nativa (flechas y línea punteada rojas). Los vídeos tanto de la aortografía como del ecocardiograma de seguimiento se han incorporado al material adicional.
Tras ajustar por emparejamiento por puntuación de la propensión para la cantidad total de calcio en la VA (71 parejas), comparado con la válvula neo, el uso de la neo2 comportó un menor riesgo de FPP ≥ leve (OR, 0,35; IC95%, 0,18-0,69; p = 0,03) y ≥ moderada (OR, 0,16; IC95%, 00,3-0,74; p = 0,19) en el seguimiento. También se empleó un modelo de emparejamiento por puntuación de la propensión ajustado por la cantidad total de calcio en el TSVI (71 parejas). En este modelo, comparado con la válvula neo, el uso de la neo2 también se asoció a un menor riesgo de FPP ≥ leve (OR, 0,39; IC95%, 0,20-0,78; p = 0,08) y se observó una tendencia no significativa hacia un menor riesgo de FPP ≥ moderada en el seguimiento (OR, 0,33; IC95%, 0,10-10,8; p = 0,66).
DISCUSIÓN
Nuestro estudio analizó casos consecutivos derivados para TAVI con tecnología ACURATE en un centro terciario de gran volumen. Los principales hallazgos del estudio son: a) la incidencia de FPP ≥ moderada se redujo drásticamente con el uso de la ACURATE neo2 comparado con su versión anterior y b) esta menor FPP residual observada con la ACURATE neo2 no estuvo determinada por diferencias observadas en el grado de calcificación en la VA.
La VCP ACURATE neo recibió la marca CE en 2014 para el tratamiento de la estenosis aórtica grave degenerativa. A pesar de que los primeros registros confirmaron el buen rendimiento de esta tecnología, los estudios clínicos que la compararon a otras VCP autoexpandibles y balón-expandibles obtuvieron peores resultados. En el estudio SCOPE-I, el TAVI con la ACURATE neo no cumplió los criterios de no inferioridad con respecto a la SAPIEN 3 (Edwards Lifesciences, Irvine, CA, Estados Unidos) y las diferencias estaban condicionadas por una mayor incidencia de FPP moderada o grave con la ACURATE (9 frente al 3%)13. En el SCOPE-2, el TAVI con la ACURATE neo tampoco alcanzó el margen de no inferioridad con respecto a la VCP CoreValve Evolut (Medtronic, Estados Unidos) en lo referente a la mortalidad o a los accidentes cerebrovasculares a los 12 meses. En este estudio, una vez más, el uso de las válvulas ACURATE se asoció a una mayor incidencia de FPP moderada o grave comparado con Evolut (10 frente al 3%)9. Estos datos llevaron al desarrollo de una nueva versión de este dispositivo, la ACURATE neo2, que incorpora una falda externa de sellado un 60% más grande para minimizar la FPP.
Hasta la fecha, son pocos los datos comparativos de ambas tecnologías ACURATE. Rück et al. dieron datos comparativos de FPP con las VCP ACURATE neo y neo214. Los autores analizaron retrospectivamente la presencia de FPP mediante angiografía en 228 pacientes tratados con tecnología ACURATE (neo = 108; neo2 = 120) de 2 centros europeos. En este estudio, ACURATE neo2 tuvo una menor incidencia de FPP entre moderada y grave (1.7 frente al 13.9%). No obstante, en este estudio, los autores no ofrecen ninguna información sobre la calcificación de la VA. Tampoco hay datos ecocardiográficos a 30 días. Recientemente, Scotti et al. facilitaron datos de los registros retrospectivos y multicéntricos NEOPRO y NEOPRO-2 (n = 2.026) sobre el rendimiento y resultados de ambas tecnologías ACURATE15. Los autores confirmaron que la incidencia de FPP moderada o grave prealta era menor en el grupo neo2 (2 frente al 5%). Esta menor FPP, además, se observó, sobre todo, en pacientes con fuerte calcificación de la VA. No obstante, este estudio presenta algunas limitaciones inherentes a su propia naturaleza pues solo se comunicaron datos ecocardiográficoas prealta (y no a los 30 días). Además, la calcificación de la VA se valoró con un sistema de puntuación basado, sólo, en estimación visual. En este sentido, nuestro estudio incorpora información valiosa adicional sobre el papel de la calcificación de la VA y el riesgo de FPP con tecnología ACURATE. En nuestro estudio, observamos que, comparada con ACURATE neo, la neo2 comportó un menor riesgo de cualquier grado de FPP, así como a un menor riesgo de FPP ≥ moderada. También se observó la existencia de una tendencia lineal significativa entre los cuartiles del volumen de calcio en la VA y el riesgo de cualquier grado de FPP. Además, el análisis de emparejamiento por puntuación de la propensión nos permitió confirmar que el menor riesgo de FPP observado en la ACURATE neo2 fue independiente de la estimación del calcio en la VA.
No obstante, también tenemos algún otro hallazgo que merece la pena valorar. Se halló una tendencia hacia una mayor incidencia de hemorragias con la válvula neo que con la neo2, tanto intrahospitalaria como a los 30 días. Esto, en principio, se explicaría por las diferencias basales en los tratamientos antitrombóticos de los 2 grupos. Los pacientes de la cohorte neo recibieron, habitualmente, inhibidores del receptor plaquetario P2Y12 y tratamiento antiagregante plaquetario doble. No obstante, la evidencia actual adoptada en la mayoría de nuestros casos neo2 ha demostrado un mayor riesgo hemorrágico asociado al tratamiento antiagregante plaquetario doble frente al uso de monoantiagregación con ácido acetilsalicílico en pacientes derivados para TAVI16-18. Nuestros datos también parecen avalar estos hallazgos. Alternativamente, la enfermedad de Von Willebrand, que se asocia a la estenosis aórtica, puede persistir tras el TAVI en pacientes con FPP residual significativa19. La mayor incidencia de FPP asociada a la válvula neo frente a la neo2 explicaría, por sí mismo, nuestro hallazgo de una tendencia hacia un mayor riesgo hemorrágico en la cohorte neo.
Somos conscientes de que la curva de aprendizaje de los dispositivos ACURATE pudo haber alterado nuestros resultados. Se halló un mayor volumen de calcio estimado en la VA de los casos neo frente a los neo2. Nuestra experiencia inicial con la válvula neo quizás haga que los cardiólogos intervencionistas que trabajan en equipos multidisciplinares se animen a optar por otras VCP, distintas a ACURATE, con un menor riesgo estimado de FPP, en pacientes con un alto grado de calcificación en la VA. Además, aunque el porcentaje de predilatación fue elevado en los 2 grupos (92 y 99%, respectivamente), este porcentaje fue superior en el grupo neo2, a pesar de que este grupo mostró una menor cantidad de calcio estimado en la VA, lo cual confirma lo importante que es la curva de aprendizaje a la hora de implantar el dispositivo. Se debe mencionar que este paso del procedimiento podría ser especialmente importante para evitar la FPP residual, sobre todo en una VCP como la ACURATE que tiene una menor fuerza radial. En cualquier caso, los beneficios de la neo2 a la hora de reducir cualquier grado de FPP incluso después de ajustar por la calcificación de la VA parecen exceder lo que podría justificarse por estos 2 posibles sesgos. Los diferentes porcentajes de posdilatación descritos entre neo y neo2, se explicarían por el hecho de que los operadores identificaron, con mayor frecuencia, e intentaron corregir FPP angiográficamente significativas inmediatamente después de implantar la VCP en el grupo neo frente al neo2.
Limitaciones
Entre las limitaciones del estudio se encuentran aquellas relacionadas con su diseño observacional y no aleatorizado. Este estudio se ve limitado por su pequeño tamaño muestral y por ser la experiencia de un único centro. Se siguió una estricta metodología para calcular el volumen de calcio mediante TCC, la información ecocardiográfica y clínica se registró prospectivamente. No obstante, el grado de FPP observado durante el seguimiento a 30 días y los resultados adversos no se asignaron independientemente sino en base a los informes clínicos. Los estándares actuales para calcular el volumen de calcio en la VA se basan en el análisis de secuencias de TCC no potenciadas por contraste. No obstante, se aplicó un método para calcular el volumen de calcio basado en TCC potenciadas con contraste, el único método que nos permitió analizar nuestros casos más antiguos puesto que, por aquel entonces, las series no potenciadas por contraste no formaban parte de nuestro protocolo TCC pre-TAVI. Por último, nuestro estudio se ve limitado por el corto periodo de seguimiento. Se necesitan seguimientos más largos que nos ayuden a valorar tanto los resultados clínicos como la implicación pronóstica de la FPP residual.
Impacto sobre la práctica clínica diaria
Con los datos disponibles de nuestro registro del mundo real, comparado con su anterior versión, el TAVI con la válvula ACURATE neo2 se asoció a menor riesgo de FPP residual. Estos resultados no se vieron afectados por diferencias en la cantidad total de calcio en la VA detectada mediante TCC.
CONCLUSIONES
Comparada con la VCP ACURATE neo, el TAVI con la neo2 se asoció a un menor riesgo de cualquier grado de FPP, así como a un menor riesgo de FPP ≥ moderada. Tras ajustar por el volumen de calcio de la VA, la ACURATE neo2 siguió asociándose a un menor riesgo de FPP frente a ACURATE neo.
FINANCIACIÓN
Este estudio está financiado, en parte, por una Beca de Educación y Formación de la European Association of Percutaneous Cardiovascular Interventions (EAPCI) concedida por la European Society of Cardiology (ESC) al autor principal del artículo (M. García-Guimarães).
CONTRIBUCIÓN DE LOS AUTORES
M. García-Guimarães, M.J. Swaans y L. Timmers participaron tanto en la idea como en el diseño del estudio. M. García-Guimaraes recopiló los datos, realizó el análisis y redactó el artículo. D.-J. Van Ginkel contribuyó a la recopilación de datos. B.J. Rensing, J.M. Ten Berg, U. Sonker, T.L. de Kroon y R.H. Heijmen realizaron una revisión crítica de todo su contenido intelectual. Todos los autores dieron su autorización final a esta versión a efectos de publicación.
CONFLICTO DE INTERESES
L. Timmers es proctor y miembro del comité científico de Boston Scientific. M.J. Swaans declaró haber recibido honorarios como conferenciante de Boston Scientific. Los demás autores no declararon ningún conflicto de intereses.
¿QUÉ SE SABE DEL TEMA?
- La presencia de FPP significativa tras TAVI se asoció a peores resultados clínicos. La calcificación de la válvula aórtica es el predictor más sólido de FPP tras el implante de TAVI. ACURATE neo es una válvula cardiaca percutánea autoexpandible para el tratamiento de la estenosis aórtica degenerativa. Su última versión, la ACURATE neo2, pretende reducir la incidencia de FPP residual.
¿QUÉ APORTA DE NUEVO?
- En nuestro estudio con datos de un registro TAVI de mundo real, comparada con la anterior versión ACURATE neo, la neo2 se asoció a un menor riesgo de FPP residual. Además, estos resultados no se vieron afectados por las diferencias observadas en la cantidad total de calcio detectado en la válvula aórtica calculado mediante tomografía computarizada cardiaca.
MATERIAL ADICIONAL
Vídeo 1. García-Guimarães M. DOI: 10.24875/RECIC.M23000369
Vídeo 2. García-Guimarães M. DOI: 10.24875/RECIC.M23000369
Vídeo 3. García-Guimarães M. DOI: 10.24875/RECIC.M23000369
Vídeo 4. García-Guimarães M. DOI: 10.24875/RECIC.M23000369
Vídeo 5. García-Guimarães M. DOI: 10.24875/RECIC.M23000369
Vídeo 6. García-Guimarães M. DOI: 10.24875/RECIC.M23000369
Vídeo 7. García-Guimarães M. DOI: 10.24875/RECIC.M23000369
Vídeo 8. García-Guimarães M. DOI: 10.24875/RECIC.M23000369
BIBLIOGRAFÍA
1. Vahanian A, Beyersdorf F, Praz F, et al. 2021 ESC/EACTS Guidelines for the management of valvular heart disease. Eur Heart J. 2022;43:561–632.
2. Writing Committee Members, Otto CM, Nishimura RA, et al. 2020 ACC/AHA Guideline for the Management of Patients With Valvular Heart Disease: Executive Summary: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. J Am Coll Cardiol. 2021;77:450-500.
3. Koshy AN, Murphy A, Farouque O, Horrigan M, Yudi MB. Outcomes of Transcatheter Versus Surgical Aortic Valve Replacement in Low-Risk Patients. Hear Lung Circ. 2020;29:1527-1533.
4. Sinning JM, Vasa-Nicotera M, Chin D, et al. Evaluation and management of paravalvular aortic regurgitation after transcatheter aortic valve replacement. J Am Coll Cardiol. 2013;62:11-20.
5. Arnold S V., Zhang Y, Baron SJ, et al. Impact of Short-Term Complications on Mortality and Quality of Life After Transcatheter Aortic Valve Replacement. JACC Cardiovasc Interv. 2019;12:362-369.
6. Wiktorowicz A, Wit A, Malinowski KP, et al. Paravalvular leak prediction after transcatheter aortic valve replacement with self-expandable prosthesis based on quantitative aortic calcification analysis. Quant Imaging Med Surg. 2021;11:652-664.
7. Ludwig S, Goßling A, Waldschmidt L, et al. TAVR for low-flow, low-gradient aortic stenosis: Prognostic impact of aortic valve calcification. Am Heart J. 2020;225:138-148.
8. Okuno T, Asami M, Heg D, et al. Impact of Left Ventricular Outflow Tract Calcification on Procedural Outcomes After Transcatheter Aortic Valve Replacement. JACC Cardiovasc Interv. 2020;13:1789-1799.
9. Tamburino C, Bleiziffer S, Thiele H, et al. Comparison of Self-Expanding Bioprostheses for Transcatheter Aortic Valve Replacement in Patients with Symptomatic Severe Aortic Stenosis: SCOPE 2 Randomized Clinical Trial. Circulation. 2020;142:2431-2442.
10. Généreux P, Piazza N, Alu MC, et al. Valve Academic Research Consortium 3: Updated Endpoint Definitions for Aortic Valve Clinical Research. J Am Coll Cardiol. 2021;77:2717-2746.
11. Angelillis M, Costa G, De Backer O, et al. Threshold for calcium volume evaluation in patients with aortic valve stenosis: correlation with Agatston score. J Cardiovasc Med (Hagerstown). 2021;22:496-502.
12. Kim WK, Möllmann H, Liebetrau C, et al. The ACURATE neo Transcatheter Heart Valve: A Comprehensive Analysis of Predictors of Procedural Outcome. JACC Cardiovasc Interv. 2018;11:1721-1729.
13. Lanz J, Kim WK, Walther T, et al. Safety and efficacy of a self-expanding versus a balloon-expandable bioprosthesis for transcatheter aortic valve replacement in patients with symptomatic severe aortic stenosis: a randomised non-inferiority trial. Lancet. 2019;394:1619-1628.
14. Rück A, Kim WK, Kawashima H, et al. Paravalvular aortic regurgitation severity assessed by quantitative aortography: Acurate neo2 versus acurate neo transcatheter aortic valve implantation. J Clin Med. 2021;10:4627.
15. Scotti A, Pagnesi M, Kim W-K, et al. Haemodynamic performance and clinical outcomes of transcatheter aortic valve replacement with the self-expanding ACURATE neo2. EuroIntervention. 2022;18:804-811.
16. Brouwer J, Nijenhuis VJ, Delewi R, et al. Aspirin with or without Clopidogrel after Transcatheter Aortic-Valve Implantation. N Engl J Med. 2020;383):1447-1457.
17. Capodanno D, Collet JP, Dangas G, et al. Antithrombotic Therapy After Transcatheter Aortic Valve Replacement. JACC Cardiovasc Interv. 2021;14:1688-1703.
18. Nijenhuis VJ, Brouwer J, Delewi R, et al. Anticoagulation with or without Clopidogrel after Transcatheter Aortic-Valve Implantation. N Engl J Med. 2020;382:1696-1707.
19. Kibler M, Marchandot B, Messas N, et al. CT-ADP Point-of-Care Assay Predicts 30-Day Paravalvular Aortic Regurgitation and Bleeding Events following Transcatheter Aortic Valve Replacement. Thromb Haemost. 2018;118:893-905.