Sr. Editor:
A pesar de las mejoras recientes que ha experimentado el abordaje y tratamiento de la hipertensión pulmonar (HP) pediátrica y el descenso de los índices de mortalidad global gracias a las terapias dirigidas a vías específicas, en la actualidad no existe una cura para la mayoría de los pacientes; la morbimortalidad sigue siendo alta y el trasplante de pulmón es la terapia de destino para muchos1,2.
Según las guías de práctica clínica, la creación de un defecto restrictivo pretricuspídeo mediante atrioseptostomía (AS) carece de evidencias sólidas. Podría, no obstante, ser una opción en pacientes con clase funcional (CF) III-IV de la OMS/Ross con síncope o fracaso ventricular derecho grave que no responden al tratamiento farmacológico máximo o como terapia puente hacia el trasplante de pulmón1,2. Se tiene, relativamente, poca experiencia en pacientes pediátricos. No obstante, la combinación AS-fármacos ha ido mejorando resultados a corto plazo tales como la CF, el síncope o la supervivencia3,4. En manos de equipos experimentados, el índice de complicaciones baja. En cualquier caso, sigue siendo todo un desafío en el contexto de pacientes de alto riesgo. Los principales eventos mortales se asocian a crisis graves de HP o a cianosis grave debido a un tamaño impredecible del shunt.
Se han descrito diferentes abordajes para crear AS restrictivas. Debido a que con la septostomía con balón (o cuchillas) se consiguen cierres espontáneos tempranos, implantar un dispositivo en el septo auricular sería una forma sencilla de evitarlo. Aunque se ha descrito el uso de un dispositivo oclusor, este se asocia a una alta incidencia de oclusiones a largo plazo y un diámetro del shunt menos predecible. En nuestro centro, solemos realizar AS implantando un stent con forma de diábolo en el septo que nos permite predecir el diámetro del shunt. No obstante, el riesgo de embolización e hiperplasia neointimal intrastent es mayor4. La alternativa es el regulador de flujo auricular (AFR, Occlutech, Turquía), un dispositivo autoexpandible de malla trenzada con alambres de nitinol compuesto por 2 discos simétricos conectados por una cintura central fenestrada. Se fabrica en diámetros de fenestración de 8 y 10 mm (4 y 6 mm para uso compasivo) con diámetros de disco de 21 y 23 mm, respectivamente. Existen 2 modelos (M y L) que se adaptan a la altura de la cintura central (5 y 10 mm) según el grosor del septo auricular. Su disco proximal alberga un conector de bola soldado para fijarlo al sistema de liberación. El AFR se ha usado, ya, en diferentes escenarios (HP en adultos y niños mayores). Aunque los datos sobre los más pequeños son más limitados, son prometedores5,6. Se necesitan más datos que avalen esta evidencia.
Se presenta nuestra primera experiencia con 2 gemelos de 4 años (de 13 y 12,5 kg) con HP diagnosticada secundariamente a síncope recurrente. Ambos presentaban HP grave con presión arterial pulmonar sistólica estimada suprasistémica, hipertrofia y dilatación grave del ventrículo derecho pero con función conservada y sin anomalías estructurales. A ambos se les administró tratamiento farmacológico (sildenafilo, bosentán y treprostinilo). El paciente nº 1 fue el que peor evolución tuvo, con síncope persistente, por lo que hubo que aumentar la medicación. El paciente nº 2, presentaba una CF deteriorada. La intervención (tabla 1) se realizó con farmacoterapia dirigida a la HP, ventilación mecánica a altas dosis de oxígeno y guiada mediante fluoroscopia y ecocardiografía transesofágica con los equipos de oxigenación extracorpórea de membrana, o ECMO, y cirugía cardiaca a la espera. Los datos invasivos confirmaron el diagnóstico. Se realizó una punción en la fosa oval del paciente nº 1 con una aguja de Brockenbrough (vídeo 1 del material adicional). En el paciente nº 2, se accedió a la aurícula izquierda a través de un foramen oval permeable. En ambos casos, se usó el modelo M del AFR con un tamaño de fenestración de 8 mm, el dispositivo más pequeño aprobado por la CE. La comunicación interauricular se dilató (vídeo 2 del material adicional) con balones más pequeños que los recomendados por el fabricante (Advance balloon, Cook Medical, Estados Unidos, 8 mm x 2 cm en el paciente nº 1 y 7 mm x 2 cm en el nº 2) para que la fenestración central del AFR estuviese ligeramente limitada por el septo interauricular, permitiendo así un shunt < 8 mm. El resto de la intervención se desarrolló igual que el cie-rre de una comunicación interauricular con un dispositivo estándar (figura 1, vídeo 3 del material adicional). Según la ecocardiografía transesofágica, los tamaños finales del shunt fueron 6,5 y 6,3 mm en los pacientes nº 1 y 2, respectivamente. No hubo complicaciones. Los 2 pacientes permanecieron < 24 horas en la unidad de cuidados intensivos donde recibieron atención posoperatoria sin incidencias. Se les dio de alta en tratamiento con ácido acetilsalicílico y terapia dirigida a la HP (sildenafilo, bosentán y treprostinilo). Las intervenciones fueron relativamente directas, más sencillas y cortas que nuestra serie de stents con forma de diábolo4.
Table 1. Características de la intervención
| Paciente nº 1 | Paciente nº 2 | |
|---|---|---|
| Sexo | Varón | Varón |
| Edad (años) | 4 | 4 |
| Peso (kg) | 13 | 12,5 |
| AD (mmHg) | 4 | 6 |
| AI (mmHg) | 6 | 8 |
| AP (mmHg) | 63/42/51 | 69/24/46 |
| Ao (mmHg) | 72/40/56 | 80/39/56 |
| Saturación O2 previa (%) | 98 | 98 |
| Saturación O2posoperatoria (%) | 94 | 96 |
| Diámetro de fenestración en la ETE (mm) | 6,5 | 6,3 |
| Dispositivo AFR (mm) | ||
| Diámetro de fenestración | 8 | 8 |
| Altura de la cintura | 5 | 5 |
| Diámetros de los discos | 21 | 21 |
| Abordaje venoso | femoral | femoral |
| Tamaño máximo del abordaje venoso (Fr) | 12 | 12 |
| Abordaje TS | Aguja de Brockenbrough | FOP |
| Dilatación con balón del SA | Advance 35 PB 8 mm × 2 cm | Advance 35 PB 7 mm × 2 cm |
| Tiempo de la intervención (min) | 116 | 74 |
| Tiempo de fluoroscopia (min) | 25 | 12 |
| Dosis de radiación (Gy/cm2) | 14,8 | 5,9 |
|
AD: presión auricular derecha media; AFR: regulador de flujo auricular; AI: presión auricular izquierda media; Ao: presión aórtica sistólica/diastólica/media; AP: presión arterial pulmonar sistólica/diastólica/media; ETE: ecocardiografía transesofágica; FOP: foramen oval permeable; PB: perfil bajo; SA: septo auricular; TS: transeptal. |
||
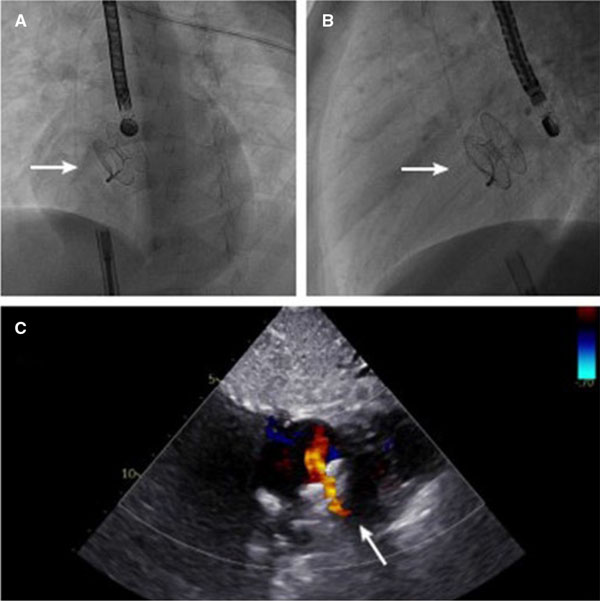
Figura 1. A y B: imágenes fluoroscópicas en proyecciones oblicua anterior izquierda (A) y lateral (B) del dispositivo regulador de flujo auricular (AFR) colocado en su ubicación final en el septo interauricular (flecha blanca). C: imagen ecocardiográfica Doppler-color transtorácica en plano subcostal del AFR (flecha blanca).
En su última visita de seguimiento (trascurridos 9 y 8 meses), los pacientes han tenido buena evolución: el dispositivo era permeable, con un shunt bidireccional pero predominantemente de izquierda a derecha (vídeos 4-6 del material adicional) sin una desaturación basal significativa (> 94%) ni síncope y con una CF normal. Los niveles del fragmento N-terminal del pro-péptido natriurético tipo B (pg/ml) fueron algo menores en los 2 pacientes (de 163 a 159 pg/ml en el paciente nº 1 y de 376 a 157 pg/ml en el nº 2). En la actualidad, no están en lista para trasplante de pulmón y siguen con el tratamiento triple ajustado conforme al aumento de peso.
Nuestros datos coinciden con los descritos5,6, lo cual convierte al AFR en una alternativa también válida en niños pequeños con HP grave de alto riesgo. Su principal ventaja es que permite crear shunts de un tamaño predecible, es técnicamente más fácil de usar y tiene un riesgo bajo de migración del dispositivo.
Los padres de los gemelos dieron su consentimiento informado explícito y por escrito tanto para la publicación de los datos y las imágenes como para la realización de la intervención.
FINANCIACIÓN
Ninguna.
CONTRIBUCIÓN DE LOS AUTORES
L. Bianco participó en la recogida de datos clínicos y en la preparación del proceso de redacción del artículo con información de todos los autores. P. Betrián Blasco realizó la intervención y supervisó la versión definitiva del artículo. A. Torrent Vernetta y A. Sabaté Rotés participaron en todo el proceso de tratamiento de los pacientes y revisaron el artículo cuya versión final fue aprobada por todos los autores.
CONFLICTO DE INTERESES
Ninguno.
MATERIAL ADICIONAL
Vídeo 1. Bianco L. DOI: 10.24875/RECIC.M23000391
Vídeo 2. Bianco L. DOI: 10.24875/RECIC.M23000391
Vídeo 3A. Bianco L. DOI: 10.24875/RECIC.M23000391
Vídeo 3B. Bianco L. DOI: 10.24875/RECIC.M23000391
Vídeo 4. Bianco L. DOI: 10.24875/RECIC.M23000391
Vídeo 5. Bianco L. DOI: 10.24875/RECIC.M23000391
Vídeo 6. Bianco L. DOI: 10.24875/RECIC.M23000391
BIBLIOGRAFÍA
1. Hansmann G, Koestenberger M, Alastalo TP, et al. 2019 updated consensus statement on the diagnosis and treatment of pediatric pulmonary hypertension: The European Pediatric Pulmonary Vascular Disease Network (EPPVDN), endorsed by AEPC, ESPR and ISHLT. J Heart Lung Transplant. 2019;38:879-901.
2. Rosenzweig EB, Abman SH, Adatia I, et al. Paediatric pulmonary arterial hypertension: updates on definition, classification, diagnostics and management. Eur Respir J. 2019;53:1801916.
3. Grady RM. Beyond transplant: Roles of atrial septostomy and Potts shunt in pediatric pulmonary hypertension. Pediatr Pulmonol. 2021;56:656–660.
4. Degano Iglesias LA, Sabaté Rotés A, Betrian Blasco P, Torrent Vernetta A, Moreno-Galdó A, Albert Brotons DC. Septostomía auricular en niños con hipertensión pulmonar. Rev Esp Cardiol. 2019;72:688-691.
5. Sivakumar K, Rohitraj GR, Rajendran M, Thivianathan N. Study of the effect of Occlutech Atrial Flow Regulator on symptoms, hemodynamics, and echocardiographic parameters in advanced pulmonary arterial hypertension. Pulm Circ. 2021;11:1-10.
6. Vanhie E, VandeKerckhove K, Haas NA, De Wolf D. Atrial flow regulator for drug-resistant pulmonary hypertension in a young child. Catheter Cardiovasc Interv. 2021;97:E830-E834.