RESUMEN
La coartación de aorta es una enfermedad congénita caracterizada por el estrechamiento de la aorta torácica, que provoca una obstrucción del flujo sanguíneo distal. Una coartación de aorta significativa se asocia con hipertensión arterial e hipoperfusión distal, así como con un mal pronóstico sin intervención. Inicialmente el tratamiento era quirúrgico, pero fueron surgiendo técnicas menos invasivas, como la angioplastia percutánea con balón, que mostró eficacia en ciertos pacientes. La incorporación del implante de stents mejoró de manera significativa los resultados, convirtiendo la reparación percutánea en la opción preferida, en especial en adolescentes y adultos. Sin embargo, siguen produciéndose complicaciones inmediatas y a largo plazo. Esto ha impulsado esfuerzos destinados a mejorar su seguridad y eficacia. Las estrategias modernas se enfocan en stents de diseño avanzado, con mejor perfil de entrega y un alto potencial de redilatación. Persisten vacíos por llenar, y nuevos datos provenientes de estudios con seguimientos más prolongados permitirán comprender mejor la evolución de estos pacientes. Esta revisión tiene como objetivo ofrecer una visión integral de estas intervenciones percutáneas, abordando los avances, los resultados y las perspectivas futuras.
Palabras clave: Coartación de aorta. Reparación percutánea. Complicaciones. Stents de diseño avanzado.
ABSTRACT
Aortic coarctation is a congenital disease that consists of the narrowing of the thoracic aorta, leading to distal blood flow obstruction. Significant aortic coarctation is associated with hypertension and distal hypoperfusion, with a poor prognosis without intervention. Initially, treatment was surgical; however, less invasive techniques such as percutaneous balloon angioplasty later emerged and proved effective in selected patients.
The introduction of stent implantation significantly improved the outcomes, making percutaneous repair the preferred option, especially in adolescents and adults.
However, immediate and long-term complications persist, which has driven research efforts aimed at improving the safety and efficacy profile. Modern strategies now focus on advanced stent designs, offering better delivery profiles and high redilatation potential. Gaps in knowledge remain, and data from studies with longer follow-up will be essential to further elucidate disease progression in these patients. This review aims to offer a comprehensive overview of these percutaneous procedures, discussing recent advancements, clinical outcomes, and future perspectives.
Keywords: Aortic coarctation. Percutaneous repair. Complications. Advanced stent designs.
INTRODUCCIÓN
La coartación de aorta (CoAo) es una cardiopatía congénita (CC) que se define como un estrechamiento de la aorta torácica1,2. Se trata de un defecto que suele localizarse en sentido distal a la arteria subclavia izquierda próximo al punto de inserción del remanente del conducto arterioso. La gravedad es variable y la CoAo puede presentarse en forma de estenosis discreta o segmento estenótico largo y tortuoso1,2. La CoAo es una de las CC más frecuentes y supone entre el 5 y 8% de este grupo de defectos3, con una incidencia de 3 a 4 casos por cada 10.000 nacidos vivos. Es más prevalente entre los varones, con una tasa de incidencia de 2:14. Esta enfermedad suele acompañarse de otros defectos cardiovasculares congénitos, con una incidencia de entre el 70 y el 87%1,5,6. El más común es la válvula aórtica bicúspide (VAB), descrita en hasta el 60% de los casos1,2.
La presentación clínica depende tanto de la gravedad de la obstrucción como de la presencia de otras CC asociadas. Los casos graves debutan durante la edad neonatal, a menudo con shock cardiogénico. En cambio, las obstrucciones menos graves pueden detectarse durante la infancia o la edad adulta con hipertensión en la parte superior del cuerpo, hipertrofia ventricular, dilatación de la aorta torácica y avance progresivo de circulación colateral7,8. Los signos y síntomas se muestran en la tabla 19.
Tabla 1. Signos y síntomas de la coartación aórtica en adultos con CoAo no reparada9
| Signos | Síntomas |
|---|---|
| Hipertensión en extremidades superiores | Intolerancia al esfuerzo/disnea |
| Pulsos femorales débiles o ausentes | Cefalea |
| Retraso braquio-femoral | Epistaxis |
| Gradiente de presión arterial entre extremidades superiores e inferiores | Mareo |
| Soplo sistólico o continuo interescapular | Claudicación de extremidades inferiores |
| Soplo de insuficiencia aórtica (en casos de raíz aórtica dilatada con o sin válvula bicúspide) | Angina abdominal |
| Impulso apical desplazado (en casos de ventrículo izquierdo dilatado) | Acúfenos |
| Pies fríos |
La historia natural de la CoAo no reparada tiene un pronóstico muy desfavorable. Campbell et al. describieron las principales causas de muerte por CoAo no tratada: insuficiencia cardiaca congestiva (25%), rotura aórtica (21%), endocarditis bacteriana (18%) y hemorragia intracraneal (11%)10. En este sentido, la reparación de la CoAo en pacientes con estenosis significativa es obligatoria para mejorar el pronóstico y la calidad de vida de los pacientes. En la actualidad, las guías de práctica clínica recomiendan intervenir cuando la CoAo se acompaña de hipertensión y un gradiente invasivo pico a pico > 20 mmHg11. La cirugía fue la primera técnica reparadora seguida del tratamiento percutáneo, que se estableció como opción terapéutica viable para pacientes seleccionados. El objetivo de esta revisión es resumir la evidencia disponible sobre las intervenciones percutáneas, analizar los avances hechos hasta la fecha, los resultados y las perspectivas futuras.
PERSPECTIVA HISTÓRICA
Crafoord realizó la primera cirugía de CoAo en 1944 consistente en una intervención de resección y anastomosis término-terminal12. Desde entonces, han aparecido otras técnicas quirúrgicas para prevenir la recoartación y formación de aneurismas, como la aortoplastia con parche, la aortoplastia con colgajo subclavio y la coartectomía con interposición de injerto2.
Aunque la cirugía ha sido el patrón oro durante años, la aparición de tratamientos percutáneos ha abierto un nuevo abanico de posibilidades. El primer tratamiento percutáneo de la CoAo fue publicado en 1982 por Singer et al. que realizaron con éxito una angioplastia con balón (ICP-balón) para tratar una CoAo en un recién nacido13. A pesar de la eficacia de esta técnica, la tasa de recoartación y formación de aneurismas fue alta14,15.
El primer caso documentado de implante de stent en un paciente con CoAo se publicó en 199116 y, posteriormente, en 1995, Suárez de Lezo et al. comunicaron la primera serie de pacientes tratados con este mismo abordaje, lo cual confirmó el perfil de seguridad y eficacia de este abordaje17. La principal ventaja del implante de stent es el soporte estructural que proporciona que, a su vez, reduce, las complicaciones18. En 1999, Gunn et al. y después, otros autores, describieron el uso de stents recubiertos con buenos resultados19-21.
En la actualidad, las guías europeas de práctica clínica recomiendan el implante de stent como primera opción en pacientes adultos con anatomías favorables11. No obstante, como la reparación quirúrgica sigue desempeñando un papel clave en determinados casos, el abordaje óptimo debe elegirse con suma cautela.
ANGIOPLASTIA CON BALÓN
Originariamente, la ICP-balón empezó empleándose en neonatos y lactantes con CoAo e insuficiencia cardiaca como estrategia de rescate o tratamiento definitivo en casos de alto riesgo quirúrgico13. No obstante, tiempo después, esta técnica empezó a probarse en niños mayores y adultos. La principal ventaja de la ICP-balón es su sencillez, con buenos resultados en coartaciones discretas. No obstante, la dilatación con balón dentro de la aorta puede provocar la rotura de la íntima, afectación de la capa media y posibles complicaciones posteriores22.
Entre sus desventajas están una menor eficacia en anatomías complejas, como la hipoplasia ístmica y la estenosis difusa23,24. Las complicaciones más frecuentes son la disección aórtica y el retroceso elástico a corto plazo y la recoartación y formación de aneurismas a largo plazo23,25,26. Un registro retrospectivo de niños tratados con ICP-balón informó de roturas/disecciones aórticas, recoartaciones y formación de aneurismas en el 2, 26 y 34% de los casos, respectivamente27. Un ensayo clínico aleatorizado que comparó la ICP-balón y el tratamiento quirúrgico en niños también informó de la formación de aneurismas y reestenosis en el 20 y 25% de los pacientes tratados con ICP-balón28. Por otro lado, en pacientes de mayor edad con coartación discreta, Walhout y Fawzy observaron una incidencia baja de recoartación (≈ 3%)29,30. La incidencia de aneurismas en adultos también parece ser menor que en niños (1,8-6%)31,32.
La ICP-balón tiene un buen perfil de eficacia en el 67-90% de los casos de coartaciones recurrentes (posoperatorias o pos-ICP-balón), especialmente en niños. Por eso, en la actualidad, la CoAo recurrente es una de las principales indicaciones para la ICP-balón25,33-35. También se emplea en el tratamiento de la coartación nativa en niños para retrasar el implante de stent hasta la edad adulta, cuando se puedan implantar stents de tamaño definitivo. A pesar de estas indicaciones principales, en casos seleccionados con obstrucción discreta y no crítica, la ICP-balón puede ser una intervención eficaz y evitar el implante de stent, tal y como ya se ha mencionado36.
IMPLANTE PERCUTÁNEO DE STENT
La introducción del implante de stent en el tratamiento de la CoAo tuvo como objetivo mejorar los resultados a corto y largo plazo tras la ICP-balón y minimizar las complicaciones asociadas a la elasticidad aórtica, el retroceso y la rotura de la pared35. La fuerza radial del stent se opone al retroceso aórtico y mejora la integridad del vaso tras el traumatismo inherente a la dilatación con balón35.
Zabal et al. observaron que el gradiente residual fue mucho menor en pacientes tratados con implante de stent que con ICP-balón. Una diferencia que fue más evidente en pacientes con coartación no discreta (coartación tubular o hipoplasia ístmica), en quienes se observó un gradiente residual > 20 mmHg en el 57% de los casos tras ICP-balón frente al 0% en el grupo que recibió un stent36. El implante de stent también reduce la incidencia de recoartación y formación de aneurismas37-39.
El implante de stent también ha demostrado ser seguro en el tratamiento de la recoartación, especialmente en pacientes ya intervenidos mediante reparación quirúrgica. Aunque se han descrito diversas complicaciones, el seguimiento a largo plazo ha mostrado una eficacia ciertamente prometedora40,41.
En la actualidad, se opta por el implante de stent en detrimento de la ICP-balón tanto en adultos como en adolescentes. Las guías europeas de práctica clínica también recomiendan el implante de stent a la reparación quirúrgica en casos con anatomías favorables42.
A pesar de sus ventajas, el implante de stent en niños menores de 8-10 años sigue estando limitado por el riesgo de complicaciones vasculares en el sitio de acceso (por el mayor tamaño de las vainas introductoras necesarias), por la limitación adicional de no poder implantar un stent de tamaño adulto en una aorta aún en crecimiento y por lo difícil que es implantar stents que se puedan posdilatar adecuadamente y adaptar al crecimiento aórtico futuro25,43.
Stents recubiertos frente a no recubiertos
En primer lugar, se debe mencionar que los stents expandibles con balón se prefieren a los autoexpandibles por la mayor fuerza radial de los primeros, lo cual mejora la dilatación de la CoAo y previene el retroceso aórtico. Entre los stents expandibles con balón, los recubiertos se prefieren a los metálicos no recubiertos en casi todos los escenarios clínicos. Los stents recubiertos crean un efecto de sellado en el lugar del implante y proporcionan una característica de seguridad adicional44.
En la actualidad, los stents recubiertos son el tratamiento percutáneo de primera línea de la CoAo nativa, la fractura del stent, la recoartación y la formación de aneurismas11. En el contexto de la CoAo nativa, se prefieren los stents recubiertos especialmente en anatomías complejas, pacientes de mayor edad y aquellos con enfermedades del tejido conectivo o síndrome de Turner (ST) para prevenir la rotura de la pared aórtica o la formación de aneurismas25,38. El «efecto de sellado» es toda una ventaja en pacientes pretratados que desarrollan aneurismas o rotura de la pared vascular45.
En niños, se opta por stents no recubiertos ante la posibilidad de redilatar el stent para adaptarlo al crecimiento aórtico. Los stents recubiertos solo pueden dilatarse hasta un diámetro específico sin dañar su material de recubrimiento, razón por la cual están indicados en pacientes adultos46.
ABORDAJES HÍBRIDOS
El abordaje híbrido que combina intervenciones quirúrgicas y tratamiento percutáneo es, en la actualidad, una opción en pacientes con CC. En el contexto de la CoAo, suele ser necesario un abordaje híbrido cuando el paciente presenta otro defecto cardiaco congénito que requiere reparación quirúrgica. Un escenario habitual es la coexistencia de dilatación de la aorta ascendente y VAB con insuficiencia o estenosis significativas47. El tratamiento de estos casos siempre es complejo ante la falta de guías y recomendaciones estandarizadas. El momento de efectuar las correcciones y la modalidad de intervención más adecuada siguen siendo objeto de debate.
Diversos autores han comunicado casos de pacientes con enfermedad de la VAB acompañada de dilatación de la aorta ascendente e insuficiencia aórtica tratados inicialmente con técnicas percutáneas para la CoAo y, después, mediante el procedimiento quirúrgico de Bentall47,48. La reparación de la CoAo previa al recambio valvular probablemente reduzca el riesgo de hipoperfusión de los órganos distales a la coartación. No obstante, y aunque la evidencia disponible todavía no es concluyente, la reparación quirúrgica de una valvulopatía en un primer acto quirúrgico ha resultado exitosa49.
Como nuevo abordaje, Russell et al. comunicaron su experiencia con un paciente con VAB, dilatación de la aorta ascendente y CoAo, tratado con un abordaje híbrido y en un único acto quirúrgico que incluyó la reparación endovascular de la raíz aórtica (CoAo) y el recambio quirúrgico de la válvula aórtica y aorta ascendente50.
IMÁGENES, SELECCIÓN DE PACIENTES Y CONSIDERACIONES PROPIAS DE LA INTERVENCIÓN
Imágenes
La evaluación mediante imágenes multimodales es obligatoria en pacientes con sospecha de CoAo para caracterizar adecuadamente la anatomía, descartar malformaciones asociadas y optar por la mejor opción terapéutica.
Ecocardiografía transtorácica
La ecocardiografía transtorácica suele ser la primera técnica de imágen que se realiza en pacientes con sospecha de CoAo. Con esta técnica, se puede ver la dilatación de la aorta ascendente y, en algunos casos, localizar la coartación en la proyección supraesternal a través de imágenes bidimensionales y Doppler color. Además, en la proyección supraesternal, el Doppler espectral permite visualizar el patrón típico en «dientes de sierra» con Doppler continuo, lo cual permite medir el gradiente en casos favorables51.
Angiotomografía computarizada
La angiografía computarizada (angio-TC) es la técnica de imágen de elección para el estudio de la aorta torácica en pacientes con alguna contraindicación para una resonancia magnética cardiaca (RMC) por ser portadores de marcapasos o desfibriladores. Además, es el patrón oro para diagnosticar la disección aórtica, una complicación conocida de la CoAo y la técnica de imágen preferida para valorar la permeabilidad luminal y descartar reestenosis o fracturas del stent en pacientes con CoAo reparada52.
Comparada con la RMC, la angio-TC proporciona una mayor resolución espacial de la aorta, precisa tiempos de adquisición más cortos y la toleran mejor los pacientes claustrofóbicos; no obstante, algunas de sus desventajas son que la radiación ionizante y el contraste IV que precisan pueden provocar afectación renal53.
Resonancia magnética cardiaca
En la actualidad, la RMC se considera la técnica de imágen de referencia para examinar pacientes adultos con sospecha de CoAo y otras CC. Esta técnica permite identificar, de forma precisa, la localización y relevancia de la coartación mediante análisis de flujo por contraste de fase. La RMC también permite medir la longitud del segmento coartado y las dimensiones aórticas para seleccionar el tamaño adecuado de stent, identifica el flujo colateral en las arterias intercostales, analiza la función cardiaca y la presencia de otras CC concomitantes. Todas estas ventajas sin necesidad de radiación ionizante54,55. La RMC también se emplea durante la vigilancia posoperatoria tras el implante de stent y la cirugía para detectar posibles complicaciones2.
Selección de pacientes e indicaciones
La reparación o recoartación de la CoAo nativa, por vía quirúrgica o percutánea, es obligatoria en pacientes hipertensos con un gradiente pico a pico confirmado > 20 mmHg (indicación clase I) y preferencia por el implante de stent siempre y cuando sea técnicamente viable según las últimas guías europeas y americanas11,56. Según las europeas, la reparación percutánea de la CoAo se debe tener en cuenta en pacientes hipertensos con estrechamientos del 50% sin gradiente pico a pico < 20 mmHg y normotensos sin gradientes significativos (indicación clase IIa)11.
La selección de la estrategia de reparación en pacientes con CoAo se debe basar en un análisis meticuloso que incorpore factores clave como la edad y el peso del paciente, las características anatómicas de la coartación y las intervenciones quirúrgicas realizadas. La reparación percutánea suele considerarse una alternativa menos arriesgada que la cirugía en pacientes bien seleccionados. La figura 1 ilustra una representación esquemática del proceso de toma de decisiones.
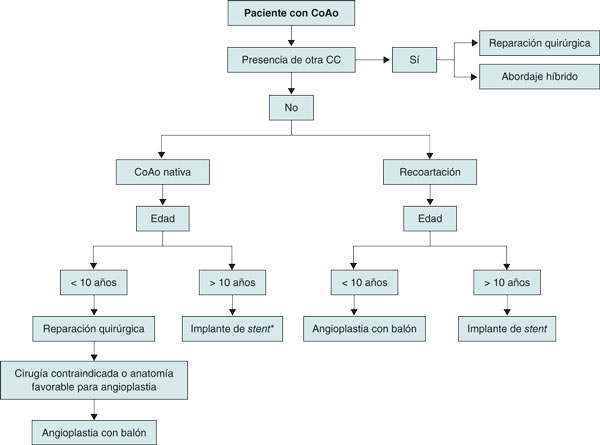
Figura 1. Algoritmo propuesto de tratamientos de primera línea según la edad de los pacientes con coartación aórtica, El abordaje sugerido en cada caso y grupo etario es general, por lo que la decisión sobre la estrategia seleccionada dependerá tanto de las características anatómicas como de la experiencia de los propios centros. CC: cardiopatía congénita; CoAo: coartación aórtica.
*Algunos autores sugieren un «umbral» de 25 kg, por debajo del cual el uso de stents estaría desaconsejado.
En lactantes y niños de 8-10 años con CoAo nativa, se prefiere la reparación quirúrgica a las técnicas percutáneas. Cuando se opta por la intervención endovascular, la ICP-balón debe ser el abordaje de elección25. Algunos autores también proponen un «umbral» de 25 kg por debajo del cual no se recomienda el implante de stent por el mayor tamaño de las vainas introductoras necesarias, lo cual supone un alto riesgo de complicaciones vasculares57.
En adolescentes y adultos, si la anatomía es favorable y en ausencia de una CC asociada que precise reparación quirúrgica, el implante de stent percutáneo se considera, en la actualidad, el tratamiento de primera línea25. Estas consideraciones dependerán de las características anatómicas de cada paciente. La experiencia de cada centro con estos casos también influye en la toma de decisiones clínicas.
Cuestiones en torno a la intervención
Una planificación adecuada resulta esencial para garantizar mejores resultados y minimizar el riesgo de complicaciones asociadas al implante de stent durante la coartación. Varios pasos pueden coincidir con los de la ICP-balón. A continuación, se describen los principales pasos y consideraciones técnicas. La figura 2 ilustra un caso de CoAo tratado con éxito mediante implante de stent.
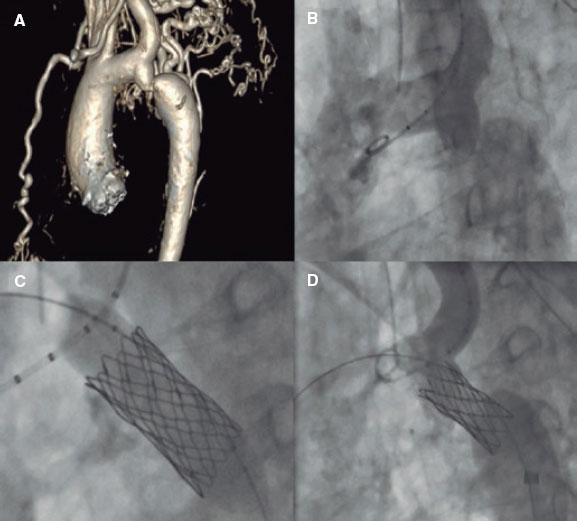
Figura 2. Tratamiento exitoso de una coartación aórtica en un adulto. A: tomografía computarizada con resultado de coartación aórtica. B: angiografía que confirma la presencia de coartación aórtica. C: angioplastia con balón e implante de stent. D: resultado fluoroscópico final tras implante de stent.
En primer lugar, antes de la intervención, resulta esencial controlar la hipertensión, ya que las crisis hipertensivas suelen ser habituales tras el implante del stent. Los bloqueadores beta ayudan a prevenir estas crisis. También se recomienda una vigilancia estricta durante el posoperatorio para detectar y tratar la hipertensión de forma eficaz y garantizar mejores resultados clínicos. Algunos autores recomiendan realizar cualquier tratamiento percutáneo bajo anestesia general. Como la dilatación de la CoAo suele ser dolorosa, este abordaje hace que la intervención sea más fácil de sobrellevar35. No obstante, en líneas generales, la sedación ligera o moderada suele bastar en pacientes adultos.
- – Vía de acceso: suele usarse la arteria femoral común (derecha o izquierda). Se debe emplear el precierre con Perclose ProGlide (Abbott Vascular, Estados Unidos). El tamaño de la vaina introductora debe ser parejo al diámetro del balón o del stent; se recomiendan vainas 2-3 Fr más grandes que el mínimo requerido para el balón. La heparina no fraccionada se administra para lograr tiempos de coagulación activados > 250 segundos. También se debe administrar una dosis profiláctica de cefazolina.
- – Cruce de la coartación: la CoAo se suele poder cruzar con una guía convencional de 0,035 pulgadas de politetrafluoroetileno y, a veces, con una guía hidrofílica. En anatomías especialmente complejas, puede hacerse necesario emplear el abordaje retrógrado desde la arteria radial con salida por la femoral. Se deben realizar nuevas mediciones del gradiente y angiografías para evaluar adecuadamente el defecto. La guía inicial se sustituirá por otra extra-rígida que se colocará en la aorta ascendente o en la subclavia izquierda (solo si la distancia desde el ostium subclavio al defecto supera los 10 mm).
- – Selección del tamaño del balón y de stent: el tamaño del stent (y del balón) debe ir parejo al diámetro del arco proximal, sin superar el diámetro de la aorta diafragmática.57 La longitud del stent debe ser lo bastante grande como para cubrir todo el segmento estenótico, teniendo en cuenta que una sobredilatación podría provocar un acortamiento de hasta el 30%. La tabla 2 muestra algunos de los stent disponibles en la actualidad para el tratamiento de la CoAo.
- – Dilatación e implante del stent: la predilatación está desaconsejada de forma sistemática, pues tanto el anclaje como el implante del stent suelen ser más eficaces cuando este se coloca directamente. No obstante, en casos de estenosis crítica, la predilatación resulta inevitable.
- Tras la dilatación, la relación entre el diámetro final del stent y la zona más estenótica de la CoAo debe ser < 3,557.
- – Eficacia: la intervención se considerará un éxito cuando el gradiente residual medido de forma invasiva no supere los 10 mmHg58.
Tabla 2. Stents empleados en la reparación de la CoAo
| Recubrimiento | Ensamblaje | Modelo de stent | Fabricante | Metal | Rango de expansión (mm) | Acortamiento | Tipo de celda* |
|---|---|---|---|---|---|---|---|
| No recubierto | Preensamblado | Formula | Cook Medical | Acero inoxidable | 8-20 | ~ 10-15% | Celda cerrada |
| No preensamblado | Andrastent XL y XXL | Andramed | Aleación cobalto-cromo | 12-32 | < 5% | Celda abierta | |
| CP stent | NuMED | Aleación platino-iridio | 12-30 | ≈ 15-20% | Celda cerrada | ||
| Optimus | AndraTec GmbH | Aleación cobalto-cromo | 10-28 | ~ 5% | Celda abierta | ||
| Recubierto | Preensamblado | Begraft aortic | Bentley Innomed GmbH | Aleación cobalto-cromo | 12-24 | < 5% | Celda cerrada |
| Atrium Advanta V12 | Maquet | Acero inoxidable | 12-16 | 0-15% | Celda cerrada | ||
| NuDEL | NuMED | Aleación platino-iridio | 12-24 | ~ 10% | Celda cerrada | ||
| No preensamblado | CP covered | NuMED | Aleación platino-iridio | 12-24 | ~ 15-20% | Celda cerrada | |
| Optimus covered | AndraTec GmbH | Aleación cobalto-cromo | 12-28 | < 5% | Celda abierta | ||
|
* Los stents de celda abierta tienen más espacios y menos struts de conexión, lo cual proporciona una mayor flexibilidad y mejor adaptación a vasos curvos. Aunque los de celda cerrada proporcionan más interconexiones, una mayor fuerza radial y una cobertura uniforme, ofrecen una menor flexibilidad y adaptabilidad a anatomías tortuosas. |
|||||||
RESULTADOS Y COMPLICACIONES
Resultados inmediatos y a corto plazo
El tratamiento percutáneo de la CoAo ha demostrado ser seguro y eficaz, con tasas de éxito que varían según el tipo de intervención y la población tratada. Las complicaciones inmediatas asociadas a la reparación percutánea incluyen la rotura de la pared aórtica, la mala aposición del stent y las complicaciones en el sitio de acceso vascular y su incidencia varía entre grupos y estudios. Steiner y Prsa observaron que la ICP-balón alcanzó tasas de éxito del 71 y 69% en el tratamiento de la CoAo nativa y recoartación, respectivamente. Por otro lado, el implante de stent tuvo una tasa de éxito del 100% en ambas situaciones59. Un metanálisis realizado por Nana et al. confirmó que la tasa de éxito técnico del implante de stent en adultos fue del 97%, con tasas de mortalidad intraoperatoria y a 30 días del 1%60. Otro metanálisis de Yang et al. informó una tasa global de éxito del 98% para el implante de stent en el tratamiento de la CoAo nativa61.
Resultados a largo plazo
El tratamiento percutáneo mediante stents, tanto metálicos como recubiertos, ha demostrado excelentes resultados a largo plazo. Schleiger et al. informaron una tasa de éxito de la intervención del 88,2% y tasas de supervivencia del 98,1, 95,6 y 95,6% a 5, 10 y 15 años, respectivamente. Las tasas de reintervención fueron del 27,8% y la mediana de seguimiento, 7,3 años, sin diferencias significativas entre stents metálicos y recubiertos62. Los estudios COAST y COAST II mostraron un buen perfil de eficacia en el seguimiento y una menor necesidad de antihipertensivos63.
Las complicaciones a largo plazo son la formación de aneurismas, la reestenosis y la fractura y migración del stent64. Se debe mencionar que los ensayos COAST y COAST II comunicaron una tasa acumulada de fracturas del stent del 24,4% en el seguimiento tardío. Las tasas de reintervención fueron del 21,3%, siendo factores predictivos una menor edad y diámetros más pequeños del stent63.
Pan et al. aportaron uno de los seguimientos más largos publicados (de 4 a 30 años). La incidencia acumulada de fractura del stent durante el seguimiento a largo plazo fue del 34% y la de formación de aneurismas, del 13%65.
En líneas generales, el implante de stent se asocia a altas tasas de éxito de la intervención, importantes beneficios de supervivencia a largo plazo y tasas más bajas hipertensión. No obstante, el seguimiento a largo plazo es esencial por el riesgo de fractura del stent, reintervenciones y complicaciones tardías como la formación de aneurismas42,56.
TRATAMIENTO DE LAS LIMITACIONES EN POBLACIONES ESPECÍFICAS
Síndrome de Turner y enfermedades del tejido conectivo
Las CC se dan en un tercio de los pacientes con ST, el 75% de los cuales son CoAo o VAB66,67. Aunque el tratamiento de primera línea de la CoAo en niños suele ser la reparación quirúrgica, los pacientes con ST tienen incidencias altas de disección aórtica (11%) y formación de aneurismas (30%) tras la cirugía68. Estos resultados se atribuyen a la debilidad intrínseca de la pared aórtica por la necrosis quística de la media propia del ST68. En este caso, en la actualidad, el tratamiento percutáneo con implante de stent recubierto es la opción preferida en pacientes con anatomías favorables. Los stents recubiertos cubren la zona lesionada de la pared y reducen el riesgo de formación de aneurismas en esta situación vascular tan especial69.
En lo referente a las enfermedades del tejido conectivo, como los síndromes de Marfan o Ehlers-Danlos, la evidencia no basta para seleccionar el tratamiento óptimo de la CoAo en estos casos. No obstante, pueden aplicarse consideraciones similares a las descritas para el ST en lo referente a la selección de stents recubiertos cuando el tratamiento percutáneo sea anatómicamente viable.
Adultos y pacientes de edad avanzada
Los pacientes de edad avanzada suelen presentar calcificación grave en el lugar de la coartación, lo que complica el implante y expansión del stent y puede conducir a resultados subóptimos y a un mayor riesgo de complicaciones. En este sentido, algunos autores recomiendan realizar varias dilataciones del stent implantado para ir restaurando poco a poco el diámetro aórtico fisiológico. Se aconseja el uso de stents recubiertos en el tratamiento de la CoAo en pacientes de edad avanzada con pared aórtica calcificada70.
En casos complejos seleccionados, como adultos con coartación grave de larga evolución conducente a oclusión aórtica completa o casi completa, el tratamiento percutáneo puede seguir siendo viable. Estos casos requieren una planificación meticulosa de la intervención, dilataciones escalonadas o stents recubiertos para restablecer de forma segura la permeabilidad aórtica. Se pueden emplear técnicas avanzadas como estrategias de escalado de guías, abordajes retrógrados o anterógrados y predilataciones meticulosas para minimizar el riesgo de lesión aórtica y optimizar el implante de stent. Casos clínicos y series pequeñas han demostrado que, con hemodinamistas experimentados y la planificación adecuada, la reparación percutánea logra resultados satisfactorios incluso en anatomías tan complicadas como estas65.
INNOVACIONES Y TÉCNICAS EMERGENTES
Avances en la tecnología de stents
Stents biodegradables
Polímeros bioabsorbibles como el PLLA (ácido poli-l-láctico) y el PLA (ácido poli-láctico)71 podrían ser una alternativa a los stents metálicos en niños y recién nacidos. Estos stents deben proporcionar soporte estructural a través de su geometría; no obstante, su menor resistencia frente los metales los hace inadecuados para vasos grandes y rígidos como la aorta72,73. En la actualidad, no hay ningún stent poliméricos bioabsorbible para el tratamiento de la CoAo en niños74. A pesar de esto, los stents bioabsorbibles podrían reducir los costes y riesgos asociados a los implantes permanentes. Los avances en la tecnología de stents pronto podrán dar soluciones biodegradables que permitan el tratamiento no quirúrgico y crecimiento normal de lactantes con CoA.
Stents expandibles
Una de las limitaciones del implante de stents en lactantes es el tamaño de la vaina introductora necesaria para implantar un stent que luego se pueda volver a dilatar a fin de adaptarse al crecimiento somático75. Los stents expandibles con balón son el patrón oro para el tratamiento de la CoAo76. No obstante, los stents autoexpandibles aún están en fase de investigación y podrían reducir el riesgo de fractura del stent, disección vascular y formación de aneurismas77.
Los intentos por abordar los desafíos asociados al crecimiento incluyen el desarrollo de stents autodisruptivos, como el Growth (QualiMed, Alemania), diseñado para el tratamiento de la CoAo. Este dispositivo consta de 2 mitades de acero inoxidable electropulido cortadas con láser y unidas mediante suturas bioabsorbibles que forman una estructura circular. Las suturas se reabsorben por completo en un plazo de 6 meses, periodo tras el cual ambas mitades se mantendrán en posición de forma segura sin limitar el crecimiento natural, lo cual permite implantar stents convencionales más grandes que podrán expandirse hasta dimensiones adultas. A pesar de las expectativas iniciales, estos stents fracasaron por las altas tasas de reintervención y por una adaptación insuficiente al crecimiento78.
En la actualidad, las últimas estrategias se centran en nuevos diseños de stents con perfiles de liberación bajos y alto potencial de redilatación, como el Palmaz Genesis XD, el Intrastent Mega y el Cheatham Platinum, siendo este último el primero aprobado para tratar la CoAo. Estos stents reducen notablemente el riesgo de reestenosis y la necesidad de implantes adicionales. El Cheatham Platinum (NuMED, Estados Unidos) está fabricado con alambres de platino e iridio dispuestos en una configuración en zigzag capaz de expandirse hasta un diámetro de 30 mm. Su importante capacidad de dilatación reduce, significativamente, la necesidad de implantar stents adicionales, lo cual se traduce en una menor tasa de reestenosis frente a otros dispositivos58,79.
Entre las tecnologías emergentes están el stent Minima (Renata Medical, Estados Unidos), diseñado para el tratamiento de la estenosis vascular congénita, permite un tamaño inicial < 4 mm para su implantación al nacimiento, puede expandirse > 22 mm manteniendo toda su integridad estructural y fuerza radial80 y el BeGrow (Bentley InnoMed, Alemania), desarrollado para el tratamiento de la estenosis de la arteria pulmonar, que permite dilataciones de hasta 11,5 mm y tiene puntos de rotura controlados para adaptarse al crecimiento y a futuras intervenciones81.
Tecnologías emergentes y de navegación
Los modelos impresos en tres dimensiones (3D) están demostrando ser muy valiosos para la planificación de intervenciones complejas en el tratamiento de CC82,83. Los modelos 3D han demostrado ser útiles durante la planificación quirúrgica y percutánea, incluida la hipoplasia del arco aórtico y el implante valvular percutáneo. Estos modelos se crean a partir de técnicas de imagen como la RMC, la angio-TC o la ecocardiografía, seguidas de segmentación e impresión. Los modelos rígidos son ideales para el posicionamiento de stents y los flexibles permiten examinar la dinámica de la pared vascular83. Desde el punto de vista clínico, la impresión 3D mejora la precisión de la intervención, acorta los tiempos de esta y reduce las complicaciones, lo cual resulta beneficioso para pacientes de alto riesgo o con anatomías complejas.
Líneas futuras
Las técnicas de imágen avanzada, las últimas tecnologías de stents74 y los abordajes híbridos son capaces de mejorar los resultados del tratamiento de la CoAo. También es fundamental contar con protocolos rigurosos de seguimiento a largo plazo para vigilar la durabilidad del tratamiento y valorar posibles complicaciones tardías en los pacientes.
Seguimos teniendo necesidades no cubiertas en el tratamiento percutáneo como falta de técnicas estandarizadas y abordajes óptimos para los distintos perfiles de los pacientes84,85. Se necesita perfeccionar los criterios de selección de los pacientes, mejorar el tratamiento de las complicaciones y recopilar datos clínicos más amplios a largo plazo que garanticen unos resultados óptimos y la seguridad del paciente.
Por último, las prioridades más importantes en materia de investigación en este campo incluyen realizar ensayos clínicos aleatorizados que comparen nuevos diseños de stents, optimizar las técnicas de implante, evaluar el papel que juega la posdilatación y el mejor momento para ello, mejorar las técnicas de imágen para guiar y valorar los resultados, determinar las indicaciones y el momento óptimo para realizar reintervenciones percutáneas y abordar el tratamiento de pacientes durante el paso de la atención pediátrica a adulta86.
No cabe duda de que la inteligencia artificial tendrá un papel relevante en el tratamiento percutáneo de las CC. En el caso de la CoAo, permitirá un análisis más preciso de las técnicas de imagen para caracterizar su gravedad. Asimismo, permitirá una mejor planificación terapéutica y posibilitará la selección del abordaje y dispositivo más adecuados y el diseño de stents individualizados adaptados al perfil de cada paciente, con vistas a optimizar los resultados a largo plazo.
CONCLUSIONES
El implante de stent percutáneo se ha convertido en el tratamiento estándar para pacientes elegibles con CoAo y viene avalado por un éxito operatorio consistente y resultados favorables a largo plazo, Los estudios que se realicen en el futuro deberían centrarse en optimizar el diseño de los dispositivos, la adaptabilidad pediátrica y los protocolos estandarizados de seguimiento.
FINANCIACIÓN
Ninguna.
DECLARACIÓN SOBRE EL USO DE INTELIGENCIA ARTIFICIAL
No se utilizó inteligencia artificial en la elaboración de esta revisión.
CONTRIBUCIÓN DE LOS AUTORES
Conceptualización: E. Flores-Umanzor, J. Galeano, O.A. Centurión y A. Ruberti; metodología: R. Luna-López, I. Morr-Verenzuela, P. Cepas-Guillén, S. Montserrat y S. Prat-González; validación: D. Pereda, R. Sanz-Ruiz, J.M. Carretero Bellón, O. Abdul-Jawad Altisent, S. Brugaletta, M. Sabaté, X. Freixa; redacción, borrador original: V. Arévalos, A. Salazar-Rodríguez y G. Velázquez; redacción, revisión y edición: V. Arévalos, A. Salazar-Rodríguez, G. Velázquez, B. Vidal, L. Sanchis, I. Anduaga y A. Fernández-Cisneros; supervisión: M. Sabaté y E. Flores-Umanzor. Todos los autores leyeron y dieron su aprobación a la versión final del manuscrito.
CONFLICTO DE INTERESES
Ninguno.
BIBLIOGRAFÍA
1. Teo LL, Cannell T, Babu-Narayan SV, Hughes M, Mohiaddin RH. Prevalence of associated cardiovascular abnormalities in 500 patients with aortic coarctation referred for cardiovascular magnetic resonance imaging to a tertiary center. Pediatr Cardiol. 2011;32:1120-1127.
2. Kim YY, Andrade L, Cook SC. Aortic Coarctation. Cardiol Clin. Aug 2020;38:337-351.
3. Ruhela M, Randhawa H, Bagarhatta P, Bagarhatta R, Jain A. Coarctation of Aorta with Supravalvular Pulmonary Stenosis in an Adult Patient:A Rare Exception of the Fetal Flow Pattern Theory. Am J Med Case Rep. 2015;3:53-58.
4. Hoffman JI, Kaplan S. The incidence of congenital heart disease. J Am Coll Cardiol. 2002;39:1890-1900.
5. Becker AE, Becker MJ, Edwards JE. Anomalies associated with coarctation of aorta:particular reference to infancy. Circulation. 1970;41:1067-1075.
6. Levy MJ, Levinsky L, Deviri E, Hauptman E, Blieden LC. Coarctation of the aorta in infancy. Tex Heart Inst J. 1983;10:57-62.
7. Mitchell ME. Aortic Coarctation Repair:How I Teach It. Ann Thorac Surg. 2017;104:377-381.
8. Chen B, Wei M. Aortic Coarctation. N Engl J Med. 2024;390:1420.
9. Baumgartner H, De Backer J, Babu-Narayan SV, et al. 2020 ESC Guidelines for the management of adult congenital heart disease. Eur Heart J. 2021;42:563-645.
10. Campbell M. Natural history of coarctation of the aorta. Br Heart J. 1970;32:633-40.
11. Mazzolai L, Teixido-Tura G, Lanzi S, et al. 2024 ESC Guidelines for the management of peripheral arterial and aortic diseases. Eur Heart J. 2024;45:3538-3700.
12. Kvitting JP, Olin CL. Clarence Crafoord:a giant in cardiothoracic surgery, the first to repair aortic coarctation. Ann Thorac Surg. 2009;87:342-346.
13. Singer MI, Rowen M, Dorsey TJ. Transluminal aortic balloon angioplasty for coarctation of the aorta in the newborn. Am Heart J. 1982;103:131-132.
14. Harris KC, Du W, Cowley CG, Forbes TJ, Kim DW. A prospective observational multicenter study of balloon angioplasty for the treatment of native and recurrent coarctation of the aorta. Catheter Cardiovasc Interv. 2014;83:1116-1123.
15. Cowley CG, Orsmond GS, Feola P, McQuillan L, Shaddy RE. Long-term, randomized comparison of balloon angioplasty and surgery for native coarctation of the aorta in childhood. Circulation. 2005;111:3453-3456.
16. O'Laughlin MP, Perry SB, Lock JE, Mullins CE. Use of endovascular stents in congenital heart disease. Circulation. 1991;83:1923-1939.
17. Suárez de Lezo J, Pan M, Romero M, et al. Balloon-expandable stent repair of severe coarctation of aorta. Am Heart J. 1995;129:1002-1008.
18. Forbes TJ, Kim DW, Du W, et al. Comparison of surgical, stent, and balloon angioplasty treatment of native coarctation of the aorta:an observational study by the CCISC (Congenital Cardiovascular Interventional Study Consortium). J Am Coll Cardiol. 2011;58:2664-2674.
19. Gunn J, Cleveland T, Gaines P. Covered stent to treat co-existent coarctation and aneurysm of the aorta in a young man. Heart. 1999;82:351.
20. de Giovanni JV. Covered stents in the treatment of aortic coarctation. J Interv Cardiol. 2001;14:187-190.
21. Forbes T, Matisoff D, Dysart J, Aggarwal S. Treatment of coexistent coarctation and aneurysm of the aorta with covered stent in a pediatric patient. Pediatr Cardiol. 2003;24:289-291.
22. Lock JE, Castaneda-Zuniga WR, Bass JL, Foker JE, Amplatz K, Anderson RW. Balloon dilatation of excised aortic coarctations. Radiology. 1982;143:689-691.
23. Beekman RH, Rocchini AP, Dick M, 2nd, et al. Percutaneous balloon angioplasty for native coarctation of the aorta. J Am Coll Cardiol. 1987;10:1078-1084.
24. Rao PS. Balloon angioplasty of native coarctation of the aorta. J Invasive Cardiol. 2000;12:407-409.
25. Luijendijk P, Bouma BJ, Groenink M, et al. Surgical versus percutaneous treatment of aortic coarctation:new standards in an era of transcatheter repair. Expert Rev Cardiovasc Ther. 2012;10:1517-1531.
26. Hernández-González M, Solorio S, Conde-Carmona I, et al. Intraluminal aortoplasty vs. surgical aortic resection in congenital aortic coarctation. A clinical random study in pediatric patients. Arch Med Res. 2003;34:305-310.
27. Rodés-Cabau J, MiróJ, Dancea A, et al. Comparison of surgical and transcatheter treatment for native coarctation of the aorta in patients >or =1 year old. The Quebec Native Coarctation of the Aorta study. Am Heart J. 2007;154:186-192.
28. Shaddy RE, Boucek MM, Sturtevant JE, et al. Comparison of angioplasty and surgery for unoperated coarctation of the aorta. Circulation. 1993;87:793-799.
29. Walhout RJ, Lekkerkerker JC, Ernst SM, Hutter PA, Plokker TH, Meijboom EJ. Angioplasty for coarctation in different aged patients. Am Heart J. 2002;144:180-186.
30. Fawzy ME, Fathala A, Osman A, et al. Twenty-two years of follow-up results of balloon angioplasty for discreet native coarctation of the aorta in adolescents and adults. Am Heart J. 2008;156:910-917.
31. Fletcher SE, Cheatham JP, Froeming S. Aortic aneurysm following primary balloon angioplasty and secondary endovascular stent placement in the treatment of native coarctation of the aorta. Cathet Cardiovasc Diagn. 1998;44:40-44.
32. Carr JA. The results of catheter-based therapy compared with surgical repair of adult aortic coarctation. J Am Coll Cardiol. 2006;47:1101-1107.
33. Hellenbrand WE, Allen HD, Golinko RJ, Hagler DJ, Lutin W, Kan J. Balloon angioplasty for aortic recoarctation:results of Valvuloplasty and Angioplasty of Congenital Anomalies Registry. Am J Cardiol. 1990;65:793-797.
34. Rao PS, Thapar MK, Wilson AD, Levy JM, Chopra PS. Intermediate-term follow-up results of balloon aortic valvuloplasty in infants and children with special reference to causes of restenosis. Am J Cardiol. 1989;64:1356-1360.
35. Batlivala SP, Goldstein BH. Current Transcatheter Approaches for the Treatment of Aortic Coarctation in Children and Adults. Interv Cardiol Clin. 2019;8:47-58.
36. Reich O, Tax P, BartákováH, et al. Long-term (up to 20 years) results of percutaneous balloon angioplasty of recurrent aortic coarctation without use of stents. Eur Heart J. 2008;29:2042-2048.
37. Zabal C, Attie F, Rosas M, Buendía-Hernández A, García-Montes JA. The adult patient with native coarctation of the aorta:balloon angioplasty or primary stenting?Heart. 2003;89:77-83.
38. Tzifa A, Ewert P, Brzezinska-Rajszys G, et al. Covered Cheatham-platinum stents for aortic coarctation:early and intermediate-term results. J Am Coll Cardiol. 2006;47:1457-1463.
39. Qureshi AM, McElhinney DB, Lock JE, Landzberg MJ, Lang P, Marshall AC. Acute and intermediate outcomes, and evaluation of injury to the aortic wall, as based on 15 years experience of implanting stents to treat aortic coarctation. Cardiol Young. 2007;17:307-318.
40. Tanous D, Collins N, Dehghani P, Benson LN, Horlick EM. Covered stents in the management of coarctation of the aorta in the adult:initial results and 1-year angiographic and hemodynamic follow-up. Int J Cardiol. 2010;140:287-295.
41. Chessa M, Carrozza M, Butera G, et al. Results and mid-long-term follow-up of stent implantation for native and recurrent coarctation of the aorta. Eur Heart J. 2005;26:2728-2732.
42. Stout KK, Daniels CJ, Aboulhosn JA, et al. 2018 AHA/ACC Guideline for the Management of Adults With Congenital Heart Disease:A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines. Circulation. 2019;139:e698-e800.
43. Bulbul ZR, Bruckheimer E, Love JC, Fahey JT, Hellenbrand WE. Implantation of balloon-expandable stents for coarctation of the aorta:implantation data and short-term results. Cathet Cardiovasc Diagn. 1996;39:36-42.
44. Ewert P, Abdul-Khaliq H, Peters B, Nagdyman N, Schubert S, Lange PE. Transcatheter therapy of long extreme subatretic aortic coarctations with covered stents. Catheter Cardiovasc Interv. 2004;63:236-239.
45. Kenny D, Hijazi ZM. Coarctation of the aorta:from fetal life to adulthood. Cardiol J. 2011;18:487-495.
46. Krasemann T, Bano M, Rosenthal E, Qureshi SA. Results of stent implantation for native and recurrent coarctation of the aorta-follow-up of up to 13 years. Catheter Cardiovasc Interv. 2011;78:405-412.
47. Koletsis E, Ekonomidis S, Panagopoulos N, Tsaousis G, Crockett J, Panagiotou M. Two stage hybrid approach for complex aortic coarctation repair. J Cardiothorac Surg. 2009;4:10.
48. Teixeira AM, Reis-Santos K, Anjos R. Hybrid approach to severe coarctation and aortic regurgitation. Cardiol Young. 2005;15:525-528.
49. Novosel L, Perkov D, Dobrota S, C´oric´V, Štern Padovan R. Aortic coarctation associated with aortic valve stenosis and mitral regurgitation in an adult patient:a two-stage approach using a large-diameter stent graft. Ann Vasc Surg. 2014;28:494.e9-e14.
50. Russell TA, Quarto C, Nienaber CA. A single-stage hybrid approach for the management of severely stenotic bicuspid aortic valve, ascending aortic aneurysm, and coarctation of the aorta with a literature review. J Cardiol Cases. 2018;17:183-186.
51. Tacy TA, Baba K, Cape EG. Effect of aortic compliance on Doppler diastolic flow pattern in coarctation of the aorta. J Am Soc Echocardiogr. 1999;12:636-642.
52. Krieger EV, Stout KK, Grosse-Wortmann L. How to Image Congenital Left Heart Obstruction in Adults. Circ Cardiovasc Imaging. 2017;10:e004271.
53. Hedgire SS, Baliyan V, Ghoshhajra BB, Kalra MK. Recent advances in cardiac computed tomography dose reduction strategies:a review of scientific evidence and technical developments. J Med Imaging (Bellingham). 2017;4:031211.
54. Julsrud PR, Breen JF, Felmlee JP, Warnes CA, Connolly HM, Schaff HV. Coarctation of the aorta:collateral flow assessment with phase-contrast MR angiography. AJR Am J Roentgenol. 1997;169:1735-1742.
55. Hom JJ, Ordovas K, Reddy GP. Velocity-encoded cine MR imaging in aortic coarctation:functional assessment of hemodynamic events. Radiographics. 2008;28:407-416.
56. Isselbacher EM, Preventza O, Hamilton Black J, 3rd, et al. 2022 ACC/AHA Guideline for the Diagnosis and Management of Aortic Disease:A Report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2022;146:e334-e482.
57. Malek R, Puckett Y, Agasthi P. Catheter Management of Coarctation. StatPearls. StatPearls Publishing;2025. Disponible en:https://www.statpearls.com/physician/cme/activity/↻9/?specialty=specialty°=md.
58. Hatoum I, Haddad RN, Saliba Z, Abdel Massih T. Endovascular stent implantation for aortic coarctation:parameters affecting clinical outcomes. Am J Cardiovasc Dis. 2020;10:528-537.
59. Steiner I, Prsa M. Immediate results of percutaneous management of coarctation of the aorta:A 7-year single-centre experience. Int J Cardiol. 2021;322:103-106.
60. Nana P, Spanos K, Brodis A, et al. A Systematic Review and Meta-analysis on Stenting for Aortic Coarctation Management in Adults. J Endovasc Ther. 2023:15266028231179919.
61. Yang L, Chua X, Rajgor DD, Tai BC, Quek SC. A systematic review and meta-analysis of outcomes of transcatheter stent implantation for the primary treatment of native coarctation. Int J Cardiol. 2016;223:1025-1034.
62. Schleiger A, Al Darwish N, Meyer M, Kramer P, Berger F, Nordmeyer J. Long-term follow-up after endovascular treatment of aortic coarctation with bare and covered Cheatham platinum stents. Catheter Cardiovasc Interv. 2023;102:672-682.
63. Holzer RJ, Gauvreau K, McEnaney K, Watanabe H, Ringel R. Long-Term Outcomes of the Coarctation of the Aorta Stent Trials. Circ Cardiovasc Interv. 2021;14:e010308.
64. Feltes TF, Bacha E, Beekman RH, 3rd, et al. Indications for cardiac catheterization and intervention in pediatric cardiac disease:a scientific statement from the American Heart Association. Circulation. 2011;123:2607-2652.
65. Pan M, Pericet C, González-Manzanares R, et al. Very long-term follow-up after aortic stenting for coarctation of the aorta. Rev Esp Cardiol. 2024;77:332-341.
66. Morgan T. Turner syndrome:diagnosis and management. Am Fam Physician. 2007;76:405-410.
67. Donadille B, Christin-Maitre S. Heart and Turner syndrome. Ann Endocrinol (Paris). 2021;82:135-140.
68. Zanjani KS, Thanopoulos BD, Peirone A, Alday L, Giannakoulas G. Usefulness of stenting in aortic coarctation in patients with the Turner syndrome. Am J Cardiol. 2010;106:1327-1331.
69. Bons LR, Van Den Hoven AT, Malik M, et al. Abnormal Aortic Wall Properties in Women with Turner Syndrome. Aorta (Stamford). 2020;8:121-131.
70. Kische S, D'Ancona G, Stoeckicht Y, Ortak J, Elsässer A, Ince H. Percutaneous treatment of adult isthmic aortic coarctation:acute and long-term clinical and imaging outcome with a self-expandable uncovered nitinol stent. Circ Cardiovasc Interv. 2015;8:e001799.
71. Qiu TY, Song M, Zhao LG. A computational study of crimping and expansion of bioresorbable polymeric stents. Mech Time Depend Mater. 2018;22:273-290.
72. Borghi Jr TC, Costa Jr JR, Abizaid A, et al. Comparação da retração aguda do stent entre o suporte vascular bioabsorvível eluidor de everolimus e dois diferentes stents metálicos farmacológicos. Rev Bras Cardiol Invasiva. 2013;21.
73. Veeram Reddy SR, Welch TR, Wang J, et al. A novel design biodegradable stent for use in congenital heart disease:mid-term results in rabbit descending aorta. Catheter Cardiovasc Interv. 2015;85:629-639.
74. Veeram Reddy SR, Welch TR, Nugent A. Biodegradable Stent Use For Congenital Heart Disease. Progress in Pediatric Cardiology. 2021;61:101349.
75. Goldstein BH, Kreutzer J. Transcatheter Intervention for Congenital Defects Involving the Great Vessels:JACC Review Topic of the Week. J Am Coll Cardiol. 2021;77:80-96.
76. Zablah JE, Morgan GJ. Pulmonary Artery Stenting. Interv Cardiol Clin. 2019;8:33-46.
77. Sadeghipour P, Mohebbi B, Firouzi A, et al. Balloon-Expandable Cheatham-Platinum Stents Versus Self-Expandable Nitinol Stents in Coarctation of Aorta:A Randomized Controlled Trial. JACC Cardiovasc Interv. 2022;15:308-317.
78. Ewert P, Peters B, Nagdyman N, Miera O, Kühne T, Berger F. Early and mid-term results with the Growth Stent--a possible concept for transcatheter treatment of aortic coarctation from infancy to adulthood by stent implantation?Catheter Cardiovasc Interv. 2008;71:120-126.
79. Cheatham JP. Stenting of coarctation of the aorta. Catheter Cardiovasc Interv. 2001;54:112-125.
80. Zahn EM, Abbott E, Tailor N, Sathanandam S, Armer D. Preliminary testing and evaluation of the renata minima stent, an infant stent capable of achieving adult dimensions. Catheter Cardiovasc Interv. 2021;98:117-127.
81. Quandt D, Knirsch W, Michel-Behnke I, et al. First-in-man pulmonary artery stenting in children using the Bentley®BeGrow™stent system for newborns and infants. Int J Cardiol. 2019;276:107-109.
82. Pluchinotta FR, Giugno L, Carminati M. Stenting complex aortic coarctation:simulation in a 3D printed model. EuroIntervention. 2017;13:490.
83. Ghisiawan N, Herbert CE, Zussman M, Verigan A, Stapleton GE. The use of a three-dimensional print model of an aortic arch to plan a complex percutaneous intervention in a patient with coarctation of the aorta. Cardiol Young. 2016;26:1568-1572.
84. Khalaj R, Tabriz AG, Okereke MI, Douroumis D. 3D printing advances in the development of stents. Int J Pharm. 2021;609:121153.
85. Capelli C, Sauvage E, Giusti G, et al. Patient-specific simulations for planning treatment in congenital heart disease. Interface Focus. 2018;8:20170021.
86. Rigatelli G, Chiastra C, Pennati G, Dubini G, Migliavacca F, Zuin M. Applications of computational fluid dynamics to congenital heart diseases:a practical review for cardiovascular professionals. Expert Rev Cardiovasc Ther. 2021;19:907-916.

