RESUMEN
Se presentan las indicaciones actuales, el material, las técnicas, las complicaciones, los resultados y las controversias de los procedimientos percutáneos que permiten abordar la patología valvular y de las ramas pulmonares. El presente artículo ofrece una perspectiva del material actualmente disponible de forma clara para el cardiólogo intervencionista.
Palabras clave: Valvuloplastia. Angioplastia. Valvulas percutaneas.
ABSTRACT
Brief review of current indications, materials, techniques, complications, results, and controversies around percutaneous procedures for the management of pulmonary valve and arterial branches disease. This article gives the interventional cardiologist a perspective on the material currently available.
Keywords: Valvuloplasty. Angioplasty. Percutaneous valve.
Abreviaturas AVP: atresia valvular pulmonar. CC: cardiopatía congénita. DCP: derivación cavopulmonar. EP: estenosis pulmonar. IP: insuficiencia pulmonar. RP: ramas pulmonares. TSVD: tracto de salida del ventrículo derecho. VD: ventrículo derecho.
ESTENOSIS VALVULAR PULMONAR
La estenosis pulmonar (EP) valvular es de origen casi exclusivamente congénito y supone el 7-10% de las cardiopatías congénitas (CC). Aunque con frecuencia es un defecto aislado, puede asociarse a otras malformaciones congénitas.
La estenosis adquirida es muy infrecuente, en relación con un síndrome carcinoide o con fiebre reumática. Una forma emergente es la estenosis de bioprótesis quirúrgicas o de conductos valvulados.
La EP valvular puede coexistir con estenosis infundibular o supravalvular pulmonar; esta última es frecuente en relación con los síndromes de Noonan, Williams o Alagille, así como en la rubeola congénita.
La presentación clínica es variable, desde la estenosis crítica o la atresia valvular pulmonar (AVP) en el recién nacido hasta la estenosis leve que no precisa tratamiento.
Aunque su presentación en la vida adulta suele ser asintomática, en casos de estenosis grave se han descrito disnea de esfuerzo, disfunción ventricular, arritmias y hasta muerte súbita. En este grupo puede presentarse como forma nativa o tras una cirugía o una valvuloplastia previa.
Etiología
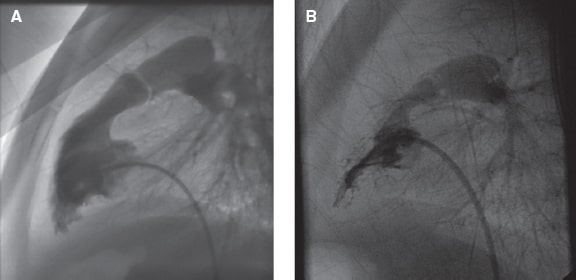
La EP puede tener 3 formas anatomopatológicas1 (figura 1):
-
– EP típica. Es la forma más habitual: válvula típicamente tricomisural, con leve engrosamiento de velos y fusión comisural. El anillo valvular muestra un desarrollo normal y es frecuente la dilatación posestenótica. La apertura valvular es típicamente en cúpula con un orificio estenótico central. Rara vez presenta calcificación.
-
– EP por válvula displásica. Se presenta en aproximadamente el 20% de todos los casos de EP, aunque es frecuente en el síndrome de Noonan. Los velos valvulares están engrosados y mixomatosos, con apertura limitada y escasa fusión comisural. Puede llevar asociada hipoplasia anular e incluso de tronco pulmonar proximal.
-
– EP asociada a otras CC, como comunicación interauricular, comunicación interventricular, transposición de grandes arterias, doble salida del ventrículo derecho (VD) o tetralogía de Fallot. La válvula a menudo es bicúspide o incluso unicúspide. Puede llevar asociada estenosis infundibular o supravalvular pulmonar e hipoplasia de anillo.
Figura 1. A: estenosis valvular por válvula displásica. B: estenosis valvular típica.
Valvuloplastia pulmonar
Desde 1982, la valvuloplastia pulmonar percutánea es la técnica de elección para el tratamiento de la estenosis valvular pulmonar desde el recién nacido hasta la vida adulta. Su objetivo es la sobredistensión de los velos y el rasgado de estos a nivel del rafe comisural.
Esta técnica con frecuencia es curativa y tiene una baja tasa de reestenosis en el seguimiento, muchas veces tratable con un segundo procedimiento.
El grado de insuficiencia pulmonar (IP) residual inmediato no suele ser mayor que leve, aunque puede progresar a lo largo de los años. A pesar de ello, es infrecuente la necesidad de reemplazo valvular por este motivo.
Indicaciones
La evolución natural de la estenosis valvular pulmonar se relaciona con el grado de obstrucción. Aunque el gradiente Doppler medio se relaciona de manera más fiable con el gradiente hemodinámico pico-pico, las guías internacionales establecen el grado de obstrucción en función del gradiente Doppler pico instantáneo2,3:
-
– Estenosis leve (gradiente Doppler pico instantáneo < 36 mmHg o velocidad pico < 3 m/s). Curso normalmente benigno, compatible con una vida normal. En los pacientes adultos se considera suficiente la evaluación cada 5 años.
-
– Estenosis moderada (gradiente Doppler pico instantáneo 36-64 mmHg o velocidad pico 3-4 m/s). Aunque con frecuencia es asintomática, la limitación al gasto cardiaco del VD puede dar lugar a la aparición de disnea o de fatiga con el ejercicio. Un 20% puede evolucionar hacia un grado mayor de obstrucción. Se realizará evaluación cada 2 años.
-
– Estenosis grave (gradiente Doppler pico instantáneo > 64 mmHg, velocidad pico > 4 m/s o gradiente Doppler medio > 40 mmHg). Se asocia con la presencia de sintomatología, disfunción del VD o cianosis. Siempre se indicará tratamiento.
Las indicaciones para el tratamiento de la estenosis valvular pulmonar se detallan en la tabla 14,5.
Tabla 1. Indicaciones de tratamiento en estenosis valvular pulmonar
| Estenosis crítica del recién nacido |
| Estenosis valvular pulmonar grave (gradiente Doppler pico > 60 mmHg o medio |
| > 40 mmHg), en paciente asintomático |
| Estenosis valvular pulmonar moderada (gradiente Doppler pico instantáneo |
| > 50 mmHg o medio > 30 mmHg) en paciente sintomático |
| Se indicará cirugía en caso de asociación con: |
| Insuficiencia pulmonar moderada o grave |
| Estenosis subvalvular o supravalvular |
| Insuficiencia tricúspide grave |
| Dilatación sintomática de arteria pulmonar por compresión extrínseca de estructuras vecinas |
| Necesidad de corrección quirúrgica de otras anomalías asociadas o cirugía de arritmia (técnica Maze) |
| La valvuloplastia percutánea puede ser la primera opción en caso de válvulas displásicas, frente a la cirugía, aunque la tasa de éxito es menor |
Técnica y material
La técnica de la valvuloplastia pulmonar percutánea ha sido ampliamente descrita1 y se puede realizar bajo sedación consciente, con anestesia local o incluso con anestesia general en los pacientes pediátricos. Se administra heparina sódica a dosis de 100 UI/kg hasta un máximo de 5000 UI. La ecocardiografía transtorácica o transesofágica no es de uso sistemático.
El acceso venoso femoral es el más frecuente, aunque son posibles otros accesos alternativos, como la vena yugular o el acceso transhepático. En caso de anillo valvular pulmonar grande pueden ser necesarios 2 accesos venosos simultáneos para realizar la técnica de doble balón. El acceso arterial es opcional.
Tras el registro basal de las presiones se realizará una ventriculografía derecha preferentemente en los planos lateral y posteroanterior con 30° de inclinación craneal. La medición del anillo pulmonar se realiza en sístole a nivel de la unión con los velos valvulares.
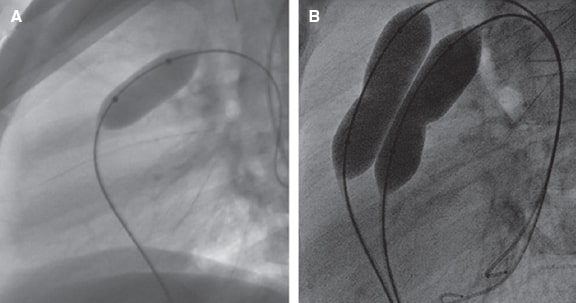
Tras cruzar con el catéter la válvula pulmonar, se posicionará una guía de intercambio y que provea alto soporte en la arteria pulmonar distal (preferentemente la arteria lobar inferior). Pueden emplearse diferentes tipos de catéter-balón y se recomienda un diámetro inicial 1,2-1,25 veces mayor que el diámetro del anillo pulmonar (figura 2A). En caso de persistir un gradiente hemodinámico > 30 mmHg y en ausencia de IP significativa, se recomienda repetir el procedimiento con un nuevo catéter-balón, hasta una relación de 1,4. No conviene sobrepasar una relación de 1,5, salvo en caso de válvulas displásicas. La longitud recomendable del balón es de 20 mm en los recién nacidos y los lactantes, de 30 mm en los pacientes pediátricos y de 40 mm en los adultos.
Figura 2. A: valvuloplastia pulmonar con un balón. B: valvuloplastia pulmonar con doble balón.
En caso de anillos valvulares grandes puede realizarse la técnica de doble balón (figura 2B); ambos balones deberán tener la misma longitud. Se ha descrito el diámetro efectivo de la combinación de 2 catéteres-balón6 (tabla 2), que puede estimarse de la siguiente forma:
Tabla 2. Diámetro efectivo con la técnica de doble balón
| Diámetro | 6 mm | 7 mm | 8 mm | 10 mm | 12 mm | 14 mm | 15 mm | 16 mm | 18 mm | 20 mm | 22 mm | 24 mm |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 6 mm | 9,0 | |||||||||||
| 7 mm | 10,7 | 11,5 | ||||||||||
| 8 mm | 11,5 | 12,3 | 13,1 | |||||||||
| 10 mm | 13,3 | 14,0 | 14,8 | 16,4 | ||||||||
| 12 mm | 15,1 | 15,8 | 16,5 | 18,0 | 19,6 | |||||||
| 14 mm | 16,9 | 17,6 | 18,3 | 19,7 | 21,3 | 22,9 | ||||||
| 15 mm | 17,8 | 18,5 | 19,2 | 20,6 | 22,1 | 23,7 | 24,5 | |||||
| 16 mm | 18,7 | 19,4 | 20,1 | 21,5 | 23,0 | 24,6 | 25,4 | 26,2 | ||||
| 18 mm | 20,6 | 21,2 | 21,9 | 23,3 | 24,7 | 26,3 | 27,0 | 27,8 | 29,5 | |||
| 20 mm | 22,5 | 23,1 | 23,7 | 25,1 | 26,5 | 28,0 | 28,8 | 29,5 | 31,1 | 32,7 | ||
| 22 mm | 24,4 | 25,0 | 25,6 | 26,9 | 28,3 | 29,7 | 30,5 | 31,2 | 32,8 | 34,4 | 36,0 | |
| 24 mm | 26,3 | 26,9 | 27,5 | 28,8 | 30,1 | 31,5 | 32,2 | 33,0 | 34,5 | 36,1 | 37,7 | 39,3 |
Diámetro efectivo = 0,82 (diámetro 1 + diámetro 2)
No se han demostrado diferencias significativas en términos de eficacia entre la valvuloplastia pulmonar percutánea con balón simple o con doble balón.
Resultados y seguimiento
La tasa de éxito inmediato del procedimiento es cercana al 90%, con una muy baja mortalidad (0,24%) y escasas complicaciones mayores (0,35%). En la válvula pulmonar displásica, la tasa de éxito es menor1. La cirugía puede reservarse como segunda opción en este tipo de anatomía valvular.
La tasa de reestenosis observada en el seguimiento es del 21% en series históricas y del 8-10% en estudios más recientes7-9. Los factores de riesgo son la presencia de válvula displásica, un gradiente hemodinámico residual ≥ 30 mmHg y el uso de una relación balón/anillo < 1,2.
En ausencia de IP de grado mayor a leve, la repetición de la valvuloplastia percutánea es de elección salvo en caso de displasia valvular, en la que puede indicarse la cirugía.
La IP está presente en el seguimiento en un 40-90% de los pacientes, con incremento a lo largo del seguimiento. Un mayor grado de estenosis inicial, una menor edad en el momento de la valvuloplastia y una mayor relación balón/anillo son factores de riesgo.
A pesar de ello, rara vez es necesario indicar el reemplazo valvular, con indicaciones que se basarán en la presencia de síntomas, así como en los volúmenes ventriculares y los parámetros de función del VD. Los estudios sugieren que podrían utilizarse los mismos parámetros de indicación que en la TOF corregida con IP residual10.
Situaciones especiales
Atresia valvular pulmonar
La AVP es una CC compleja caracterizada por la obstrucción completa al flujo pulmonar que se manifiesta en los primeros días de vida, tras el cierre fisiológico del conducto arterioso, y dejada a su evolución natural es incompatible con la vida.
El marcador anatómico fundamental es la atresia valvular, generalmente membranosa, con velos fusionados y anillo valvular hipodesarrollado. Son frecuentes otras lesiones secundarias a esta anomalía principal, entre las que destaca el hipodesarrollo variable del VD y de la válvula tricúspide, así como las anomalías en la circulación coronaria. El tronco y las arterias pulmonares suelen ser normales.
El tratamiento de estos pacientes incluye una estabilización inicial mediante el mantenimiento temporal de la permeabilidad ductal con infusión de prostaglandina E1. El enfoque de tratamiento definitivo dependerá de la gravedad de las lesiones acompañantes. En los pacientes con pronóstico más favorable, en términos de desarrollo suficiente del VD y de la válvula tricúspide, y en ausencia de circulación coronaria dependiente del VD, estará indicada la apertura inicial de la válvula.
Esta técnica se realiza frecuentemente por vía percutánea11,12 (vídeos 1 a 8 del material adicional), accediendo por vía venosa al VD y al tracto de salida del VD (TSVD), donde se posiciona un catéter con curva coronaria derecha (JR) o mamaria interna, bajo el plano valvular imperforado. Por su interior, una vez asegurada la adecuada posición, se avanza por un sistema compuesto por microcatéter y guía de radiofrecuencia, con la que se atraviesa el plano valvular, y con posterioridad se realiza una valvuloplastia secuencial con catéter-balón.
Aunque tras este procedimiento se consigue establecer un flujo anterógrado desde el VD, de forma muy infrecuente este flujo es suficiente para mantener una adecuada saturación de oxígeno arterial, debido a diferentes factores: persistencia de la obstrucción en el TSVD a nivel valvular/infundibular, comportamiento restrictivo del VD e hipodesarrollo de la válvula tricúspide. Todo ello condiciona un insuficiente flujo pulmonar por la vía natural y la persistencia de un importante cortocircuito interatrial de derecha a izquierda, con la consiguiente desaturación. Por este motivo, de forma habitual es necesaria una fuente accesoria de flujo pulmonar, que habrá de extenderse más allá del periodo neonatal.
Una alternativa emergente en los últimos años es el implante de un stent coronario en el conducto arterioso. Este procedimiento puede realizarse en la misma intervención o en un segundo procedimiento, mediante acceso anterógrado venoso o retrógrado arterial. El objetivo será implantar un stent coronario de 3-4 mm, de forma que cubra toda la longitud ductal, evitando su protrusión en el extremo aórtico o pulmonar.
Esta técnica permite mantener un flujo pulmonar y una saturación de oxígeno arterial suficientes hasta conseguir un adecuado desarrollo del VD. El stent ductal tiende al cierre espontáneo por proliferación endoluminal a lo largo del primer año de vida. En algunos casos, puede ser necesario un nuevo implante de stent intra-stent en el seguimiento.
Valvuloplastia pulmonar fetal
La valvuloplastia pulmonar fetal es una técnica poco frecuente, aplicable a fetos con diagnóstico prenatal de estenosis valvular pulmonar crítica o AVP, y riesgo de evolución hacia hipoplasia del VD. Habitualmente se realiza entre las semanas 21 y 28 de gestación. Su objetivo es promover un mayor desarrollo intrauterino de las estructuras cardiacas derechas, favoreciendo así una fisiología biventricular tras el nacimiento.
Mediante control ecográfico simultáneo, y tras conseguir una adecuada posición fetal, se realiza una punción transuterina, transtorácica fetal y cardiaca, y se accede al TSVD con una aguja de Chiva 22 G. La válvula pulmonar se atraviesa directamente mediante punción con la aguja en caso de atresia, posicionando distalmente una guía coronaria de 0,014 pulgadas. Sobre esta guía, por el interior de la aguja, se avanza un catéter-balón coronario de muy bajo perfil, con el que se realiza la dilatación valvular.
En cuanto a sus resultados, se trata de una técnica compleja, que requiere experiencia y colaboración multidisciplinaria. Una de sus dificultades reside en conseguir una adecuada orientación de la aguja, debido al pequeño tamaño de la cavidad del VD y a su compleja geometría. Presenta una alta frecuencia de complicaciones, que incluyen arritmias fetales, derrame pericárdico e incluso muerte fetal.
Un estudio internacional multicéntrico13 ha documentado la realización de este procedimiento en 58 fetos, con un 55% de complicaciones, incluyendo 7 muertes. Comparando la evolución de los pacientes tratados con una cohorte similar de fetos que no recibieron tratamiento, se evidenció posnatalmente una mayor tendencia a la fisiología biventricular en el primer grupo (87 frente a 43%). A pesar de ello, en la actualidad no están establecidos los criterios de indicación de esta técnica, y hay que sopesar en cada caso particular los riesgos, la experiencia del grupo y los beneficios esperables.
Válvulas pulmonares percutáneas
Muchas CC requieren una reconstrucción del TSVD, bien sea con un parche, con una bioprótesis o con un conducto entre el VD y la arteria pulmonar. En la tetralogía de Fallot, el 90% de los pacientes operados en edad infantil alcanzarán la edad adulta y un número significativo tendrán insuficiencia o EP como consecuencia de la sección del anillo o del empleo de conductos. Es motivo de controversia tanto el momento como la forma de tratarlas, pues no existe consenso entre los expertos y las guías clínicas americanas, canadienses y europeas5 establecen bases generales, con niveles de evidencia subóptimos; además, es frecuente que cada caso particular tenga características que no se recogen en los algoritmos propuestos.
Los cirujanos han utilizado distintos materiales para resolver las disfunciones: aloinjertos, prótesis biológicas de pericardio porcino –con y sin soporte–, prótesis mecánicas y conductos valvulados (artesanalmente) y no valvulados. En las dos últimas décadas, el intervencionismo percutáneo ha irrumpido con fuerza empujado por el desarrollo de la industria de bioprótesis, soportadas sobre stents, pero todavía es cuestionable cuándo tratar pacientes asintomáticos: la precocidad en el recambio se asocia a un deterioro más rápido y un mayor número de intervenciones –cada una con su propio riesgo–, mientras que las actuaciones tardías pueden no impedir o revertir el deterioro de la función y de los volúmenes ventriculares.
La morfología del TSVD disfuncional es muy compleja y determina el material del abordaje (la forma en «pirámide» es poco compatible con válvulas autoexpandibles), y además tiene un comportamiento muy dinámico. La ecocardiografía no es suficiente y se requiere la tomografía computarizada para conocer la anatomía coronaria; la resonancia magnética cardiaca (no puede realizarse en todos los casos, por problemas con clips, marcapasos o prótesis que generan interferencias) permite calcular los volúmenes y la función, y visualizar ese comportamiento dinámico. Actualmente se da más importancia a la función que al tamaño del VD, tanto para indicar el implante como para valorar el seguimiento. La anatomía coronaria no siempre refleja el comportamiento durante o después del implante, y de hecho, los cambios en las medidas del TSVD durante el implante no conllevan cambios lineales en las arterias coronarias, por lo que la coronariografía sigue siendo esencial. Las válvulas autoexpandibles tienen una longitud notablemente mayor que las expandibles por balón (y que las quirúrgicas), por lo que la distancia total en la zona prevista para el implante se convierte en crucial. Desde hace años se sabe que la válvula pulmonar no es igual que la válvula aórtica en arquitectura ni en funcionamiento, y que las mismas prótesis funcionan de manera distinta en posición aórtica o pulmonar (pueden llegar a no cerrar de manera efectiva)14.
Indicaciones y perspectiva histórica
Las indicaciones para las válvulas pulmonares percutáneas contempladas en las guías europeas5 y norteamericana15 son similares a las del recambio quirúrgico. Los pacientes sintomáticos plantean pocas dudas. Para los pacientes asintomáticos hay que recurrir a datos electrocardiográficos (prolongación absoluta del QRS > 180 o progresión de esta) y hemodinámicos (como una relación de presiones entre el VD y el ventrículo izquierdo > 0,7), gradientes Doppler pico y medios > 50 y > 30, respectivamente, y sobre todo a los hallazgos de la resonancia magnética en los casos de regurgitación pulmonar significativa (fracción de regurgitación > 30%): volúmenes telediastólicos ventriculares derechos > 160 ml/m2, volumen telediastólico derecho doble que el izquierdo, volumen telesistólico > 80 ml/m2 y fracción de eyección del VD < 0,40-0,45 (o evolución negativa de esta).
La primera válvula cardiaca implantada percutáneamente fue la pulmonar, por Bonhoeffer en el año 2000, a partir de la idea de suturar una vena yugular bovina con válvula en un stent vascular. Se comercializó con el nombre de Melody (Medtronic Inc, Estados Unidos), con marcado CE y canadiense en 2006 y de la Food and Drug Administration en 2010, y está indicada para pacientes mayores con conductos quirúrgicos disfuncionantes. Su utilización fuera de las indicaciones aprobadas ha crecido y se utiliza en pacientes de hasta 20 kg de peso y en TSVD nativos16, con modificaciones técnicas (implante de stent previo en la zona de implante) para minimizar algunas de las complicaciones más frecuentes (fractura del stent), pero con precauciones debido a las cifras significativas de endocarditis infecciosa (problema compartido por su homóloga bovina quirúrgica Contegra, Medtronic, Estados Unidos). Además, la limitación de tamaños disponibles de las válvulas (18, 20 y 22 mm) es otro problema porque muchos pacientes con regurgitación tienen grandes calibres del tronco pulmonar, hecho que ha generado numerosas soluciones imaginativas para extender su uso.
En 2008, la válvula Edwards SAPIEN (Edwards Lifesciences LLC, Estados Unidos) para posición aórtica empezó a utilizarse en posición derecha gracias al ensayo clínico COMPASSION, en el que se demostró que era segura y eficaz para conductos con regurgitación pulmonar moderada o grave, con o sin estenosis17. Sus tamaños son mayores (23, 26 y 29 mm), no presenta fracturas y la incidencia de endocarditis infecciosa es menor (aunque la literatura no es «robusta» en este aspecto). En 2016 obtuvo la aprobación de las agencias reguladoras europea y norteamericana la utilización de la Edwards SAPIEN XT en niños y adultos con insuficiencia o EP; la actual SAPIEN 3 solo está autorizada para posición aórtica, pero existen numerosos implantes fuera de indicación en posición pulmonar.
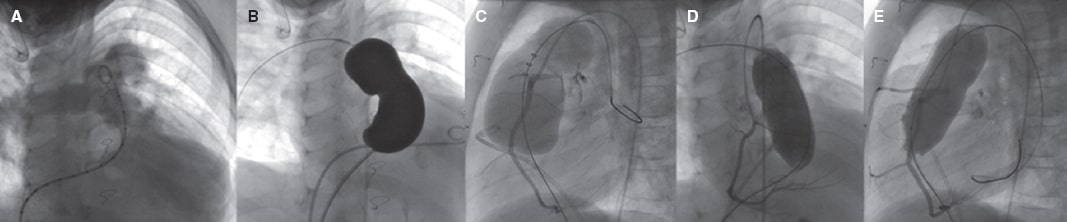
El procedimiento exige una cuidadosa planificación. Son necesarios un acceso arterial y 2 venosos, preferiblemente femoral, pero también puede implantarse por vía venosa yugular. El estudio angiográfico (figura 3) tiene 2 objetivos: a) estudiar la anatomía y las dimensiones del «tronco» o conducto y las ramas pulmonares (RP), para lo que son necesarias varias proyecciones (la salida del VD se delinea mejor en oblicua anterior derecha 20° y craneal 20°, y en lateral, pero exige modificaciones en cada caso) e inyectar contraste tanto en el tronco como en el VD mientras se ocluye el tronco con un catéter-balón, y b) estudiar las relaciones anatómicas de proximidad, porque las estructuras adyacentes pueden verse comprimidas (la propia aorta ascendente o las arterias coronarias). Para ello, mientras se mantiene el catéter-balón inflado en la arteria pulmonar se realiza un aortograma o una coronariografía, o ambos. El catéter-balón puede ser del tipo «tallado de comunicación interauricular» de 34 o 35 mm, que es muy distensible, pero que en no raras ocasiones se distiende más allá del diámetro objetivo del implante y causa compresión coronaria o aórtica, por lo que debe disponerse de otros tipos de balones de diámetro idéntico al objetivo del implante. Si se trata de un conducto calcificado, la aproximación será progresiva debido al riesgo de rotura. En caso de emplear una válvula Melody, previamente debe implantarse un stent en todos los casos –stent recubierto si el conducto está calcificado–, lo que no es obligado para el resto de las válvulas.
Figura 3. Ejemplos de angiografías. A: de tronco pulmonar, personalizada, en proyección oblicua anterior derecha 20° y craneal 40°. B: con catéter-balón de medición de comunicación interauricular para estimar medidas y morfología, en la misma proyección. C: en proyección lateral mostrando cómo la sobredistensión produce obstrucción de la arteria coronaria descendente anterior, que nace desde la coronaria derecha. D: coronariografía selectiva con balón del mismo diámetro de la válvula que se va a implantar, sin obstrucción coronaria, en la misma proyección que en A. E: con el mismo balón que en D, en proyección lateral.
No hay uniformidad acerca de si todo el procedimiento debe realizarse en una sola sesión o en dos, dedicando la primera al estudio anatómico/fisiológico y al implante del stent.
Prótesis valvulares pulmonares disponibles
Existen 2 grandes grupos de prótesis: las expandibles por balón y las autoexpandibles. Las primeras tienen más recorrido histórico, están aprobadas por las agencias reguladoras, se han realizado 10.000 implantes en todo el mundo, tienen mayor fuerza radial, permiten un mayor control del diámetro que se debe alcanzar, se acortan al dilatarlas y son muy exigentes desde el punto de vista técnico. Las autoexpandibles son más recientes, están en desarrollo con varios ensayos clínicos para obtener la aprobación, alcanzan mayores diámetros, son más largas y puede haber problemas en la porción distal del tronco pulmonar, ya que no se acortan y no se tiene control sobre el diámetro (alcanzan su valor nominal) ni permiten redilataciones. En la figura 4 se muestran las prótesis disponibles para uso pulmonar.
Figura 4. Válvulas pulmonares percutáneas. A: Melody (Medtronic, Estados Unidos). B: Edwards XT (Edwards Lifesciences LLC, Estados Unidos). C: Venus (Venus MedTech, China). D: Harmony (Medtronic, Estados Unidos). E: Pulsta (Taewoong Medical, Corea del Sur).
Melody TPV
La Melody TPV (Medtronic Inc, Estados Unidos)18 es una prótesis expandible por balón. Se construye a partir de vena yugular bovina con una válvula nativa de 18 mm suturada a un stent CP de platino-iridio (NuMED, Canadá). La longitud del conjunto es de 28 mm y se acorta de acuerdo con el diámetro final. Puede expandirse desde 16 hasta 22 mm de diámetro (y probablemente también funcione hasta los 24 mm). La válvula se crimpa a mano y se transporta y libera a través del sistema propio de Medtronic Ensemble –adaptación del doble balón de angioplastia BIB (NuMED Inc, Estados Unidos)– con un perfil de 22 Fr en su porción distal y de 16 Fr en su porción proximal, de 100 mm de longitud; se avanza a través de una guía de alto soporte alojada en una rama pulmonar (preferiblemente la izquierda).
Edwards SAPIEN
La prótesis valvular Edwards SAPIEN (Edwards Lifesciences LLC, Estados Unidos)18 es expandible sobre balón, con velos de pericardio porcino montado sobre un stent de cromocobalto y con menos altura que la Melody. El modelo SAPIEN XT THV es el autorizado para posición pulmonar y se fabrica en 23 (altura de 14,3 mm), 26 (altura de 17,2 mm) y 29 mm (altura de 19,1 mm). Se crimpa con un dispositivo específico, proximal a la posición del balón, y se «monta» sobre el mismo cuando ya se encuentra en la vena cava inferior, transportándose y liberándose a través de un sistema propio Novaflex (Edwards Lifesciences, Estados Unidos) de perfil 18, 19 o 20 Fr, según el diámetro de la válvula, muy rígido y no fácil de avanzar ni retirar, en especial si se ha realizado un implante previo de stent, y que puede dañar la válvula tricúspide. El modelo SAPIEN 3 THV se fabrica en los mismos diámetros (con alturas de 18, 20 y 22,5 mm), pero es una evolución cuya porción recubierta interna es bastante más corta (9,3, 10,2 y 11.6 mm), con una protección externa de tereftalato de polietileno para minimizar la posibilidad de fugas, y cuyo stent tiene geometrías diferentes en las porciones proximal y distal para que se acorte más en su extremo proximal; las de 23 y 26 mm se transportan a través del sistema «defectable» Edwards Commander Delivery System 14 Fr, y las de 29 mm a través de uno de 16 Fr con un introductor propio (Edwards eSheath). Existen comunicaciones en las que mediante un inflado con mayor volumen que el nominal la SAPIEN 3 puede llegar a los 30 mm.
Válvula Venus
La válvula Venus (Venus MedTech, China) está diseñada para tractos nativos. Es autoexpandible, trivalvar de pericardio porcino, con stent de nitinol de 30 mm de longitud, recubierto por pericardio porcino –excepto en su porción distal– que se dilata en ambos extremos (1 cm en cada extremo), con marcas radiopacas para facilitar su localización; el diámetro de la válvula es el de la porción no dilatada (18-34 mm). El sistema de transporte es propio, con un calibre distal de 20-22 Fr y proximal de 16 Fr, y necesita un introductor de 22-24 F. Se crimpa a mano, sumergida en solución salina fisiológica fría19.
Hay 2 ensayos clínicos para conseguir la marca CE, uno en China y otro en Europa, ambos concluidos y en fase de evaluación de datos, con criterios de inclusión similares a los utilizados para el resto de las válvulas.
Harmony mTPV 25
La prótesis Harmony mTPV 25 (Medtronic, Estados Unidos) consta de una estructura de nitinol autoexpandible, recubierto de poliéster y con una válvula de pericardio porcino cosida en el centro. Su desarrollo conceptual es enorme: los primeros ensayos empezaron en los Estados Unidos en 2013, pero la válvula sigue modificándose (Harmony TPV 22, Harmony TPV 25, Harmony TPV 25 modificada) y en la actualidad solo está disponible para investigación.
Válvula PULSTA
La válvula PULSTA20 (Taewoong Medical, Corea del Sur) está diseñada para tractos nativos. Es autoexpandible, de nitinol, trivalvar de pericardio porcino, recubierta también de pericardio porcino excepto en sus porciones proximal y distal (mayor), y tiene marcas radiopacas para delimitar la zona recubierta. La numeración corresponde a la zona más estrecha –que es el nivel de las comisuras–, desde los 18 a los 32 mm, y se escoge un diámetro 1-2 mm mayor que el del tronco pulmonar; la zona acampanada mide 4 mm más que la zona estrecha. Se fabrica en 2 longitudes: 33 y 38 mm. El calibre del sistema de transporte es de 18 Fr hasta los 28 mm y de 20 Fr para los tamaños mayores. Su fuerza radial es menor que la de las válvulas Melody y SAPIEN, y por ello no es de elección para conductos estenóticos.
En la actualidad, la mayoría de los implantes se han realizado en Asia y está en marcha un ensayo clínico en Europa, que comenzó en diciembre de 2019 y en el que participa España, con criterios de inclusión similares a los considerados para el resto de las válvulas.
Complicaciones y limitaciones
Las complicaciones y las limitaciones de estas prótesis son:
-
– Compresiones: aproximadamente en el 5% de los pacientes, durante el procedimiento, se identifica riesgo de compresión coronaria. Con las prótesis grandes puede producirse distorsión de la raíz aórtica con insuficiencia.
-
– Roturas: del conducto, sobre todo si está calcificado, durante la predilatación, que precisa implante inmediato de un stent cubierto; la navegación de las válvulas es difícil y requiere guías de alto soporte que pueden perforar las RP; durante el avance y la retirada puede dañarse la válvula tricúspide y producir insuficiencia.
A pesar de todo ello, la mortalidad durante el procedimiento es de alrededor del 1,4%21.
En el seguimiento, las fracturas fueron frecuentes (12,4%) con los antiguos implantes Melody cuando no se realizaba implante previo de stent, y los factores de riesgo eran la edad joven, el mayor gradiente antes del procedimiento y residual posterior, el menor tamaño del conducto, la proximidad al esternón y la observación de recoil tras la liberación22. La segunda complicación en frecuencia es la endocarditis infecciosa (4,9%), la mayoría sobre Melody, con una incidencia mayor que en los casos quirúrgicos y sobre la cual existen varias hipótesis: daño de la válvula durante el montaje, no observación estricta de esterilidad, endocarditis previa, resultado hemodinámico no satisfactorio, higiene dental deficiente, piercings y tatuajes, etc.)23.
Existen datos, procedentes de registros24 y de estudios multicéntricos, sobre la evolución de la válvula Melody a medio plazo y las reintervenciones sobre la misma25. En un periodo de seguimiento de algo más de 5 años, se realiza algún procedimiento en el 14,4-15% de los casos, la mayoría por fractura. Existe una gran variación de las indicaciones entre instituciones, y en el 65% de los procedimientos se ha realizado un reimplante sobre la válvula previa (valve in valve), lo que confirma que la endocarditis infecciosa sigue siendo el talón de Aquiles de la válvula Melody, con una incidencia de 2,4% pacientes-año. No existen datos suficientes sobre otro tipo de válvulas.
TRATAMIENTO PERCUTÁNEO DE LAS RAMAS PULMONARES
El abordaje percutáneo en estenosis de RP se ha generalizado gracias al desarrollo de nuevos materiales y avanzada tecnología, y hoy en día es la primera opción debido a los pobres resultados quirúrgicos. La estenosis de RP puede ser congénita, asociada a síndromes (Williams-Beuren, Alagille, etc.) o a infecciones connatales como la rubeola, o formar parte de CC complejas como la tetralogía de Fallot, la atresia pulmonar o el sling de la arteria pulmonar. Sin embargo, la estenosis es el resultado evolutivo o residual de la cirugía en esas mismas CC y en otras como en el switch arterial de Jatene (Lecompte), o cuando es necesario colocar un conducto entre el VD y las RP. El tratamiento percutáneo pretende mejorar el gasto cardiaco y aliviar la presión del VD, reequilibrar la distribución del flujo a ambos pulmones y mejorar la clase funcional, la capacidad de esfuerzo (VO2 y VE/VCO2) y el pronóstico en los pacientes con fisiología univentricular y biventricular. Como criterios de repercusión hemodinámica se consideran un gradiente ≥ 20 mmHg, una estenosis angiográfica ≥ 50%, una presión del VD o de la arteria pulmonar ≥ 60% de la sistémica (biventricular) o una asimetría ≥ 30% en la perfusión pulmonar por resonancia magnética o por gammagrafía; esta asimetría del flujo puede generar que estenosis unilaterales significativas no se traduzcan en gradientes de presión al tratarse de un flujo en paralelo26.
Generalidades
Angioplastia con balón
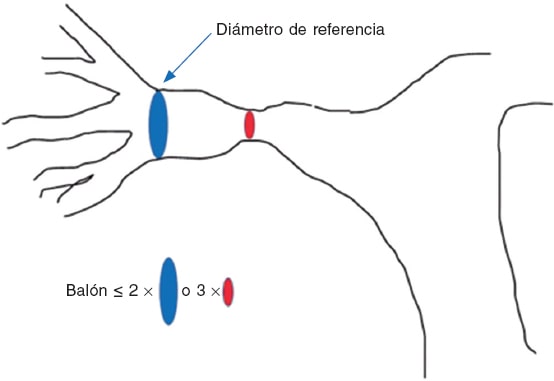
La angioplastia con balón se reserva para pacientes de bajo peso, cuando la anatomía impide colocar un stent o cuando se trata de segmentos implicados en futuras cirugías. La reestenosis, de hasta un 50% inmediatamente por recoil o compresión extrínseca, es más frecuente que con un stent. Es un procedimiento seguro, con menos del 1% de complicaciones mayores. Tomando como referencia del vaso el diámetro hiliar, se seleccionan balones de hasta el triple del diámetro crítico de la estenosis, sin sobrepasar el doble del diámetro de referencia (figura 5). Para que sea eficaz debe desaparecer la muesca y producirse un desgarro intimomedial controlado que remodele excéntricamente; es decir, los resultados pueden no ser inmediatos. Se considera exitoso el procedimiento si se produce un incremento de la luz ≥ 50% del diámetro mínimo, una reducción
Figura 5. Diámetros de referencia en el tratamiento percutáneo de las ramas pulmonares.
≥ 20% de presión en el VD o sistémica, o un incremento ≥ 20% en el flujo al pulmón tratado27. Utilizando los recientes balones de alta presión no distensibles y los balones con microtomos o cutting balloons mejoran los resultados en angioplastias que no responden a balones convencionales, o especialmente resistentes, como las de las ramas lobares en los pacientes con síndromes genéticos. Los cutting balloons habituales alcanzan los 8 mm de diámetro y precisan ser colocados en la zona que se va a tratar a través de una vaina para evitar lesionar la válvula tricúspide o la válvula pulmonar en su avance o retirada (figura 6).
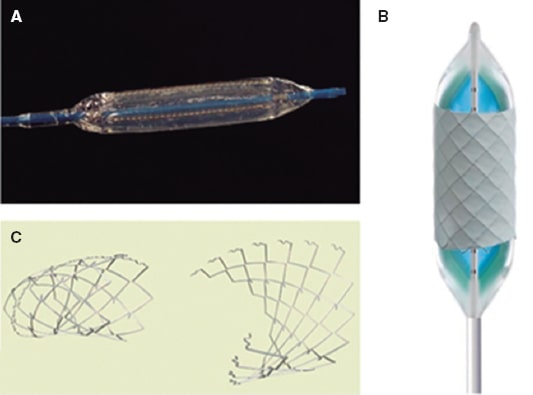
Figura 6. A: cutting balloon. B: balón BIB con stent CP cubierto montado. C: stent BeGrow.
Angioplastia con stent
La angioplastia con stent, descrita por Mullins en los años 1980, proporciona el soporte estructural y evita la reestenosis inmediata por recoil o plegamiento, y sus resultados a medio y largo plazo son mejores que los de la angioplastia convencional. El perfeccionamiento de los perfiles y del diseño en celdas semiabiertas o abiertas, que permiten la redilatación, ha conseguido acercar esta técnica a pacientes de menor edad y peso, a expensas de sucesivas redilataciones necesarias para adaptarlos al tamaño del vaso por el crecimiento o para dilatar el origen de ramas enjauladas. Varios trabajos demuestran que estas redilataciones sucesivas son efectivas y seguras. Los stents de celda cerrada son más estables en el crimpado manual y tienen en general mayor fuerza radial. Habitualmente tienen que navegar sobre el balón dentro de una vaina hasta la estenosis para evitar dañar las válvulas derechas y la migración del stent, y para poder ser reposicionados antes de la implantación28. El perfil de esta vaina es proporcional al diámetro del balón sobre el que se monta y tienen mejor perfil los premontados de un tamaño equivalente; existen incluso algunos modelos que no requieren el uso de introductores largos para su implante. Uno de los balones más usados es el doble balón BIB, de 8-30 mm de diámetro, que consiste en dos balones concéntricos en los que el inflado del interior permite predecir el comportamiento del stent en la estenosis, expandir secuencialmente y reposicionar si es necesario (figura 6). Considerando un índice de Nakata normal de 250-300 mm2/m2, un paciente adulto de 2 m2 de superficie corporal necesitará un stent que pueda alcanzar un diámetro ideal de 18-20 mm en cada rama. Los stents autoexpandibles mejoran el perfil al no requerir balón para su implantación; no son redilatables, pero en la actualidad están aprobados para otras localizaciones, como la vía biliar y el eje femoropoplíteo29.
En general se implantan stents desnudos y se reservan los cubiertos para casos en los que se pretende reparar la pared del vaso lesionado o regular mediante una forma de diábolo el flujo a una u otra rama, o a través de un shunt sistémico pulmonar (tabla 3).
Tabla 3. Stents empleados actualmente en las ramas pulmonares
Nuevas tecnologías
Las nuevas tecnologías incluyen:
-
– Balones liberadores de fármacos: balones no expandibles revestidos de sustancias antiproliferativas, como los análogos de la rapamicina o paclitaxel, aprobados para estenosis arteriales periféricas, pero especialmente útiles para tratar la reestenosis por proliferación intimal en los stents30.
-
– Stents bioabsorbibles: evitan la necesidad de redilataciones en pacientes en crecimiento. Pueden estar compuestos de polímeros orgánicos o de aleaciones de metales corrosibles, como hierro o magnesio. Algunos trabajos muestran una respuesta inflamatoria en la pared del vaso y dudas en cuanto a reestenosis significativas. Todavía sin aprobación por la Food and Drug Administration, el Pediatric Bioresorbable Stent (480 Biomedical Stent Inc, Estados Unidos) es el diseño con estudios en fases más avanzadas y ha sido específicamente desarrollado para el tratamiento de estenosis de RP en CC en niños.
-
– Stents fracturables: celdas con bisagras programadas para su rotura con un balón, como el BeGrow (Bentley, Alemania), o su reabsorción, como el Growth Stent (QualiMeD, Alemania), que consiste en 2 mitades unidas por suturas biodegradables que desaparecen en 5 meses y permiten crecer al vaso (figura 6).
Complicaciones
Los procedimientos percutáneos sobre RP son de riesgo moderado (angioplastia) o alto (stent). Suelen realizarse con anestesia general y heparina no fraccionada a dosis de 100 UI/kg, con un máximo de 5.000 UI y un tiempo de coagulación activado ≥ 250 s. Las complicaciones más frecuentes y los factores de riesgo se detallan en la tabla 4; son más frecuentes cuando el procedimiento es urgente y cuanto menor es la edad del paciente, alcanzando el 38% en neonatos. Como norma general, se recomienda colocar la guía del soporte necesario en la rama lobar inferior y no volver a sondar con guías ni avanzar nuevamente la vaina por el segmento recién dilatado una vez retirados. La rotura o la disección son más frecuentes en la angioplastia simple. Muchas veces no tienen repercusión clínica, pero en caso contrario se deben tratar revirtiendo la anticoagulación, inflando de nuevo un balón en la zona de fuga, colocando un stent o recurriendo a la cirugía. La reestenosis de los stent se debe fundamentalmente a la proliferación intimal, pero también puede suceder si el stent se fractura y pierde su integridad estructural, o por compresión extrínseca. Ocurre con menos frecuencia con los diseños de celda semiabiertos y con la mayor flexibilidad de los autoexpandibles. No existen recomendaciones claras sobre el tratamiento antitrombótico tras el implante. La endotelización sucede a los 6 meses del implante y, aunque la trombosis es rara, la práctica habitual es mantener durante este tiempo un fármaco antiagregante31.
Tabla 4. Complicaciones y sus factores de riesgo más frecuentes
| Complicaciones | Factores de riesgo |
|---|---|
| Daño vascular | Sobredilatación, guía demasiado rígida, parches quirúrgicos, cirugía reciente |
| Trombosis | Derivación cavopulmonar, cianosis, ramas pequeñas, corto tiempo de coagulación activado, no antiagregación |
| Embolización del stent | Bajo peso, desproporción, bifurcación, malposición, emergencia, crimpado manual |
| Edema por reperfusión | Cianosis crónica, mayor edad |
| Discordancia | Implante precoz, diseño no dilatable |
| Reestenosis | Solapamiento corto, síndrome genético, derivación cavopulmonar, bifurcación, cintura residual, sobredimensión, compresión externa, stent autoexpandible |
Situaciones específicas
Bifurcaciones
Existen 2 opciones técnicas para reparar estas estenosis sin comprometer el flujo en la rama contralateral:
-
– Implantar 2 stents simultáneamente, cada uno sobre su guía y su vaina, procurando tamaños parecidos, e inflando ambos balones de manera progresiva y simultánea (figura 1A del material adicional).
-
– Colocar un stent largo, de celda abierta, desde una de las ramas hasta el tronco pulmonar para después recruzar hacia la rama contralateral con otra guía e implantar un segundo stent más corto (figura 1B del material adicional); esta técnica es útil cuando solo se dispone de un acceso venoso o se prevé colocar una prótesis pulmonar que precisa pre-stent.
Derivación cavopulmonar
En la frágil fisiología univentricular tipo Fontan –un circuito pulmonar no pulsátil y sin bomba– los criterios en los que se basa la indicación están en un umbral más bajo que en la fisiología biventricular, y prácticamente cualquier grado de estenosis angiográfica o gradiente hemodinámico son significativos, pues pueden generar grandes elevaciones de la presión venosa central y considerables asimetrías en la distribución del flujo a ambos pulmones. Asegurar una distribución lo más simétrica posible del flujo en los pulmones es esencial para evitar el desarrollo de fístulas arteriovenosas. Para esto puede ser necesario reducir el flujo de una fístula creada previamente o a una de las ramas mediante un stent cubierto en forma de diábolo (figura 2 del material adicional). Estos procedimientos son complejos por los accesos (femoral, yugular o transhepático) y porque son pacientes multiintervenidos, con mayor riesgo de trombosis (poliglobulia, flujo lento no pulsátil), con lechos quirúrgicos a veces recientes, de corta edad, etc. La angioplastia de RP es el procedimiento más frecuentemente realizado en una cohorte moderna extensa de pacientes con derivación cavopulmonar (DCP) total, tanto tras la DCP superior, como tras completarse la DCP inferior, solo por detrás de la angioplastia del conducto extracardiaco (figura 3 del material adicional). La estenosis es más frecuente en la RP izquierda (segmento proximal de la RP derecha originalmente) debido a su mayor recorrido, por la compresión de la vecina aorta ascendente y por presentar menor flujo en la fase entre el Glenn pulsátil y la DCP total32.
El tamaño final de las RP, y por tanto su flujo, están directamente relacionados con el éxito a largo plazo de esta fisiología y con la clase funcional de los pacientes, pero suele ser necesario revisar de manera invasiva y periódica el estado de los stents implantados para ajustarlos al crecimiento, pues los métodos no invasivos pueden no ser lo bastante sensibles. Tras el implante de un stent, las guías de la American Heart Association recomiendan tratamiento anticoagulante durante 3-6 meses.
Estado posoperatorio
La reparación de algunas CC conlleva un riesgo de estenosis residual o evolutiva de RP. Con la maniobra de Lecompte, asociada al switch arterial para reparar la d-transposición de grandes arterias, aparece estenosis de RP hasta en el 28% de forma precoz, y la estenosis supravalvular pulmonar es la principal causa de reintervención en la infancia. El tratamiento percutáneo es técnicamente demandante, pues son pacientes pequeños, con suturas a veces recientes, en bifurcación y con compromiso de espacio con la vena cava superior y la aorta ascendente (figuras 4 y 5 del material adicional). Por ello, la angioplastia simple puede ser la única opción, aunque es eficaz en menos de la mitad de los casos33.
Otras CC con frecuente estenosis residual de RP tras la cirugía son la tetralogía de Fallot, el truncus arterioso, el sling de arteria pulmonar, etc., y todas las condiciones que impliquen colocar un conducto entre el VD y las RP, como las intervenciones de Ross, Rastelli, Yasui, Sano, etc.
El desarrollo tecnológico actual, tanto en técnicas de imagen como en materiales y dispositivos, ha revolucionado las posibilidades del tratamiento percutáneo de las lesiones del tronco, las válvulas y las RP, por lo que las indicaciones referidas en las vías clínicas están siendo modificadas.
FINANCIACIÓN
Trabajo no financiado.
CONTRIBUCIÓN DE LOS AUTORES
F. Gutiérrez-Larraya Aguado ha coordinado el conjunto y revisado la edición final; C. Abelleira Pardeiro y E.J. Balbacid Domingo han redactado parte del texto y procurado figuras.
CONFLICTO DE INTERESES
No existen conflictos de los autores relativos al material expuesto.
MATERIAL ADICIONAL
Vídeo 1. Gutiérrez-Larraya Aguado F. DOI: 10.24875/RECIC.M20000193
Vídeo 2. Gutiérrez-Larraya Aguado F. DOI: 10.24875/RECIC.M20000193
Vídeo 3. Gutiérrez-Larraya Aguado F. DOI: 10.24875/RECIC.M20000193
Vídeo 4. Gutiérrez-Larraya Aguado F. DOI: 10.24875/RECIC.M20000193
Vídeo 5. Gutiérrez-Larraya Aguado F. DOI: 10.24875/RECIC.M20000193
Vídeo 6. Gutiérrez-Larraya Aguado F. DOI: 10.24875/RECIC.M20000193
Vídeo 7. Gutiérrez-Larraya Aguado F. DOI: 10.24875/RECIC.M20000193
Vídeo 8. Gutiérrez-Larraya Aguado F. DOI: 10.24875/RECIC.M20000193
BIBLIOGRAFÍA
1. Rao PS. Percutaneous Balloon Pulmonary Valvuloplasty:State of the Art. Catheter Cardiovasc Interv. 2007;69:747-763.
2. Baumgartner H, Hung J, Bermejo J, et al. Echocardiographic assessment of valve stenosis:EAE/ASE recommendations for clinical practice. American Society of Echocardiography, European Association of Echocardiography. J Am Soc Echocardiogr. 2009;22:1.
3. Silvilairat S, Cabalka AK, Cetta F, et al. Echocardiographic assessment of isolated pulmonary valve stenosis:which outpatient Doppler gradient has the most clinical validity. J Am Soc Echocardiogr. 2005;18:1137.
4. Warnes CA, Williams RG, Bashore, et al. TMACC/AHA 2008 Guidelines for the Management of Adults with Congenital Heart Disease:a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. Circulation. 2008;118:e714.
5. Baumgartner H, De Backer J, Babu-Narayan S, et al. 2020 ESC Guidelines for the management of adult congenital heart disease (ACHD). Eur Heart J. 2021;42:563-645.
6. Narang R, Das G, Dev V, et al. Effect of the balloon-annulus ratio on the intermediate and follow-up results of pulmonary balloon valvuloplasty. Cardiology. 1997;88:271-276.
7. McCrindle BW. Independent predictors of long-term results after balloon pulmonary valvuloplasty. Valvuloplasty and Angioplasty of Congenital Anomalies (VACA) Registry Investigators. Circulation. 1994;89:1751-1759.
8. Voet A, Rega F, Van de Bruaene A, et al. Long-term outcome after treatment of isolated pulmonary valve stenosis. Int J Cardiol. 2012;156:11-15.
9. Devanagondi R, Peck D, Sagi J, et al. Long-Term Outcomes of Balloon Valvuloplasty for Isolated Pulmonary Valve Stenosis. Pediatr Cardiol. 2017;38:247-254.
10. Ruckdeschel E, Kim YY. Pulmonary valve stenosis in the adult patient:pathophysiology, diagnosis and management. Heart. 2019;105:414-422.
11. Petit CJ, Glatz AC, Qureshi AM, et al. Outcomes After Decompression of the Right Ventricle in Infants With Pulmonary Atresia With Intact Ventricular Septum Are Associated With Degree of Tricuspid Regurgitation:Results From the Congenital Catheterization Research Collaborative. Circ Cardiovasc Interv. 2017;10:e004428.
12. Morgan GJ, Narayan SA, Goreczny S, et al. A low threshold for neonatal intervention yields a high rate of biventricular outcomes in pulmonary atresia with intact ventricular septum. Cardiol Young. 2020;30:649-655.
13. Hogan WJ, Grinenco S, Armstrong A, et al. Fetal Cardiac Intervention for Pulmonary Atresia with Intact Ventricular Septum:International Fetal Cardiac Intervention Registry. Fetal Diagn Ther. 2020;47:731-739.
14. Pragt H, van Melle JP, Verkerke GJ, Mariani MA Ebels T. Pulmonary versus aortic pressure behavior of a bovine pericardial valve. J Thorac Cardiovasc Surg. 2020;159:1051-1059.e1.
15. Stotut KK, Daniels CJ, Aboulhosn JA, et al. 2018 AHA/ACC guideline for the management of adults with congenital heart disease:executive summary:a report of the American College of Cardiology/American Heart Association task force on clinical practice guidelines. Circulation. 2019;139:e637-697.
16. Boshoff DE, Cools BL, Heying R, et al. Off label use of percutaneous pulmonary valved stents in the right ventricular outflow tract:time to rewrite the label?Catheter Cardiovasc Interv. 2013;81:987-995.
17. Kenny D, Rhodes J, Fleming G, et al. 3-Year outcomes of the Edwards SAPIEN Transcatheter heart valve for conduit failure in the pulmonary position from the COMPASSION multicenter clinical trial. J Am Coll Cardiol Interv. 2018;11:1920-1929.
18. Fleming GA, Hill KD, Green AS, et al. Percutaneous pulmonary valve replacement. Prog Ped Cardiol. 2012;33:143-150.
19. Cao QL, Kenny D, Zhou D, et al. Early clinical experience with a novel self-expanding percutaneous stent-valve in the native right ventricular outflow tract. Catheter Cardiovasc Interv. 2014:84:1131-1137.
20. Kim GB, Song MK, Bae EJ, et al. Successful feasibility human trial of a new self-expandable percutaneous pulmonary valve (Pulsta valve) implantation using knitted nitinol wire backbone and trileaflet α-gal-free porcine pericardial valve in the native right ventricular outflow tract. Circulation Cardiovasc Interv. 2018;11:e006494.
21. Virk SA, Liou K, Chandrakumar D, Gupta S, Cao C. Percutaneous pulmonary valve implantation:a systematic review of clinical outcomes. Int J Cardiol. 2015;201:487-489.
22. Ansari MM, Cardoso R, Garcia D, et al. Percutaneous pulmonary valve implantation:present status and evolving future. J Am Coll Cardiol. 2015;66:2246-2255.
23. Sharma A, Cote AT, Hosking MCK, et al. A systematic review of infective endocarditis in patients with bovine jugular vein valves compared with other valve types. J Am Coll Cardiol Interv. 2017;10:1449-1458.
24. Nordmeyer J, Ewert P, Gewillig M, et al. Acute and midterm outcomes of the postapproval MELODY registry:a multicenter registry of transcatheter pulmonary valve implantation. Eur Heart J. 2019;40:2255-2264.
25. Shahanavaz S, Berger F, Jones TJ, et al. Outcomes of transcatheter reintervention for dysfunction of a previously implanted transcatheter pulmonary valve. J Am Coll Cardiol. 2020;13:1529-1540.
26. Feltes TF, Bacha E, Beekman RH, et al. Indications for Cardiac Catheterization and Intervention in Pediatric Cardiac Disease:A scientific Statement from the American Heart Association. Circulation. 2011;123:2607-2652.
27. Patel AB, Ratnayaka K, Bergersen L. A review:Percutaneous pulmonary artery stenosis therapy:state-of-the-art and look to the future. Cardiol Young. 2019;29:93-99.
28. Hiremath G, Qureshi AM, Prieto L, et al. Balloon Angioplasty and Stenting for Unilateral Branch Pulmonary Artery Stenosis Improve Exertional Performance. JACC Cardiovasc Interv. 2019;12:289-297.
29. Zablah JE, Morgan GJ. Pulmonary Artery Stenting. Interv Cardiol Clin. 2019;8:33-46.
30. Cohen JL, Glickstein JS, Crystal MA. Drug-Coated Balloon Angioplasty:A novel treatment for pulmonary artery in-stent stenosis in a patient with Williams syndrome. Pediatr Cardiol. 2017;38:1716-1721.
31. Giglia TM, Massicotte MP, Tweddell JS, et al. Prevention and treatment of thrombosis in pediatric and congenital heart disease:a scientific statement from the American Heart Association. Circulation. 2013;128:2622-2703.
32. Franco Díez E, Balbacid Domingo E, Arreo del Val V, et al. Percutaneous Interventions in Fontan Circulation. Int J Cardiol Heart Vasc. 2015;8:138-146.
33. Nakanishi T, Matsumoto Y, Seguchi M, et al. Balloon Angioplasty for Postoperative Pulmonary Artery Stenosis in Transposition of the Great Arteries. J Am Coll Cardiol. 1993;22:859-866.