El Dr. Bruno Scheller es profesor de Cardiología Intervencionista Clínica y Experimental en la Universidad del Sarre y subdirector de la Clínica de Medicina Interna III en el Hospital Universitario del Sarre, en Hamburgo (Alemania). Como jefe de Cardiología Intervencionista, supervisa intervenciones con catéter para el tratamiento de la enfermedad coronaria y cardiopatías estructurales, incluyendo el implante percutáneo de válvula aórtica y la reparación percutánea de borde a borde. Su grupo de investigación está a la vanguardia en estudios preclínicos y clínicos sobre administración local de fármacos y desarrollo de nuevos tratamientos intervencionistas con catéter.
Empecemos desde el principio: ¿recuerda qué despertó su interés por estudiar Medicina?
Nací en una familia de clase obrera. Mi padre, minero del carbón, me enseñó habilidades relacionadas con el trabajo manual de las que sigo haciendo uso en la sala de hemodinámica. En secundaria, mi fuerte eran la física y las matemáticas. Hacia el final de mis estudios escolares, trabajé a tiempo parcial en una fábrica para ayudar a pagar mis estudios. Intenté decidir qué carrera estudiar mientras hacía las prácticas. A finales del verano de 1988, la región donde vivía se vio afectada por el desastre aéreo del festival de Ramstein. Nuestro hospital universitario fue uno de los centros que atendió a las víctimas civiles del siniestro. Por aquel entonces, estaba con las prácticas de enfermería en la unidad de cuidados intensivos, que asumió buena parte de la carga asistencial de la respuesta. La actitud profesional del personal de enfermería me dejó una impresión indeleble y me decidí a estudiar Medicina. No obstante, durante los primeros años de carrera, seguía dudando de si había elegido bien.
¿Por qué se especializó en cardiología? ¿Por qué decidió hacerse cardiólogo intervencionista?
Durante una clase de Medicina Interna en el invierno de 1990, nuestros cardiólogos demostraron con orgullo ser capaces de reabrir una coronaria derecha taponada en un paciente con infarto agudo de miocardio con elevación del segmento ST (IAMCEST) durante la noche. Por aquel entonces, la intervención coronaria percutánea (ICP) para el tratamiento del IAMCEST se consideraba, todavía, una práctica experimental. Fue entonces cuando me di cuenta de que la cardiología intervencionista era mi vocación.
Háblenos de su interés inicial y su trabajo con los balones farmacoactivos. ¿Cuáles fueron los ensayos preclínicos?
Hice mi tesis doctoral sobre los efectos de los medios de contraste radiológicos en la microcirculación. Este trabajo contó con el apo- yo del jefe del departamento de I+D de medios de contraste de Schering AG en Berlín (Alemania), el profesor Ulrich Speck. En diciembre de 1999 me invitó a Berlín, poco después de asistir, por primera vez en mi vida, al congreso Transcatheter Cardiovascular Therapeutics (TCT) en Washington D. C. (Estados Unidos), donde me impresionaron los datos preclínicos de los stents farmacoactivos. En Berlín, hablamos sobre cómo usar medios de contraste como portadores de agentes antiproliferativos.
Algunos meses después, el profesor Speck se trasladó al Departamento de Radiología del Hospital Charité, en Berlín, para ocupar una cátedra bajo la dirección de Bernd Hamm. Desarollamos un modelo porcino de reestenosis intrastent (RIS) y realizamos el primer estudio de formulaciones de agente de contraste con taxanos. Demostramos que un contacto de corta duración entre fármacos antiproliferativos como el paclitaxel y la pared vascular tenía un efecto biológico duradero y dependiente de la dosis. No obstante, seguía haciendo falta una técnica más específica para el tratamiento de las lesiones. De forma destacable, el recubrimiento de un catéter-balón convencional de angioplastia con un agente de contraste sumado al paclitaxel inhibió significativamente la formación neoin- timal tras el implante experimental de un stent en el modelo porcino. Esta observación marcaría el inicio de la tecnología en la que se basan los balones farmacoactivos (BFA).
Cuando presentamos los resultados preclínicos del BFA a principios de la década de 2000, la reacción de casi todo el mundo fue que no funcionaría, que aunque funcionara en cerdos no lo haría en humanos; y que, aunque lo hiciera, nadie iba a necesitar una tecnología como esta y mucho menos la utilizaría.
Cuéntenos brevemente su investigación clínica con los BFA en el tratamiento de la RIS y en lesiones de novo.
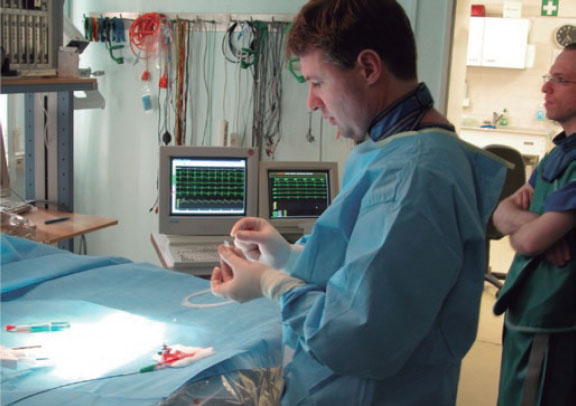
Estudio experimental en la sala de hemodinámica animal (2006).
En 2003, debatimos varias opciones para llevar a cabo un primer estudio en humanos. Por aquel entonces, no era posible predecir a partir de los datos en animales si la eficacia llegaría a demostrarse clínicamente o si los pacientes podrían resultar perjudicados por un efecto excesivo. Mi propuesta fue comenzar con una indicación segura que, además, representara una necesidad clínica no cubierta, la RIS, en la que ya hay un stent implantado y cubierto por una cantidad importante de tejido. Nuestro primer ensayo clínico1 en la indicación de la RIS tuvo éxito y allanó el camino para la indicación de los BFA en el tratamiento de la RIS. En la actualidad, nuestro ensayo Paccocath ISR se considera un hito en cardiología intervencionista2.
La idea de tratar lesiones de novo la propusieron inicialmente colegas que realizaban intervenciones vasculares periféricas. Gunnar Tepe y Thomas Zeller nos animaron a avalar un ensayo sobre el tratamiento de lesiones femoropoplíteas, un abordaje con el que me mostré muy escéptico al principio. Afortunadamente, el ensayo THUNDER3 demostró la utilidad de los BFA en arterias periféricas y trasformó de manera fundamental las estrategias empleadas en intervención vascular periférica.
Uno de los primeros estudios con lesiones coronarias de novo fue el PEPCAD I4. Se trató de una serie prospectiva no aleatorizada de pacientes con coronarias pequeñas. Por aquel entonces, desconocíamos muchas cosas sobre la preparación de las lesiones y solo teníamos BFA con diámetros de 2,5 mm, que intentamos emplear en lesiones que iban de los 2,0 a los 2,75 mm. El resultado positivo fue que aproximadamente el 70% de las lesiones pudieron tratarse con éxito solo con BFA, con una tasa de episodios dentro del rango de un único dígito. Por otro lado, aprendimos que combinar el tratamiento con BFA y el implante de stents era perjudicial, especialmente en casos de desajuste geográfico del tratamiento.
En este sentido, poco después de la Pascua de 2010 organizamos la primera reunión del Grupo de Consenso sobre BFA (inicialmente en Alemania y, después, a nivel internacional), coincidiendo oportunamente con el congreso anual de la German Cardiac Society celebrado en Mannheim (Alemania). Mi idea era predilatar las lesiones para identificar aquellas que pudiesen precisar implante de stent. Franz Kleber y yo propusimos el concepto, ampliamente aceptado en la actualidad, de «solo BFA», centrado en preparar la lesión para decidir si optar por un stent farmacoactivo (SFA) o un BFA como tratamiento final5.
Los criterios se eligieron de forma pragmática. Se consideró esencial alcanzar un grado de flujo TIMI 3 y la clasificación de las disecciones por debajo del tipo C se basó en datos antiguos de los pioneros días de Grüntzig. El umbral del porcentaje de estenosis por diámetro del 30% surgió tras reconocer lo difícil que era llegar al 10-20% con una angioplastia convencional (todavía no se conocían las ventajas de los balones especiales por aquel entonces); al mismo tiempo, un porcentaje de estenosis por diámetro del 50% sería indicativo, por definición, de reestenosis. Así, propusimos un valor de corte del 30%, que se ha mantenido como el patrón oro hasta nuestros días. No cabe duda de que estos criterios no son la última palabra y que debemos trabajar para tener mejores estándares. Hasta entonces, seguiremos utilizándolos. En coronarias pequeñas este umbral ha tenido un buen rendimiento en el ensayo Basket Small 26,7 y en estudios más amplios, como el Selution De Novo, que también han implementado con éxito estos criterios.
¿Cuáles eran, y siguen siendo, los principales desafíos técnicos en el desarrollo y evolución de esta tecnología?
El objetivo fundamental de la tecnología de los BFA es administrar la mayor cantidad posible de fármaco a la pared vascular durante el mayor tiempo posible, a pesar del corto tiempo de contacto entre balón y pared. Por eso las mejoras se han centrado en optimizar la trasferencia del fármaco a la pared vascular, crear un efecto depósito en esta y reducir la pérdida del recubrimiento hacia la periferia.
No todos los balones farmacoactivos son iguales. ¿En qué se parecen los BFA basados en paclitaxel a los basados en limus en términos de eficacia y resultados clínicos?
La cuestión más importante no es tanto qué fármaco es mejor o peor, sino cuán buena o deficiente es la tecnología de recubrimiento. En la actualidad, existen diferencias significativas y clínicamente relevantes a este respecto, tanto para el paclitaxel como para el sirolimus.
¿Qué papel juegan los BFA hoy en día en la práctica clínica?
En el contexto actual, depende en gran medida de cada centro, del investigador y, lo más importante, de la región geográfica. En muchos países de Asia, los BFA ya se utilizan en aproximadamente un 40% de los casos; en Europa nos vamos acercando poco a poco al 20% y en Estados Unidos apenas han empezado con esta tecnología.
Durante muchos años, nuestro centro ha seguido el principio de poner el foco en la preparación de la lesión, lo hacemos siempre para todas las lesiones. En última instancia, esto nos conduce a una combinación de BFA más SFA, en la que el número de lesiones y, sobre todo, la longitud de estas, ha llevado a un predominio de los BFA. En la actualidad, hallamos RIS prácticamente solo en pacientes portadores de stents largos implantados en otros centros.
¿Por qué están ahora en auge los BFA?
Es una pregunta que me hago todos los días y para la que, sinceramente, no tengo una respuesta concluyente. Llevamos 15 años siguiendo los principios básicos de preparación de la lesión y decisión entre BFA y SFA. En mi caso, la práctica diaria no ha cambiado mucho. El auge que vivimos en la actualidad es, sin duda, de índole psicológica. Lo importante es aprovechar esta nueva dinámica para generar evidencias clínicas sólidas y fiables.
¿Hacia dónde cree que se dirige esta técnica terapéutica en los próximos 5 a 10 años?
Aquí no soy imparcial. Patrick Serruys acaba de publicar una previsión en el European Heart Journal en la que vaticina que el SFA y el BFA se emplearán casi por igual para el año 20328. Que esto se haga realidad va a depender de muchos factores. En mi opinión, lo más importante es que llevemos a cabo investigaciones científicas de alto nivel.
Antes de terminar, ¿qué hace cuando no está trabajando?
Lo más importante de mi vida es mi familia. Dedico deliberadamente mi tiempo libre, en exclusiva, a mi esposa, mi hijo y el perrito que tenemos.
FINANCIACIÓN
Ninguna.
DECLARACIÓN SOBRE EL USO DE INTELIGENCIA ARTIFICIAL
No se utilizó.
CONFLICTO DE INTERESES
Ninguno.
SOBRE EL AUTOR
Fernando Alfonso es editor asociado de REC: Interventional Cardiology y su interés investigador se centra en los balones farmacoactivos.
BIBLIOGRAFÍA
1. Scheller B, Hehrlein C, Bocksch W, et al. Treatment of coronary in-stent restenosis with a paclitaxel-coated balloon catheter. N Engl J Med. 2006;355:2113-2124.
2. Byrne RA, Stone GW, Ormiston J, Kastrati A. Coronary balloon angioplasty, stents, and scaffolds. Lancet. 2017;390:781-792.
3. Tepe G, Zeller T, Albrecht T, et al. Local delivery of paclitaxel to inhibit restenosis during angioplasty of the leg. N Engl J Med. 2008;358:689-99.
4. Unverdorben M, Kleber FX, Heuer H, et al. Treatment of small coronary arteries with a paclitaxel-coated balloon catheter. Clin Res Cardiol. 2010;99:165-174.
5. Kleber FX, Mathey DG, Rittger H, Scheller B, German Drug-eluting Balloon Consensus G. How to use the drug-eluting balloon:recommendations by the German consensus group. EuroIntervention. 2011;7 Suppl K:K125-K128.
6. Jeger RV, Farah A, Ohlow MA, et al. Drug-coated balloons for small coronary artery disease (BASKET-SMALL 2):an open-label randomised non-inferiority trial. Lancet. 2018;392:849-856.
7. Jeger RV, Farah A, Ohlow MA, et al. Long-term efficacy and safety of drug-coated balloons versus drug-eluting stents for small coronary artery disease (BASKET-SMALL 2):3-year follow-up of a randomised, non-inferiority trial. Lancet. 2020;396:1504-1510.
8. Serruys PW, Oshima A, Ferraz-Costa G, et al. Coronary revascularization:a long-term perspective. Eur Heart J. 2025. https://doi.org/10.1093/eurheartj/ehaf883.


