RESUMEN
Introducción y objetivos: El implante percutáneo de válvula aórtica (TAVI) se ha consolidado como tratamiento de la estenosis aórtica grave. Como toda intervención, su seguridad y su efectividad deben monitorizarse en condiciones de práctica real. Para ello, se han analizado los datos del Sistema Nacional de Salud disponibles entre los años 2014 y 2017.
Métodos: Se evaluaron todos los pacientes mayores de 50 años con TAVI por vía transfemoral incluidos en el Registro de Actividad de Atención Especializada entre 2014 y 2017 procedentes de centros públicos o concertados. Se hicieron análisis de regresión logísticos para evaluar los factores asociados con la mortalidad y las complicaciones, y modelos binomiales negativos para la estancia media hospitalaria. Se usaron tasas estandarizadas para ajustar diferencias en las variables de efectividad y seguridad entre las diferentes comunidades autónomas, de acuerdo con el alto y bajo volumen de implantación de la técnica, considerando como referencia la mediana nacional (37 implantes por 105 habitantes) durante el periodo de tiempo analizado.
Resultados: En total se analizaron 5.454 casos de TAVI. La mortalidad intrahospitalaria pasó del 4,89% en 2014 al 2,7% en 2017. La estancia media hospitalaria descendió de 13,1 días en 2014 a 11,3 en 2017. A pesar de no observar diferencias en la mortalidad entre comunidades autónomas, aquellas con mayor volumen de implantes tuvieron una menor estancia media hospitalaria (OR = 0,88; IC95%, 0,86-0,91; p < 0,01), menor riesgo de infecciones (OR = 0,54; IC95%, 0,32-0,9; p = 0,02) y menor necesidad de marcapasos permanente (OR = 0,77; IC95%, 0,65-0,91; p < 0,01).
Conclusiones: El uso de TAVI crece progresivamente en España con resultados cada vez mejores respecto al éxito del implante y la morbimortalidad perioperatoria. La variabilidad interregional en las tasas de implante no se relaciona con la mortalidad observada, pero sí con la morbilidad y la estancia hospitalaria.
Palabras clave: Estenosis aórtica. Reemplazo de la válvula aórtica. Registro de Actividad de Atención Especializada. Enfermedad de las válvulas cardiacas. Implante percutáneo de válvula aórtica. TAVI.
Abstract
Introduction and objectives: Transcatheter aortic valve implantation (TAVI) has become the treatment of choice for the management of symptomatic severe aortic stenosis. As it happens with all procedures, the safety and effectiveness of TAVI must be monitored. To this end, we assessed the data available from the Spanish National Health Service from 2014 through 2017.
Methods: The study included patients aged > 50 years treated with TAVI and registered in the Activity Registry of Specialized Health Care from 2014 through 2017 from public and private hospitals in compliance with the National Health System. Multivariate logistic regression analyses were performed to identify factors associated with mortality and complications, and negative binomial models for the mean hospital length of stay (LoS). Standardized rates were used to discriminate both the effectiveness and safety among regions with higher and lower levels of implementation of the technique using the national median as the threshold, (37 implants x 105 habitants) in the 4-year period.
Results: A total of 5454 TAVIs were analyzed. The in-hospital mortality rate dropped from 4.89% in 2014 to 2.7% in 2017. The LoS decreased from 13.1 days in 2014 to 11.3 days in 2017. No differences in mortality were observed among the regions. However, the LoS of regions with a high volume of implants was significantly lower (OR, 0.88; 95%CI, 0.86-0.91; P < .01), as well as the risk of infections (OR, 0.54; 95%CI, 0.32-0.9; P = .02), and pacemaker implantation (OR, 0.77; 95%CI, 0.65-0.91; P < .01).
Conclusions: The use of TAVI in Spain is safe and has grown progressively with improved outcomes regarding morbidity and mortality. Differences among regions have been highlighted regarding patient access to TAVI. This heterogeneity was not associated with mortality but with differences in the morbidity rates.
Keywords: Aortic stenosis. Surgical aortic valve replacement. Valvular heart disease. Activity Registry of Specialized Health Care. Transcatheter aortic valve implantation. TAVI
Abreviaturas
EmH: estancia media hospitalaria. MPP: implante de marcapasos permanente. RAE-CMBD: Registro de Actividad de Atención Especializada - Conjunto Mínimo Básico de Datos. TAVI: implante percutáneo de válvula aórtica.
INTRODUCCIÓN
La estenosis aórtica es la valvulopatía adquirida más frecuente, con una prevalencia en torno al 3% en la población ≥ 65 años, que llega hasta el 7,4% en edades más avanzadas (≥ 85 años)1. Es además la primera causa de cirugía valvular en adultos2. Entre los factores de riesgo, destacan la edad y el sexo (mayor incidencia en varones)3,4. Una vez que aparecen los síntomas, presenta una elevada mortalidad (hasta del 50%) en los años siguientes5,6. En nuestro país, debido al progresivo incremento de la población de mayor edad7, se prevé una importante carga de la enfermedad asociada a la estenosis aórtica8, con el consiguiente desafío asistencial.
Hasta hace 14-15 años, la única opción terapéutica era el reemplazo quirúrgico de la válvula. En los pacientes considerados como inoperables, bien por su edad o por su comorbilidad, la alternativa de tratamiento se limitaba al control sintomático. El implante percutáneo (mínimamente invasivo) de válvula aórtica (TAVI) abrió un nuevo escenario de oportunidad terapéutica, en principio para los pacientes inoperables o de riesgo elevado, luego para los de riesgo intermedio y, finalmente, para los de bajo riesgo9-13. A pesar de esto, la tasa de tratamiento con TAVI en España es significativamente inferior a la del resto de los países europeos14. Si bien en Europa son numerosas las publicaciones y los registros sobre los resultados clínicos del TAVI, en España existe poca evidencia sobre los resultados autóctonos con fuentes de titularidad pública, a pesar de haber transcurrido más de 10 años desde el primer implante en abril de 200714.
En este trabajo se presenta la evidencia de la práctica clínica real disponible en nuestro país sobre el uso de TAVI, con la descripción del perfil de los casos tratados, los resultados obtenidos en términos de mortalidad, complicaciones y estancia media hospitalaria (EmH), y se analizan los principales factores asociados, siempre desde la perspectiva del Sistema Nacional de Salud, empleando como fuente de información el Registro de Actividad de Atención Especializada (RAE-CMBD) del Ministerio de Sanidad, Consumo y Bienestar Social.
MÉTODOS
Conjunto Mínimo Básico de Datos
Este trabajo se nutre de la información recogida en el RAE-CMBD del Ministerio de Sanidad, Consumo y Bienestar Social. Incluye el detalle sobre las características demográficas de los pacientes ingresados, variables administrativas y variables clínicas relacionadas con los diagnósticos y los procedimientos, tanto del paciente como del episodio de atención recibida. Los diagnósticos y los procedimientos registrados se codifican de acuerdo con la Clasificación Internacional de Enfermedades, 9.ª edición, Modificación Clínica (CIE-9-MC) para los años 2014-2015 y la Clasificación Internacional de Enfermedades, 10.ª edición, Modificación Clínica (CIE-10-ES) para 2016 y 2017, lo que permite una mayor especificidad en los diagnósticos.
En el presente análisis se incluyeron todos los episodios registrados entre 2014 y 2017 de pacientes mayores de 50 años, con ingreso en centro público o concertado debido a la realización de los procedimientos «Sustitución endovascular de válvula aórtica» (código 35.05 de la CIE-9-MC) y «Sustitución de válvula aórtica, con tejido zooplástico, abordaje percutáneo» (código 02RF38Z de la CIE-10-ES). Se excluyeron los casos en que se realizó un procedimiento de circulación extracorpórea (código 39.61 de la CIE-9-MC y código 5A1221Z de la CIE-10-ES) por considerar que el TAVI no precisa esta técnica y, por tanto, podría ser un error de codificación del episodio. Igualmente, se eliminaron los episodios de reingreso hospitalario para finalizar la recuperación del paciente.
Para el análisis de seguridad se incluyeron las complicaciones codificadas en la CIE-9-MC en el capítulo 17, específicamente con los códigos de la categoría 996, «Complicaciones propias de ciertos procedimientos especificados», que incluye las complicaciones, no clasificadas bajo otros conceptos, en el empleo de sustitutos artificiales que implican el implante de dispositivos internos, entre otros. Por su parte, en la más reciente clasificación CIE-10-ES, este tipo de complicaciones se encuentran en la categoría T82, «Complicaciones de prótesis, implantes e injertos cardiacos y vasculares». Además, por su potencial relación con el TAVI y su gran interés desde el punto de vista clínico, se consideraron también eventos como el fallo renal agudo, el infarto agudo de miocardio, la disección de aorta, el ictus, la sepsis y el implante de marcapasos permanente (MPP).
Análisis estadístico
Se hizo un análisis descriptivo de las variables de estudio, expresando las continuas como medias y desviación estándar, y las categóricas como frecuencias absolutas y relativas. Las diferencias entre 2 grupos independientes se contrastaron con los estadísticos t de Student o U de Mann-Whitney-Wilcoxon, en función de su distribución (paramétrica o no paramétrica, respectivamente). En las variables categóricas se usó la prueba de χ2 o la prueba exacta de Fisher. Se implementaron modelos multivariados para identificar los factores asociados con el riesgo de mortalidad intrahospitalaria y complicaciones importantes (regresión logística) y EmH (regresión binomial negativa). Como variables explicativas, se exploraron variables demográficas y clínicas: edad, sexo o tasa de implantes en la comunidad autónoma donde se llevó a cabo el procedimiento, complicaciones y gravedad de cada caso, según la clasificación RAE-CMBD (estratificado, según las características del paciente, los diagnósticos y los procedimientos, en 4 niveles15,16: menor, moderado, mayor o extremo —Grupos Relacionados por el Diagnóstico [GRD] severidad—).
Para analizar posibles diferencias entre comunidades autónomas en el volumen de TAVI, se calcularon las tasas de implante estandarizadas por 100.000 habitantes (105). Se tomó como referencia la población estacional de cada región en el periodo, ajustando por grupo de edad (50-74, 75-84 y ≥ 85 años) y sexo17. La discriminación entre regiones de alto y bajo volumen se hizo mediante la categorización de las tasas de implante, y se consideraron de alto volumen aquellas con una tasa superior a la mediana nacional (37 implantes por 105 habitantes) durante el periodo considerado. Las diferencias en las características basales de los pacientes tratados en las comunidades autónomas de alto y bajo volumen se tuvieron en cuenta al ajustar los modelos multivariados.
Las variables independientes de todos los modelos de regresión logística y binomial negativa fueron revisadas por los expertos clínicos para asegurar su sentido clínico, y seleccionadas posteriormente de manera que el modelo resultante minimizara el criterio de información de Akaike18. Una vez determinado el mejor modelo en cada caso, se calcularon las odds ratios (OR) y sus intervalos de confianza del 95% (IC95%) para determinar si un determinado factor se asociaba a un mayor riesgo (OR > 1) ante un resultado particular y comparar la magnitud de varios factores.
En relación con el análisis multivariante de las complicaciones, cuando el número de casos registrados era reducido y, por tanto, la potencia estadística del contraste era limitada, se agruparon las complicaciones relevantes, siguiendo de nuevo el criterio clínico. De esta forma, se identificaron y evaluaron los factores relacionados con el riesgo de hemorragia y punción o laceración accidental (CIE-9-MC 998.11 y 998.2 | CIE-10-ES: I97.4, I97.6 y I97.5*), infarto agudo de miocardio (CIE-9-MC 410.*1 | CIE-10-ES: I21*), MPP (CIE-9-MC 37.8 | CIE-10-ES: 5A1223Z), sepsis e infecciones (CIE-9-MC 995.91, 995.92 y 998.5 | CIE-10-ES: T81.4XXA y A41*), fallo renal agudo (CIE-9-MC: 584 | CIE-10-ES: N17*) y accidente cerebrovascular (CIE-9-MC 997.02, 434 y 435 | CIE-10-ES: I97.8*0, I66, I63.3, I63.4, I63.5, G45*, I67.82).
Todos los contrastes estadísticos fueron bilaterales y las diferencias se consideraron estadísticamente significativas cuando el valor de p era < 0,05. El análisis se llevó a cabo con el programa estadístico R (versión 3.6.1).
RESULTADOS
En total se contabilizaron 5.454 pacientes a quienes se implantó percutáneamente por vía transfemoral una prótesis aórtica: 763 casos registrados en 2014, 1.171 en 2015, 1.477 en 2016 y 2.043 en 2017. El implante fue más frecuente en las mujeres (52,2%), mayoritariamente en pacientes entre 81 y 85 años, tanto en varones (37%) como en mujeres (44%), y la edad media fue de 81,12 ± 6,43 años durante todo el periodo. En conjunto, los diagnósticos más frecuentes que motivaron el ingreso de los pacientes fueron los de trastornos de la válvula aórtica (79,7%, códigos CIE-9-MC: 424.1 y CIE-10-ES: I35), insuficiencia de válvula mitral y estenosis reumática (3,1%, códigos CIE-9-MC: 396.2 y CIE-10-ES: T82.0*XA) e insuficiencia cardiaca congestiva (2,9%, códigos CIE-9-MC: 428.0 y CIE-10-ES: I08.0).
Tasa de TAVI transfemoral, mortalidad y estancia hospitalaria
El número de procedimientos de TAVI, aunque variable a lo largo de los años, creció progresivamente, con un incremento notable entre 2014 y 2017, tanto en el número de centros que llevan a cabo el procedimiento como en el total de TAVI realizados. Así, la tasa de implante nacional (por 105 habitantes) se duplicó, y la media durante el periodo de estudio fue de 33 intervenciones por 105 habitantes (tabla 1).
Tabla 1. Tasa de implante por 100.000 habitantes, estancia media hospitalaria y mortalidad intrahospitalaria por comunidad autónoma
| TI total periodo 2014-2017 | Estancia | Mortalidad | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Ajustada | 2014 | 2015 | 2016 | 2017 | Total periodo | Porcentaje registrado en periodo | ||||||||||
| Comunidad autónoma | TAVI (n) | Población estacional | Est (x 105 hab) | IC95% LI | IC95% LS | EmH | DE | EmH | DE | EmH | DE | EmH | DE | EmH | DE | |
| 1 | 945 | 2.805.282 | 37 | 34,6 | 39 | 14,8 | 11,9 | 13,2 | 12,7 | 12,1 | 10,3 | 11,7 | 11,3 | 12,7 | 11,5 | 4,2 |
| 2 | 62 | 520.240 | 11 | 8,2 | 14 | 24,6 | 34,2 | 14,6 | 9,9 | 20,8 | 20 | 12,4 | 6,4 | 16,3 | 16,9 | 1,6 |
| 3 | 238 | 486.637 | 45 | 39,5 | 51 | 9,8 | 7,6 | 10,9 | 9,2 | 11,1 | 10,3 | 8,6 | 5,9 | 10 | 8,4 | 5,5 |
| 4 | 49 | 357.975 | 16 | 11,6 | 21 | 14,5 | 9,5 | 11,7 | 10,3 | 8,2 | 3,5 | 12 | 8,9 | 11,4 | 8,4 | 6,1 |
| 5 | 112 | 699.707 | 20 | 16,3 | 24 | 17,9 | 15,3 | 20,1 | 15,7 | 16,3 | 19,5 | 23,2 | 22,7 | 20,4 | 19,5 | 2,7 |
| 6 | 204 | 232.793 | 85 | 73,5 | 97 | 12,7 | 9,6 | 11,2 | 5,7 | 10,6 | 6,5 | 9,1 | 4 | 10,7 | 6,5 | 1,5 |
| 7 | 114 | 720.493 | 14 | 11,7 | 17 | 15,7 | 9,3 | 11,2 | 8,1 | 15 | 14 | 13 | 10 | 13,4 | 10,6 | 2,6 |
| 8 | 413 | 1.067.664 | 32 | 29,0 | 35 | 12 | 6,5 | 13,9 | 14,5 | 9,7 | 7,5 | 11,8 | 9,7 | 11,6 | 9,9 | 2,9 |
| 9 | 671 | 2.656.228 | 25 | 23,3 | 27 | 12,9 | 11,7 | 14,2 | 11,8 | 15,4 | 13,5 | 13,8 | 13,7 | 14,2 | 13,2 | 3,7 |
| 10 | 251 | 1.798.755 | 15 | 13,1 | 17 | 8,6 | 5,3 | 9,3 | 7,8 | 10,4 | 9,4 | 7,2 | 7,8 | 8,9 | 8,1 | 3,6 |
| 11 | 69 | 418.558 | 15 | 12,0 | 19 | 11,4 | 6,2 | 15 | 14,6 | 12,6 | 6,8 | 9,7 | 5,2 | 11,7 | 8,4 | 7,2 |
| 12 | 673 | 1.153.586 | 50 | 46,6 | 54 | 10,6 | 9,2 | 10,2 | 10,4 | 10,5 | 11,9 | 11,1 | 9,5 | 10,7 | 10,2 | 3,7 |
| 13 | 1.126 | 2.206.886 | 53 | 49,9 | 56 | 14,8 | 16,3 | 12,6 | 17 | 12,2 | 12,8 | 10,1 | 7,9 | 11,9 | 13 | 2,9 |
| 14 | 211 | 456.332 | 49 | 42,9 | 57 | 8,2 | 7,1 | 6 | 4,9 | 6,7 | 6,2 | 7,8 | 9,9 | 7,1 | 7,5 | 3,3 |
| 15* | 91 | 236.596 | 37 | 29,4 | 45 | 11 | 7,1 | 13,6 | 12,7 | 10,9 | 7,6 | 9,9 | 8,1 | 11 | 8,7 | 5,5 |
| 16* | 225 | 890.671 | 25 | 21,5 | 28 | 13,7 | 14,8 | 9,6 | 6,1 | 11,1 | 7,2 | 10,2 | 8,2 | 10,9 | 9,2 | 3,1 |
| Nacional | 5.454 | 16.708.405 | 33 | 31,8 | 34 | 13,1 | 12,5 | 12,1 | 12,6 | 11,9 | 11,3 | 11,3 | 10,6 | 11,9 | 11,5 | 3,6 |
|
DE: desviación estándar; EmH: estancia media hospitalaria (días); IC95%: intervalo de confianza del 95%; LI: límite inferior; LS: límite superior; TAVI: implante percutáneo de válvula aórtica; TI: tasa de implante. * Debido a las particularidades en la prestación del servicio en estas regiones, la tasa de implante puede desviarse respecto a la clínica habitual en ellas. Los valores de mortalidad más altos vienen dados por resultados negativos en los primeros años (por ejemplo: en la comunidad autónoma 3 se parte en 2014 del 16,7% y se llega en 2017 al 3,3%; en la 4: del 25% en 2014 al 7,4% en 2017; en la 11: del 14,3% en 2014 al 6,7% en 2017). En todos los casos se observó una tendencia claramente positiva en la reducción de la mortalidad asociada al procedimiento. |
||||||||||||||||
La mortalidad global en todo el periodo considerado fue del 3,6%, con un claro decremento entre 2014 (4,8%) y 2017 (2,7%), a pesar de que el perfil de gravedad asignado a los pacientes se mantuvo constante en los 4 años evaluados (el 70% presentaban un grado de GRD extremo).
Respecto a la duración del ingreso asociado al procedimiento, la EmH observada en 2014 fue de 13,1 ± 12,5 días, y disminuyó de forma progresiva hasta los 11,3 ± 10,6 días en 2017, con una gran variabilidad entre comunidades autónomas (tabla 1). Cuando se eliminaron los casos extremos (definidos como aquellos con duraciones por encima de 2 desviaciones estándar de la media), la estancia media nacional fue de 8,9 ± 4,69 días y las diferencias entre comunidades autónomas disminuyeron, oscilando entre 6,07 ± 4,8 y 11,35 ± 4,31 días (tabla 1).
Complicaciones asociadas al TAVI
La tabla 2 describe las complicaciones asociadas al TAVI. Igual que en la mortalidad, se observó una disminución progresiva en la incidencia de complicaciones más relevantes desde 2014 hasta 2017. La necesidad de MPP fue del 12,2%, también con gran variabilidad de esta complicación entre comunidades autónomas.
Tabla 2. Complicaciones asociadas al TAVI
| Complicación | Total | CIE-9-MC | 2014 | 2015 | CIE-10-ES | 2016 | 2017 | |||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| n | % | n | % | n | % | n | % | n | % | |||
| Complicación mecánica prótesis válvula cardiaca | 218 | 4 | 996.02 | 56 | 7,3 | 47 | 4 | T82.0*XA | 49 | 3,3 | 66 | 3,2 |
| Otra complicación implante de prótesis válvula cardiaca | 143 | 2,6 | 996.71 | 13 | 1,7 | 27 | 2,3 | T82.8*7A, T82.9XXA | 39 | 2,6 | 64 | 3,1 |
| Disección de aorta | 15 | 0,3 | 441 | 2 | 0,3 | 3 | 0,3 | I71.0* | 3 | 0,2 | 7 | 0,3 |
| Hemorragia o infarto cerebrovascular iatrogénico | 40 | 0,7 | 997.02 | 4 | 0,5 | 9 | 0,8 | I97.8*0 | 11 | 0,7 | 16 | 0,8 |
| Oclusión de arterias cerebrales | 46 | 0,8 | 434 | 8 | 1 | 11 | 0,9 | I66, I63.3, I63.4, I63.5 | 11 | 0,7 | 16 | 0,8 |
| Isquemia cerebral transitoria | 27 | 0,5 | 435 | 3 | 0,4 | 6 | 0,5 | G45*, I67.82 | 9 | 0,6 | 9 | 0,4 |
| Infarto agudo de miocardio | 87 | 1,6 | 410.*1 | 14 | 1,8 | 14 | 1,2 | I21* | 25 | 1,7 | 34 | 1,7 |
| Implante de marcapasos permanente | 663 | 12,2 | 37.8 | 146 | 19,1 | 149 | 12,7 | 5A1223Z | 155 | 10,5 | 213 | 10,4 |
| Fallo renal agudo | 441 | 8,1 | 584 | 74 | 9,7 | 90 | 7,7 | N17* | 119 | 8,1 | 158 | 7,7 |
| Shock posoperatorio | 55 | 1 | 998 | 10 | 1,3 | 14 | 1,2 | T81.1*XA | 16 | 1,1 | 15 | 0,7 |
| Hemorragia que complica un procedimiento | 314 | 5,8 | 998.11 | 54 | 7,1 | 63 | 5,4 | I97.4*, I97.6* | 90 | 6,1 | 107 | 5,2 |
| Punción o laceración accidental durante un procedimiento | 156 | 2,9 | 998.2 | 31 | 4,1 | 45 | 3,8 | I97.5* | 36 | 2,4 | 44 | 2,2 |
| Infección posoperatoria | 45 | 0,8 | 998.5 | 11 | 1,4 | 13 | 1,1 | T81.4XXA | 12 | 0,8 | 9 | 0,4 |
| Sepsis | 28 | 0,5 | 995.91, 995.92 | 6 | 0,8 | 6 | 0,5 | A41* | 8 | 0,5 | 8 | 0,4 |
|
TAVI: implante percutáneo de válvula aórtica. Códigos (CIE-10-ES): T82.0*XA Complicación mecánica de prótesis valvular cardiaca (contacto inicial); T82.8*7A Otras complicaciones especificadas de prótesis, implantes e injertos cardiacos y vasculares (contacto inicial); T82.9XXA Complicación no especificada de prótesis, implantes e injertos cardiacos y vasculares (contacto inicial); I71.0* Disección de aorta; I97.8*0 Otras complicaciones intraoperatorias y trastornos posprocedimiento del aparato circulatorio (cirugía cardiaca); I66 Oclusión y estenosis de las arterias cerebrales; I63.3 Infarto cerebral debido a trombosis de las arterias cerebrales; I63.4 Infarto cerebral debido a embolia de las arterias cerebrales; I63.5 Infarto cerebral debido a oclusión o estenosis no especificada de las arterias cerebrales; G45 Accidentes isquémicos cerebrales transitorios y síndromes relacionados; I67.82 Isquemia cerebral; I21 Infarto agudo de miocardio; 5A1223Z Implante de marcapasos permanente; N17 Fallo renal agudo; T81.1*XA Shock después de un procedimiento (contacto inicial); I97.4* Hemorragia y hematoma intraoperatorios de órgano o estructura de aparato circulatorio que complica un procedimiento; I97.6* Hemorragia, hematoma y seroma posprocedimiento de un órgano o estructura del aparato circulatorio después de un procedimiento; I97.5* Punción y desgarro accidentales de órgano o estructura del aparato circulatorio durante un procedimiento; T81.4XXA Infección después de un procedimiento (contacto inicial); A41 Sepsis. |
||||||||||||
Factores relacionados con el riesgo de mortalidad, estancia hospitalaria y complicaciones asociadas al TAVI
En la tabla 3 se describe el perfil de los casos atendidos y los resultados de los procedimientos en las regiones de alto y bajo volumen. Las comunidades autónomas de mayor volumen trataron a pacientes más añosos (80,47 frente a 81,91; p < 0,001) y con un índice de riesgo extremo ligeramente más bajo (70,3%, en las comunidades autónomas de bajo volumen frente al 67,1% en las de alto volumen; p = 0,013). En estas comunidades autónomas también se observó en la población intervenida una menor incidencia de comorbilidad, como diabetes, hipertensión arterial, insuficiencia cardiaca, enfermedad pulmonar obstructiva crónica o tabaquismo (tabla 3).
Tabla 3. Análisis comparativo entre comunidades autónomas de alto y bajo volumen de TAVI
| Bajo volumen (n = 3.002) | Alto volumen (n = 2.452) | p | |||
|---|---|---|---|---|---|
| Características del paciente | |||||
| Edad (años); media (DE) | 80,47 | 6,48 | 81,91 | 6,29 | < 0,001* |
| Grupo de edad (años); n (%) | |||||
| 50-74 | 455 | 15,2 | 275 | 11,2 | < 0,001* |
| 75-84 | 1.749 | 58,3 | 1.228 | 50,1 | |
| ≥ 85 | 798 | 26,6 | 949 | 38,7 | |
| Sexo (% mujeres), n (%) | 1.520 | 50,6 | 1.327 | 54,1 | 0,011* |
| Nivel de gravedad, n (%) | |||||
| Menor | 13 | 0,4 | 20 | 0,8 | 0,013* |
| Moderado | 44 | 1,5 | 18 | 0,7 | |
| Mayor | 835 | 27,8 | 768 | 31,3 | |
| Extremo | 2.110 | 70,3 | 1.646 | 67,1 | |
| Diabetes mellitus; n (%) | 1.059 | 35,3 | 706 | 28,8 | < 0,001* |
| Hipercolesterolemia; n (%) | 1.365 | 45,5 | 1.070 | 43,6 | 0,185 |
| Obesidad; n (%) | 381 | 12,7 | 273 | 11,1 | 0,085 |
| Hipertensión arterial; n (%) | 1.742 | 58,0 | 1.234 | 50,3 | < 0,001* |
| Fibrilación auricular; n (%) | 1.037 | 34,5 | 904 | 36,9 | 0,079 |
| Insuficiencia cardiaca; n (%) | 611 | 20,4 | 357 | 14,6 | < 0,001* |
| EPOC; n (%) | 330 | 11,0 | 207 | 8,4 | 0,002* |
| Insuficiencia renal crónica; n (%) | 634 | 21,1 | 482 | 19,7 | 0,194* |
| Tabaquismo; n (%) | 450 | 15,0 | 283 | 11,5 | < 0,001* |
| Uso de anticoagulantes; n (%) | 511 | 17,0 | 485 | 19,8 | 0,01* |
| Resultados del procedimiento | |||||
| Fallecimiento; n (%) | 113 | 3,8 | 81 | 3,3 | 0,401 |
| Estancia hospitalaria (días); media (DE) | 12,72 | 11,82 | 10,85 | 11,08 | < 0,001* |
| Punción/laceración; n (%) | 89 | 3,0 | 67 | 2,7 | 0,667 |
| Hemorragia que complica el procedimiento; n (%) | 156 | 5,2 | 158 | 6,4 | 0,056 |
| IAM; n (%) | 56 | 1,9 | 31 | 1,3 | 0,098 |
| Implante de marcapasos permanente; n (%) | 400 | 13,3 | 263 | 10,7 | 0,004* |
| Sepsis y eventos infecciosos; n (%) | 47 | 1,6 | 21 | 0,9 | 0,026 |
| Fallo renal agudo; n (%) | 215 | 7,2 | 226 | 9,2 | 0,007 |
| Accidente cerebrovascular; n (%) | 54 | 1,8 | 41 | 1,7 | 0,801 |
|
DE: desviación estándar; EPOC: enfermedad pulmonar obstructiva crónica; IAM: infarto agudo de miocardio. * Diferencias estadísticamente significativas entre las comunidades autónomas de bajo y alto volumen. Alto volumen de implantes definido como tasa implante mayor que la mediana nacional de 37 implantes por 105 habitantes. Nivel de gravedad según la clasificación RAE-CMBD. |
|||||
Los resultados del procedimiento también variaron entre las comunidades autónomas de alto y bajo volumen: en las de alto volumen se observó una duración menor de la EmH y un menor riesgo de aparición de algunas complicaciones, como necesidad de MPP y sepsis o infecciones. Sin embargo, presentaron un riesgo mayor de fallo renal agudo en el análisis bivariante (tabla 3).
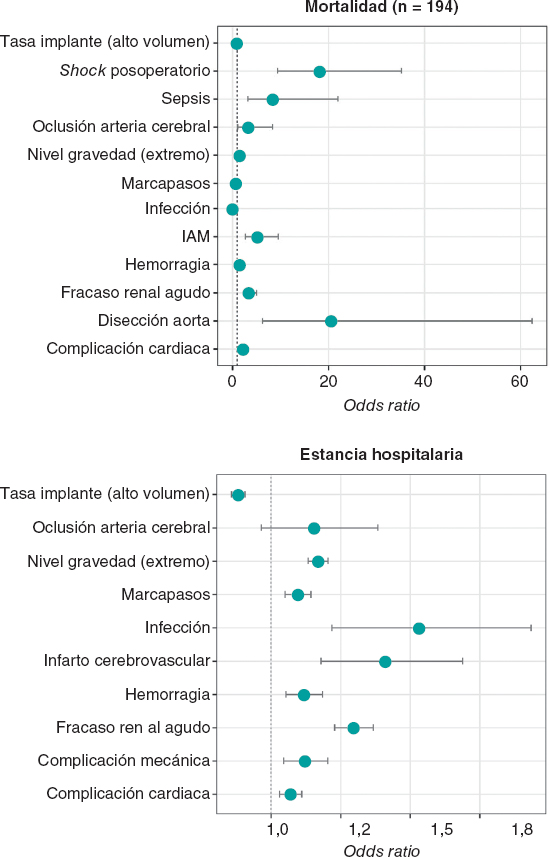
Debido a estas diferencias, la edad, el sexo y el nivel de gravedad de cada caso se consideraron en los modelos multivariantes programados para ajustar los análisis de las variables explicativas asociadas a la mortalidad hospitalaria. La figura 1 muestra que la disección de aorta (OR = 20,58; IC95%, 6,27-62,40; p < 0,01) y el shock posoperatorio (OR = 18,16; IC95%, 9,43-35,16; p < 0,01) se asociaron de manera significativa con la tasa de mortalidad tras la intervención. El peso explicativo de otras complicaciones, como el infarto agudo de miocardio, el fallo renal agudo, la oclusión arterial cerebral o las complicaciones cardiacas, fue significativamente menor. Las diferencias en mortalidad entre las comunidades autónomas de alto y bajo volumen no alcanzaron significación estadística en el conjunto del periodo analizado (figura 1).
Figura 1. Mortalidad y estancia hospitalaria registradas de acuerdo con las tasas de implante y de aparición de complicaciones en los procedimientos. Las figuras representan la influencia sobre cada complicación de las variables independientes seleccionadas en los modelos multivariados logísticos (mortalidad) o binomial negativa (estancia hospitalaria). Entre las variables candidatas siempre se consideraron el sexo, la edad, el volumen de implantes ajustado por región y el nivel de gravedad (RAE-CMBD). Los ejes en el plano de coordenadas varían debido a las magnitudes de las odds ratios presentadas. IAM: Infarto agudo de miocardio.
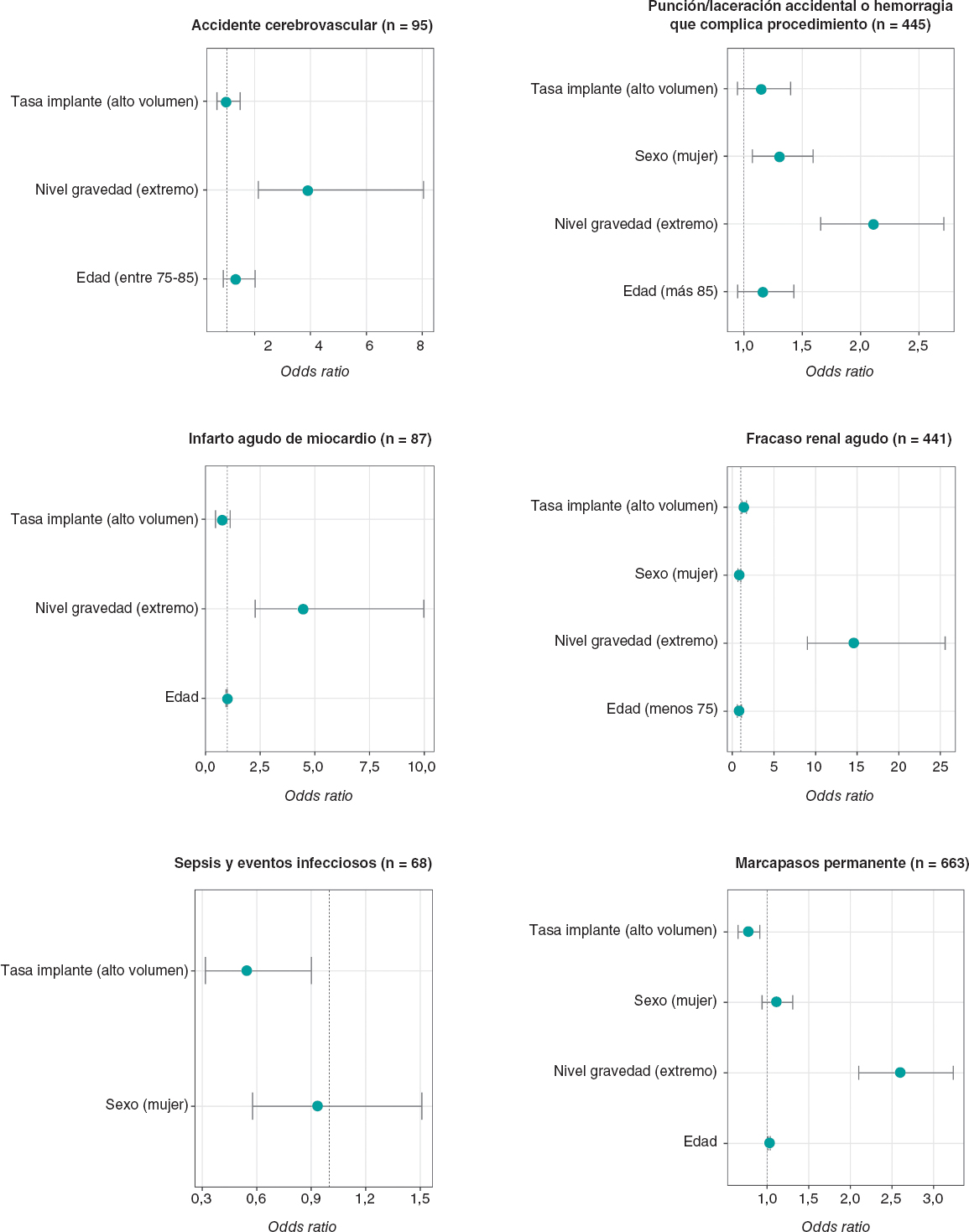
Por otra parte, la mayor gravedad de los casos y la aparición de algunas complicaciones contribuyeron a un aumento significativo de la duración de la EmH (figura 1). El grado de gravedad fue también el factor más fuertemente relacionado con la aparición de complicaciones como hemorragias y punción o laceración accidental, infarto agudo de miocardio, MPP, fallo renal agudo y accidente cerebrovascular (figura 2). En las comunidades autónomas de alto volumen, el riesgo de sepsis o infecciones y de requerir MPP fue significativamente inferior que en las de bajo volumen (OR = 0,77; IC95%, 0,65-0,91; p < 0,01, y OR = 0,54; IC95%, 0,32-0,9; p = 0.02, respectivamente). Finalmente, hay que indicar que las comunidades autónomas de alto volumen también presentaban una reducción significativa de la EmH, que era un 12% menor que en las de bajo volumen (OR = 0,88; IC95%, 0,86-0,91; p < 0,01), como se muestra en la figura 1.
Figura 2. Resultados del análisis de regresión logística sobre el riesgo de complicaciones clínicas. Las figuras representan la influencia sobre cada complicación de las variables independientes seleccionadas en los modelos multivariados (selección mediante algoritmo genético, siguiendo el criterio de información de Akaike). Entre las variables candidatas siempre se consideraron el sexo, la edad, el volumen de implantes ajustado por región y el nivel de gravedad (RAE-CMBD). Los ejes en el plano de coordenadas varían debido a las magnitudes de las odds ratios presentadas.
DISCUSIÓN
El principal hallazgo de nuestro estudio es que el implante transfemoral de una prótesis aórtica es efectivo y seguro en España. En segundo lugar, con el incremento del número de procedimientos realizados por año, y por tanto también de la experiencia obtenida, la tasa de complicaciones no mortales, así como la tasa de mortalidad (2,7% en el último año evaluado), se han ido reduciendo de manera progresiva.
Es indudable que el TAVI es un procedimiento seguro y efectivo, a juzgar también por la evidencia científica procedente de estudios clínicos12,13,19 y metanálisis20,21, y de ahí probablemente que su indicación se haya ampliado desde los pacientes inoperables a los de alto riesgo y luego a los de riesgo intermedio y bajo. El presente trabajo aporta evidencia basada en las fuentes propias del Ministerio de Sanidad, Consumo y Bienestar Social, con datos de la práctica asistencial real en nuestro país.
En España, tanto los datos del Registro Nacional de Actividad en Cardiología Intervencionista de la Sociedad Española de Cardiología, Sección de Hemodinámica y Cardiología Intervencionista22, como nuestros datos procedentes del RAE-CMBD, muestran un considerable aumento en todas las comunidades autónomas del número de casos tratados en el periodo 2014-201722. Aun así, en España la tasa de TAVI sigue siendo significativamente inferior a la de otros países14. Es importante destacar la mejora progresiva tanto de las tasas de mortalidad (reducción del 56,25% en el periodo considerado) como de las complicaciones no mortales, así como de la EmH. Y esto, a pesar de unos porcentajes elevados (en torno al 70%) de casos con gravedad extrema, según la codificación de casos en el RAE-CMBD.
Los datos no muestran diferencias importantes por sexo, a diferencia de trabajos previos que reflejaban un peor pronóstico en los varones tras el implante23. Los factores que efectivamente parecen asociados a un mayor riesgo de mortalidad son el shock posoperatorio, la sepsis, la disección de la aorta y el infarto de miocardio. En este caso, el índice de riesgo del paciente y el volumen de implante no se asocian claramente a una diferente tasa de mortalidad, lo que podría estar relacionado con la ganancia de experiencia en el procedimiento en el conjunto del país. En esta misma línea, también se ha descrito, con datos del CMBD, una mejora en la mortalidad tras la cirugía convencional de reemplazo valvular aórtico, que se situaba en 2017 en un 3,3% (3,6% en pacientes de 70-80 años y 4,3% en pacientes > 80 años)24.
La tasa de MPP encontrada fue comparable a la publicada por otros autores en nuestro país22. En este caso, la codificación de la gravedad de los casos intervenidos sí se asoció con un mayor riesgo. La necesidad de MPP tras el TAVI se ha asociado sobre todo al tipo de válvula utilizada (mayor con las autoexpandibles)25. En nuestro análisis no es posible diferenciar el tipo de válvula por no recogerse en la base de datos del RAE-CMBD. Tanto la necesidad de MPP posimplante como la aparición de procesos infecciosos y sepsis secundarios a la intervención se asociaron inversamente con un mayor volumen de intervenciones. Esta asociación entre volumen de procedimientos y reducción de las complicaciones ha sido muy señalada en diferentes contextos, como tras la revascularización coronaria26 o tras la cirugía convencional de reemplazo valvular aórtico24, entre otros.
Además de los beneficios clínicos, el TAVI se ha consolidado como una alternativa coste-eficaz respecto a la cirugía de sustitución valvular aórtica convencional. Que los resultados del procedimiento de TAVI hayan sido progresivamente más seguros y efectivos, con menor morbimortalidad y una reducción de la EmH, es probable que esté relacionado con el incremento de la experiencia de los cirujanos, con el volumen de procedimientos realizados y con los avances técnicos y tecnológicos acontecidos24.
El aumento de la población anciana en nuestro país y la expansión de las indicaciones son causa del aumento considerable en el número de pacientes candidatos a TAVI1,11. En este sentido, es importante sumar nuevas evidencias que contribuyan a la evaluación en términos de resultados de salud de estos procedimientos27, con el objeto de garantizar unos servicios de calidad homogénea en nuestro Sistema Nacional de Salud y dotar de mecanismos de evaluación a las líneas estratégicas definidas en salud cardiovascular28, ya que el TAVI se ha consolidado como una alternativa coste-eficaz respecto a la cirugía aórtica convencional29,30.
Limitaciones
El uso de una base de datos administrativa para obtener información tiene claras ventajas e inconvenientes. Por una parte, permite contar con gran parte del censo nacional, por su carácter de obligatoriedad de registro, y una alta estandarización de los datos, lo que es uno de los principales puntos fuertes27. Sin embargo, teniendo en cuenta que el RAE-CMBD es un registro administrativo cuyas variables clínicas se basan en el informe de alta, la exhaustividad de la codificación y las posibles inconsistencias entre los centros en cuanto a la aplicación de los códigos podrían influir en la precisión de los resultados. No obstante, como el periodo analizado es de 4 años, se podría inferir que no habría cambios sustanciales en la codificación que pudieran variar en gran medi- da los resultados. Aun así, se debe hacer constar que es posible que los códigos específicos de complicaciones de la CIE-9-MC no recojan todas las complicaciones que pueden acontecer duran- te un procedimiento de TAVI. A pesar de ello, en este trabajo se analizan todas las complicaciones de mayor significancia desde el punto de vista clínico para el análisis de los resultados de los procedimientos. Por otro lado, en el análisis que se ha llevado a cabo se han considerado los datos del RAE CMBD hasta 2017, los más recientes hasta el momento, y sería conveniente analizar los datos de los últimos años para ver la evolución de los resultados. Cabría esperar que estos fueran incluso mejores, considerando el aumento del volumen de intervenciones transcatéter, la mayor experiencia de los cirujanos y la mejora de la tecnología disponi- ble. Esta cuestión debe ser objeto de estudio en publicaciones posteriores.
Además de lo anterior, se debe indicar que la información que se recoge en este análisis proviene de procedimientos registrados en centros públicos o privados con actividad concertada, y por tanto pueden existir discrepancias con los datos publicados por el Registro Nacional de Actividad en Cardiología Intervencionista de la Sociedad Española de Cardiología, Sección de Hemodinámica y Cardiología Intervencionista, en términos absolutos22. Aun así, ambas fuentes apenas difieren en el porcentaje de casos que requieren MPP (diferencia total del 2% en 2016 y del 0,1% en 2017, siendo mayor el dato del Registro de la Sección de Hemodinámica y Cardiología Intervencionista).
Una última limitación del análisis reside en que solo se puede analizar el episodio en que se hace el implante y no hay posibilidad de obtener el resultado a largo plazo, lo cual aportaría información de gran valor para evaluar todo el alcance y el coste de la atención sanitaria. No obstante, los resultados del presente trabajo son de interés en la medida en que aportan información clave sobre aspectos que permiten abundar en la generación de argumentos de gestión asistencial de calidad.
CONCLUSIONES
El TAVI es un procedimiento seguro y efectivo, cuya realización está aumentando, aunque en España existe una gran variabilidad entre comunidades autónomas y hospitales. Es una intervención que se realiza fundamentalmente en pacientes mayores de 75 años, con unas cifras de morbimortalidad bajas y absolutamente comparables a las de la cirugía convencional, y que han ido disminuyendo en los 4 años analizados (2014-2017), con una reducción también progresiva de la EmH tras la intervención, en especial en las comunidades autónomas con mayor tasa de implante.
FINANCIACIÓN
El presente trabajo ha sido financiado por Edwards Lifesciences S.L.
CONTRIBUCIÓN DE LOS AUTORES
M. Álvarez-Bartolomé y J. Cuervo llevaron a cabo la validación de los datos y el tratamiento estadístico. Todos los autores contribuyeron al diseño del estudio, revisaron críticamente el manuscrito, dieron la aprobación final y se hacen responsables de todos los aspectos del trabajo, asegurando su integridad y exactitud.
CONFLICTO DE INTERESES
B. Martí-Sánchez es miembro de Edwards Lifesciences S.L., que ha financiado el presente trabajo. J. Cuervo es miembro de Axentiva Solutions, que recibió honorarios de consultoría científica de Edwards Lifesciences S.L.
¿QUÉ SE SABE DEL TEMA?
- La tasa de TAVI por vía transfemoral es significativamente menor en España que en el resto de los países europeos. Además, tras haber transcurrido más de una década desde el primer implante, aún hay poca evidencia sobre el uso y los resultados de este procedimiento en nuestro país.
¿QUÉ APORTA DE NUEVO?
- El estudio aporta información sólida y precisa sobre la seguridad, la efectividad y los resultados del uso de TAVI en la población española.
- Existe variabilidad interterritorial en el uso de TAVI, pero los resultados muestran una tasa de morbimortalidad baja y una disminución progresiva en la estancia media hospitalaria en el periodo considerado.
- La incidencia de complicaciones y la mortalidad parecen disminuir a medida que aumenta el número de procedimientos TAVI realizados.
- Una mayor tasa de implante se relacionó con una menor estancia hospitalaria y con menos riesgo de implante de marcapasos permanente y de infecciones durante el ingreso.
BIBLIOGRAFÍA
1. Ferreira-González I, Pinar-Sopena J, Ribera A, et al. Prevalence of calcific aortic valve disease in the elderly and associated risk factors:a population-based study in a Mediterranean area. Eur J Preventive Cardiol. 2013;20:1022-1030.
2. Salinas P, Moreno R, Calvo L, et al. Seguimiento a largo plazo tras implante percutáneo de válvula aórtica por estenosis aórtica grave. Rev Esp Cardiol. 2016;69:37-44.
3. Izquierdo-Gómez MM, Hernández-Betancor I, García-Niebla J, Marí-López B, Laynez-Cerdeña I, Lacalzada-Almeida J. Valve Calcification in Aortic Stenosis:Etiology and Diagnostic Imaging Techniques. BioMed Res Int. 2017;5178:1-12.
4. Stewart BF, Siscovick D, Lind BK, et al. Clinical Factors Associated With Calcific Aortic Valve Disease fn1fn1This study was supported in part by Contracts NO1-HC85079 through HC-850086 from the National Heart, Lung, and Blood Institute, National Institutes of Health, Bethesda, Maryland. J Am Coll Cardiol. 1997;29:630-634.
5. Ramaraj R, Sorrell VL. Degenerative aortic stenosis. BMJ. 2008;336:550-555.
6. Otto CM, Lind BK, Kitzman DW, Gersh BJ, Siscovick DS. Association of Aortic-Valve Sclerosis with Cardiovascular Mortality and Morbidity in the Elderly. N Engl J Med. 1999;341:142-147.
7. INE. Nota de prensa 20 de octubre de 2016. Proyecciones de Población 2016-2066. 2016;2066. Disponible en: https://www.ine.es/prensa/np994.pdf. Consultado 29 Jun 2020.
8. Thaden JJ, Nkomo VT, Enriquez-Sarano M. The Global Burden of Aortic Stenosis. Prog Cardiovasc Dis. 2014;56:565-571.
9. Leon MB, Smith CR, Mack M, et al. Transcatheter Aortic-Valve Implantation for Aortic Stenosis in Patients Who Cannot Undergo Surgery. N Engl J Med. 2010;363:1597-1607.
10. Duncan A, Ludman P, Banya W, et al. Long-term outcomes after transcatheter aortic valve replacement in high-risk patients with severe aortic stenosis:the U.K. Transcatheter Aortic Valve Implantation Registry. JACC Cardiovasc Interv. 2015;8:645-653.
11. Baumgartner H, Falk V, Bax JJ, et al. 2017 ESC/EACTS Guidelines for the management of valvular heart disease. Eur Heart J. 2017;38:2739-2791.
12. Mack MJ, Leon MB, Thourani VH, et al. Transcatheter Aortic-Valve Replacement with a Balloon-Expandable Valve in Low-Risk Patients. N Engl J Med. 2019;380:1695-1705.
13. Popma JJ, Deeb GM, Yakubov SJ, et al. Transcatheter Aortic-Valve Replacement with a Self-Expanding Valve in Low-Risk Patients. N Engl J Med. 2019;380:1706-1715.
14. Biagioni C, Tirado-Conte G, Nombela-Franco L, et al. Situación actual del implante transcatéter de válvula aórtica en España. Rev Esp Cardiol. 2017;70(Supl 1):6-8.
15. Ministerio de Sanidad, Consumo y Bienestar Social. Grupos Relacionados de Diagnóstico APR-GRD V32. Norma Estatal 2017;2019. Disponible en: https://www.mscbs.gob.es/estadEstudios/estadisticas/docs/CMBD/Nota_difus_Norma_Estatal_2017.pdf. Consultado 3 Jul 2020.
16. Subdirección General de Información Sanitaria e Innovación. Ministerio de Sanidad, Servicios Sociales e Igualdad. Norma Estatal RAE-CMBD 2016 –NotaInformativa;2018. Disponible en: https://www.mscbs.gob.es/estadEstudios/estadisticas/docs/CMBD/Nota_difus_Norma_Estatal_2016.pdf. Consultado 29 Jun 2020.
17. Instituto Nacional de Estadística. Tablas de Mortalidad por Año, Comunidades y Ciudades Autónomas, Sexo, Edad y Funciones. Disponible en: https://www.ine.es/jaxiT3/Tabla.htm?t=27154&L=0. Consultado 29 Jun 2020.
18. Calcagno V, de Mazancourt C. glmulti:An R Package for Easy Automated Model Selection with (Generalized) Linear Models. J Statistical Software. 2010;34:1-29.
19. Castrodeza J, Amat-Santos IJ, Blanco M, et al. Propensity score matched comparison of transcatheter aortic valve implantation versus conventional surgery in intermediate and low risk aortic stenosis patients:A hint of real-world. Cardiol J. 2016;23:541-551.
20. Sardar P, Kundu A, Chatterjee S, et al. Transcatheter versus surgical aortic valve replacement in intermediate-risk patients:Evidence from a meta-analysis. Catheter Cardiovasc Interv. 2017;90:504-515.
21. Khan SU, Lone AN, Saleem MA, Kaluski E. Transcatheter vs surgical aortic-valve replacement in low- to intermediate-surgical-risk candidates:A meta-analysis and systematic review. Clin Cardiol. 2017;40:974-981.
22. Sección de Hemodinámica y Cardiología Intervencionista. Sociedad Española de Cardiología. Registro Nacional de Actividad en Cardiología Intervencionista 2017;2018. Disponible en: https://www.hemodinamica.com/wp-content/uploads/2018/11/PRESENTACIO%CC%81N-DEFINITIVA-REGISTRO-2017.pdf. Consultado 27 Jun 2020.
23. European Society of Cardiology. Women less likely to die after TAVI than men. Published online 2013. Disponible en: https://www.escardio.org/The-ESC/Press-Office/Press-releases/Women-less-likely-to-die-after-TAVI-than-men. Consultado 29 Jun 2020.
24. Carnero-Alcázar M, Maroto-Castellanos LC, Hernández-Vaquero D, et al. Isolated aortic valve replacement in Spain:national trends in risks, valve types, and mortality from 1998 to 2017. Rev Esp Cardiol. 2021;74:700-707.
25. Deharo P, Bisson A, Herbert J, et al. Impact of Sapien 3 Balloon-Expandable Versus Evolut R Self-Expandable Transcatheter Aortic Valve Implantation in Patients With Aortic Stenosis:Data From a Nationwide Analysis. Circulation. 2020;141:260-268.
26. Goicolea Ruigómez FJ, Elola FJ, Durante-López A, Fernández Pérez C, Bernal JL, Macaya C. Coronary artery bypass grafting in Spain. Influence of procedural volume on outcomes. Rev Esp Cardiol. 2020;73:488-494.
27. Íñiguez Romo A, Bertomeu Martínez V, Rodríguez Padial L, et al. The RECALCAR Project. Healthcare in the Cardiology Units of the Spanish National Health System, 2011 to 2014. Rev Esp Cardiol. 2017;70:567-575.
28. Ministerio de Sanidad. El Ministerio de Sanidad traslada a las CCAA el borrador de la Estrategia en Salud Cardiovascular del SNS. Disponible en: https://www.mscbs.gob.es/gabinete/notasPrensa.do?id=4993. Consultado 20 Oct 2020.
29. Ribera A, Slof J, Andrea R, et al. Transfemoral transcatheter aortic valve replacement compared with surgical replacement in patients with severe aortic stenosis and comparable risk:Cost-utility and its determinants. International J Cardiol. 2015;182:321-328.
30. Baron SJ, Wang K, House JA, et al. Cost-Effectiveness of Transcatheter Versus Surgical Aortic Valve Replacement in Patients With Severe Aortic Stenosis at Intermediate Risk. Circulation. 2019;139:877-888.