RESUMEN
Introducción y objetivos: Los avances en la tecnología de implante percutáneo de válvula aórtica (TAVI) han dado lugar a mejores resultados y menos complicaciones en comparación con las generaciones anteriores. Se estudió la incidencia y los determinantes de las fugas periprotésicas (FPP) con las válvulas Evolut PRO y SAPIEN 3, así como otros resultados periprocedimiento y hospitalarios.
Métodos: Se seleccionó aleatoriamente a 110 pacientes consecutivos con estenosis aórtica grave programados para TAVI transfemoral para recibir una válvula SAPIEN 3 (n = 59) o una Evolut PRO (n = 51). Las dimensiones anulares se determinaron mediante el dimensionamiento del balón guiado por ecocardiografía transesofágica. Tras el procedimiento y durante la hospitalización se evaluaron los siguientes objetivos: FPV, defectos de conducción, embolización de la válvula, necesidad de una segunda válvula, rotura anular, accidente vascular cerebral, complicaciones vasculares, daño renal agudo y mortalidad intrahospitalaria. También se estudiaron los posibles determinantes anatómicos de la FPV.
Resultados: No hubo diferencias basales relevantes entre los 2 grupos en cuanto a las características clínicas y ecocardiográficas. Las complicaciones intrahospitalarias fueron comparables entre ambos tipos de válvulas, excepto una incidencia significativamente mayor de FPV (de grado II o superior) inmediata tras el procedimiento y al alta con las válvulas Evolut PRO en comparación con las SAPIEN 3 (19,6 frente a 6,8% y 5,9 frente a 1,7%, respectivamente). De las variables anatómicas, el ángulo entre el tracto de salida del ventrículo izquierdo y la aorta ascendente, la angulación aórtica y la calcificación tuvieron un impacto significativo en la FPV en las válvulas Evolut PRO. El ángulo entre el tracto de salida del ventrículo izquierdo y la aorta ascendente tuvo una correlación negativa con la profundidad de implantación en las válvulas Evolut PRO, pero no en las válvulas SAPIEN 3.
Conclusiones: Ambas válvulas demostraron resultados favorables comparables, excepto por una incidencia significativamente mayor de FPV en los pacientes con válvulas Evolut PRO.
Palabras clave: Estenosis aórtica. Implante percutáneo de válvula aórtica. TAVI. SAPIEN 3. Evolut PRO.
ABSTRACT
Introduction and objectives: Advances made in transcatheter aortic valve implantation (TAVI) valvular technology have resulted in better outcomes and fewer complications compared with older generations. We studied the rate and determinants of paravalvular leak (PVL) using Evolut PRO vs SAPIEN 3 valves as well as other perioperative and in-hospital outcomes.
Methods: A total of 110 consecutive patients with severe aortic stenosis scheduled for transfemoral TAVI were randomly selected to receive the SAPIEN 3 (N = 59) or the Evolut PRO valve (N = 51). Annular dimensions were determined by transesophageal echocardiography guided balloon sizing. The following postoperative and in-hospital endpoints were assessed: PVL, conduction defects, valve embolization, need for a second valve, annular rupture, stroke, vascular complications, acute kidney injury, and in-hospital mortality. We also studied the possible anatomical determinants of PVL.
Results: There were no relevant baseline differences between the 2 groups regarding clinical and echocardiographic characteristics. In-hospital complications were comparable between both valves apart from a significantly higher rate of immediate postoperative PVL and at discharge (≥ grade II) between the Evolut PRO and the SAPIEN 3 valves (19.6% vs 6.8%) and (5.9% vs 1.7%), respectively. Of the anatomical variables described, the left ventricular outflow tract/ascending aorta angle, aortic angulation, and calcification had a significant impact on PVL in the Evolut PRO valves. The left ventricular outflow tract/ascending aorta angle revealed a negative correlation with implantation depth in the Evolut PRO valves but not in the SAPIEN 3 ones.
Conclusions: Both valves demonstrated favorable comparable outcomes except for a significantly higher rate of PVL in patients implanted with Evolut PRO valves.
Keywords: Aortic stenosis. Transcatheter aortic valve implantation. TAVI. SAPIEN 3. Evolut PRO.
Abreviaturas
EA: estenosis aórtica; FPP: fuga periprotésica; TAVI: implante percutáneo de válvula aórtica. VARC: Valve Academic Research Consortium.
INTRODUCCIÓN
Durante la pasada década, la válvula autoexpandible CoreValve (Medtronic Ltd, Estados Unidos) y la prótesis balón expandible SAPIEN (Edwards Lifesciences Ltd, Estados Unidos) han sido las más empleadas para realizar implantes transcatéter de válvula aórtica (TAVI)1.
Son pocos los estudios que han comparado ambas válvulas, Evolut PRO (Medtronic Ldt, Estados Unidos) y SAPIEN 3 (Edwards Lifesciences Ltd, Estados Unidos), como el SMART, que estudió anillos aórticos pequeños2, y el registro de pacientes no seleccionado ALSTER-TAVI3. No obstante, no hay ensayos clínicos aleatorizados comparativos. Por eso se diseñó este estudio aleatorizado para realizar una comparativa directa entre ambas válvulas incluyendo datos de la intervención y resultados intrahospitalarios, sobre todo, de la fuga periprotésica (FPP). Aunque las prótesis valvulares cardiacas percutáneas empleadas en este estudio no son las válvulas de última generación de las familias CoreValve y SAPIEN (en la actualidad, la Evolut-Pro Plus y la SAPIEN Ultra), este es el primer estudio clínico aleatorizado que compara una válvula autoexpandible con falda externa de sellado y una válvula de balón autoexpandible (también con falda externa).
MÉTODOS
Población del estudio
Se aleatorizó a un total de 110 pacientes consecutivos con estenosis aórtica sintomática grave aptos para el TAVI a recibir la válvula Evolut PRO (51 pacientes) o la SAPIEN 3 (59 pacientes) en el Duisburg Heart Center de Duisburg (Alemania) entre diciembre de 2019 y mayo de 2020. Se incluyó a todos los pacientes tratados de TAVI por estenosis aórtica grave con la SAPIEN 3 y la Evolut PRO mediante abordaje femoral. Se excluyó a los pacientes tratados de TAVI con otros tipos de dispositivos tales como válvulas aórticas implantadas transapicalmente, válvulas aórticas bicúspides e implantes de prótesis valvulares biológicas de «válvula dentro de otra válvula». Todas las intervenciones se realizaron tras obtener el consentimiento informado, por escrito, de los pacientes de acuerdo con los estándares éticos del comité nacional de investigación.
Aspectos de la intervención
El TAVI se realizó bajo anestesia local y sedación consciente. Se empleó en todos los pacientes. Se realizaron incisiones femorales en todos los pacientes. Las dimensiones anulares se obtuvieron mediante dimensionamiento del balón guiado por ecocardiografía transesofágica durante la intervención. Gracias a esta técnica se pudieron medir los anillos mediante ecocardiografía transesofágica para luego elegir un balón del mismo tamaño que el anillo. El inflado del balón, tanto durante la estimulación cardiaca rápida como durante la angiografía aórtica, se realizó teniendo 3 posibilidades distintas en mente: a) el balón llena el anillo por completo sin fuga periprotésica ni cintura, lo cual es indicativo de que el tamaño del anillo y del balón es el mismo; b) la fuga parabalón es indicativa de que el anillo es entre 1 y 2 mm más grande que el tamaño del balón; c) la cintura del balón es indicativa de que el anillo es entre 1 y 2 mm más pequeño que el tamaño del balón4. El tipo de válvula (SAPIEN 3 o Evolut PRO) se seleccionó aleatoriamente (empleando el método de aleatorización simple; los casos de los lunes con la Evolut y los de los jueves con la SAPIEN). El tamaño de la válvula estuvo en función de las dimensiones anulares sugeridas por los fabricantes. Según los diámetros anular y valvular finalmente seleccionados, se calculó el llamado índice de cobertura5.
Objetivos
Nuestros objetivos primarios fueron la FPP, la mortalidad intrahospitalaria y el índice de implante de marcapasos permanente (IMP). Los objetivos secundarios fueron la embolización de la válvula, la necesidad de una segunda prótesis, la rotura o disección aórticas, el accidente cerebrovascular o el accidente isquémico transitorio, las complicaciones vasculares mayores y el daño renal agudo. Los objetivos se definieron según las definiciones del Valve Academic Research Consortium-2 (VARC-2)6.
Valoración de la FPP
La FPP inmediata se valoró semicuantitativamente con la clasificación de Seller 7: 0/4 (ausente), 1/4 (leve), 2/4 (moderada), 3/4 (moderada a grave) y 4/4 (grave)7. Los gradientes de presión transvalvular se obtuvieron invasivamente empleando el método de retirada automática. Se calculó, asimismo, la incidencia de la insuficiencia aórtica (IA)8.
En presencia de FPP significativa ≥ grado II, caso de ser necesario, se posdilató con los balones VACS III o NUCLEUS (NuMED, Estados Unidos) o se empleó una segunda válvula. Al alta hospitalaria se empleó la ETT para cuantificar el grado de FPP según los principales criterios del VARC-29.
Valoración de los factores anatómicos asociados posiblemente a la FPP
Se tomaron las siguientes mediciones empleando software de Philips (Philips Medical, Países Bajos): el ángulo del tracto de salida del ventrículo izquierdo/aorta ascendente (TSVI/AA) se definió como el ángulo descrito entre el eje de los primeros 4 cm de la aorta ascendente (superficie de contacto con la parte superior de la prótesis) y el eje del TSVI (zona de anclaje) indicado por una línea perpendicular al plano del anillo valvular aórtico)10.
El ángulo de angulación aórtica (AngA) se definió como el ángulo descrito entre el plano horizontal y el plano del anillo aórtico11. Se clasificó en < 48° y ≥ 48°12.
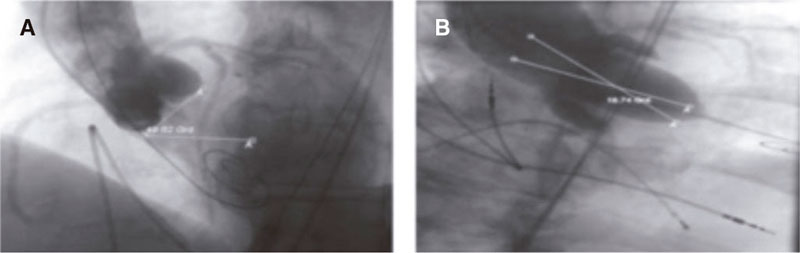
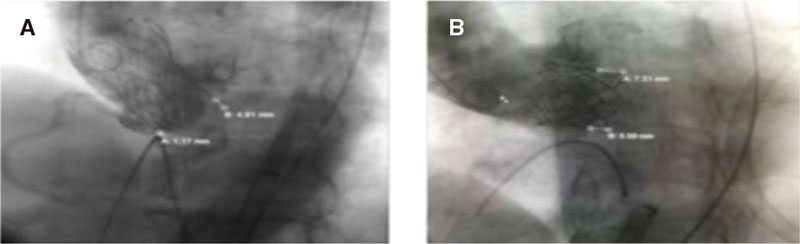
Ambos ángulos se midieron en la posición fluoroscópica óptima de despliegue con las 3 cúspides coronarias en el mismo plano (figura 1). La profundidad de implantación de la válvula se midió en la posición de despliegue en la fluoroscopia desde el margen anular aórtico nativo del lado de la cúspide no coronaria (CNC) y cúspide coronaria izquierda hasta el borde proximal de la válvula desplegada en el lado correspondiente13 (figura 2). A nivel fluoroscópico, la calcificación de la raíz aórtica fue prácticamente inexistente, leve (puntos calcificados aislados pequeños), moderada (muchos puntos calcificados grandes) o grave (calcificación extensa)13. También se registró la presencia o ausencia del TSVI, así como la calcificación anual mitral.
Figura 1. Medición de los diferentes ángulos. AngA: angulación aórtica (49,62º). B: ángulo TSVI/AA (18,74º). AA: aorta ascendente; TSVI: tracto de salida del ventrículo izquierdo.
Figura 2. Medición de la profundidad de implantación de las válvulas Evolut PRO. A: [A = 1,17 mm asociada a la CNC y B = 4,91 mm asociada a la CCI] y SAPIEN 3. B: [A = 5,65 mm asociada a la CNC y B = 7,31 mm asociada a la CCI]. Adviértase la mayor profundidad de implantación asociada a la CNC por el mayor ángulo TSVI/AA de la Evolut PRO (A) a diferencia de la SAPIEN 3 (B). AA: aorta ascendente; CCI, cúspide coronaria izquierda; CNC, cúspide no coronaria; TSVI: tracto de salida del ventrículo izquierdo.
Análisis estadístico
Los datos se recopilaron y analizaron con el paquete de software estadístico SPSS (Statistical Software Package for the Social Sciences, versión 20, IBM, Estados Unidos). Los datos continuos se expresaron con media ± DE o mediana (rango). Los datos nominales se expresaron como frecuencia (porcentaje). Para comparar los datos nominales y continuos se emplearon la prueba de la X2 y la prueba de la t de Student, respectivamente. Se usó el coeficiente de correlación Pearson para la correlación existente entre la profundidad de implantación con los ángulos TSVI y AngA según el tipo de válvula empleada. El nivel de confianza se mantuvo en el 95%, razón por la cual los valores p < 0,05 se consideraron estadísticamente significativos. Se realizó un análisis de regresión logística univariable para los predictores de FPP significativa. El análisis ROC se realizó para el valor óptimo de corte del ángulo TSVI/AA para el resultado de FPP significativa.
En lo que al tamaño de la muestra se refiere, asumiendo una proporción de 1:1 en las asignaciones del tratamiento y un índice estimado del objetivo primario compuesto (FPP, mortalidad intrahospitalaria e índice de implante de marcapasos) del 8% en cada grupo, calculamos que harían falta 52 pacientes en cada grupo para que el estudio alcanzase un potencial estadístico del 80% a un nivel alfa unilateral del 0,05.
RESULTADOS
Características basales
Se aleatorizó a 110 pacientes consecutivos con estenosis aórtica sintomática grave aptos para el TAVI a recibir las válvulas Evolut PRO (51 pacientes) o SAPIEN 3 (59 pacientes). No hubo cruzamientos entre uno y otro grupo del estudio. Las características clínicas basales fueron parecidas entre los 2 tipos de válvulas salvo por un índice de masa corporal que fue mucho mayor en los pacientes del grupo SAPIEN 3 y un bloqueo basal de rama derecha, también mucho mayor en el grupo SAPIEN (tabla 1).
Tabla 1. Características de los pacientes asociadas al tipo de válvula implantada
| Tipo de válvula | p | ||
|---|---|---|---|
| Evolut PRO (n = 51) |
SAPIEN 3 (n = 59) |
||
| Edad (años) | 82,6 ± 6,4 | 81,2 ± 5,8 | 0,22 |
| Sexo | 0,39 | ||
| Hombre | 54,9 | 59,3 | |
| Mujer | 45,1 | 40,7 | |
| Índice de masa corporal (kg/m2) | 26,4± 4,7 | 28,7 ± 4,7 | 0,01a |
| Área de superficie corporal (m2) | 1,9 ± 0,4 | 1,9 ± 0,2 | 0,08 |
| Enfermedad arterial periférica | 11,8 | 6,8 | 0,28 |
| Hipertensión | 76,5 | 83,1 | 0,26 |
| Diabetes mellitus | 29,4 | 37,3 | 0,25 |
| Cardiopatía isquémica | 62,0 | 45,8 | 0,06 |
| Revascularización previa (ICP/CABG) | 41,2 | 37,3 | 0,53 |
| Antecedentes de accidente cerebrovascular | 5,9 | 5,1 | 0,58 |
| Marcapasos previo | 9,8 | 6,8 | 0,40 |
| Enfermedad torácica crónica | 9,8 | 23,7 | 0,31 |
| Clase NYHA | 0,09 | ||
| II | 13,7 | 15,3 | |
| III | 86,3 | 78,0 | |
| IV | 0,0 | 6,8 | |
| Puntuación STS | 3,8 ± 2,6 | 3,5 ± 2,2 | 0,51 |
| Clase STS (%) | 0,65 | ||
| Baja (< 4%) | 58,8 | 66,1 | |
| Intermedia (del 4 al 8%) | 35,3 | 27,1 | |
| Alta (> 8%) | 5,9 | 6,8 | |
| Hallazgos ECG | 0,95 | ||
| Ritmos sinusales | 43,1 | 45,8 | |
| Estimulación o pacing | 7,8 | 6,8 | |
| Fibrilación auricular | 49,0 | 47,5 | |
| Trastornos en la conducción cardiaca preoperatorios totales | 19,6 | 22,0 | 0,47 |
| BRD basal | 0,0 | 16,9 | 0,001b |
|
A menos que se indique lo contrario, los datos expresan n (%). Los trastornos en la conducción cardiaca preoperatorios incluyeron bloqueo auriculoventricular, retraso de la conducción intraventricular, hemibloqueo anterior izquierdo, bloqueo de rama izquierda y BRD. BRD: bloqueo de rama derecha; CABG: cirugía de revascularización coronaria; EPOC: enfermedad pulmonar obstructive crónica; ICP: intervención coronaria percutánea; SAOS: síndrome de apnea obstructive del sueño; STS: escala de riesgo de la Society of Thoracic Surgery. |
|||
Hallazgos ecocardiográficos y fluoroscópicos
Los hallazgos basales ecocardiográficos y fluoroscópicos de los 2 grupos fueron parecidos (tabla 2).
Tabla 2. Datos ecocardiográficos y fluoroscópicos entre los diferentes grupos de estudio
| Tipo de válvula | p | ||
|---|---|---|---|
| Evolut PRO (n = 51) |
SAPIEN 3 (n = 59) |
||
| GP medio (mmHg) | 42,3 ± 7,7 | 42,8 ± 9,9 | 0,78 |
| GP máximo (mmHg) | 68,5 ± 10,5 | 67,3 ± 12,0 | 0,56 |
| Área valvular aórtica (mm) | 0,9 ± 0,7 | 0,9 ± 0,2 | 0,46 |
| Fracción de eyección (%) | |||
| Fracción de eyección | 48,4 ± 11,7 | 50,9 ± 11,7 | 0,25 0,76 |
| Conservada (> 50%) | 62,7 | 67,8 | |
| Levemente deteriorada (del 40 al 50%) | 17,6 | 15,3 | |
| Moderadamente deteriorada (del 30 al 40%) | 9,8 | 11,9 | |
| Gravemente deteriorada (< 30%) | 9,8 | 5,1 | |
| Gradiente / flujo (%) | |||
| AFAG | 74,5 | 71,2 | 0,91 |
| BFBG/FE deteriorada | 19,6 | 22,0 | |
| BFBG/FE conservada | 5,9 | 6,8 | |
| Mediciones aórticas (mediante ETE) | |||
| Área valvular aórtica (mm) | 0,7 ± 0,1 | 0,7 ± 0,2 | 0,22 |
| Anillo (mm) | 23,8 ± 2,1 | 24,5 ± 1,9 | 0,07 |
| TSVI (mm) | 21,1 ± 2,1 | 21,6 ± 2,4 | 0,26 |
| Seno de Valsalva (mm) | 30,7 ± 3,6 | 31,2 ± 3,8 | 0,45 |
| Unión sinotubular (mm) | 25,9 ± 3,1 | 26,4 ± 3,5 | 0,37 |
| Aorta ascendente (mm) | 33,3 ± 5,9 | 33,7 ± 4,6 | 0,68 |
| Distancia UST/TSVI (mm) | 20,1 ± 10,5 | 19,4 ±3,2 | 0,62 |
| Calcificación de la raíz aórtica (%) | |||
| Calcificación anular | 0,49 | ||
| Leve | 66,7 | 71,2 | |
| Moderada | 27,5 | 27,1 | |
| Grave | 5,9 | 1,7 | |
| Calcificación sinotubular | 5,9 | 8,5 | 0,44 |
| Calcificación del TSVI | 19,6 | 11,9 | 0,19 |
| Calcificación anular mitral | 15,7 | 18,6 | 0,44 |
| Ángulo TSVI/AA (°) | 13,7 ± 5,1 | 13,9 ± 5,2 | 0,84 |
| Ángulo AngA (°) | 46,5 ± 9,4 | 47,5 ± 12,1 | 0,62 |
|
A: aorta; AngA: angulación aórtica; AFAG: alto flujo-alto gradiente; BFBG: bajo flujo-bajo gradiente; ETE: ecocardiografía transesofágica; FE: fracción de eyección; GP: gradiente de presión; TSVI: tracto de salida del ventrículo izquierdo; UST: unión sinotubular. |
|||
Datos de la intervención según el tipo de válvula empleada
Se observaron pocas diferencias en los datos de la intervención en lo relativo al diseño de la válvula y al tamaño de la vaina tal y como se muestra en la tabla 3.
Tabla 3. Datos de la intervención asociados a cada tipo de válvula
| Tipo de válvula | p | ||
|---|---|---|---|
| Evolut PRO (n = 51) |
SAPIEN 3 (n = 59) |
||
| Vía de acceso (%) | 0,51 | ||
| Femoral derecha | 60,8 | 59,3 | |
| Femoral izquierda | 39,2 | 40,7 | |
| Anillo mediante ETE (mm) | 23,8 ± 2,1 | 24,5 ± 1,9 | 0,07 |
| Tamaño del balón (mm) | 22,5 ± 1,9 | 22,6 ± 1,9 | 0,63 |
| Dimensionamiento del balón (mm) | 23,4 ± 1,7 | 23,6 ± 1,9 | 0,44 |
| Tamaño de la válvula (%) | |||
| 23 | 0,0 | 30,5 | |
| 26 | 43,1 | 45,8 | |
| 29 | 56,9 | 23,7 | |
| Tamaño de la vaina (Fr) | 16,0 | 14,5 ± 0,9 | < 0,001 |
| Diámetro exterior de la vaina (mm) | 7,3 ± 0,1 | 6,2 ± 0,3 | < 0,001 |
| Diámetro de la arteria femoral (mm) | 7,9 ±1,1 | 8,2 ± 0,9 | 0,20 |
| Coeficiente vaina a arteria femoral | 0,9 ± 0,1 | 0,8 ± 0,1 | < 0,001 |
| Índice de cobertura (%) | |||
| ETE | 16,4 ± 5,6 | 5,2 ± 4,2 | < 0,001 |
| Balón | 18,3± 3,3 | 8,9 ± 3,3 | < 0,001 |
| Gradiente presión protésico medio | 9,8 | 12,2 | 0,01 |
| Incidencia de IA (%) | 28,4 ± 7,8 | 30,7 ± 7,4 | 0,11 |
| Profundidad de implantación (mm) | |||
| CCI | 5,8 ± 2,3 | 4,2 ± 1,7 | < 0,001 |
| CNC | 6,3 ± 2,5 | 5,27 ± 1,7 | 0,01 |
| Cantidad de contraste (ml) | 145,5 ± 48,8 | 128,6 ± 33,2 | 0,03 |
| Radiación (mGy) | 4944,4 ± 2294,8 | 4557,8 ± 3133,9 | 0,46 |
|
CCI: cúspide coronaria izquierda; CNC: cúspide no coronaria; ETE, ecocardiografía transesofágica; IA: insuficiencia aórtica. |
|||
Resultados según el tipo de válvula empleada
Sí se observó una diferencia significativa en la FPP (tanto inmediata como al alta hospitalaria) y, consecuentemente, más posdilatación con balón en el grupo Evolute que en el SAPIEN 3. El uso de cantidades mucho mayores contraste con las válvulas Evolut PRO explicaría el mayor daño renal agudo descrito en este grupo comparado con el SAPIEN. Los resultados fueron favorables a la válvula SAPIEN 3 con independencia de los objetivos de accidente cerebrovascular o mortalidad intrahospitalaria. No obstante, no se observó ninguna diferencia significativa. Los índices de éxito del dispositivo (ausencia de FPP significativa [≥ grado II] al alta hospitalaria, necesidad de implantar una segunda válvula, embolización de la prótesis, rendimiento de la prótesis valvular y mortalidad) fueron del 86 y 98% con las válvulas Evolut PRO y SAPIEN 3, respectivamente; p = 0,01 (tabla 4).
Tabla 4. Resultados intrahospitalarios en pacientes tratados con la válvula Evolut PRO frente a la SAPIEN 3
| Tipo de válvula | p | ||
|---|---|---|---|
| Evolut PRO (n = 51) |
SAPIEN 3 (n = 59) |
||
| FPP inmediata | 0,01 | ||
| Sin rastro | 19 (37,3) | 46 (78) | |
| Grado I | 22 (43,1) | 9 (15,2) | |
| ≥ grado II | 10 (19,6) | 4 (6,8) | |
| Posdilatación con balón | 8 (15,7) | 3 (5,1) | 0,35 |
| FPP al alta | 0,01 | ||
| Sin rastro | 26 (50,9) | 49 (83,1) | |
| Grado I | 22 (43,1) | 9 (15,3) | |
| Grado II | 2 (3,9) | 1 (1,7) | |
| Grado III | 1 (2) | 0 | |
| Grado IV | 0 | 0 | |
| Trastornos de la conducción cardiaca globales de nueva aparición | 9 (17,6) | 10 (16,9) | 0,56 |
| BRI de nueva aparición | 4 (7,8) | 4 (6,7) | 0,40 |
| Implante posoperatorio de marcapasos | 4 (7,8) | 3 (5,1) | 0,25 |
| Complicaciones vasculares | 0,66 | ||
| Complicaciones vasculares mayores | 2 (3,9) | 2 (3,4) | |
| Complicaciones vasculares menores | 4 (7,9) | 3 (5,1) | |
| Complicaciones hemorrágicas | 0 | 0 | |
| Daño renal agudo* | 3 (5,9) | 2 (3,4) | 0,28 |
| Accidente cerebrovascular | 1 (2) | 0 | 0,46 |
| Embolización de la válvula | 1 (2) | 0 | 0,46 |
| Necesidad de una segunda válvula | 2 (3,9) | 0 | 0,30 |
| Incidencia de mortalidad intrahospitalaria | 2 (3,9) | 0 | 0,30 |
|
Los datos expresan n (%). FPP: fuga periprotésica. |
|||
Impacto de los factores anatómicos en la FPP
La calcificación y el ángulo TSVI/AA influyeron más en la FPP de la válvula Evolut PRO que en la de la SAPIEN 3. El ángulo TSVI/AA se clasificó según el valor de corte para el objetivo de FPP significativa ≥ grado II obtenido a partir de la curva receiver operating characteristic (ROC): valor de corte = 11º, sensibilidad del 80% y especificidad del 35,8%, área bajo la curva (0,57; intervalo de confianza del 95%, 0,474-0,666; p = 0,37.) Por otro lado, no se observó una relación estrecha ni significativa entre el ángulo AngA y la FPP en ninguno de los 2 grupos (tabla 5).
Tabla 5. Relación entre los factores anatómicos y la FPP en pacientes tratados con las válvulas Evolut PRO o SAPIEN 3
| Válvula Evolut PRO (n = 51) | Válvula SAPIEN 3 (n = 59) | pa | pb | pc | |||
|---|---|---|---|---|---|---|---|
| < FPP leve | ≥ FPP leve | < FPP leve | ≥ FPP leve | ||||
| Número | 37,3 | 62,7 | 77,9 | 22,0 | 0,010 | ||
| Calcificación anular | 0,03 | 0,2 | |||||
| Leve | 31,4 | 35,3 | 59,3 | 11,9 | 0,001 | ||
| Moderada | 5,9 | 21,6 | 16,9 | 10,2 | 0,024 | ||
| Grave | 0,0 | 5,9 | 1,7 | 0,0 | 0,046 | ||
| Calcificación del TSVI | 1,7 | 17,6 | 3,4 | 8,5 | 0,04 | 0,001 | 0,323 |
| Calcificación anular mitral | 0,0 | 15,7 | 15,3 | 3,4 | 0,001 | 0,2 | 0,035 |
| Ángulo TSVI/AAa | 0,01 | 0,001 | |||||
| < 11° | 17,6 | 15,7 | 25,4 | 1,7 | 0,02 | ||
| ≥ 11° | 19,6 | 47,1 | 52,5 | 20,3 | 0,03 | ||
| Ángulo AngA (%) | 0,78 | 0,34 | |||||
| < 48º | 23,5 | 37,2 | 45,8 | 15,2 | 0,03 | ||
| > 48º | 13,7 | 25,5 | 32,2 | 6,8 | 0,01 | ||
| AA: aorta ascendente; AngA: angulación aórtica; TSVI: tracto de salida del ventrículo izquierdo. Un ángulo TSVI/AA del 11º es el valor de corte para la incidencia de FPP detectado por la curva ROC. Los datos expresan porcentaje (%). a Valor p dentro del grupo Evolut PRO. b Valor p dentro del grupo SAPIEN 3. c Valor p en base a la puntuación de la X2 entre los 2 grupos. |
|||||||
La tabla 6 revela el análisis univariado de predictores de FPP ≥ grado II inmediatamente después de la intervención FPP. Tal y como quedó demostrado, la calcificación valvular moderada y grave, la calcificación del TSVI y el ángulo TSVI/AA contribuyen a la FPP significativamente.
Tabla 6. Análisis univariado de predictores de FPP posoperatoria inmediata significativa (grado ≥ 2)
| Variable | Univariado | |
|---|---|---|
| OR (IC95%) | p | |
| Calcificación grave | 35,000 (3,138-390,431) | 0,004 |
| Calcificación del TSVI | 10,921 (3,208-37,174) | < 0,001 |
| Ángulo TSVI/AA | 1,047 (0,940-1,165) | 0,003 |
| AngA | 1,016 (0,967-1,067) | 0,524 |
| Tipo de válvula (Evolut PRO) | 2,750 (0,872-8,669) | 0,084 |
| Índice de cobertura según ETE | 1,099 (1,018-1,188) | 0,016 |
| Índice de cobertura según dimensionamiento del balón | 1,108 (1,001-1,226) | 0,049 |
| Profundidad de implantación asociada a la CCI | 1,199 (0,953-1,510) | 0,122 |
| Profundidad de implantación asociada a la CCD | 1,167 (0,914-1,489) | 0,215 |
|
Los valores p < 0,05 se consideraron significativos a nivel estadístico. AA: aorta ascendente; AngA: angulación aórtica; CCD: cúspide coronaria derecha; CCI: cúspide coronaria izquierda; ETE: ecocardiografía transesofágica; FPP: fuga periprotésica; IA: insuficiencia aórtica; IC95%: intervalo de confianza del 95%; TSVI: tracto de salida del ventrículo izquierdo. |
||
Impacto de los ángulos TSVI/AA y AngA en la profundidad de implantación
Se observó una correlación significativamente negativa entre la profundidad de implantación de la válvula Evolut PRO en la CNC y los ángulos TSVI/AA (r = -0.38; p = 0,01), correlación que no se observó con la válvula SAPIEN 3 (tabla 7).
Tabla 7. Correlación de la profundidad de implantación (en las 2 válvulas) con los ángulos TSVI/AA y AngA
| Tipo de válvula | ||||
|---|---|---|---|---|
| Evolut PRO | SAPIEN 3 | |||
| CCI | CNC | CCI | CNC | |
| Ángulo TSVI/AA (°) | -0,23 (0,09) | -0,38 (0,01) | 0,09 (0,46) | 0,16 (0,21) |
| Ángulo AngA (°) | 0,13 (0,33) | 0,06 (0,65) | 0,02 (0,87) | 0,06 (0,61) |
|
Los valores r y p se refieren, respectivamente, a la fortaleza de la correlación y a la significación de la misma. Los valores p < 0,05 fueron significativos a nivel estadístico. AA: aorta ascendente; AngA: angulación aórtica; CCI: cúspide coronaria izquierda; CNC: cúspide no coronaria; TSVI: tracto de salida del ventrículo izquierdo. |
||||
DISCUSIÓN
En este estudio, se hicieron 2 importantes hallazgos. En primer lugar, el implante de la válvula Evolut PRO se asoció a un mayor riesgo de FPP significativa comparada con la SAPIEN 3. En segundo lugar, el índice de IMP fue el mismo en los 2 grupos. Por lo demás, las 2 válvulas tuvieron resultados similares.
Reducir la FPP supone un reto importante a la hora de realizar el TAVI puesto que se asocia a peores resultados, sobre todo, al emplear estos dispositivos, en la actualidad, en pacientes de menor riesgo14.
Una comparativa aleatorizada entre las válvulas CoreValve y SAPIEN XT realizada en el estudio CHOICE reveló una incidencia más baja de FPP de moderada a grave en el grupo SAPIEN XT15. En el estudio SOLVE-TAVI se describió la no inferioridad de las 2 válvulas (SAPIEN 3 y Evolut R) en el objetivo compuesto primario de eficacia (muerte, accidente cerebrovascular, insuficiencia periprotésica y nuevo implante de marcapasos)16. En la actualidad, los primeros resultados obtenidos con las válvulas SAPIEN 3 Ultra y Evolut PRO+ han sido favorables17.
En nuestro estudio, la FPP significativa (≥ grado II) fue más habitual en los pacientes que recibieron la Evolut PRO que en los que recibieron la SAPIEN 3 (9,6 frente al 6,8%, respectivamente). Enríquez-Rodríguez et al. describieron una incidencia más baja (2,5%) de FPP de moderada a grave con las válvulas SAPIEN 3 debido, posiblemente, a la presencia del manguito de sellado externo18.
Es obvio que los factores anatómicos contribuyen a la ocurrencia de la FPP. Se observó que un mayor ángulo TSVI/AA estuvo asociado a una incidencia más alta de FPP, sobre todo, en la válvula Evolut PRO. Sherif et al. demostraron que el riesgo de FPP aumenta cuanto mayores son los ángulos TSVI/AA10. También se observó que el ángulo TSVI/AA influye en la profundidad de implantación asociada a la CNC con la Evolut PRO, no así con la SAPIEN 3. No es, pues, de extrañar que la profundidad de implantación influya en la incidencia de la FPP.
Sherif et al. fueron los primeros en describir la relación que existe entre ángulos AngA más grandes y la FPP posoperatoria en las válvulas autoexpandibles10. Posteriormente, un estudio retrospectivo realizado por Abramowitz et al. describió un mayor índice de complicaciones (tales como FPP posoperatoria) en pacientes con aortas horizontales (definidas por AngA ≥ 48º observados en la TC cardiaca) tratados con válvulas autoexpandibles11. Se pudo observar cómo los ángulos AngA influían en la FPP de pacientes que recibieron válvulas Evolut PRO aunque ángulos fueran < 48º, no observándose ninguna otra diferencia significativa en la incidencia de FPP para ángulos AngA < 48º o ≥ 48º.
En este estudio también se observó a 6 pacientes con ángulos AngA ≤ 30º (3 pacientes con la válvula Evolut PRO y otros 3 con la SAPIEN 3). Todos quedaron libres de FPP inmediatamente después de desplegar la válvula. Se podría especular con la posibilidad de los ángulos AngA ≤ 30º son los que mejor funcionan al implantar la Evolut PRO, aunque lo cierto es que, con una muestra de este tamaño, no se pueden extraer conclusiones definitivas.
En nuestro estudio, los índices de éxito del dispositivo determinados por la ausencia de FPP significativa (≥ grado II) al alta hospitalaria, la necesidad de implantar una segunda válvula, la embolización de la prótesis valvular, el rendimiento de la misma y la mortalidad según la definición del VARC9 fueron del 86 y 98% con las válvulas Evolut PRO y SAPIEN 3, respectivamente. Asimismo, Li et. al confirmaron un índice de éxito del dispositivo parecido tanto con la SAPIEN 3 como con la Evolut R (94 y 96%, respectivamente)19.
Se hallaron índices similares de trastornos de la conducción cardiaca posoperatorios e IMP tanto en la Evolut PRO como en la SAPIEN 3 (del 7,8 y 5,1%, respectivamente). Popma et al.20 y Vlastra et al.21 describieron índices más bajos de IMP con prótesis balón expandible de nueva generación que con válvulas autoexpandibles de nueva generación. Los índices parecidos de trastornos de la conducción e IMP descritos con una y otra válvula en nuestro estudio probablemente se debieron a una menor profundidad de implantación de las válvulas Evolut PRO.
Li et al. describieron índices más altos de posdilatación de hasta el 30% con la válvula Evolut R que con la SAPIEN 3.19 No obstante, esto es algo que no detectamos en nuestro estudio (15,7 y 5,1%, respectivamente; p = 0,35) probablemente por el correcto posicionamiento de la Evolut PRO y predilatación rutinaria de todos nuestros casos.
En este estudio, la mortalidad intrahospitalaria fue parecida en los 2 grupos valvulares. Li et al. también aseguraron que la mortalidad no se asoció al tipo de válvula implantada19. El estudio CHOICE también mostró un índice de mortalidad parecido al de las válvulas de antigua generación (CoreValve y SAPIEN XT)15.
La incidencia de los accidentes cerebrovasculares fue parecida tanto con la Evolut PRO como con la SAPIEN 3 aunque menor que la descrita en dispositivos de antigua generación15,19,22,23. La experiencia de los operadores y las mejoras experimentadas por los sistemas de liberación probablemente sean la razón del menor riesgo de complicaciones tromboembólicas descrito.
Con independencia del tipo de válvula empleado, parece que el daño renal agudo fue algo más habitual en nuestro estudio (5,9 y 3,5% para la Evolut PRO y la SAPIEN 3, respectivamente) que lo descrito anteriormente. Husser et al.24 describieron una incidencia del 2,7% en las válvulas SAPIEN 3 mientras que Kodali et al.25 hablan de incidencias cercanas al 1,7%. No obstante, los estudios multicéntricos grandes suelen tener criterios de inclusión más estrictos, razón por la cual la función renal basal de los pacientes incluidos fue mejor19.
A pesar de que los coeficientes vaina a arteria femoral de la Evolut PRO fueron mayores, el índice de hemorragias o complicaciones vasculares fue parecido al de la SAPIEN 3. Li et al.19 y Panchal et al.26 describieron resultados similares.
Limitaciones
Este fue un estudio de un único centro con una muestra de pequeño tamaño y un potencial estadístico limitado. Como en nuestro estudio no se realizaron tomografías computarizadas de forma rutinaria no se obtuvo información específica sobre la anatomía de la raíz aórtica ni se realizaron ajustes en base a las dimensiones anulares o al grado/distribución de la calcificación anular aórtica. Por otro lado, las mediciones angiográficas de los ángulos TSVI/AA y AngA podrían no ser exactas. No obstante, esto podría haber ayudado a excluir el sesgo de selección de algunos operadores que son reacios a usar válvulas autoexpandibles en presencia de calcificaciones mayores o angulaciones graves.
El seguimiento se limitó a la duración de la estancia hospitalaria (de media, 1 semana). No obstante, parece razonable pues nos centramos en los aspectos de la intervención. Además, en otros estudios similares, los resultados intrahospitalarios y del seguimiento a 30 días fueron bastante parecidos.
CONCLUSIONES
Este estudio aleatorizado arrojó resultados de la intervención e intrahospitalarios parecidos entre las válvulas Evolut PRO y SAPIEN 3 salvo por una incidencia mucho mayor de FPP asociada a las válvulas Evolut PRO. La FPP descrita se asoció al ángulo TSVI/AA en el grupo Evolut PRO, lo cual podría haber influido negativamente en la profundidad de implantación de este tipo de válvula.
FINANCIACIÓN
Ninguna.
CONTRIBUCIÓN DE LOS AUTORES
Idea y diseño: H. M. Elnaggar, M. S. Mahmoud, W. Schoels y Y. T. Kishk. Apoyo administrativo: W. Schoels, M. Kullmer y M. Dia. Provisión de materiales del estudio o pacientes: M. S. Mahmoud, M. Algowhary y H. M. Elnaggar. Recopilación y organización de datos: M. S. Mahmoud, M. Kullmer y M. Dia. Análisis e interpretación de los datos: M. S. Mahmoud, Y. T. Kishk, M. Algowhary y H. M. Elnaggar. Redacción del manuscrito y aprobación final: todos los autores.
CONFLICTOS DE INTERÉS
Ninguno.
¿QUÉ SE SABE DEL TEMA?
- Tanto las válvulas autoexpandibles (Evolut platform) como las prótesis balón expandible (serie SAPIEN) son los dispositivos TAVI más empleados.
- Los resultados obtenidos entre las 2 válvulas son parecidos, salvo un relativo aumento de la FPP y los trastornos en la conducción cardiaca con la válvula Evolut.
- También se plantean ciertos retos anatómicos durante el despliegue de las válvulas autoexpandibles como, por ejemplo, la angulación aórtica grave (aorta horizontal).
- No existe ningún ensayo clínico aleatorizado prospectivo que compare las válvulas Evolut PRO (válvula autoexpandible con falda externa de sellado) y SAPIEN 3.
¿QUÉ APORTA DE NUEVO?
- Se trata del primer ensayo clínico aleatorizado y prospectivo en realizar una comparativa entre las válvulas Evolut PRO (válvula autoexpandible con falda externa de sellado) y SAPIEN 3.
- Este estudio demostró resultados favorables parecidos entre ambas válvulas con independencia de una FPP mucho mayor en el grupo Evolut PRO.
- También en nuestro estudio, la angulación TSVI/AA y AngA influyeron en la FPP del grupo Evolut PRO frente al SAPIEN 3. No obstante, la angulación AngA no influyó en la FPP en ninguno de los 2 grupos
- El ángulo TSVI/AA se asoció negativamente a la profundidad de implantación en el caso de la válvula Evolut PRO sin ningún efecto sobre la SAPIEN 3, lo cual podría haber influido en el desarrollo de la FPP del grupo Evolut PRO.
BIBLIOGRAFÍA
1. Athappan G, Patvardhan E, Tuzcu EM, et al. Incidence, predictors, and outcomes of aortic regurgitation after transcatheter aortic valve replacement: meta-analysis and systematic review of literature. J Am Coll Cardiol. 2013;61:1585-1595.
2. Herrmann HC, Abdel-Wahab M, Attizzani GF, et al, Rationale and design of the SMall Annuli Randomized to Evolut or SAPIEN Trial (SMART Trial). Am Heart J. 2022;243:92-102.
3. Paitazoglou C, Meincke F, Thorsten Hanke M, et al. The ALSTER-TAVI All-Comers Registry: Procedural and 1-Year Clinical Outcomes of Balloon-Expandable vs Self-Expanding Contemporary TAVI Valves. J Invasive Cardiol. 2021;33:E356-E364.
4. Mahmoud MS, Kishk YT, Algowhary M, et al. Balloon Sizing for Transcatheter Aortic Valve Implantation Using 3 rd Generation Valves, Does It Still Work? Int Med J. 2021;28:604-609.
5. Détaint D, Lepage L, Himbert D, et al. Determinants of significant paravalvular regurgitation after transcatheter aortic valve implantation: impact of device and annulus discongruence. JACC Cardiovasc Interv. 2009;2:821-827.
6. Wang J, Yu W, Jin Q, et al. Risk factors for post-TAVI bleeding according to the VARC-2 bleeding definition and effect of the bleeding on short-term mortality: a meta-analysis. Can J Cardiol. 2017;33:525-534.
7. Sellers RD, Levy MJ, Amplatz K, Lillehei CW. Left retrograde cardioangiography in acquired cardiac disease: Technic, indications and interpretations in 700 cases. Am J Cardiol. 1964;14:437-447.
8. Sinning JM, Hammerstingl C, Vasa-Nicotera M, et al. Aortic regurgitation index defines severity of peri-prosthetic regurgitation and predicts outcome in patients after transcatheter aortic valve implantation. J Am Col Cardiol. 2012;59:1134-1141.
9. Kappetein AP, Head SJ, Généreux P, et al. Updated standardized endpoint definitions for transcatheter aortic valve implantation: the Valve Academic Research Consortium-2 consensus document. J Thorac Cardiovasc Surg. 2013;145:6-23.
10. Sherif MA, Abdel-Wahab M, Stöcker B, et al. Anatomic and procedural predictors of paravalvular aortic regurgitation after implantation of the Medtronic CoreValve bioprosthesis. J Am Col Cardiol. 2010;56:1623-1629.
11. Abramowitz Y, Maeno Y, Chakravarty T, et al., Aortic angulation attenuates procedural success following self-expandable but not balloon-expandable TAVR. JACC Cardiovasc Imaging. 2016;9:964-972.
12. Di Stefano D, Colombo A, Mangieri A, et al. Impact of horizontal aorta on procedural and clinical outcomes in second-generation transcatheter aortic valve implantation. EuroIntervention. 2019;15:e749-e756.
13. Mostafa AE, Richardt G, and Abdel-Wahab M. Clinical utility of a predictive model for paravalvular aortic regurgitation after transcatheter aortic valve implantation with a self-expandable prosthesis. Egypt Heart J. 2017;69:253-259.
14. Reardon MJ, Van Mieghem NM, Popma JJ, et al. Surgical or transcatheter aortic-valve replacement in intermediate-risk patients. N Engl J Med. 2017;376:1321-1331.
15. Abdel-Wahab M, Mehilli J, Frerker C, et al. Comparison of balloon-expandable vs self-expandable valves in patients undergoing transcatheter aortic valve replacement: the CHOICE randomized clinical trial. JAMA Cardiol. 2014;311:1503-1514.
16. Webb J, Wood D, Sathananthan J, Landes U. Balloon-expandable or self-expandable transcatheter heart valves. Which are best? Eur Heart J. 2020;41:1900-1902.
17. Jiang T, Hasan SM, Faluk M, Patel J. Evolution of Transcatheter Aortic Valve Replacement| Review of Literature. Curr Probl Cardiol. 2021;46:100600.
18. Enríquez-Rodríguez E, Amat-Santos IJ Jiménez-Quevedo P, et al. Comparison of the hemodynamic performance of the balloon-expandable SAPIEN 3 versus self-expandable Evolut R transcatheter valve: a case-matched study. Rev Esp Cardiol. 2018;71:735-742.
19. Li Y-M, Tsauo J-Y, Liao Y-B, Zhao Z-G, Chen M. Comparison of Third Generation Balloon-Expandable Edwards Sapien 3 Versus Self-Expandable Evolut R in Transcatheter Aortic Valve Implantation: A Meta-Analysis. Ann Palliat Med. 2020;9:700-708.
20. Popma JJ, Reardon MJ, Khabbaz K, et al. Early clinical outcomes after transcatheter aortic valve replacement using a novel self-expanding bioprosthesis in patients with severe aortic stenosis who are suboptimal for surgery: results of the Evolut R US study. JACC Cardiovasc Interv. 2017;10:268-275.
21. Vlastra W, Chandrasekhar J, Muñoz-Garcia AJ, et al. Comparison of balloon-expandable vs. self-expandable valves in patients undergoing transfemoral transcatheter aortic valve implantation: from the CENTER-collaboration. Eur Heart J. 2019;40:456-465.
22. Smith CR, Leon MB, Mack MJ, et al. Transcatheter versus surgical aortic-valve replacement in high-risk patients. N Engl J Med. 2011;364:2187-2198.
23. Adams DH, Popma JJ, Reardon MJ, et al. Transcatheter aortic-valve replacement with a self-expanding prosthesis. N Engl J Med. 2014;370:1790-1798.
24. Husser O, W.-K. Kim, et al. Multicenter comparison of novel self-expanding versus balloon-expandable transcatheter heart valves. JACC Cardiovasc Interv. 2017;10:2078-2087.
25. Kodali S, Thourani VH, White J, et al. Early clinical and echocardiographic outcomes after SAPIEN 3 transcatheter aortic valve replacement in inoperable, high-risk and intermediate-risk patients with aortic stenosis. Eur Heart J. 2016;37:2252-2262.
26. Panchal HB, Barry N, Bhatheja S, Albalbissi K, Mukherjee D, Paul T. Mortality and major adverse cardiovascular events after transcatheter aortic valve replacement using Edwards valve versus CoreValve: A meta-analysis. Cardiovasc Revasc Med. 2016;17:24-33.