A lo largo del último medio siglo, hemos sido testigos de un avance notable en el campo del intervencionismo coronario percutáneo (ICP), pasando de los primeros casos de angioplastia tradicional con balón simple a los stents convencionales y, de forma más destacada, al uso extendido de los stents farmacoactivos (SFA). La llegada de los SFA redujo significativamente las tasas de reestenosis al proporcionar no solo un andamiaje mecánico sino también la liberación sostenida de un fármaco antiproliferativo (al principio, taxanos para, después, pasar a derivados de la rapamicina). Teniendo en cuenta su carácter permanente y estático, estos implantes metálicos no están exentos de limitaciones tales como una posible cicatrización tardía, inflamación crónica, inhibición del remodelado vascular positivo y necesidad de tratamiento antitrombótico largo1,2. Por eso surgió el concepto de andamiajes vasculares bioabsorbibles, con la promesa de proporcionar un soporte temporal que «no dejara nada atrás». No obstante, esta promesa inicial se vio comprometida por la trombosis tardía del andamiaje y la alta tasa de fracaso de la lesión diana3. Paralelamente, se desarrollaron balones farmacoactivos (BFA) como alternativa «sin metal». Estos dispositivos administraban un fármaco antiproliferativo a la pared vascular sin dejar un implante permanente al tiempo que preservaban la anatomía y función vasculares y posibilitaban el remodelado adaptativo. En la actualidad, los BFA son la opción más viable en las intervenciones coronarias percutáneas (ICP) para el tratamiento de la reestenosis intrastent (RIS) y, por ende, de la enfermedad nativa de vasos pequeños. No obstante, el papel de los BFA en las coronarias nativas de mayor calibre sigue siendo objeto de debate, dada la limitada evidencia disponible procedente de ensayos clínicos aleatorizados (ECA) pequeños y con seguimientos relativamente cortos4.
En este contexto, en un reciente artículo publicado en REC: Interventional Cardiology, Sorolla Romero et al. presentan un riguroso y oportuno metanálisis de ECA que compara BFA y SFA en pacientes con enfermedad coronaria de vaso nativo grande (PROSPERO CRD42024602012)5. Se incluyó a un total de 2.961 pacientes (n = 1.476 con BFA y n = 1.485 con SFA) procedentes de 7 ECA publicados entre 2016 y 2024. Comparados con los SFA, los BFA se asociaron a un riesgo similar del objetivo primario de revascularización de la lesión diana, mortalidad total y cardiovascular, infarto de miocardio y eventos cardiovasculares adversos mayores y a un riesgo más de 2 veces superior de revascularización del vaso diana. En lo que respecta a los resultados angiográficos, los BFA se asociaron a una menor pérdida luminal tardía, pero también a un menor diámetro luminal mínimo en el seguimiento. A la luz de estos resultados, el presente documento pretende aportar perspectivas actuales y futuras sobre el papel de los BFA en el tratamiento de la enfermedad coronaria de vaso nativo grande.
CARACTERÍSTICAS DE LA LESIÓN
El tipo de lesiones incluidas en los ECA analizados es un factor clave para la validez externa de los hallazgos, y a continuación se señalan consideraciones relevantes:
- – En los 7 ECA, se excluyó sistemáticamente a aquellos pacientes con alta complejidad clínica y anatómica (tabla 1)6-12. Se debe mencionar que no se valoró a pacientes con enfermedad coronaria extensa (como, por ejemplo, lesiones largas o múltiples, enfermedad de 3 vasos o necesidad de varios dispositivos), calcificación grave, enfermedad de tronco común izquierdo u oclusiones coronarias totales crónica. Entre los criterios de exclusión también figuraban características que, paradójicamente, podrían representar escenarios favorables para la angioplastia con BFA, tales como la necesidad de hemodiálisis, lesiones bifurcadas con requerimiento de tratamiento de ambas ramas o tortuosidad coronaria grave. Esta selección contrasta con recientes estudios observacionales sobre BFA para el tratamiento de la enfermedad coronaria de vaso nativo grande, que han examinado escenarios más complejos donde los SFA podrían ser menos efectivos, difíciles de implantar a nivel técnico o poco aconsejables para evitar largos segmentos de stents o mútiples solapamientos (figura 1)13-15.
- – También destaca el grado de variabilidad entre los distintos estudios, especialmente si se tiene en cuenta la desproporcionada contribución de algunos ECA. Tal y como bien apuntan los autores, el estudio REC-CAGEFREE I7 por sí solo representa aproximadamente el 75% de toda la población de pacientes y todos cada uno de los análisis de exclusión ofrecen resultados distintos. Además, los periodos de inclusión abarcan 8 años (2014-2022), lo cual introduce posibles variaciones en las técnicas intervencionistas, la tecnología de los dispositivos y la farmacoterapia adyuvante. Tanto los intervalos de predicción como las medidas de heterogeneidad observadas avalan esta consideración.
- – Se debe reconocer la variabilidad clínica en la definición de enfermedad coronaria de vaso nativo grande. Este metanálisis aplicó un valor de corte ≥ 2,5 mm para la definición de grandes vasos, que se sitúa en el límite inferior de lo que muchos considerarían gran calibre. En diferentes estudios incluidos, los pacientes fueron elegibles con independencia del diámetro de referencia del vaso tratado y algunos ECA permitieron lesiones en vasos de tan solo 2,0 mm (tabla 1).
Tabla 1. Características clínicas, angiográficas e intervencionista que excluyeron pacientes en cada estudio incluido en el metanálisis
| Características | Nishiyama et al.6 (SCC) N = 60 |
REC-CAGEFREE I7 (45% SCC; 55% SCA) N = 2.271 |
Yu et al.8 (11% SCC; 89% SCA) N = 170 |
REVELATION9 (IAMCEST) N = 120 |
Wang et al.10 (IAMCEST) N = 184 |
Gobi´c et al.11 (IAMCEST) N = 75 |
Hao et al.12 (IAMCEST) N = 80 |
|---|---|---|---|---|---|---|---|
| Edad, años | > 70 | > 80 | |||||
| Hemodiálisis | X | ||||||
| IM previo | X | ||||||
| ICP/CABG previa | Dentro de 6 meses | Dentro de 6 meses | |||||
| Tamaño del vaso, mm | < 2,25 o > 4,0 | < 2,0 o > 4,0 | < 2,5 o > 4,0 | ||||
| Longitud de la lesión, mm | ≥ 25 | > 30 | |||||
| N.º de SFA o BFA / longitud total del SFA o BFA, mm | ≥ 3 / > 60 | ||||||
| EC extensa | ≥ 3 lesiones/vasos | X | |||||
| Calcificación grave o aterectomía | X | X | X | X | |||
| Tronco común izquierdo | X | X | |||||
| OTC | X | X | |||||
| Bifurcación con requerimiento de tratamiento en ambas ramas | X | ||||||
| Injertos | X | ||||||
| Tortuosidad coronaria grave | X | ||||||
|
BFA: balón farmacoactivo; CABG: cirugía de revascularización coronaria; EC: enfermedad coronaria; IAMCEST: infarto agudo de miocardio con elevación del segmento ST; ICP: intervención coronaria percutánea; IM: infarto de miocardio; OTC: oclusión coronaria total crónica; SCA: síndrome coronario agudo; SCC: síndrome coronario crónico; SFA: stent farmacoactivo. |
|||||||
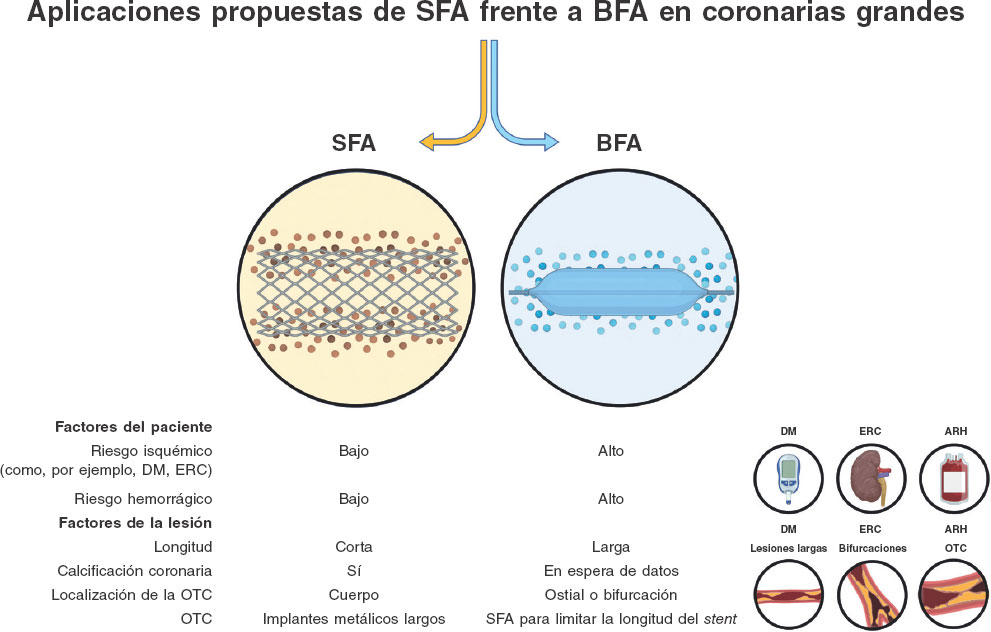
Figura 1. Factores del paciente y de la lesión que se deben tener en cuenta al valorar la enfermedad coronaria de vasos nativos grandes para la realización de intervenciones coronarias percutáneas. La presencia de cualquiera de los factores señalados bajo BFA debe llevar al operador a plantear un abordaje destinado a limitar el número de implantes coronarios permanentes. ARH: alto riesgo hemorrágico; BFA: balón farmacoactivo; DM: diabetes mellitus; ERC: enfermedad renal crónica; OTC: oclusión coronaria crónica total; SCA: síndrome coronario agudo; SFA: stent farmacoactivo.
Los análisis de subgrupos dentro de cada estudio proporcionan información más específica sobre los pacientes tratados con dispositivos de mayor calibre. Ante la importante interacción del valor de p en el análisis de subgrupo sobre el tamaño de los vasos del ECA más grande incluido7, parece razonable plantearse si los resultados globales habrían sido superponibles en el supuesto de que el análisis se hubiese limitado a vasos de mayor tamaño. Estas observaciones se deben interpretar a la luz de la discusión previa sobre el tipo de lesiones incluidas. Por último, este aspecto podría variar según el sexo: aunque las mujeres suelen presentar vasos coronarios de menor diámetro, un vaso de un determinado calibre podría ser más proximal e irrigar un mayor territorio miocárdico en mujeres que en varones, lo cual tendría una mayor relevancia clínica16.
PREPARACIÓN DE LAS LESIONES
La preparación de la lesiones es un punto de importante heterogeneidad entre los ECA del metanálisis. Por ejemplo, el estudio REVELATION9, realizado en pacientes con infarto agudo de miocardio con elevación del segmento ST, permitió proceder con angioplastias con BFA con porcentajes residuales de estenosis por diámetro del 50% tras la predilatación y trombectomías ante la presencia de trombos visibles, lo cual es contrario al umbral fijado ≤ 30% habitualmente aceptado5. Por otro lado, el momento en que se llevó a cabo la aleatorización complica, si cabe, la comparativa entre las distintas técnicas intervencionistas, ya que 2 estudios aleatorizaron pacientes antes de evaluar el resultado de la preparación de la lesión10,11. También fueron distintos los métodos de preparación de las lesiones, así, un estudio recomendaba el uso de balón semidistensible previo al inflado del BFA12. El éxito de la angioplastia con BFA depende de una estrategia operatoria específica basada en una meticulosa preparación de la lesión y una cuidada evaluación posoperatoria, matiz que a menudo se pierde al comparar resultados entre distintas metodologías15,17,18.
CARACTERÍSTICAS DE LOS BFA
El campo de los BFA se caracteriza por la diversidad de plataformas, fármacos antiproliferativos y recubrimientos. Aunque los ECA incluidos se centraron mayoritariamente en balones recubiertos con paclitaxel, cada vez hay más evidencia de distintas respuestas vasculares, efectos a distancia y farmacocinética en función de la tecnología empleada, lo cual sugiere que la elección tanto del fármaco como del recubrimiento podría influir en los resultados clínicos. Recientemente, los balones recubiertos con sirolimus han dado resultados prometedores en distintos escenarios clínicos. De cara al futuro, será necesario seguir diferenciando entre distintas tecnologías, teniendo en cuenta que el rendimiento clínico de estas podría no ser el mismo19,20. También se deben tener en cuenta aspectos tales como el recubrimiento del balón y el mecanismo de liberación del fármaco. Las tecnologías de todos los BFA analizados en este metanálisis usaban paclitaxel, pero con plataformas distintas: solo 3 estudios evaluaron el mismo dispositivo (SeQuent Please, B. Braun, Alemania) y los restantes emplearon sistemas distintos, incluido uno de liberación controlada por ultrasonidos10. Por último, el tiempo de inflado, esencial para la liberación del fármaco, no fue el mismo en los estudios incluidos, con tiempos de inflado recomendados de tan solo 30 segundos6. Los ensayos en marcha en la actualidad (MAGICAL SV [NCT06271590] y Prevail Global [NCT06535854]) también varían ligeramente en este aspecto y aún está por dilucidar si estas variaciones tendrán, o no, repercusiones clínicas.
RESULTADOS CLÍNICOS Y ANGIOGRÁFICOS
El implante de SFA suele proporcionar un mayor incremento luminal agudo que la angioplastia con balón, un concepto que también refleja el ensayo REVELATION9, en el que los umbrales de estenosis residual para definir el éxito variaron entre la angioplastia con BFA (< 30%) y el implante del SFA (< 20%). Aunque el metanálisis informa del objetivo de pérdida luminal tardía, reconocemos que esta medida no refleja del todo la eficacia relativa de ambas tecnologías. Futuros estudios deberían incluir objetivos tales como la ganancia luminal neta y ofrecer una comparativa más integral y significativa entre estas estrategias y centrarse en el efecto terapéutico global sobre la luz vascular y no solo en la respuesta reestenótica tras la intervención. También se debe mencionar la limitación de comparar las tasas de eventos cardiovasculares adversos mayores cuando cada componente es distinto de un estudio a otro. Por último, subrayamos lo importante que es que futuros estudios informen sistemáticamente sobre la trombosis del vaso diana, un objetivo de seguridad clave poco informado en este metanálisis y que sigue preocupando a nivel clínico y es un factor determinante para la adopción generalizada de la estrategia basada en BFA (COPERNICAN [NCT06353594]).
CONCLUSIONES
El metanálisis de Sorolla Romero et al.5 proporciona una síntesis oportuna de la evidencia actual sobre el uso de BFA en vasos nativos grandes; sus hallazgos también aportan evidencia generadora de hipótesis que cuestiona el paradigma establecido de los SFA como tratamiento de elección de cualquier lesión. Este trabajo pone de manifiesto que la ICP está en constante evolución e invita a reconsiderar los algoritmos terapéuticos hacia abordajes más individualizados en los que elección entre BFA y SFA se guíe por factores específicos de cada paciente y lesión (figura 1). De cara al futuro, será fundamental centrar los esfuerzos en refinar la selección de pacientes, optimizar las técnicas intervencionistas y llevar a cabo ECA adicionales con seguimientos más largos a fin de aclarar el papel que juegan los BFA en este nuevo paradigma terapéutico.
FINANCIACIÓN
Ninguna.
CONFLICTO DE INTERESES
Ninguno.
BIBLIOGRAFÍA
1. Colombo A, Leone PP. Redefining the way to perform percutaneous coronary intervention:a view in search of evidence. Eur Heart J. 2023; 44:4321-4323.
2. Colombo A, Leone PP, Ploumen EH, von Birgelen C. Drug-coated balloons as a first choice for patients with de novo lesions:pros and cons. EuroIntervention. 2024;20:120-122.
3. Regazzoli D, Latib A, Ezhumalai B, et al. Long-term follow-up of BVS from a prospective multicenter registry:Impact of a dedicated implantation technique on clinical outcomes. Int J Cardiol. 2018;270:113-117.
4. Camaj A, Leone PP, Colombo A, et al. Drug-Coated Balloons for the Treatment of Coronary Artery Disease:A Review. JAMA Cardiol. 2025; 10:189-198.
5. Sorolla Romero JA, Novelli L, LLau Garcia J, et al. Drug-coated balloons vs drug-eluting stents for the treatment of large native coronary artery disease. Meta-analysis of randomized controlled trials. REC Interv Cardiol. 2025. https://doi.org/10.24875/RECICE.M25000527.
6. Nishiyama N, Komatsu T, Kuroyanagi T, et al. Clinical value of drug-coated balloon angioplasty for de novo lesions in patients with coronary artery disease. Int J Cardiol. 2016;222:113-118.
7. Gao C, He X, Ouyang F, et al. Drug-coated balloon angioplasty with rescue stenting versus intended stenting for the treatment of patients with de novo coronary artery lesions (REC-CAGEFREE I):an open-label, randomised, non-inferiority trial. Lancet. 2024;404:1040-1050.
8. Yu X, Wang X, Ji F, et al. A Non-inferiority, Randomized Clinical Trial Comparing Paclitaxel-Coated Balloon Versus New-Generation Drug-Eluting Stents on Angiographic Outcomes for Coronary De Novo Lesions. Cardiovasc Drugs Ther. 2022;36:655-664.
9. Vos NS, Fagel ND, Amoroso G, et al. Paclitaxel-Coated Balloon Angioplasty Versus Drug-Eluting Stent in Acute Myocardial Infarction:The REVELATION Randomized Trial. JACC Cardiovasc Interv. 2019;12:1691-1699.
10. Wang Z, Yin Y, Li J, et al. New Ultrasound-Controlled Paclitaxel Releasing Balloon vs. Asymmetric Drug-Eluting Stent in Primary ST-Segment Elevation Myocardial Infarction-A Prospective Randomized Trial. Circ J Off J Jpn Circ Soc. 2022;86:642-650.
11. Gobi´c i D, Tomuli´c V, Luli´c D, et al. Drug-Coated Balloon Versus Drug-Eluting Stent in Primary Percutaneous Coronary Intervention:A Feasibility Study. Am J Med Sci. 2017;354:553-560.
12. Hao X, Huang D, Wang Z, Zhang J, Liu H, Lu Y. Study on the safety and effectiveness of drug-coated balloons in patients with acute myocardial infarction. J Cardiothorac Surg. 2021;16:178.
13. Leone PP, Oliva A, Regazzoli D, et al. Immediate and follow-up outcomes of drug-coated balloon angioplasty in de novo long lesions on large coronary arteries. EuroIntervention. 2023;19:923-925.
14. Tartaglia F, Gitto M, Leone PP, et al. Validation of complex PCI criteria in drug-coated balloon angioplasty. Clin Res Cardiol. 2025;114:1059-1070.
15. Leone PP, Gitto M, Gao C, Sanz Sánchez J, Latib A, Colombo A. Rethinking coronary artery metal implants. Prog Cardiovasc Dis. 2025. https://doi.org/10.1016/j.pcad.2025.07.005.
16. Leone PP, Testa L, Greco A, et al. Two-Year Clinical Outcomes in Female and Male Patients After Sirolimus-Coated Balloon Angioplasty for Coronary Artery Disease. Circ Cardiovasc Interv. 2025;18: 014814.
17. Gitto M, Leone PP, Gioia F, et al. Coronary Artery Dissection in Drug-Coated Balloon Angioplasty:Incidence, Predictors, and Clinical Outcomes. Am J Cardiol. 2025;239:28-35.
18. Leone PP, Mangieri A, Regazzoli D, et al. Drug-Coated Balloon Angioplasty Guided by Postpercutaneous Coronary Intervention Pressure Gradient:The REDUCE-STENT Retrospective Registry. JACC Cardiovasc Interv. 2023;16:363-365.
19. Leone PP, Heang TM, Yan LC, et al. Two-year outcomes of sirolimus-coated balloon angiopla,sty for coronary artery disease:the EASTBOURNE Registry. EuroIntervention. 2024;20:831-833.
20. Leone PP, Calamita G, Gitto M, et al. Sirolimus- Versus Paclitaxel-Coated Balloons for Treatment of Coronary Artery Disease. Am J Cardiol. 2025;255:74-82.