Sr. Editor:
La administración de tratamiento anticoagulante solo ha demostrado ser eficaz contra la embolia pulmonar (EP) aguda de riesgo bajo y de bajo a intermedio1. No obstante, la EP de riesgo intermedio-alto y alto está asociada a un riesgo considerablemente alto de colapso circulatorio a corto plazo, muerte o hipertensión pulmonar tromboembólica crónica de entre el 3 y el 10% cuando se trata solo con anticoagulación1. Aunque la fibrinólisis sistémica reduce este riesgo en un 50%, este tratamiento aumenta significativamente el riesgo de sangrado mayor, tal y como describió el ensayo PEITHO2, lo cual ha limitado el uso de la fibrinólisis sistémica a pacientes de alto riesgo, tal y como recomienda la guía vigente3.
Esta limitación ha generado un interés creciente en las terapias dirigidas por catéter (TDC) en pacientes con EP aguda de alto riesgo y una contraindicación o fracaso de la fibrinolisis sistémica, así como en pacientes de riesgo intermedio-alto que desarrollan deterioro hemodinámico a pesar de la anticoagulación3. Las TDC permiten una resolución más rápida de los defectos de perfusión y una mejora hemodinámica sin los efectos hemorrágicos sistémicos asociados a la trombolisis sistémica.
A pesar del mayor uso de estas TDC, la evidencia clínica sobre sus beneficios sigue siendo escasa al no haber ensayos aleatorizados controlados que cuenten conlas herramientas estadísticas necesarias, teniendo en cuenta además que los estudios actuales se limitan a una mejora hemodinámica inmediata o a marcadores indirectos de imágenes4-6.
El objetivo de este estudio fue valorar la seguridad, viabilidad y efectos a medio plazo de las TDC. Entre 2020 y 2022, se inscribió prospectivamente a pacientes consecutivos con EP de riesgo alto e intermedio-alto tratados de TDC en un único centro terciario. Los criterios de selección incluyeron a pacientes de alto riesgo con fibrinolisis contraindicada o fallida y a aquellos de riesgo intermedio-alto y deterioro hemodinámico a pesar de la anticoagulación. Se excluyó a los pacientes con EP de más de 2 semanas de evolución o con trombos en tránsito.
Se llevó a cabo un cateterismo cardiaco derecho (CCD) y una angiografía pulmonar bilateral vía vena basílica femoral o antecubital derecha antes de la intervención. Los operadores tuvieron que decidir si se hacía una fibrinolisis in situ, una trombectomía mecánica o ambas intervenciones según la carga de trombos, su localización, el estado hemodinámico del paciente y el riesgo de sangrado. Se indujo fibrinolisis local dirigida por catéter mediante la infusión de alteplasa de 1 mg/h durante 12 horas seguido de 1 bolo de 1 mg. La trombectomía mecánica dirigida por catéter empleó el sistema de aspiración Indigo de 8 y 12 Fr (Penumbra, Estados Unidos) para restaurar la perfusión en tantas ramas como fuera posible hasta obtener un buen resultado angiográfico o una aspiración de sangre de 300 a 350 ml. El protocolo de seguimiento incluyó un ecocardiograma, una angiotomografía computarizada, el ya citado CCD y una angiografía pulmonar 3 meses después de la TDC.
Se analizó a 39 pacientes. Las características basales se muestran en la tabla 1, que muestra niveles altos de lactato sérico, troponina y del péptido natriurético tipo B pro-N-terminal en el 30, 97 y 92% de los pacientes, respectivamente. En el momento del ingreso, el 18% de los pacientes fueron estratificados como de alto riesgo. El ecocardiograma realizado durante el ingreso confirmó la dilatación del ventrículo derecho (VD) en el 95% de los pacientes, con disfunción sistólica del VD en el 69% de estos.
Tabla 1. Características basales y datos de la intervención
| Características basales (n = 39) | |
| Años, edad | 60,0 ± 17,6 |
| Género, masculino | 46,2% (18) |
| TEV previo | 12,8% (5) |
| Enfermedad oncológica | 10,3% (4) |
| Hallazgos clínicos y de laboratorio (n = 39) | |
| Síncope en la presentación | 28,2% (11) |
| Disnea en la presentación | 76,9% (30) |
| Días desde que cursaron síntomas | 1,0 [1,8] |
| Embolia pulmonar de alto riesgo | 17,9% (7) |
| Fibrinólisis sitémica fallida | 0% |
| Contraindicación a la fibrinólisis | 10,3% (4) |
| Presión arterial sistólica, mmHg | 116 ± 26 |
| Frecuencia cardiaca, lpm | 102 ± 21 |
| Relación PaO2/FiO2 | 262 ± 96 |
| Lactato sérico, mmol/l (N < 1,8) | 1,7 ± 1,6 |
| hs-troponina I, pg/ml (N < 14) | 262 [520] |
| NT-proBNP, pg/ml (N < 150) | 2.775 [3.910] |
| Pico de D-dímero, ng/ml (N < 500) | 8.835 [12 254] |
| Lactato positivo | 30,8% (12) |
| Troponina positiva | 97,4% (38) |
| NT-proBNP positivo | 92,3% (36) |
| Hallazgos de las imágenes – valoración inicial (n = 39) | |
| EP central en la angio-TC | 34,2% (13) |
| Cociente VD/VI en la angio-TC | 1,4 ± 0,2 |
| VD dilatado en el ETT | 94,6% (35) |
| Disfunción del VD en el ETT | 69,4% (25) |
| Datos de la intervención y complicaciones (n = 39) | |
| Trombectomía + fibrinólisis local | 17,9% (13) |
| Trombectomía aislada | 10,3% (4) |
| Fibrinólisis local aislada | 71,2% (28) |
| Cualquier complicación de la intervención | 5,1% (2) |
| Muerte cardiovascular | 2,6% (1) |
| Shock cardiogénico | 2,6% (1) |
| Sangrado mayor | 0% |
| Taponamiento cardiaco | 0% |
| Perforación de la arteria pulmonar | 0% |
| Disección de la arteria pulmonar | 2,6% (1) |
| Avulsión de la fresa del dispositivo Penumbra | 2,6% (1) |
| IP entre moderada y grave | 0% |
| IT entre moderada y grave (previa) | 25,6% (10) |
| IT entre moderada y grave (posterior) | 7,7% (3) |
|
angio-TC: angiotomografía computarizada; EP: embolia pulmonar; ETT, ecocardiograma transtorácico; IP: insuficiencia pulmonar; IT: insuficiencia tricuspídea; NT-proBNP: péptido natriurético cerebral prohormonal de la porción N-terminal; TEV: tromboembolismo venoso; VD: ventrículo derecho; VI: ventrículo izquierdo. Los datos expresan n (%), media ± desviación estandar o mediana [rango intercuartílico]. |
|
Se indujo fibrinólisis local en el 71% de los pacientes, el dispositivo de aspiración Penumbra se empleó en el 10% y la terapia combinada en el 18%. No se observaron sangrados mayores conducentes a la muerte ni que requirieran intervención médica o transfusión durante ni después de la intervención. Sobrevino 1 disección de la arteria pulmonar y 1 avulsión parcial de la fresa del dispositivo Penumbra, ambas tratadas conservadoramente con buenos resultados. Un paciente tuvo shock cardiogénico persistente y refractario que finalmente le provocó la muerte. Los datos de la intervención se muestran en la tabla 1.
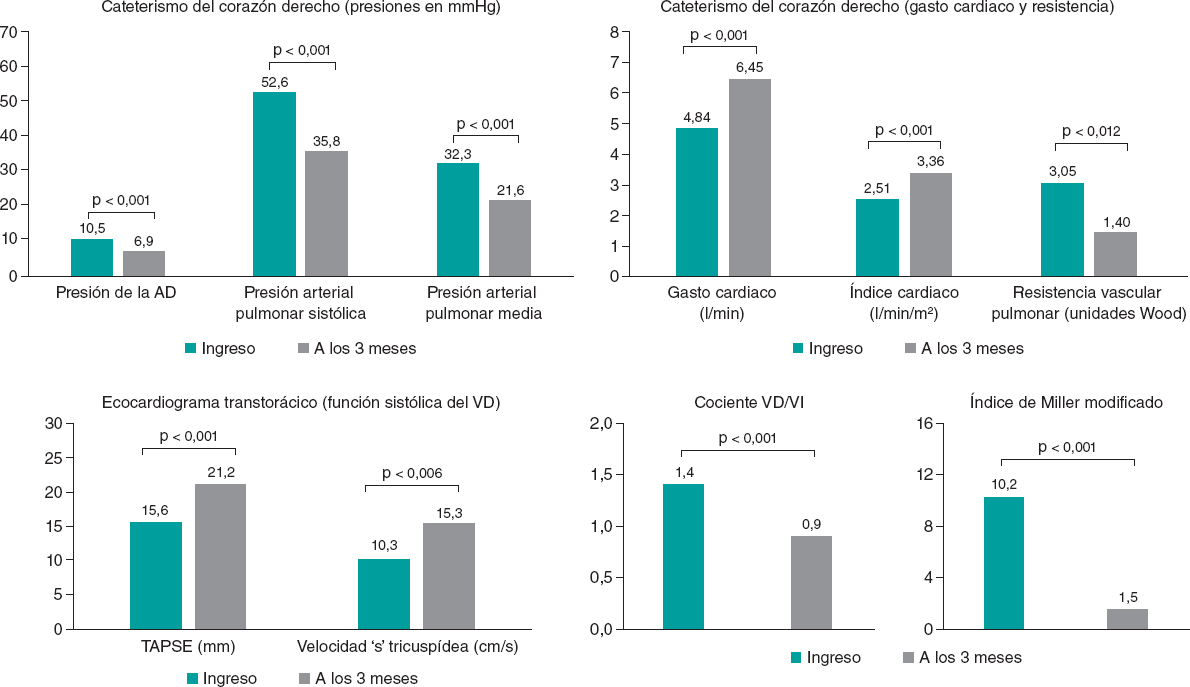
Un total de 23 pacientes completaron el seguimiento de 3 meses de duración con resultado de 4 fallecimientos, principalmente por causas no cardiovasculares. Se observó una tasa significativa de seguimiento incompleto por varias razones, incluidos 4 pacientes extranjeros que no pudieron completar el seguimiento, 5 que retiraron su consentimiento y 3 que se perdieron en el seguimiento. El estado hemodinámico mejoró significativamente entre los 23 pacientes que sí lo completaron.. Los datos del CCD confirmaron caídas de las presiones de la aurícula derecha, arteria pulmonar sistólica y arteria pulmonar a una media de 3,6, 16,8 y 10,7 mmHg, respectivamente (p < 0,001). También se observaron subidas del gasto e índice cardiacos (medias de 1,61 y 0,85 l/min/m2, respectivamente) (p < 0,001) y un descenso de 1,65 unidades Wood en la resistencia vascular pulmonar (p = 0,012). También se observó una mejora en los defectos de perfusión, con un descenso medio de 8,7 puntos en el índice de Miller modificado (p < 0,001) y mejoras en la función del VD, un descenso medio de 0,5 en el cociente VD/VI en la tomografía computarizada (TC) (p < 0,001), una subida media de 5,4 mm en la excursión sistólica del plano del anillo tricúspide (TAPSE) (p < 0,001) y una subida media de 5,0 cm/s en la velocidad de sístole del anillo tricúspide (S’) (p = 0,006). Estos resultados se muestran en la figura 1. A los 3 meses, 9 de los 23 pacientes (39%) presentaban valores medios de presión arterial pulmonar > 20 mmHg.
Figura 1. Datos invasivos de hemodinámica, ecocardiográficos, morfológicos y de la carga trombótica al ingreso y a los 3 meses. AD: aurícula derecha; TAPSE: excursión sistólica del plano del anillo tricúspide. VD: ventrículo derecho; VI: ventrículo izquierdo.
Durante el periodo de seguimiento, fallecieron 4 pacientes, lo cual arrojó una tasa de mortalidad global del 10,3%. No obstante, solo hubo 1 fallecimiento de origen cardiaco secundario a un empeoramiento del shock cardiogénico refractario. Un paciente falleció por el avance de su enfermedad oncológica y 2 por causas no cardiovasculares.
Este estudio comunica una tasa de complicaciones menores asociadas a la intervención del 5,1%, lo cual mejora la viabilidad y seguridad de las TDC. El estudio EXTRACT-PE informó de tasas de complicaciones asociadas a la intervención, sangrados mayores y lesiones vasculares pulmonares asociadas al dispositivo del 2,5, 1,7 y 0,8%, respectivamente5. Además, ninguna de las 2 complicaciones fue mortal y el tratamiento fue conservador, con buenos resultados angiográficos en la reevaluación. Estas complicaciones se asociaron al uso de dispositivos de trombectomía mecánica y ambas sobrevinieron al principio de la curva de aprendizaje de este dispositivo, lo cual lleva a los autores a pensar que la incidencia de estas complicaciones podría reducirse a medida que el operador va teniendo más experiencia. A pesar de inducir fibrinolisis dirigida por catéter a casi el 90% de los pacientes, no hubo eventos hemorrágicos mayores ni potencialmente mortales en las primeras 48 horas tras la intervención, posiblemente por la dosis tan baja de alteplasa utilizada.
La mayoría de los ensayos realizados con anterioridad empleaban parámetros de imagen como marcadores indirectos para valorar el efecto inmediato de la TDC. El parámetro más utilizado es el cociente VD/VI, tal y como se aprecia en los estudios SEATTLE II (Estudio prospectivo, de brazo único, multicéntrico de fibrinólisis de baja dosis guiada por ultrasonido y dirigida por catéter para el tratamiento de embolias pulmonares masivas y submasivas), EXTRACT-PE y FLARE (Estudio prospectivo, de brazo único y multicéntrico de trombectomía mecánica dirigida por catéter para el tratamiento de embolias pulmonares agudas de riesgo intermedio)4-6. Nuestro estudio proporciona datos más extensos y a medio plazo sobre los beneficios de la TDC, incluida una valoración directa invasiva del perfil hemodinámico y no de parámetros de imagen indirectos. A los 3 meses, se observó, de media, un descenso del cociente VD/VI de 0,5 similar a las tasas descritas en anteriores estudios. Además, nuestro estudio también confirmó que la función sistólica del VD experimentó una mejoría significativa según la ecocardiografía transtorácica, un descenso significativo de las presiones y resistencia vascular pulmonar y un aumento del gasto cardiaco, ambos medidos invasivamente 3 meses después de la intervención.
El tratamiento óptimo de la EP de riesgo intermedio aún no está bien establecido y las guías actuales recomiendan solo tratamiento anticoagulante y dejan la intervención con catéter para pacientes que no responden al tratamiento conservador3. El ensayo PEITHO confirmó que la fibrinólisis sistémica redujo significativamente el objetivo primario compuesto de muerte o deterioro clínico, a expensas de un aumento significativo de los sangrados mayores y las hemorragias intracraneales2. Aunque las TDC no se han comparado directamente con el tratamiento solo anticoagulante en estos pacientes, los autores creen que las TDC tienen varias ventajas. En primer lugar, la fibrinólisis dirigida por catéter proporciona los mismos beneficios intrapulmonares que la fibrinólisis sistémica sin el riesgo de sangrado mayor. En segundo lugar, los sistemas de aspiración permiten una reperfusión más rápida e inmediata de las ramas principales, evitando un mayor deterioro que sería irreversible en pacientes inestables. En tercer lugar, la trombectomía mecánica dirigida por catéter es una opción segura y eficaz en aquellos pacientes que no pueden recibir agentes fibrinolíticos. En cuarto lugar, ambas técnicas parecen ofrecer un beneficio adicional en la anticoagulación a largo plazo al reducir la perfusión, las presiones vasculares pulmonares y, por ende, el avance de la hipertensión pulmonar tromboembólica crónica.
La valoración del estado hemodinámico a los 3 meses ofrece nuevas perspectivas sobre las altas tasas de pacientes que desarrollan hipertensión pulmonar, lo cual tiene una importancia capital al considerar el nuevo punto de corte de 20 mmHg para la presión arterial pulmonar media fijado por las guías de la ESC de 2022 sobre el manejo de la hipertensión pulmonar.
La principal limitación de este estudio es la ausencia de un grupo comparador. Otras limitaciones son el seguimiento incompleto de casi el 33% de los pacientes, un tamaño muestral pequeño y el uso de 2 estrategias diferentes dirigidas por catéter.
En conclusión, para pacientes con EP de riesgo intermedio-alto y alto, la TDC es una opción de tratamiento viable y segura que mejora la hemodinámica, la función del VD y los defectos de perfusión 3 meses después de la intervención.
FINANCIACIÓN
Ninguna.
CONSIDERACIONES ÉTICAS
Este estudio se llevó a cabo de conformidad con los principios de la Declaración de Helsinki y fue aprobado por el comité de ética local. Se obtuvo el consentimiento informado de todos los participantes del estudio. Las posibles variables de sexo y género se han tenido en cuenta según las guías SAGER.
DECLARACIÓN SOBRE EL USO DE INTELIGENCIA ARTIFICIAL
No se empleó inteligencia artificial durante la realización de este estudio ni durante la redacción de este manuscrito.
CONTRIBUCIÓN DE LOS AUTORES
A. Grazina y L. Almeida Morais diseñaron el protocolo del estudio y contaron con la colaboración de A. Fiarresga y D. Cacela. A. Grazina y B. Lacerda Teixeira recopilaron y analizaron los datos. A. Grazina y B. Lacerda Teixeira redactaron el manuscrito con la colaboración de L. Almeida Morais. A. Fiarresga y D. Cacela coordinaron el proyecto. Todos los autores leyeron y aprobaron este manuscrito.
CONFLICTO DE INTERESES
Los autores declaran que este es un artículo original, no publicado previamente ni enviado a otra revista. Los autores no declararon ningún conflicto de intereses.
BIBLIOGRAFÍA
1. Giri J, Sista AK, Weinberg I et al. Interventional therapies for acute pulmonary embolism:current status and principles for the development of novel evidence:a scientific statement from the American Heart Association. Circulation. 2019;140:774-801.
2. Meyer G, Vicaut E, Danays T et al;PEITHO Investigators. Fibrinolysis for patients with intermediate-risk pulmonary embolism. N Engl J Med. 2014;370:1402–1411.
3. Konstantinides S, Meyer G, Becattini C et al. 2019 ESC Guidelines for the diagnosis and management of acute pulmonary embolism. Eur Heart J. 2019;41:543-603.
4. Piazza G, Hohlfelder B, Jaff MR et al. A prospective, Single-Arm, Multicenter Trial of Ultrasound-Facilitated, Catheter-Directed, Low-Dose Fibrinolysis for Acute Massive and Submassive Pulmonary Embolism:The SEATTLE II Study. JACC Cardiovasc Interv. 2015;8:1382-1392.
5. Sista AK, Horowitz JM, Tapson VF et al. Indigo Aspiration System for Treatment of Pulmonary Embolism:Results of the EXTRACT-PE Trial. JACC Cardiovasc Interv. 2021;14:319-329.
6. Tu T, Toma C, Tapson VF et al. A prospective, Single-Arm, Multicenter Trial of Catheter-Directed Mechanical Thrombectomy for Intermediate-Risk Acute Pulmonary Embolism:The FLARE Study. JACC Cardiovasc Interv. 2019;12:859-869.