RESUMEN
La hipertensión arterial es el factor de riesgo cardiovascular más prevalente. A pesar del tratamiento farmacológico, un alto porcentaje de pacientes no consiguen un adecuado control. La denervación renal es una intervención mínimamente invasiva para el tratamiento de la hipertensión que implica la interrupción de los nervios simpáticos renales mediante un abordaje con catéter. Los estudios iniciales mostraron resultados prometedores, pero los controvertidos resultados del ensayo SYMPLICITY HTN-3 llevaron al abandono de la técnica. En los últimos 3 años han aparecido los resultados de nuevos ensayos clínicos, con nuevos dispositivos y en diferentes poblaciones, que demuestran definitivamente la eficacia de la denervación renal.
En este documento de posicionamiento conjunto de la Sociedad Española de Hipertensión-Liga Española para la Lucha contra la Hipertensión Arterial (SEH-LELHA) y la Asociación de Cardiología Intervencionista de la Sociedad Española de Cardiología (ACI-SEC) se revisa la evidencia disponible sobre la eficacia y la seguridad de la denervación renal en el tratamiento de la hipertensión. A partir de los resultados de los ensayos clínicos, se generan recomendaciones sobre qué pacientes y en qué condiciones podrían ser candidatos a una denervación renal.
Palabras clave: Hipertensión arterial. Denervación renal. Presión arterial.
ABSTRACT
Hypertension is the most prevalent cardiovascular risk factor. Despite pharmacological treatment, a high percentage of patients do not achieve an adequate blood pressure control. Renal sympathetic denervation is a minimally invasive intervention for the management of hypertension involving the interruption of the renal artery sympathetic nervous system using a catheter-based approach. The early studies showed promising results, but the controversial results coming from the SYMPLICITY HTN-3 trial sent this technique into oblivion. Over the last 3 years, new clinical trials have appeared including new devices used in different populations, which definitively proves the effectiveness of renal sympathetic denervation.
This joint position statement from the Spanish Society of Hypertension-Spanish League for Combating High Blood Pressure (SEH-LELHA), and the Interventional Cardiology Association of the Spanish Society of Cardiology (ACI-SEC) reviews the evidence available on the efficacy and safety profile of renal sympathetic denervation for the management of hypertension. Based on the results of clinical trials, recommendations have been established on what patients may be eligible for renal sympathetic denervation and under what circumstances.
Keywords: Hypertension. Renal sympathetic denervation. Blood pressure.
Abreviaturas
DR: denervación renal. HTA: hipertensión arterial. HTA-R: hipertensión resistente. LOMH: lesión orgánica mediada por hipertensión arterial. MAPA: monitorización ambulatoria de la presión arterial. PA: presión arterial. PAD: presión arterial diastólica. PAS: presión arterial sistólica.
INTRODUCCIÓN
El papel que juega el sistema nervioso simpático en la fisiopatología de la hipertensión arterial (HTA) es bien conocido. En 2007, se realizaron las primeras intervenciones de denervación renal (DR) para el tratamiento de pacientes con HTA resistente (HTA-R). Los primeros estudios observacionales que se realizaron dieron resultados positivos y el uso de la DR empezó a ser una realidad en centros de todo el mundo1,2. Sin embargo, en 2014, la publicación de un estudio en el que se incluyó un grupo control con procedimiento simulado en el que no se consiguió demostrar la eficacia de la DR para el control de la presión arterial (PA)3 hizo que el interés de la comunidad científica por esta intervención, así como por su aplicación clínica, fuera desvaneciéndose. El mejor conocimiento de la anatomía renal combinado con el desarrollo de nuevos dispositivos ha llevado a nuevos estudios, también con grupo control simulado, en los que se demuestra la eficacia de la DR4-7. Si bien el camino por recorrer es largo, las nuevas evidencias auguran un nuevo papel para la DR en el tratamiento de pacientes con HTA.
En 2018, las guías de práctica clínica sobre el tratamiento de la hipertensión publicadas por la Sociedad Europea de Cardiología, así como por la Sociedad Europea de Hipertensión (ESC/ESH) desaconsejaban la DR como tratamiento de la HTA y recomendaban su uso únicamente dentro de ensayos clínicos8. A pesar del poco tiempo que ha pasado desde la publicación de estas guías, los datos que arrojan los nuevos ensayos clínicos vendrían a justificar el tratamiento de pacientes seleccionados con DR.
Este documento revisa la evidencia disponible en materia de DR para el tratamiento de la HTA, analiza posibles indicaciones y sugiere estrategias para identificar a los pacientes potencialmente aptos, a partir de la opinión de un panel de expertos seleccionados por la Sociedad Española de Hipertensión Arterial-Liga Española para la Lucha contra la Hipertensión Arterial (SEH-LELHA) y por la Asociación de Cardiología Intervencionista de la Sociedad Española de Cardiología (ACI-SEC). La redacción del documento corrió a cargo de profesionales propuestos por ambas sociedades científicas que firmaron su trabajo en base a su experiencia en el abordaje de pacientes tratados mediante DR. Tras el primer borrador, otros expertos, con y sin experiencia en la realización de DR, llevaron a cabo una revisión crítica del documento consensuando una serie de cambios que consideraron apropiado hacer.
EVIDENCIA CLÍNICA SOBRE EL PAPEL QUE JUEGA LA DENERVACIÓN RENAL EN EL TRATAMIENTO DE LA HIPERTENSIÓN
El material adicional detalla las características epidemiológicas de la HTA (sección 1), así como el papel que desempeña el sistema nervioso simpático en la HTA (sección 2), lo cual nos ayuda a entender mejor los ensayos clínicos. La tabla 1 del material adicional muestra los principales estudios que han analizado la eficacia de la DR.
Tabla 1. Estudios previos a la denervación renal en pacientes con hipertensión no controlada
| Evaluación del tratamiento farmacológico |
| Tipo y número de fármacos |
| Dosis adecuada del fármaco |
| Valorar el uso de un antagonista de la aldosterona |
| Valorar la falta de adherencia al tratamiento |
| Valorar la intolerancia al tratamiento farmacológico |
| Estudio MAPA durante 24 horas |
| Descartar hipertensión seudoresistente o por efecto de bata blanca |
| Confirmar hipertensión no controlada (valores PAS > 130 mmHg/PAD > 80 mmHg durante un periodo de 24 horas o valores PAS > 135/PAD > 85 mmHg en los niveles del día) |
| Descartar causas secundarias de la hipertensión (tabla 2) |
| Valorar el riesgo cardiovascular |
| Coexistencia de otros factores de riesgo cardiovascular tales como dislipemia, diabetes o tabaquismo |
| Presencia de LOMH |
| Presencia de enfermedad cardiovascular o renal establecida |
| Imágenes de la anatomía renal mediante tomografía computarizada o resonancia magnética nuclear (valorar estenosis oclusiva, ramas accesorias, diámetro arterial) |
| Pruebas adicionales recomendadas: |
| Hemograma, parámetros de la función renal, perfiles hepático y lipídico y pruebas de sedimento urinario para detectar la presencia de microalbuminuria |
| Determinaciones analíticas específicas: |
| Cociente basal de aldosterona-actividad de renina plasmática |
| Hormonas tiroideas |
| Metabolismo calcio-fósforo con niveles de la hormona paratiroidea |
| Cortisol (coeficientes en orina basales y a las 24 horas) |
| Catecolaminas con los niveles de metanefrinas urinarias a las 24 horas |
| Polisomnografía |
|
LOMH: lesión orgánica mediada por hipertensión arterial; MAPA: monitorización ambu-latoria de la presión arterial; PAD: presión arterial diastólica; PAS: presión arterial sistólica. |
En 2009 se publicó el primer estudio sobre DR en pacientes con HTA-R, el SYMPLICITY HTN-1. Un estudio que sugería un perfil de eficacia alto de la DR y descenso de la presión arterial sistólica (PAS) en consulta hasta 27 mm Hg a los 12 meses libre, además, de complicaciones importantes1.
El SYMPLICITY HTN-3 fue el primer estudio en incluir un grupo de control con una intervención simulada y con determinación de PA de 24 horas. A los seis meses de seguimiento no se observaron diferencias entre los dos grupos de tratamiento en cuanto a la eficacia del control de la PA3. La discrepancia entre los resultados de este estudio y los anteriores, así como la identificación de varios factores de confusión como la inexperiencia de muchos intervencionistas, la heterogeneidad en la respuesta a la DSRP de distintas subpoblaciones y la interferencia del uso de fármacos9, puso de manifiesto la necesidad de diseñar nuevos estudios dirigidos específicamente a resolver estas cuestiones.
La evidencia definitiva sobre la eficacia de la DR procede de los estudios SPYRAL HTN y RADIANCE-HTN. El estudio SPYRAL HTA-ON MED incluyó a pacientes con HTA no controlada, tratados con entre 1 y 3 fármacos antihipertensivos, aleatorizados para recibir una DR o una intervención simulada. Tanto los niveles de PAS y PA diastólica (PAD) ambulatorios durante un periodo 24 horas como los niveles de PAS y PAD en consulta se redujeron significativamente en el grupo DR frente al control simulado tras 6 meses de seguimiento4. Con un diseño parecido, el estudio SPYRAL HTA-OFF MED Pivotal incluyó a pacientes con HTA no controlada y niveles de PAS en consulta entre 150 y 180 mmHg en ausencia de tratamiento antihipertensivo. Los valores de PAS durante un periodo 24 horas, así como los niveles de PAS en consulta se conocieron tras 3 meses de seguimiento5. El estudio RADIANCE-HTN SOLO incluyó a pacientes con HTA y valores de PA en la monitorización ambulatoria de la presión arterial (MAPA) ≥ 135/85 mmHg y ≤ 170/105 mmHg, en ausencia de tratamiento farmacológico. Tanto los niveles de PAS y PAD ambulatorios durante un periodo 24 horas como los niveles de PAS y PAD en consulta descendieron significativamente en el grupo DR comparado con el control simulado tras 2 meses de seguimiento6. Finalmente, el RADIANCE-HTN TRIO incluyó a pacientes con HTA-R a tratamiento con una dosis fija de 1 polipíldora consistente en un bloqueador del canal de calcio, un bloqueador del receptor de la angiotensina y un diurético tiazídico. Los pacientes fueron aleatorizados a recibir una DR mediante un catéter de ultrasonidos o una intervención simulada. Tanto los niveles de PAS y PAD ambulatorios durante un periodo 24 horas como los niveles de PAS y PAD en consulta descendieron significativamente en el grupo DR comparado con el grupo de control simulado tras 2 meses de seguimiento7.
Los registros del mundo real, que han incluido ya a más de 3.500 pacientes tratados mediante DR, han confirmado descensos de los niveles de MAPA y PA en consulta. Algunos, de hecho, han demostrado que la bajada de PA no está asociada a la carga de medicación ni a un mayor número de fármacos antihipertensivos. La DR ha demostrado ser una intervención segura con un índice bajo de complicaciones asociadas a dicha intervención10. El registro GLOBAL SYMPLICITY, con más de 2.900 pacientes, es el análisis más extenso y de mayor duración jamás realizado hasta la fecha sobre DR y confirma el perfil de seguridad y eficacia de la DR en el mundo real10. La tabla 2 del material adicional ofrece un resumen de los distintos registros que existen sobre DR.
Tabla 2. Causas de hipertensión secundaria
| Enfermedades parenquimatosas renales | Glomerulopatías Enfermedad poliquística Tumores renales Uropatía obstructiva |
| Enfermedades renovasculares | Fibrodisplasia Aterosclerosis |
| Enfermedades suprarrenales | Hiperaldosteronismo primario Síndrome de Cushing Déficit de 17-alfa-hidroxilasa Feocromocitoma Aparente exceso de mineralocorticoides |
| Enfermedades vasculares | Coartación aórtica Vasculitis de grandes vasos |
| Enfermedades endocrino-metabólicas | Disfunción tiroidea Hiperparatiroidismo Acromegalia |
| Enfermedades neurológicas | Disautonomía Hipertensión intracraneal Psicogénicas |
| Enfermedades tóxico-farmacológicas | Corticosteroides Fármacos anti-inflamatorios no esteroideos Ciclosporinas Antidepresivos tricíclicos Fármacos anovulatorios Eritropoyetina Regaliz Cocaína Dosis altas de cafeína |
| Enfermedades de origen genético | Formas monogénicas Síndrome de Liddle |
La DR ha demostrado ser una intervención segura. La tasa de incidencia tanto de las complicaciones inmediatas asociadas a la intervención como de las complicaciones renales y vasculares a corto y medio plazo (6-12 meses) es muy baja y se asocia, principalmente, a problemas locales en el sitio de punción; las complicaciones renales graves tales como disección de la arteria renal o estenosis son puramente anecdóticas. La tabla 3 del material adicional recoge los datos de seguridad de los principales ensayos clínicos aleatorizados que suelen tener un seguimiento clínico a corto plazo.
Tabla 3. Precauciones y contraindicaciones de la denervación renal
| • La denervación renal no se ha estudiado en pacientes embarazadas, lactantes, mujeres que desean quedarse embarazadas ni en pacientes con diabetes mellitus tipo I, angioplastia renal previa, stents ureterales permanentes, injertos aórticos o anatomía renal anómala |
| • Sujetos en quienes una bajada de la presión arterial podría ser peligrosa (como, por ejemplo, pacientes con valvulopatías hemodinámicamente significativas) |
| • Tanto los marpacasos implantables como los desfibriladores cardioversores implantables pueden verse afectados por la ablación por radiofrecuencia. Se debe decidir si apagar, o no, el desfibrilador cardioversor implantable durante la ablación, hacer uso de fuentes externas temporales de estimulación y desfibrilación que pueda haber disponibles durante la ablación y realizar un análisis completo de la funcionalidad del dispositivo implantado tras la ablación |
| • Evitar tratar arterias con diámetros < 3 mm o > 8 mm |
| • Evitar tratar arterias con enfermedad significativa u obstrucciones limitantes del flujo |
POSIBLES INDICACIONES PARA LA DENERVACIÓN RENAL CON DATOS DE LOS ÚLTIMOS ESTUDIOS CLÍNICOS REALIZADOS
Los datos tanto de ensayos clínicos aleatorizados como de registros demuestran que la DR reduce la PA de un modo seguro y eficaz, y que esto se observa de manera consistente en diferentes poblaciones (incluidos subgrupos de alto riesgo) y con distintos dispositivos. La sección 3 del material adicional ofrece una revisión de varios documentos de consenso y recomendaciones publicados con anterioridad por diferentes sociedades científicas previo a la publicación de los ensayos clínicos SPYRAL HTN y RANDIANCE-HTN.
La DR puede ser una opción a tener en cuenta en pacientes con HTA resistente (PA > 140/90 mmHg a pesar de cambios en el estilo de vida y de estar a tratamiento con ≥ 3 antihipertensivos en dosis óptimas, uno de los cuales es un diurético o en pacientes con HTA controlada con ≥ 4 fármacos)8. También puede ser una opción en pacientes con HTA no controlada (PA > 140/90 mmHg en pacientes con mala adherencia terapéutica) y alto riesgo cardiovascular.
Denervación renal en pacientes con hipertensión resistente
Los pacientes con HTA-R fueron el primer grupo en quienes se estudió el papel de la DR. El SYMPLICITY HTN-3 no consiguió demostrar una mayor eficacia de la DR frente a la intervención simulada en pacientes con HTA-R3. No obstante, un subsiguiente análisis reveló limitaciones tanto en el diseño como en la ejecución del estudio que arrojan dudas sobre los resultados9. En el estudio RADIANCE-HTN TRIO recientemente publicado, los pacientes con HTA-R bajo tratamiento con un policomprimido triple estandarizado experimentaron bajadas de la PA 2 meses después de la DR comparado con la intervención simulada. Si el efecto reductor de los niveles de PA y la seguridad de la DR se mantienen a largo plazo, la DR podría ser convertirse en una alternativa a la prescripción de más fármacos antihipertensivos en pacientes con HTA-R.
Denervación renal en pacientes con hipertensión no controlada
La nueva evidencia disponible introduce un cambio del paradigma para una técnica que se concibió, originalmente, para el tratamiento de la HTA-R cuando fracasan las demás opciones terapéuticas y que, en la actualidad, es una opción a tener en cuenta en pacientes con PA > 140/90 mmHg a pesar del tratamiento farmacológico.
El concepto de HTA no controlada incluye a un alto porcentaje de pacientes hipertensos (quizá incluso por encima del 60%) con características clínicas y riesgo cardiovascular muy heterogéneos. Dada la naturaleza invasiva de la DR, y en espera de más información sobre la reducción de eventos cardiovasculares en subgrupos de pacientes más específicos, existen varias situaciones de alto riesgo en las que el control de la PA es esencial para minimizar el riesgo de sufrir eventos cardiovasculares:
a) Pacientes con frecuentes crisis hipertensivas. Crisis hipertensivas con valores de PAS > 180 mmHg y/o de PAD > 110 mmHg pueden provocar daños cerebrales, cardiacos o microvasculares. Las visitas a urgencias por crisis hipertensivas superan el 4% de todas las visitas a urgencias11. Aún en ausencia de lesión orgánica mediada por hipertensión arterial (LOMH) los episodios de crisis hipertensivas pueden acarrear implicaciones a largo plazo hasta el punto de que estos pacientes corren un riesgo > 50% de sufrir eventos cardiovasculares comparados con pacientes con hipertensión controlada, a pesar de que fuera de las crisis presenten niveles de PA parecidos12.
b) Pacientes con mala adherencia al tratamiento farmacológico. El tratamiento farmacológico de la HTA suele ser una opción a largo plazo y, en la mayoría de los casos, de por vida. La mala adherencia terapéutica es un problema habitual hasta el punto de que casi un tercio de todos los pacientes hipertensos no empiezan una nueva prescripción de fármacos antihipertensivos13 y alrededor del 50% se vuelven no adherentes al tratamiento durante el primer año después de haberlo iniciado13. En los estudios SPYRAL HTN, En los estudios SPYRAL, la MAPA de 24 horas mostró una disminución de la PA a lo largo de las 24 horas en pacientes tratados con DR frente a no cambios en el grupo control en ausencia de fármacos o control incompleto en presencia de éstos5. Además, en el estudio SPYRAL OFF-MED, el grupo tratado experimentó una reducción promedio de 9,2 mmHg en la PAS clínica. Un meta-análisis de 123 estudios con 613.815 pacientes mostró que una reducción en las cifras de PAS clínica de 10 mmHg se asoció a una disminución en el riesgo de eventos cardiovasculares muy importante: un 17% de reducción en cardiopatía isquémica, un 27% de reducción en ictus, un 28% de reducción en insuficiencia cardiaca y un 13% de reducción en mortalidad cardiovascular14. La mala adherencia al tratamiento sigue siendo un problema grave de salud pública ya que estos pacientes en quienes no se logra controlar la PA adecuadamente, incluso por una mala adherencia terapéutica, tienen un riesgo cardiovascular alto15. No obstante, se debe mencionar que la DR, por sí sola, no puede reducir los niveles de PA lo bastante como para controlar la PA en la mayoría de los pacientes. En el estudio RADIANCE-HTN SOLO, la MAPA durante 24 horas confirmó que solo el 25% de los pacientes tratados con DR alcanzaron valores < 130/80 mmHg6. En estos pacientes no adherentes al tratamiento, la principal fortaleza de la DR radica en su efecto «siempre activo» con independencia de la farmacocinética o de la adherencia a los fármacos.
c) Pacientes con lesión orgánica mediada por hipertensión arterial. La presencia de LOMH identifica a un grupo de pacientes de alto riesgo cardiovascular en quienes el tratamiento convencional no ha logrado evitar el avance de la enfermedad16. Alcanzar los niveles de PA recomendados es muy importante en estos pacientes porque, durante las primeras fases de la enfermedad, algunos tipos de LOMH son reversibles. En las fases más avanzadas de la enfermedad, la LOMH es ya irreversible con independencia de un control adecuado de la PA, pero el control es importante dado que enlentece el avance de la enfermedad al tiempo que reduce el riesgo cardiovascular de estos pacientes de alto riesgo17. Un metanálisis que incluyó a 698 pacientes tratados con DR reveló un efecto independiente de la DR sobre las LOMH, lo cual viene a avalar el uso de la DR en este grupo de pacientes de alto riesgo18.
d) Pacientes de alto riesgo cardiovascular. Las guías europeas sobre el tratamiento de la HTA establecen claramente los factores que influyen sobre el riesgo cardiovascular en pacientes hipertensos, y que comprenden características clínicas (sexo, edad, tabaquismo, antecedentes familiares de enfermedad cardiovascular precoz o factores psicosociales o socioeconómicos), características analíticas (diabetes, niveles de colesterol, niveles de ácido úrico), presencia de DODMH (rigidez arterial, hipertrofia ventricular, microalbuminuria, enfermedad renal, retinopatía) o enfermedad cardiovascular o renal establecidas (enfermedad cerebrovascular, enfermedad arterial coronaria, insuficiencia cardiaca, vasculopatía periférica, fibrilación auricular o presencia de placas de ateroma en técnicas de imagen). Todos estos factores establecen un riesgo cardiovascular a 10 años que se clasifica en 4 grupos: riesgo bajo, moderado, alto o muy alto hasta el punto de que, por ejemplo, en pacientes de alto riesgo, el índice de mortalidad cardiovascular estimado es del 5% y en pacientes de muy alto riesgo está por encima del 10%8. La valoración del riesgo cardiovascular debería jugar un papel esencial en el proceso de toma de decisiones hasta el punto de que cuanto mayor sea el riesgo, mayores beneficios cabe esperar de un mejor control de la PA. Por lo tanto, los pacientes de riesgo alto o muy alto podrían ser candidatos para recibir la DR en aquellos casos en los que el control de la PA no sea el adecuado.
Empoderamiento del paciente hipertenso en un marco de toma de decisiones compartidas
La toma de decisiones compartida ha emergido en los últimos años como el modelo de la toma de decisiones clínicas en distintas patologías. En el campo de la DR, una encuesta reciente reveló que el 38% de los pacientes hipertensos que aún no toman medicación antihipertensiva preferirían la DSRP al tratamiento farmacológico de por vida, incluso sabiendo que ésta probablemente no reemplazará la medicación en muchos casos, pero que de por sí reduce la PA de forma significativa19. Con la evidencia proporcionada en recientes estudios, la DR podría ser una opción de tratamiento válida en pacientes con HTA no controlada y con riesgo cardiovascular alto en los que se consensue con el paciente la indicación. De todos modos, es importante destacar que el tratamiento de la HTA requiere siempre la adopción de unos hábitos de vida saludables, así como que las recomendaciones a los pacientes deben recoger el tratamiento farmacológico como primera opción.
ESTUDIO PREVIO A LA DENERVACIÓN RENAL
Los pacientes deben ser evaluados en una unidad especializada en HTA y riesgo vascular en los 3 meses previos a la intervención en un centro con acreditada experiencia20. La tabla 1 resume los estudios realizados en pacientes candidatos para recibir una DR.
La HTA no controlada se debe confirmar mediante MAPA durante 24 horas21. Tras confirmar la presencia de HTA no controlada, se deben identificar y, en su caso, corregir las situaciones clínicas que aumentan los niveles de PA tales como la obesidad o la apnea obstructiva del sueño. Además, sustancias como la sal o ciertos fármacos que pueden ser desencadenantes de HTA deben suspenderse o minimizarse. La no adherencia al tratamiento, algo muy habitual y que no siempre identifica el propio paciente, si no se investiga rigurosamente, debe descartarse22. Las causas secundarias de HTA (tabla 2) deben estar correctamente identificadas y tratadas, aunque algunas no sean una contraindicación absoluta para la realización de la técnica23.
INTERVENCIÓN DE DENERVACIÓN RENAL CON DISPOSITIVOS DE RADIOFRECUENCIA
La sección 4 del material adicional muestra aspectos los técnicos de la DR en mayor detalle. La figura 1 del material adicional resume la intervención DR.
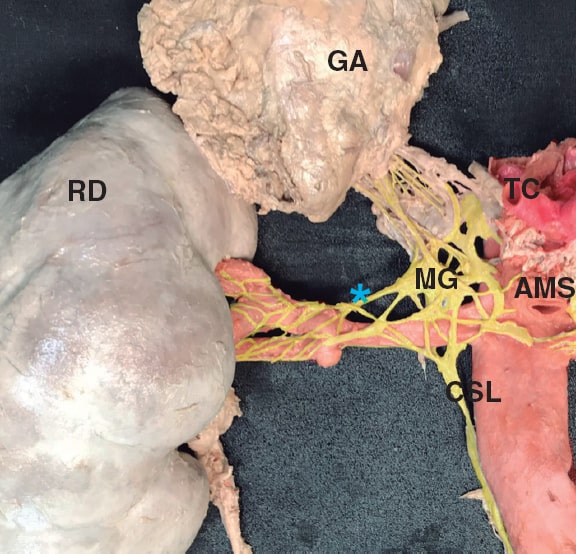
Figura 1. Detalle de inervación simpática renal. Los nervios renales suelen disponerse en grandes haces nerviosos y solo forman un verdadero plexo cuando están próximos a entrar en el riñón. Algunos nervios puentean la arteria renal principal y se unen, distalmente, a las diferentes divisiones arteriales de la arteria renal principal (nervios con llegada tardía). En este caso, se observa un nervio con llegada tardía que se une al tercio proximal de la división anterior de la arteria renal principal (asterisco azul). También se aprecia cómo la arteria renal proximal está ocupada por ganglios fusionados del plexo solar (MG) y por la cadena simpática lumbar (CSL). Ambas estructuras inervan los riñones además de otros órganos abdominales y pélvicos que, accidentalmente, pueden quedar denervados si se trata el tercio proximal de la arteria renal principal. La imagen también muestra que la proximidad máxima de las fibras nerviosas a la pared arterial sobreviene, principalmente, a nivel de las ramas y del tronco principal. Esta será la zona diana para el tratamiento evitando, siempre, la aplicación de radiofrecuencia a nivel de la pelvis renal. AMS: arteria mesentérica superior; CSL: cadena simpática lumbar; GA: glándula adrenal; MG: masa gangliónica formada por los ganglios aórtico-renales y celíacos; RD: riñón derecho; TC: tronco celíaco; asterisco azul: nervio con señal de llegada tardía. En rojo, estructuras arteriales. En amarillo, tejido nervioso.
Conocer mejor la anatomía de los nervios renales24 y el desarrollo de nuevos dispositivos de ablación han optimizado la técnica de tratamiento5,6 que se basa en 3 objetivos principales:
Tratamiento del tronco principal de la arteria renal y ramas accesorias
Contrariamente a lo que se pensaba, es frecuente que los nervios renales lleguen al riñón sin pasar por la arteria renal principal. Con la capacidad de penetración de los dispositivos de DR actuales (4-6 mm con la radiofrecuencia y 7,5 mm con el ultrasonido), la presencia de estos nervios con llegada tardía implica que no se consigue una denervación completa si solo se aplican en la arteria renal principal24. En el modelo animal se ha comprobado además que la aplicación de radiofrecuencia combinada en el tronco principal y en las ramas de la arteria renal produce una mayor disminución del contenido tisular renal de norepinefrina, así como de la densidad axonal cortical, ambos relacionados con la respuesta a DR25.
En pacientes tratados con DR, la presencia de arterias accesorias no tratadas acarrea una menor respuesta hipotensiva26. Su identificación y tratamiento es fundamental y, en caso de que por diámetro sean susceptibles de tratamiento (diámetro mínimo de 3 mm), recomendamos el tratamiento de arterias polares.
Por último, el espacio perivascular que rodea al ostium y al tercio proximal de la arteria renal principal suele estar ocupado por ganglios del plexo solar y por la cadena simpática lumbar (figura 1). Ambos inervan los riñones, pero también otros órganos abdominales y pélvicos que se podrían denervar accidentalmente si el tratamiento se aplica al ostium y al tercio proximal de la arteria renal principal. Por lo tanto, hasta que no tengamos más información al respecto, parece razonable ser cautos a la hora de tratar la porción más ostial de las arterias renales24.
Tratamiento de los 4 cuadrantes de la arteria renal
La distribución de fibras nerviosas alrededor de la arteria renal sigue un patrón diferente en cada individuo27. Estudios preclínicos realizados en un modelo porcino demuestran que la aplicación de radiofrecuencia en un punto determinado tiene efectos en, aproximadamente, el 25% de la circunferencia radial27 y que las intervenciones que emplean múltiples ablaciones helicoidales escalonadas en los 4 cuadrantes son más eficaces para disminuir el contenido tisular renal de norepinefrina28.
Aplicación del máximo número posible de puntos de ablación
En un análisis post hoc del estudio SYMPLICITY HTN-3 se observó que los pacientes con un mayor número de aplicaciones de radiofrecuencia presentaban una mayor disminución de las cifras de PA, sin que esto se asociara a efectos adversos9. Se recomienda aplicar el número máximo de puntos de ablación que sea posible respetando, siempre, una distancia de 5 mm entre ellos y una distribución en 4 cuadrantes.
La sección 4 del material adicional muestra cómo realizar una DR empleando un catéter de radiofrecuencia tetrapolar. La tabla 3 muestra las precauciones y contraindicaciones en torno a la intervención DR.
Cuidados tras una intervención de denervación renal
Tras finalizar la intervención, es importante asegurar una hemostasia adecuada en la punción femoral. Normalmente, si no hay complicaciones, los pacientes suelen ser dados de alta entre 24 y 48 horas después de la intervención con el mismo tratamiento antihipertensivo que seguían antes de ser intervenidos, o bien, con ajustes de este en casos que responden inmediatamente. En cualquier caso, con citas médicas para ajustar el tratamiento entre 5 y 7 días después de la intervención. Cabe destacar que los efectos de esta pueden tardar semanas en verse29.
TRATAMIENTO CLÍNICO TRAS DENERVACIÓN RENAL
El principal objetivo del seguimiento debe ser confirmar el perfil de seguridad de la intervención, la ausencia de complicaciones a corto, medio y largo plazo y monitorizar la evolución tanto de los niveles de PA como de los ajustes del tratamiento farmacológico.
Durante el seguimiento clínico es importante contar con un equipo multidisciplinario igual que durante la selección de los candidatos. La tabla 4 muestra el tratamiento clínico tras una DR.
Tabla 4. Tratamiento clínico tras denervación renal*
| Control de la presión arterial |
| Se recomienda medir los valores de presión arterial en el domicilio para comprobar las bajadas de presión arterial |
| Se debe formar a los pacientes en la detección de síntomas de hipotensión |
| Se debe llevar a cabo una desescalada farmacológica, cuando sea necesaria |
| Se debe realizar una monitorización ambulatoria de la presión arterial durante un periodo 24 horas entre 3 y 6 meses después de la intervención para valorar la respuesta a la DR |
| Se debe realizar una monitorización ambulatoria de la presión arterial durante un periodo de 24 horas para valorar la durabilidad a largo plazo de la denervación renal |
| Función renal: los pacientes en riesgo de nefropatía por contraste deben controlarse después de 7-10 días (de forma individualizada y atendiendo a criterios clínicos) |
| No se recomienda la realización rutinaria de técnicas de imagen renal (ecocardiografía, tomografía computarizada o resonancia magnética) tras la intervención |
|
* El control tras la denervación renal se debe llevar a cabo en una unidad especializada en el tratamiento de la hipertensión como parte de un programa regulado de denervación renal. |
REQUISITOS DE UN PROGRAMA DE DENERVACIÓN RENAL
El éxito de un programa de DR se fundamenta en la existencia de un equipo multidisciplinario que realice una valoración integral del paciente, desde la selección de candidatos, pasando por la valoración previa a la intervención, el procedimiento de DR y el seguimiento posterior. Este proceso se debe llevar a cabo en unidades específicas especializadas en el tratamiento de la HTA y en colaboración con unidades de cardiología intervencionista. La figura 2 muestra el proceso de selección de los pacientes aptos.
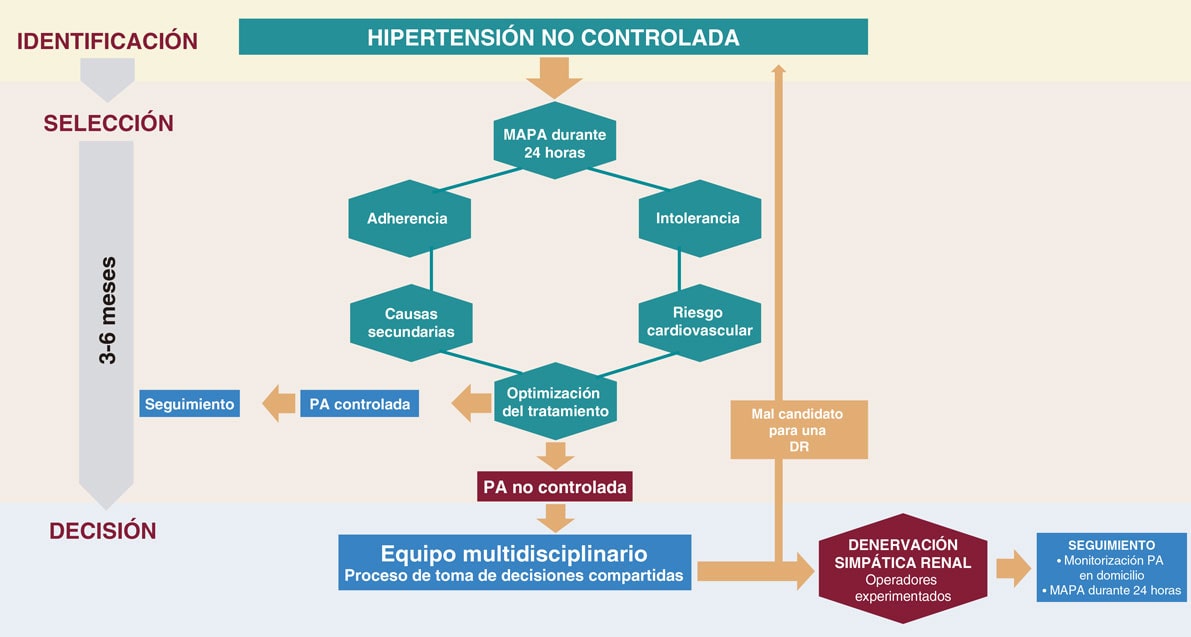
Figura 2. Proceso de identificación, selección de pacientes y toma de decisiones sobre una DR. Los pacientes con HTA no controlada (PA > 140/90 mmHg a pesar del tratamiento) deberán ser valorados en una Unidad de HTA. Se deberá confirmar la falta de control mediante MAPA, valorar la adherencia/intolerancia a fármacos, descartar causas secundarias y el riesgo cardiovascular. Si tras la optimización del tratamiento persiste la falta de control, en pacientes con riesgo elevado o muy elevado, y de forma consensuada con el paciente, se puede indicar la realización de DR. La adherencia se define como el grado en que la conducta de una persona, a tratamiento, a dieta o inmerso en un proceso de cambio de hábitos de vida, es consistente con una serie de recomendaciones dadas por un profesional sanitario. La intolerancia farmacológica se define como la incapacidad de tolerar los efectos adversos de una medicación, a menudo en dosis terapéuticas o sub-terapéuticas. La optimización del tratamiento se refiere a los cambios en los hábitos de vida y a las recomendaciones farmacológicas, incluidas las dosis diana, recomendados por las guías de práctica clínica8. DR: denervación renal; MAPA, monitorización ambulatoria de la presión arterial; PA: presión arterial.
Se desaconseja encarecidamente realizar intervenciones aisladas fuera de un entorno controlado. Una DR no debería realizarse en centros con volúmenes < 10 casos/año. Aquellos centros que no cuenten con un programa DR bien organizado, pero sí con pacientes candidatos a esta intervención, deberían derivarlos a un centro experimentado y evitar realizar intervenciones aisladas.
Las DR deben realizarlas operadores experimentados en el manejo de tratamientos endovasculares. El análisis post hoc del estudio SYMPLICITY HTN-3 mostró la importancia de la ejecución de la intervención en el resultado final de la misma, y uno de los factores que influyó de forma notable en los resultados negativos del estudio fue la falta de experiencia del operador9. Este hecho nos lleva a recomendar que los procedimientos se realicen únicamente en centros con acreditada experiencia y que, en aquellos centros que carezcan de experiencia, haya la posibilidad de una monitorización de la indicación, así como de «proctorización» de la selección del paciente y de la realización del procedimiento hasta que se alcance una experiencia suficiente que asegure un resultado óptimo.
CONCLUSIONES
Este documento de consenso elaborado por expertos ha revisado la información disponible en torno a la DR para el tratamiento de pacientes con HTA. También ha establecido, por primera vez, una indicación para la DR en casos de HTA no controlada, especialmente en pacientes de alto riesgo cardiovascular con LOMH o enfermedad cardiovascular, teniendo en cuenta la opinión del paciente dentro de un proceso de toma de decisiones compartida y siempre que ésta se realice dentro de un equipo multidisciplinario y se lleve a cabo por operadores con experiencia.
FINANCIACIÓN
Ninguna.
CONTRIBUCIÓN DE LOS AUTORES
Idea del estudio y diseño: O. Rodríguez-Leor y J.A. García-Donaire; redacción del manuscrito: O. Rodríguez-Leor, F. Jaén-Águila, J. Segura, I. J. Nuñez-Gil, A. García-Touchard, E. Rubio, M. Troya, J. Diego-Mediavilla y J.A. García-Donaire; revisión crítica: O. Rodríguez-Leor, Á. Cequier, R. Moreno, N. Martell, P. Beltrán y E. Molina.
CONFLICTO DE INTERESES
O. Rodríguez-Leor y J. A. García-Donaire han declarado haber recibido honorarios de Medtronic fuera del ámbito de este estudio. A. García-Touchard ha declarado haber recibido subvenciones de Medtronic y honorarios de Medtronic, también, fuera del ámbito de este estudio. Á. Cequier ha declarado haber recibido subvenciones y honorarios de Abbott Vascular, subvenciones y honorarios de Biosensors, subvenciones de Boston Scientific, subvenciones y honorarios de Medtronic, subvenciones de Biomenco, Cordis, Orbus Neich, así como de la Sociedad Española de Cardiología; también ha declarado haber recibido honorarios de Ferrer International, Terumo, Astra Zeneca y Biotronik aunque, siempre, fuera del ámbito de este estudio. R. Moreno es editor asociado de REC: Interventional Cardiology. Se ha seguido el procedimiento editorial establecido en la revista para garantizar la gestión imparcial del manuscrito. F. Jaén-Águila, J. Segura, I. J. Núñez-Gil, E. Rubio, M. Troya, J. Diego-Mediavilla, R. Moreno, N. Martell, P. Beltrán y E. Molina no han declarado ningún conflicto de intereses relevante en relación a este estudio.
BIBLIOGRAFÍA
1. Krum H, Schlaich M, Whitbourn R, et al. Catheter-based renal sympathetic denervation for resistant hypertension:a multicentre safety and proof-of-concept cohort study. Lancet 2009;373:1275-1281.
2. Esler MD, Krum H, Sobotka PA, Schlaich MP, Schmieder RE, Böhm M. Renal sympathetic denervation in patients with treatment-resistant hypertension (The Symplicity HTN-2 Trial):a randomised controlled trial. Lancet. 2010;376:1903-1909.
3. Bhatt DL, Kandzari DE, O'Neill WW, et al. A controlled trial of renal denervation for resistant hypertension. N Engl J Med. 2014;370:1393-1401.
4. Kandzari DE, Böhm M, Mahfoud F, et al. Effect of renal denervation on blood pressure in the presence of antihypertensive drugs:6-month efficacy and safety results from the SPYRAL HTN-ON MED proof-of-concept randomised trial. Lancet. 2018;391:2346-2355.
5. Böhm M, Kario K, Kandzari DE, et al. Efficacy of catheter-based renal denervation in the absence of antihypertensive medications (SPYRAL HTN-OFF MED Pivotal):a multicentre, randomised, sham-controlled trial. Lancet. 2020;395:1444-1451.
6. Azizi M, Schmieder RE, Mahfoud F, et al. Endovascular ultrasound renal denervation to treat hypertension (RADIANCE HTN-SOLO):a multicentre, international, single-blind, randomised, sham controlled trial. Lancet. 2018;391:2335-2345.
7. Azizi M, Sanghvi K, Saxena M, et al. Ultrasound renal denervation for hypertension resistant to a triple medication pill (RADIANCE-HTN TRIO):a randomised, multicentre, single-blind, sham-controlled trial. Lancet. 2021;397:2476-2486.
8. Williams B, Mancia G, Spiering W, et al. 2018 Practice Guidelines for the management of arterial hypertension of the European Society of Hypertension and the European Society of Cardiology:ESH/ESC Task Force for the Management of Arterial Hypertension. Eur Heart J. 2018;39:3021-3104.
9. Kandzari DE, Bhatt DL, Brar S, et al. Predictors of blood pressure response in the Symplicity HTN-3 trial. Eur Heart J. 2015;36:219-227.
10. Mahfoud F, Böhm M, Schmieder R, et al. Effects of renal denervation on kidney function and long-term outcomes:3-year follow-up from the Global SYMPLICITY Registry. Eur Heart J. 2019;40:3474–3482.
11. Janke AT, McNaughton CD, Brody AM, Welch RD, Levy PD. Trends in the incidence of hypertensive emergencies in US emergency departments from 2006 to 2013. J Am Heart Assoc. 2016;5:e004511.
12. Vleck M, Bur A, Woisetschläger C, Herkner H, Laggner AN, Hirschl MM. Association between hypertensive urgencies and subsequent cardiovascular events in patients with hypertension. J Hypertens. 2008;26:657-662.
13. Fischer MA, Stedman MR, Lii J, et al. Primary medication non-adherence:analysis of 195,930 electronic prescriptions. J Gen Intern Med. 2010;25:284-290.
14. Ettehad D, Emdin CA, Kiran A, et al. Blood pressure lowering for prevention of cardiovascular disease and death:a systematic review and meta-analysis. Lancet. 2016;387:957-967.
15. Gupta P, Patel P, Strauch B, et al. Risk factors for nonadherence to antihypertensive treatment. Hypertension. 2017;69:1113-1120.
16. Cordero A, Morillas P, Bertomeu-Gonzalez V, et al. Prevalence of Peripheral Arterial Disease in Patients with Acute Coronary Syndrome Investigators. Clustering of target organ damage increases mortality after acute coronary syndromes in patients with arterial hypertension. J Hum Hypertens. 2011;25:600-607.
17. Lonnebakken MT, Izzo R, Mancusi C, et al. Left ventricular hypertrophy regression during antihypertensive treatment in an outpatient clinic (the Campania Salute Network). J Am Heart Assoc. 2017;6:e004152.
18. Kordalis A, Tsiachris D, Pietri P, et al. Regression of organ damage following renal denervation in resistant hypertension:a meta-analysis. J Hypertens. 2018;36:1614-1621.
19. Schmeider RE, Hogerl K, Jung S, Bramlage P, Veelken R, Ott C. Patient preference for therapies in hypertension:a cross-sectional survey of German patients. Clin Res Cardiol. 2019;108:1331-1342.
20. Schmieder RE, Redon J, Grassi G, et al. ESH Position Paper:Renal denervation - an interventional therapy of resistant hypertension. J Hypertens. 2012;30:837-841.
21. Banegas JR, Messerli FH, Waeber B, et al. Discrepancies between office and ambulatory blood pressure:clinical implications. Am J Med. 2009;122:1136-1141.
22. Burnier M, Wuerzner G, Struijker-Boudier H, Urquhart J. Measuring, analyzing, and managing drug adherence in resistant hypertension. Hypertension. 2013;62:218-225.
23. Rimoldi SF, Scherrer U, Messerli FH. Secondary arterial hypertension:when, who, and how to screen?Eur Heart J. 2014;35:1245-1254.
24. García-Touchard A, Maranillo E, Mompeo B, Sañudo JR. Microdissection of the Human Renal Nervous System:Implications for Performing Renal Denervation Procedures. Hypertension. 2020;76:1240-1246.
25. Mahfoud F, Tunev S, Ewen S, et al. Impact of lesion placement on efficacy and safety of catheter-based radiofrequency renal denervation. J Am Coll Cardiol. 2015;66:1766-1775.
26. Id D, Kaltenbach B, Bertog SC, et al. Does the presence of accessory renal arteries affect the efficacy of renal denervation?JACC Cardiovasc Interv. 2013;6:1085-1091.
27. Tzafriri AR, Mahfoud F, Keating JH, et al. Procedural and anatomical determinants of multi-electrode renal denervation efficacy –Insights from preclinical models. Hypertension. 2019;74:546-554.
28. Tzafriri AR, Mahfoud F, Keating JH, et al Innervations patterns may limit response to endovascular renal denervation. J Am Coll Cardiol. 2014;64:1079-1087.
29. Fink G, Phelps JT. Can we predict the blood pressure response to renal denervation?Auton Neurosci. 2017;204:112-118.