Sr. Editor:
La angioplastia con balón farmacoactivo (BFA) se ha asociado al agrandamiento tardío de la luz (ATL), un fenómeno que provoca que las dimensiones del vaso aumenten con el paso del tiempo en ausencia de un armazón permanente1. Aunque esta observación angiográfica está bien documentada, la evolución temporal de la fisiología coronaria tras el tratamiento con BFA no está caracterizada del todo. Estudios publicados revelan que la reserva fraccional de flujo mejora desde los valores basales hasta el posoperatorio y se mantiene estable durante el seguimiento2,3; no obstante, la mejoría funcional evaluada de forma pareada desde el posoperatorio hasta el seguimiento no se ha documentado específicamente. Por eso, se realizó una evaluación temporal de forma pareada de la ganancia funcional tardía (GFT), definida como la mejoría fisiológica progresiva que ocurre tras la finalización la intervención inicial, en pacientes sometidos a angioplastia con BFA por lesiones coronarias de novo.
El presente estudio analizó pacientes consecutivos sometidos a tratamiento con BFA por lesiones coronarias de novo entre enero de 2018 y diciembre de 2024 del registro prospectivo y unicéntrico CARDIO-FR (NCT04185285), que incluyó sistemáticamente a todos los pacientes consecutivos sometidos a intervención coronaria percutánea en el Hospital & University Fribourg. El protocolo del estudio fue aprobado por el comité ético local y se llevó a cabo de conformidad con los principios establecidos en la Declaración de Helsinki. Se obtuvo el consentimiento informado por escrito de todos los pacientes. Los pacientes elegibles tenían ≥ 18 años y disponían de angiografías coronarias basales, posoperatorias y de seguimiento realizadas ≥ 7 días tras la intervención inicial, con una calidad de imagen adecuada para analizar el cociente de flujo cuantitativo basado en la ley de Murray (µCFC) en todos los tiempos del estudio. La angiografía de seguimiento no formaba parte del protocolo del registro CARDIO-FR; no obstante, para el presente análisis, solo se incluyeron pacientes con angiografías de seguimiento tras la angioplastia con BFA. Dos analistas independientes cegados mediante AngioPlus Gallery (Pulse Medical Imaging Technology, China) realizaron el estudio del µCFC. Para cada lesión, se seleccionó la proyección angiográfica que mejor mostrara el vaso desde el ostium coronario hasta el segmento distal, con minimización de la superposición y acortamiento. Se empleó la misma proyección para el estudio del µCFC en los 3 momentos a fin de asegurar la reproducibilidad. Se excluyeron todas aquellas lesiones cuya calidad de imagen fuera inadecuada o cuyas proyecciones no se pudiesen emparejar en diferentes momentos del estudio. Las intervenciones con los BFA siguieron protocolos institucionales estandarizados, con preparación de la lesión a criterio del operador. Los análisis estadísticos incluyeron pruebas pareadas para comparaciones temporales y análisis de regresión para la identificación de predictores de mejoría funcional.
Entre el 1 de enero de 2018 y el 31 de diciembre de 2024, se incluyó a un total de 4.725 pacientes en el registro, 120 de los cuales fueron sometidos a intervención coronaria percutánea solo con BFA para el tratamiento de lesiones coronarias de novo. De estos, 59 pacientes (66 lesiones) cumplieron todos los criterios de inclusión y fueron incluidos en el análisis. Se analizaron 132 angiogramas de estos 59 pacientes (edad = 70 ± 8 años; 22%, mujeres; 37%, diabéticos) con 66 lesiones de novo (diámetro de referencia del vaso = 2,5 [rango intercuartílico (RIC) = 1,8-2,8] mm). En la preparación de la lesión se emplearon balones semidistensibles (88%), no distensibles (62%), de tallado (28,8%) y litotricia intravascular (5,1%). Las plataformas BFA incluyeron SELUTION SLR (M.A. Med Alliance, Irlanda; n = 46, 78,0%, recubierto de sirolimus), Prevail (Medtronic, Estados Unidos; n = 10, 16,9%, recubierto de paclitaxel), MagicTouch (Concept Medical, Estados Unidos; n = 2, 3,4%, recubierto de sirolimus) y AGENT BFA (Boston Scientific, Estados Unidos; n = 1, 1,7%, recubierto de paclitaxel). El seguimiento angiográfico mediano de 8,5 meses [RIC = 6,2-12,3 meses] confirmó la revascularización de la lesión diana (RLD) en 14 (21,2%) de las 66 lesiones. El µCFC mejoró significativamente de 0,88 ± 0,08 a nivel basal a 0,90 ± 0,07 durante el seguimiento (+ 0,02; IC95%, 0,00-0,04; p = 0,007). El diámetro luminal mínimo aumentó de 1,68 ± 0,40 a 1,78 ± 0,40 mm (+ 0,09 mm; IC95%, 0,01-0,18; p = 0,036) (figura 1). Las trayectorias fisiológicas fueron heterogéneas, con mejoría funcional observada predominantemente en lesiones sin RLD. Tras excluir la RLD, la GFT fue aún más pronunciada con + 0,04 (IC95%, 0,01-0,06; p < 0,001) y un aumento del diámetro luminal mínimo de + 0,05 mm (IC95%, 0,01-0,18; p = 0,034).
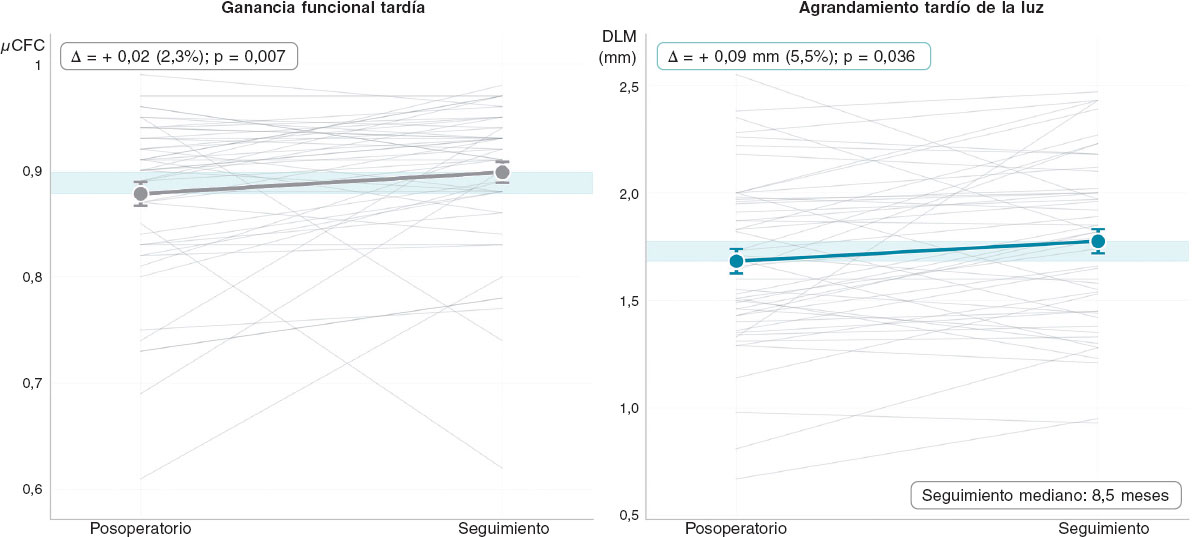
Figura 1. Análisis pareado del diámetro luminal mínimo y cociente de flujo cuantitativo basado en la ley de Murray desde el posoperatorio hasta el seguimiento (n = 66 lesiones pareadas). Las trayectorias de cada paciente se muestran en líneas grises y los valores medios en barras de error estándar en gris (GFT, izquierda) y verde (ATL, derecha). Se muestran los cambios absolutos y relativos. ATL: agrandamiento tardío de la luz; GFT: ganancia funcional tardía; μCFC: cociente de flujo cuantitativo basado en la ley de Murray.
Una ratio más alta diámetro BFA-vaso y un mayor tiempo de inflado fueron predictores de mejoría funcional (+ 0,01 por cada incremento de 0,1 en la ratio; p = 0,015; + 0,0041 por segundo; p = 0,011; respectivamente). La ratio máxima diámetro-vaso durante la predilatación fue el predictor binario más potente (odds ratio [OR] = 17,23; p = 0,006), seguido de la ratio máxima diámetro BFA-vaso (OR = 14,38; p = 0,011). Se identificaron umbrales exploratorios en la ratio balón-vaso > 1,31 (IC95%, 1,03-1,45) y un tiempo de inflado > 72 segundos, ambos asociados a una mayor ganancia funcional (+ 0,05 frente a + 0,02; p = 0,012; + 0,04 frente a + 0,02; p = 0,008, respectivamente). Las características de preparación de la lesión más allá de la ratio diámetro-vaso, incluido el tipo de balón especializado, no tuvieron un valor predictivo para la mejoría funcional (todos p > 0,20). En cuanto al ATL, solo el tiempo de inflado del BFA predijo el agrandamiento (+ 0,011 mm por segundo; p = 0,015). El uso de balones liberadores de sirolimus mostró una tendencia hacia una menor probabilidad de ganancia luminal (OR = 0,22; IC95%, 0,04-1,10; p = 0,07).
Este estudio exploratorio presenta una evaluación temporal de forma pareada del µCFC de la GFT tras angioplastia con BFA que sugiere una mejoría fisiológica coronaria progresiva desde el inicio del posoperatorio hasta el seguimiento a medio plazo en lesiones sin revascularización. La GFT se refiere a la recuperación funcional continua más allá del resultado agudo de la intervención, conceptualmente distinta pero complementaria al fenómeno angiográfico establecido del ATL1. Aunque la asociación temporal entre el ATL anatómico y la mejoría funcional sugiere la existencia de una posible relación mecanística, el diseño observacional no permite establecer inferencias causales definitivas. Evaluaciones fisiológicas previas con el µCFC en el ensayo PICCOLETO II mostraron un rendimiento funcional parecido entre el BFA y stents farmacoactivos en el seguimiento, con recuperación funcional relativa en el grupo BFA a lo largo del tiempo4. Datos recientes también han descrito trayectorias fisiológicas tardías heterogéneas tras tratamiento con BFA, incluido el deterioro tardío del CFC en un subgrupo de pacientes5. Nuestros hallazgos amplían estas observaciones al identificar determinantes operatorios asociados a la mejoría funcional en un diseño pareado intraindividuo. Esta observación generadora de hipótesis aporta información adicional sobre los efectos biológicos del tratamiento con BFA y sugiere que la cicatrización vascular podría continuar más allá de la intervención inicial6. A diferencia de los stents farmacoactivos, donde la reserva fraccional de flujo puede deteriorarse con el paso tiempo y de la angioplastia con balón simple, que suele asociarse a deterioro funcional, el tratamiento con BFA podría fomentar una mejoría fisiológica progresiva, potencialmente a través de efectos antiproliferativos, remodelado positivo del vaso1 y restauración de la función endotelial.
Nuestros hallazgos identifican 2 determinantes operatorios asociados a la mejoría funcional. En primer lugar, una preparación adecuada de la lesión induce la disrupción de la placa y facilita la penetración óptima del fármaco en la pared vascular. En segundo lugar, una administración optimizada del BFA mediante un dimensionamiento adecuado e inflado prolongado, proporciona soporte mecánico que previene el recoil y estabiliza los planos de disección, evitando así tener que implantar un stent de rescate. Aunque la transferencia del fármaco desde un balón liberador de sirolimus dura unos 30-45 segundos, el inflado prolongado probablemente aporte un beneficio mecánico adicional más allá de la propia liberación del fármaco. El consenso actual recomienda dimensionar el BFA a una ratio balón-vaso de 0,9-1,36. Nuestros resultados sugieren que ratios en un rango superior podrían asociarse a una mayor ganancia funcional; no obstante, estos hallazgos siguen siendo exploratorios y deben individualizarse según la anatomía de cada vaso, las características de la lesión y la experiencia del operador.
Son varias las limitaciones a tener en cuenta. El diseño observacional unicéntrico y el tamaño muestral modesto del estudio limitan la extrapolación de estos hallazgos, que deben considerarse generadores de hipótesis. En segundo lugar, la cohorte incluyó plataformas BFA heterogéneas con diferentes recubrimientos farmacológicos, lo cual impide poder extraer conclusiones sobre efectos de clase. La tendencia observada hacia una menor probabilidad de ATL con balones liberadores de sirolimus podría responder a diferencias específicas del dispositivo en la formulación del fármaco, tecnología de recubrimiento o cinética de liberación, más que a un verdadero efecto de clase. Como no se ha establecido un efecto de clase entre los BFA, se recomienda cautela a la hora de extrapolar estos resultados; además, los análisis específicos por dispositivo se vieron limitados por el pequeño tamaño muestral. En tercer lugar, la ausencia de un laboratorio central independiente de imagen podría haber introducido variabilidad tanto en la adquisición de imágenes como en el análisis del µCFC. En cuarto lugar, la tasa observada de RLD supera las tasas descritas habitualmente en ensayos clínicos aleatorizados con BFA, lo cual probablemente sea reflejo de los criterios de inclusión del estudio y limite la extrapolación de los hallazgos fisiológicos observados. Por último, como la angiografía de seguimiento no estaba incluida en el protocolo, el estudio introduce un sesgo de selección inherente hacia individuos con indicaciones clínica de nueva imagen, lo cual resulta en indicaciones clínicas heterogéneas y tiempos de seguimiento variables.
En conclusión, este estudio aporta evidencia de la GFT evaluada mediante µCFC y sugiere una mejoría fisiológica progresiva desde el posoperatorio hasta el seguimiento a medio plazo tras angioplastia con BFA.
FINANCIACIÓN
Este estudio fue financiado por el Fonds Scientifique Cardiovasculaire y Fondation Cecil de Recherche Cardiovasculaire.
CONSIDERACIONES ÉTICAS
Este estudio se llevó a cabo de conformidad con los principios establecidos en la Declaración de Helsinki y fue aprobado por el comité ético local (análisis del registro CARDIO-FR, identificador ClinicalTrials.gov: NCT04185285). Se obtuvo el consentimiento informado por escrito de todos los pacientes participantes previo a su inclusión en el estudio. Se tuvieron en cuenta las guías SAGER durante el diseño, análisis y presentación del estudio. No obstante, no se realizaron análisis por subgrupos según sexo y género debido al tamaño muestral limitado, que impidió realizar comparaciones significativas. La distribución por sexo y género de los participantes se presenta en las características basales.
DECLARACIÓN SOBRE EL USO DE INTELIGENCIA ARTIFICIAL
Se utilizaron herramientas basadas en inteligencia artificial únicamente para la corrección del idioma inglés durante la preparación de este manuscrito. Todos los aspectos del estudio, incluida la concepción, diseño, recogida de datos, análisis, interpretación de resultados y redacción del manuscrito, fueron realizados íntegramente por los autores sin la asistencia de inteligencia artificial. Los autores asumen plena responsabilidad tanto sobre el contenido como sobre la integridad del trabajo.
CONTRIBUCIÓN DE LOS AUTORES
D. Garin concibió y diseñó el estudio. D. Garin y R. Mohand Saidi realizaron la recogida de datos, el análisis de datos y redactaron el manuscrito. J.F. Iglesias y C. Seydoux contribuyeron a la interpretación de los datos y revisaron críticamente el manuscrito por su contenido intelectual relevante. M. Togni y S. Cook proporcionaron supervisión senior, contribuyeron al diseño del estudio y revisaron críticamente el manuscrito. D. Garin supervisó el proyecto global, contribuyó a la interpretación de los datos y realizó la revisión crítica del manuscrito. Todos los autores leyeron y aprobaron la versión final del manuscrito.
CONFLICTO DE INTERESES
J.F. Iglesias declara haber recibido honorarios como conferenciante o asesor de Abbott Vascular, Biotronik, Biosensors, Bristol Myers Squibb/Pfizer, Cordis, Concept Medical, Medtronic, Penumbra Inc. y ReCor Medical y consultor de Biotronik, ReCor Medical, Cordis y Medtronic. El centro de J.F. Iglesias recibió fondos de investigación ilimitados de Biotronik, Concept Medical, Terumo Corp. y SMT. Ninguna de estas relaciones influyó en el diseño, realización o comunicación de esta investigación. El resto de los autores no declaró ningún conflicto de intereses.
BIBLIOGRAFÍA
1. Kleber FX, Schulz A, Waliszewski M, et al. Local paclitaxel induces late lumen enlargement in coronary arteries after balloon angioplasty. Clin Res Cardiol. 2015;104:217-225.
2. Ann SH, Balbir Singh G, Lim KH, et al. Anatomical and physiological changes after paclitaxel-coated balloon for atherosclerotic de novo coronary lesions:Serial IVUS-VH and FFR study. PLoS One. 2016;11:0147057.
3. Shin E-S, Bang LJ, Jun EJ, et al. Fractional flow reserve-guided coronary angioplasty using paclitaxel-coated balloons without stent implantation:Feasibility, safety and 6-month results by angiography and optical coherence tomography. EuroIntervention. 2016;12:1004-1014.
4. Fezzi S, Trevisanello A, Buccheri D, et al. Physiological performance of drug-coated balloons in small coronary arteries PICCOLETO II µFR. Catheter Cardiovasc Interv. 2025;105:643-649.
5. Zhu Y, Hu T, Bian Q, et al. Predictors for quantitative flow ratio loss in patients with de novo coronary artery disease treated with drug-coated balloons. Scientific Reports. 2025;15:21479.
6. Fezzi S, Scheller B, Cortese B, et al. Definitions and standardized endpoints for the use of drug-coated balloon in coronary artery disease:Consensus document of the Drug Coated Balloon Academic Research Consortium. Eur Heart J. 2025;46:2498-2519.

