RESUMEN
Introducción y objetivos: Esta revisión sistemática con metanálisis evalúa si una estrategia de intervención coronaria percutánea (ICP) multivaso por etapas o inmediata proporciona resultados clínicos superiores en pacientes hemodinámicamente estables con infarto agudo de miocardio con elevación del segmento ST y enfermedad coronaria multivaso sometidos a revascularización de lesiones no culpables.
Métodos: Se realizaron búsquedas en PubMed, Embase y Cochrane hasta septiembre de 2025 según las directrices PRISMA. Los resultados incluyeron muerte por causa cardiaca, muerte por cualquier causa, reinfarto, lesión renal aguda y accidente vascular cerebral. Se estimaron los riesgos relativos y se realizó un análisis secuencial de ensayos en desenlaces seleccionados. Además, se calcularon las tasas de incidencia relativa (IRR) y se realizó una metarregresión.
Resultados: Se incluyeron 6 ensayos clínicos aleatorizados con 4.267 pacientes. En el seguimiento al año no se encontraron diferencias significativas entre la ICP por etapas y la inmediata en el riesgo de muerte por causa cardiaca (RR = 1,26; IC95%, 0,89-1,79), muerte por cualquier causa (RR = 1,18; IC95%, 0,93-1,50), lesión renal aguda (RR = 0,91; IC95%, 0,64-1,31) o accidente vascular cerebral (RR = 1,17; IC95%, 0,66-2,05). La ICP inmediata se asoció con un menor riesgo de reinfarto (RR = 0,63; IC95%, 0,40-0,98), confirmado por el análisis de tasa de incidencia relativa (IRR = 0,60; IC95%, 0,39-0,94; I² = 0%). La metarregresión no mostró asociación significativa entre el riesgo de reinfarto y el momento de la ICP por etapas o la comorbilidad basal.
Conclusiones: La ICP inmediata en pacientes con infarto agudo de miocardio con elevación del segmento ST y enfermedad multivaso se asoció con un menor riesgo de reinfarto, sin diferencias significativas en la mortalidad por causa cardiaca ni en la mortalidad por cualquier causa frente a la ICP por etapas. Aunque el análisis secuencial de ensayos indicó que la evidencia actual aún carece de suficiente poder estadístico, la consistencia en la dirección del efecto a través de múltiples enfoques analíticos respalda la seguridad y la posible ventaja clínica de la revascularización completa inmediata, lo que justifica su confirmación en futuros ensayos aleatorizados adecuadamente dimensionados. (PROSPERO: CRD42023485163.I).
Palabras clave: Enfermedad coronaria. Infarto agudo de miocardio con elevación del segmento ST. Enfermedad multivaso. Intervención coronaria percutánea inmediata. Intervención coronaria percutánea por etapas.
ABSTRACT
Introduction and objectives: To compare clinical outcomes of immediate vs staged multivessel percutaneous coronary intervention (PCI) for non-culprit lesions in hemodynamically stable patients with ST-segment elevation myocardial infarction and multivessel coronary artery disease.
Methods: We conducted this systematic review and meta-analysis according to PRISMA guidelines. PubMed, Embase, and Cochrane databases were searched throughout September 2025. Outcomes included cardiac death, all-cause mortality, reinfarction, acute kidney injury, and stroke. Risk ratios were calculated, and trial sequential analysis, incidence rate ratio (IRR) analyses, and meta-regression were conducted.
Results: Six randomized controlled trials including 4267 patients were analyzed. At the 1-year follow-up, there were no significant differences between immediate and staged PCI regarding cardiac death (RR, 1.26; 95%CI, 0.89-1.79), all-cause mortality (RR, 1.18; 95%CI, 0.93-1.50), acute kidney injury (RR, 0.91; 95%CI, 0.64-1.31), or stroke (RR, 1.17; 95%CI, 0.66-2.05). Immediate PCI was associated with a lower risk of reinfarction (RR, 0.63; 95%CI, 0.40-0.98), a finding confirmed by IRR analysis (IRR, 0.60; 95%CI, 0.39-0.94; I2 = 0%). Exploratory meta-regression analyses did not identify procedural timing or baseline comorbidities as significant effect modifiers.
Conclusions: In patients with ST-segment elevation myocardial infarction and multivessel disease, immediate PCI was associated with a lower risk of reinfarction, without any significant differences being reported in cardiac death or all-cause mortality compared with staged PCI. Although trial sequential analysis indicates that current evidence remains underpowered for certain outcomes, the consistency of findings across multiple analytical approaches supports the safety profile of immediate complete revascularization, pending confirmation in adequately powered randomized trials. (PROSPERO: CRD42023485163.I).
Keywords: Coronary artery disease. ST-segment elevation myocardial infarction. Multivessel disease. Immediate percutaneous coronary intervention. Staged percutaneous coronary intervention.
Abreviaturas
IAMCEST: infarto agudo de miocardio con elevación del segmento ST. ICP: intervención coronaria percutánea. LRA: lesión renal aguda.
INTRODUCCIÓN
La enfermedad coronaria multivaso se define como la presencia de estenosis luminal ≥ 70% en, como mínimo, 2 arterias coronarias epicárdicas principales secundaria a la acumulación de placa ateroesclerótica. Aproximadamente, al 40% de los pacientes que sufren un infarto agudo de miocardio con elevación del segmento ST (IAMCEST) presentan enfermedad coronaria multivaso, que está asociada a un mayor riesgo de reinfarto y mortalidad1-3. La evidencia proveniente de ensayos clínicos aleatorizados confirma las ventajas que se derivan de una revascularización completa mediante intervención coronaria percutánea (ICP) multivaso frente a una ICP solo de la lesión culpable, con descensos notables del riesgo de mortalidad cardiovascular, reinfarto y revascularización motivada por la isquemia trascurrido 1 año4-6. Existen 2 estrategias para el tratamiento de lesiones no culpables: la ICP inmediata, que implica la revascularización de las lesiones culpables y no culpables durante la primera intervención y la ICP por etapas, en la cual el tratamiento de las lesiones no culpables se difiere a una etapa posterior.
Las guías de práctica clínica de 2021 del American College of Cardiology/ American Heart Association (ACC/AHA) le dan a la revascularización de vasos no culpables una recomendación clase IIb para pacientes con IAMCEST7. No obstante, saber cuál es el mejor momento para revascularizar las lesiones no culpables sigue planteando un desafío a nivel clínico7,8. Aunque la ICP de lesiones no culpables ha demostrado ser superior a la estrategia de tratamiento de una única lesión culpable4-6, el momento de la intervención, inmediato o por etapas, carece de evidencia concluyente8,9.
El objetivo del presente metanálisis fue comparar la ICP por etapas frente a la ICP inmediata en el tratamiento de lesiones no culpables de pacientes hemodinámicamente estables con IAMCEST y enfermedad coronaria multivaso. Nuestra hipótesis fue que tanto la ICP por etapas como la ICP inmediata de vasos no culpables tendrían niveles parecidos de seguridad, eficacia y tasa de complicaciones.
MÉTODOS
El presente estudio se realizó de conformidad con la declaración PRISMA (Preferred Reporting Items for Systematic reviews and Meta-Analyses)10. Asimismo, todos los pasos se realizaron de acuerdo con los criterios establecidos en el Cochrane Handbook of Systematic Reviews and Meta-Analysis of Interventions (versión 6,3)11. El protocolo del presente metanálisis fue registrado en PROSPERO el 4 de diciembre de 2023 con el Nº de identificación CRD42023485163. Durante el proceso de revisión por pares, se actualizó la búsqueda bibliográfica empleando la misma estrategia de búsqueda, bases de datos y criterios de elegibilidad descritos en el material adicional S1 para la identificación de nuevas evidencias aleatorizadas publicadas.
Criterios de los estudios incluidos
Se analizaron ensayos clínicos aleatorizados que comparaban la ICP inmediata y la ICP por etapas en lesiones no culpables en adultos con IAMCEST y enfermedad coronaria multivaso. Se exigía que los estudios elegibles informaran datos numéricos extraíbles de, como mínimo, 1 resultado clínico preespecificado de los que se definen a continuación. Los ensayos que informaban los resultados clínicos solo como curvas de Kaplan-Meier sin recuento de episodios ni estimaciones de efecto correspondientes, o como objetivos compuestos sin datos desagregados fueron excluidos de la síntesis cuantitativa. No se aplicó límite temporal de publicación; no obstante, la búsqueda se limitó a estudios publicados en español, inglés o alemán. Se excluyeron estudios de casos y controles, estudios transversales, revisiones sistemáticas, metanálisis, casos clínicos, investigaciones básicas, resúmenes de congresos y cartas al editor.
Estrategia de búsqueda bibliográfica
Se realizó una búsqueda sistemática exhaustiva en 3 bases de datos (PubMed, EMBASE y COCHRANE) desde su inicio hasta el 28 de septiembre de 2025. Las palabras clave fueron «enfermedad coronaria», «intervención coronaria percutánea multivaso inmediata», «intervención coronaria percutánea multivaso por etapas», «síndrome coronario agudo», «enfermedad coronaria multivaso», «infarto de miocardio», «eventos cardiovasculares adversos mayores» e «infarto de miocardio con elevación del segmento ST». Estas palabras clave se combinaron empleando los operadores booleanos Y y O. Los detalles de la búsqueda para cada base de datos se muestran en el material adicional S1.
Selección de los resultados de la búsqueda bibliográfica
Se eliminaron los duplicados empleando el gestor de referencias Zotero. Los registros se seleccionaron inicialmente por título y resumen por un autor (E. Andrade-Arbaiza) y, después, se revisó el texto completo de los registros potencialmente elegibles. Dos autores independientes (D. Paulino-González y L.H. García-Mena) revisaron los textos completos para determinar tanto la inclusión como la calidad metodológica de los estudios; las discrepancias se resolvieron por consenso o mediante un tercer evaluador (D.A. Navarro-Martínez). Los estudios fueron excluidos en la fase de lectura a texto completo cuando no presentaban datos numéricos extraíbles para los resultados clínicos preespecificados o cuando no informaban los resultados aisladamente, lo cual impedía su síntesis cuantitativa. La lista detallada de los estudios excluidos y los motivos de exclusión se muestra en la tabla S1. También se revisaron manualmente las referencias bibliográficas de los estudios incluidos.
Extracción de datos
Los datos recopilados se plasmaron en hojas de cálculo de Excel con las características basales de la población, las características más importantes de los estudios, las medidas de resultado expresadas como tasas de riesgo (RR) y los dominios a efectos de evaluación cualitativa. Los datos de los resultados solo se incluyeron siempre y cuando la información numérica estuviese directamente disponible o pudiese extraerse de forma segura sin reconstrucción de curvas de supervivencia.
Valoración del riesgo de sesgo
El riesgo de sesgo de los ensayos clínicos aleatorizados incluidos se valoró utilizando la versión 2 de la herramienta Cochrane Risk of Bias para ensayos aleatorizados (RoB 2) de conformidad con los criterios establecidos en el Cochrane Handbook of Systematic Reviews of Interventions11.
Objetivos
Los objetivos preespecificados fueron la mortalidad cardiovascular, la mortalidad por cualquier causa, el accidente cerebrovascular, el reinfarto y la lesión renal aguda (LRA). Teniendo en cuenta las variaciones mínimas observadas en las definiciones de los objetivos entre los estudios, se ofrecen definiciones detalladas de dichos objetivos en la tabla S2. Los resultados se analizaron como variables dicotómicas utilizando recuentos y porcentajes de episodios; también se calcularon las tasas de riesgo con intervalos de confianza del 95% (IC95%).
Análisis de datos
Los resultados dicotómicos se analizaron empleando datos agrupados de episodios de los estudios incluidos que se informan como tasas de riesgo con IC95%. Los valores p < 0,05 se consideraron significativos a nivel estadístico. Las relaciones entre los resultados y la ICP inmediata frente a la ICP por etapas se evaluaron empleando un modelo de efectos aleatorios (método de DerSimonian-Laird) para informar sobre la heterogeneidad entre estudios12. Tanto los análisis estadísticos como los diagramas de bosque se generaron utilizando RevMan versión 5,4,1 (Cochrane Collaboration) para MacOS.
Análisis estadístico
La RR y la tasa de incidencia relativa (IRR) combinadas se calcularon empleando modelos de efectos aleatorios con ajustes apropiados; la heterogeneidad se calculó empleando el estadístico I2. Se realizaron análisis de sensibilidad, análisis secuencial de ensayos y metarregresión para evaluar la solidez de los hallazgos y explorar posibles modificadores del efecto. Los procedimientos metodológicos se detallan en el material adicional S2.
Valoración de la heterogeneidad
La heterogeneidad se calculó mediante la prueba Q de Cochran (p < 0,10) y se cuantificó con el estadístico I2; valores > 50% se consideraron indicativos de heterogeneidad significativa.
RESULTADOS
Seis estudios13-18 cumplieron los criterios de inclusión predefinidos y fueron incluidos en el análisis. El proceso de selección de los estudios se resume en el diagrama de flujo PRISMA y se muestra en la figura 1. Todos los estudios incluidos analizaron la ICP inmediata o por etapas en arterias no culpables de pacientes con IAMCEST y enfermedad coronaria multivaso.
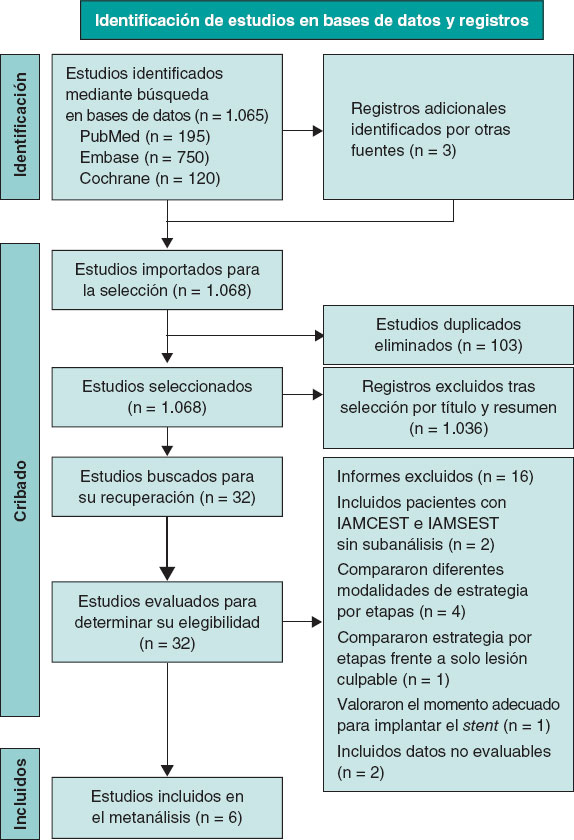
Figura 1. Figura 1. Diagrama de flujo PRISMA. El diagrama refleja la búsqueda inicial y actualizada realizada durante la revisión por pares utilizando la misma estrategia y criterios de elegibilidad (material adicional S1). IAMCEST: infarto agudo de miocardio con elevación del segmento ST; IAMSEST: infarto agudo de miocardio sin elevación del segmento ST.
En la estrategia por etapas, la ICP de las lesiones no culpables se realizó, de media, 18,6 días (RIC = 7–34) después de la primera intervención. La población total incluida en nuestro metanálisis fue de 4.267 pacientes, 2.479 de los cuales fueron sometidos a ICP inmediata y 1.788 a ICP por etapas. Tanto el resumen como las características basales se muestran en la tabla 1. Las características de los estudios incluidos se resumen en la tabla 2.
Tabla 1. Características basales y tratamiento de las poblaciones incluidas en los estudios
| Información del estudio | Características basales | Tratamientos y posterior intervención | |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ID del estudio | País | Tamaño poblacional total | Intervención | Tamaño poblacional | Mediana [RIC] Edad | Sexo | Comorbilidades | Arteria culpable | Arteria no culpable | Lugar de acceso 1ª intervención | Lugar de acceso 1ª intervención + por etapas | Stent utilizado 1ª intervención | Stent utilizado 1ª intervención + por etapas | Volumen de contraste 1ª intervención | Volumen de contraste 1ª intervención + por etapas | Estancia hospitalaria 1ª intervención | Estancia hospitalaria 1ª intervención + por etapas | ||
| Kim et al.18 2025 | Multicéntrico | 994 | Inmediata | 498 | 66 RIC [57-76] |
M: 102 H: 396 |
Sí | Tronco común izquierdo | ND | Tronco común izquierdo | ND | Radial: 371 Femoral: ND |
Radial: 379 Femoral: ND |
2 | ND | 180 (140-225) | ND | 4 (3-6) | ND |
| ND | ND | ||||||||||||||||||
| Descendente anterior | 221 | Descendente anterior | 222 | ||||||||||||||||
| 234 | 212 | ||||||||||||||||||
| Por etapas | 496 | 65 RIC [58-76] |
M: 103 H: 393 |
Circunfleja izquierda | 62 | Circunfleja izquierda | 218 | 1 | 2 | 130 (100-180) | 220 (170-298) | ND | 5 (4-8) | ||||||
| 67 | 215 | ||||||||||||||||||
| Coronaria derecha | 215 | Coronaria derecha | 162 | ||||||||||||||||
| 195 | 167 | ||||||||||||||||||
| Stähli et al.13 2023 | Multicéntrico | 840 | Inmediata | 418 | 66 RIC [58-74] |
M: 97 H: 321 |
Sí | Tronco común izquierdo | 0 | Tronco común izquierdo | 1 | Radial: 301 Femoral: 117 |
Radial: -- Femoral: 296 |
3 (2-4) | ND | 250 (199-320) | ND | 4 (3-6) | ND |
| 1 | 4 | ||||||||||||||||||
| Descendente anterior | 163 | Descendente anterior | 205 | ||||||||||||||||
| 176 | 180 | ||||||||||||||||||
| Por etapas | 422 | 64 RIC [55-73] |
M: 81 H: 341 |
Circunfleja izquierda | 67 | Circunfleja izquierda | 196 | Radial: 311 Femoral: 111 |
Radial: -- Femoral: 90 |
1 (1-2) | 3 (2-4) | 170 (130-220) | 333 (258-411) | 4 (3-6) | 5 (4-7) | ||||
| 77 | 152 | ||||||||||||||||||
| Coronaria derecha | 188 | Coronaria derecha | 134 | ||||||||||||||||
| 169 | 124 | ||||||||||||||||||
| Politi et al.14 2010 | Italia | 130* | Inmediata | 65 | 64,5 ± 11,7 | M: 15 H: 50 |
Sí | Tronco común izquierdo | ND | Tronco común izquierdo | ND | ND | ND | ND | ND | ND | ND | 4,8 ± 2,6 | ND |
| ND | ND | ||||||||||||||||||
| Descendente anterior | ND | Descendente anterior | ND | ||||||||||||||||
| ND | ND | ||||||||||||||||||
| Por etapas | 65 | 64,5 ± 11,1 | M: 13 H: 52 |
Circunfleja izquierda | ND | Circunfleja izquierda | ND | ND | ND | ND | ND | ND | ND | 5,4 ± 3,1 | ND | ||||
| ND | ND | ||||||||||||||||||
| Coronaria derecha | ND | Coronaria derecha | ND | ||||||||||||||||
| ND | ND | ||||||||||||||||||
| Park et al.15 2023 | Multicéntrico | 209* | Inmediata | 103 | 63,3 ± 10,4 | M: 21 H: 82 |
Sí | Tronco común izquierdo | 1 | Tronco común izquierdo | 4 | Radial: 27 | – | 2,58 ± 0,86 | – | ND | – | ND | ND |
| 1 | 3 | ||||||||||||||||||
| Descendente anterior | 45 | Descendente anterior | 79 | ||||||||||||||||
| 48 | 82 | ||||||||||||||||||
| Por etapas | 106 | 62,2 ± 10,9 | F: 18 H: 88 |
Circunfleja izquierda | 12 | Circunfleja izquierda | 60 | Radial: 25 | ND | 2,62 ± 1,00 | ND | ND | ND | ND | ND | ||||
| 17 | 55 | ||||||||||||||||||
| Coronaria derecha | 46 | Coronaria derecha | 78 | ||||||||||||||||
| 42 | 80 | ||||||||||||||||||
| 228 | 65 | ||||||||||||||||||
| Maamoun et al.16 2011 | Yemen | 78 | Inmediata | 36 | 52,33 ± 7,1 | H: 32 M: 4 | Sí | ND | ND | ND | ND | Femoral | Femoral | 2,38 ± 0,49 | 2,31 ± 0,47 | ND | ND | ND | ND |
| Por etapas | 42 | 54,52 ± 10,3 | H: 40 M: 2 | ||||||||||||||||
| Wood et al.17 2019 | Canadá | 4.401* | Inmediata | 1.353 | 61,8 ± 10,5 | H: 1.079 M: 274 |
Sí | ND | ND | Tronco común izquierdo | 4 | Radial | Radial | ND | ND | ND | ND | ND | ND |
| 6 | |||||||||||||||||||
| Descendente anterior | 683 | ||||||||||||||||||
| 384 | |||||||||||||||||||
| Por etapas | 663 | 61,2 ± 11,0 | H: 544 M: 119 |
Circunfleja izquierda | 654 | ||||||||||||||
| 294 | |||||||||||||||||||
| Coronaria derecha | 463 | ||||||||||||||||||
| 207 | |||||||||||||||||||
|
H: hombre; M: mujer; ND: no descrito; RIC: rango intercuartílico. * Análisis de subgrupo. |
|||||||||||||||||||
Tabla 2. Resumen de los estudios incluidos
| Autor y año | Revista | País | Diseño del estudio | Tamaño poblacional (incluido) | Intervenciones comparadas | Tiempo hasta ICP por etapas | Seguimiento medio | Hallazgos principales |
|---|---|---|---|---|---|---|---|---|
| Kim et al.18 2025 | The Lancet | Corea del Sur | Ensayo clínico aleatorizado | 994 | Revascularización inmediata frente a RE | 3 días | 1 año |
|
| Stähli et al.13 2023 | New England Journal of Medicine | Europa | Ensayo clínico aleatorizado | 840 | Revascularización inmediata frente a RE | 19-45 días | 30 días (± 7 días) 6 meses (± 14 días) 1 año (± 14 días) |
|
| Park et al.15 2023 | American Heart Journal | Corea del Sur | Ensayo clínico aleatorizado | 209 | Revascularización inmediata frente a RE | 14 días | 7 días 1 mes 1 año |
|
| Wood et al.17 2019 | Journal of the American College of Cardiology | Canadá | Ensayo clínico aleatorizado | 4.041 | Revascularización inmediata frente a RE | 23 días (12,5-33,5) | 3 años |
|
| Maamoun et al.16 2011 | The Egyptian Heart Journal | Yemen | Ensayo clínico aleatorizado | 78 | Revascularización inmediata frente a RE | 7 días | 1 año |
|
| Politi et al.14 2010 | Heart | Italia | Ensayo clínico aleatorizado | 263 (130) | Revascularización inmediata frente a RE | 56,8 ± 12,9 días | 2,5 ± 1,4 años |
|
|
ANRI: arteria no relacionada con el infarto; HR: hazard ratio; IAMCEST: infarto agudo de miocardio con elevación del segmento ST; IC95%: intervalo de confianza del 95%; ICP: intervención coronaria percutánea; IM: infarto de miocardio; MACE: episodios cardiovasculares adversos mayores; RC: revascularización completa; RE: revascularización por etapas; RR: tasa de riesgo. |
||||||||
Mortalidad cardiovascular
No se observaron diferencias significativas entre la ICP inmediata y la ICP por etapas en lo referente al riesgo de mortalidad cardiovascular (RR = 1,26; IC95%, 0,89–1,79; p = 0,19). Tampoco se observó heterogeneidad entre los estudios incluidos (I2 = 0%). Estos hallazgos se muestran en la figura 2A.
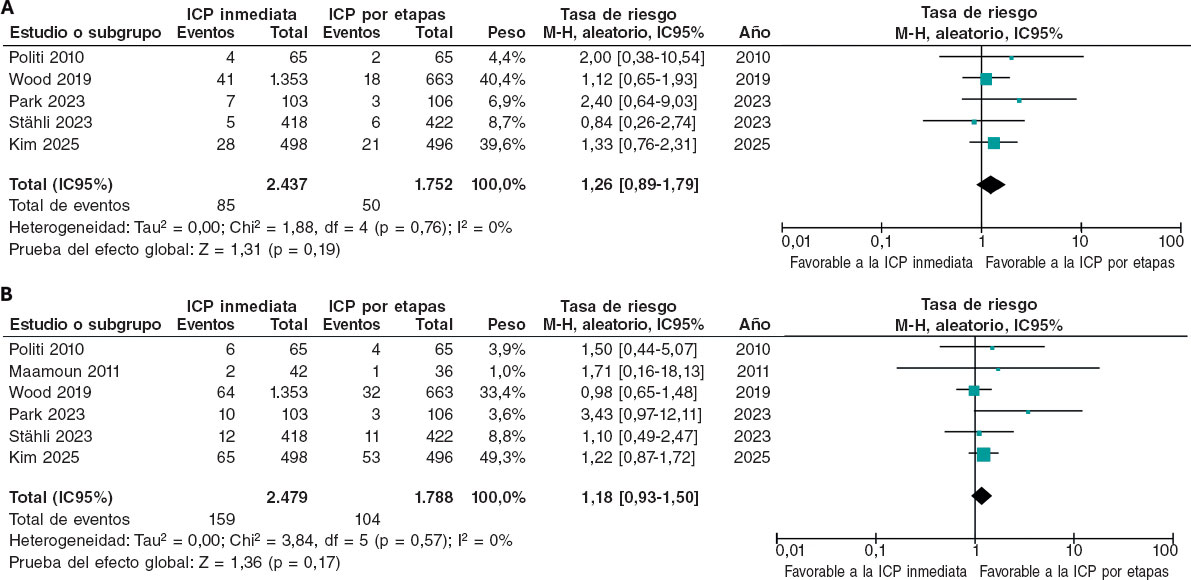
Figura 2. Tasas de riesgos de mortalidad cardiovascular y por cualquier causa. A: mortalidad cardiovascular: las tasas de riesgo (RR) de los estudios incluidos se expresan mediante cuadrados sólidos, con líneas horizontales indicadoras de intervalos de confianza del 95% (IC95%). B: mortalidad por cualquier causa: las RR de los estudios se muestran mediante cuadrados sólidos, con IC95% indicados por líneas horizontales. Aleatorio: modelo de efectos aleatorios; M-H: método Mantel-Haenszel. Las referencias bibliográficas citadas en esta figura corresponden a los siguientes estudios: Politi et al.14 (2010), Maamoun et al.16 (2011), Wood et al.17 (2019), Park et al.15 (2023), Stähli et al.13 (2023) y Kim et al.18 (2025).
Mortalidad por cualquier causa
Tampoco hubo diferencias significativas en el riesgo de mortalidad por cualquier causa entre los pacientes sometidos a ICP por etapas y los tratados con ICP inmediatas (RR = 1,18; IC95%, 0,93–1,50; p = 0,17). Tampoco se observó heterogeneidad entre los estudios (I2 = 0%) (figura 2B).
Reinfarto
El análisis informó de un riesgo mucho menor de reinfarto con la ICP inmediata que con la ICP por etapas (RR = 0,63; IC95%, 0,40–0,98; p = 0,04), lo cual supone un descenso relativo del 37% asociado a la ICP inmediata. No se observó heterogeneidad entre los ensayos (I2 = 0%). Estos hallazgos se muestran en la figura 3A.
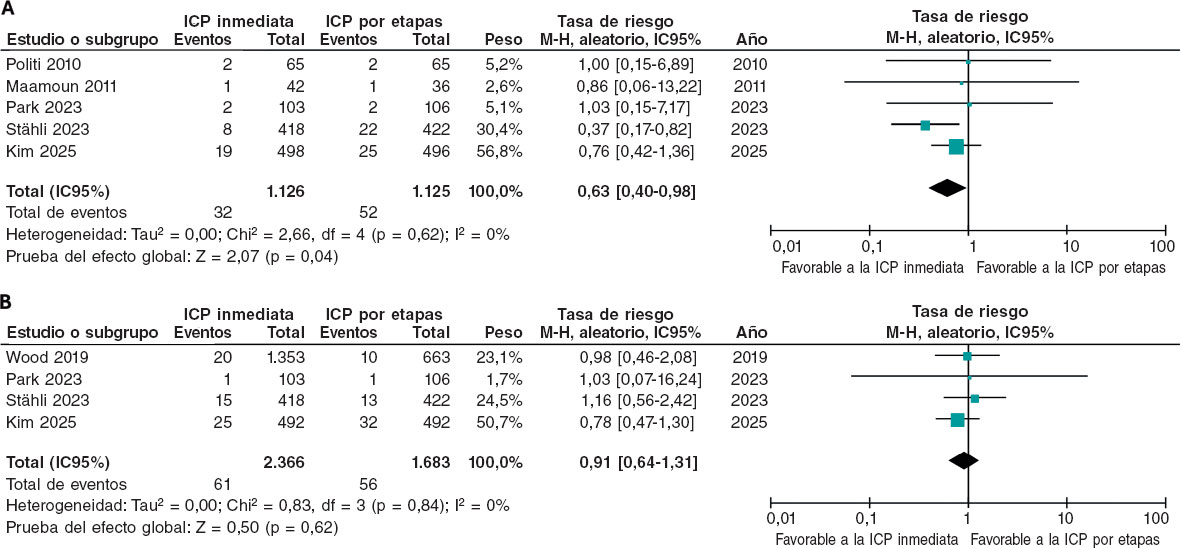
Figura 3. Tasas de riesgos para el reinfarto y la lesión renal aguda. A: reinfarto: las tasas de riesgo (RR) de los estudios incluidos se expresan mediante cuadrados sólidos, con líneas horizontales indicadores de intervalos de confianza del 95% (IC95%). B: lesión renal aguda: las RR de los estudios se muestran mediante cuadrados sólidos, con IC95% indicados por líneas horizontales. Aleatorio: modelo de efectos aleatorios; M-H: método Mantel-Haenszel. Las referencias bibliográficas citadas en esta figura corresponden a los siguientes estudios: Politi et al.14 (2010), Maamoun et al.16 (2011), Wood et al.17 (2019), Park et al.15 (2023), Stähli et al.13 (2023) y Kim et al.18 (2025).
Lesión renal aguda
Tampoco se observaron diferencias significativas entre ambas estrategias (RR = 0,91; IC95%, 0,64–1,31; p = 0,62), lo cual es indicativo de que no existe una relación clara entre una u otra estrategia de revascularización y el riesgo de LRA. Tampoco se observó heterogeneidad entre los estudios incluidos (I2 = 0%). Estos resultados se muestran en la figura 3B.
Accidente cerebrovascular
El accidente cerebrovascular se informó en solo 3 de los estudios incluidos y nuestro análisis no reveló diferencias significativas entre la ICP por etapas y la ICP inmediata para este resultado (RR = 1,17; IC95%, 0,66–2,05; p = 0,59). Tampoco se observó heterogeneidad entre los estudios incluidos (I2 = 0%). Estos resultados se muestran en la figura S1.
El sesgo de publicación se estudió mediante gráficos en embudo, regresión de Egger y análisis de recorte y relleno (trim and fill) para el reinfarto, la mortalidad cardiovascular y la mortalidad por cualquier causa. No se observó evidencia visual de asimetría en los gráficos en embudo (figura S2). Para el reinfarto, el análisis de recorte y relleno imputó 1 estudio potencialmente faltante y el efecto combinado se mantuvo estadísticamente significativo (IRR = 0,59; IC95%, 0,38–0,90). Tanto para la mortalidad cardiovascular como para la mortalidad por cualquier causa, se imputaron 2 estudios en cada análisis; sin embargo, los efectos combinados siguieron siendo no significativos a nivel estadístico y tampoco se observó heterogeneidad (I2 = 0%). En líneas generales, aunque estos resultados sugieren una ausencia de sesgo de publicación significativa, el número limitado de estudios incluidos reduce el potencial estadístico de las pruebas formales para la detección de asimetría en el gráfico en embudo.
Análisis de sensibilidad
Los análisis de sensibilidad de validación cruzada dejando uno fuera confirmaron la solidez de las estimaciones combinadas para todos los objetivos primarios (figura S3). En lo que respecta a la mortalidad por cualquier causa y cardiovascular, excluir determinados estudios no modificó sustancialmente los resultados y las RR combinadas se mantuvieron dentro de los intervalos de confianza de los modelos principales (I2 = 0% en todos los escenarios). En lo que respecta al reinfarto, las estimaciones fueron favorables consistentemente a la ICP inmediata (rango de RR = 0,46–0,75; I2 = 0%), lo cual avala la consistencia interna de los hallazgos.
Tasa de incidencia relativa
En el seguimiento a 1 año, el análisis de la IRR confirmó que la ICP inmediata tuvo una tasa de reinfarto más baja que la ICP por etapas. En el modelo de efectos aleatorios, la IRR combinada fue de 0,60 (IC95%, 0,39–0,94; I2 = 0%), lo cual coincide con el modelo de efectos fijos (IRR = 0,59; IC95%, 0,38–0,92) y avala la solidez de este hallazgo (figura S4). En cambio, no se observaron diferencias significativas entre las estrategias en lo referente a la mortalidad cardiovascular (IRR = 1,26; IC95%, 0,90–1,77; I2 = 0%) o mortalidad por cualquier causa (IRR = 1,17; IC95%, 0,84–1,64; I2 = 0%), lo cual es indicativo de estimaciones estables con heterogeneidad despreciable entre los estudios (figuras S5-S6).
Análisis secuencial de ensayos
Se realizaron análisis secuenciales de ensayos para la mortalidad cardiovascular, mortalidad por cualquier causa y reinfarto (figura 4A–C). Tanto para la mortalidad cardiovascular como por cualquier causa, el tamaño muestral acumulado supuso el 33 y 58% del tamaño de información requerido, respectivamente; en ambos análisis y las curvas Z acumuladas se mantuvieron dentro de los límites de no significación, es decir, evidencia insuficiente para confirmar o descartar un descenso relativo del riesgo del 30%. En lo referente al reinfarto, solo se alcanzó el 3,4% del tamaño de información requerido manteniéndose la curva Z dentro de la zona de futilidad, con una tendencia no significativa favorable a la ICP inmediata. En líneas generales, estos resultados demuestran que con los datos actuales todavía no se puede extraer conclusiones definitivas en todos los resultados, a pesar de la existencia de un patrón numérico consistente favorable a la revascularización inmediata.
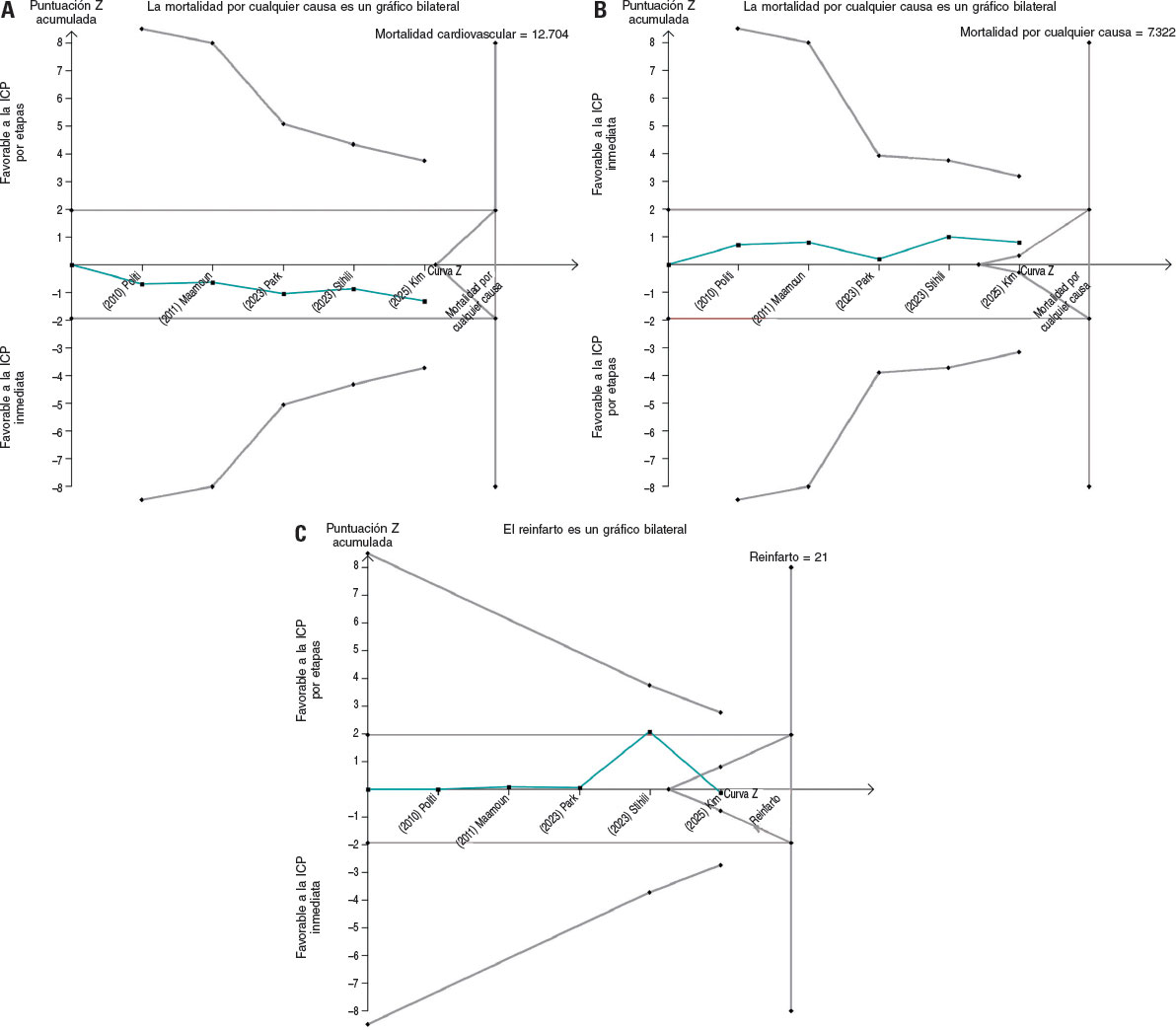
Figura 4. Análisis secuencial de ensayos. Análisis secuencial de ensayos para (A) la mortalidad cardiovascular, (B) la mortalidad por cualquier causa y (C) el reinfarto. En todos los paneles, las curvas Z acumuladas se muestran en color azul, los límites de monitorización secuencial del ensayo en color rojo y los umbrales convencionales de significación como líneas horizontales de color morado. ICP: intervención coronaria percutánea. Las referencias bibliográfi- cas citadas en esta figura corresponden a los siguientes estudios: Politi et al.14 (2010), Maamoun et al.16 (2011), Wood et al.17 (2019), Park et al.15 (2023), Stähli et al.13 (2023) y Kim et al.18 (2025).
Metarregresión
Se realizaron análisis exploratorios de metarregresión para valorar si el momento en que se realizó la intervención o las comorbilidades basales influyeron en los resultados del reinfarto. La relación entre el tiempo trascurrido hasta la realización de la ICP por etapas y el riesgo de reinfarto mostró una pendiente negativa no significativa (β = –0,016 por día; IC95%, –0,042 a 0,010; p = 0,22), sin heterogeneidad residual (I2 = 0%), lo cual es indicativo de efectos consistentes entre los estudios (figura S7). La prevalencia de diabetes (β = 0,021 por incremento del 1%; IC95%, –0,017 a 0,058; p = 0,22) e hipertensión (β = –0,064 por incremento del 1%; IC95%, –0,214 a 0,085; p = 0,40) tampoco guardaron una relación estrecha con el riesgo de reinfarto, sin observarse heterogeneidad residual (I2 = 0% para ambas patologías) (figuras S8–S9). En líneas generales, estos hallazgos sugieren que ni el momento en que se realizó la intervención ni la carga de comorbilidades modificaron de manera sustancial el riesgo comparativo de reinfarto entre la ICP inmediata y la ICP por etapas; no obstante, teniendo en cuenta el diseño exploratorio y basado en datos a nivel de estudio de estos análisis, los resultados deben interpretarse con cautela.
Valoración del riesgo de sesgo
La valoración del riesgo de sesgo se realizó utilizando la versión 2 de la herramienta Cochrane Risk of Bias para ensayos aleatorizados (RoB 2) de conformidad con los criterios establecidos en el Cochrane Handbook of Systematic Reviews of Interventions11. Cuatro ensayos clínicos se consideraron de bajo riesgo global de sesgo y el estudio de Maamoun et al.16 fue el único ciertamente preocupante (tabla 3).
Tabla 3. Resumen del riesgo de sesgo en estudios aleatorizados (RoB 2)
| Estudio | Sesgo derivado del proceso de aleatorización | Sesgo debido a desviaciones de las intervenciones previstas | Sesgo debido a datos de resultados faltantes | Sesgo en la medición de los resultados | Sesgo en la selección de los resultados informados | Riesgo global de sesgo |
|---|---|---|---|---|---|---|
| Politi et al.14 2010 | Bajo | Bajo | Bajo | Bajo | Bajo | Bajo |
| Maamoun et al.16 2011 | Bajo | Preocupante | Bajo | Preocupante | Bajo | Preocupante |
| Wood et al.17 2019 | Bajo | Bajo | Bajo | Bajo | Bajo | Bajo |
| Park et al.15 2023 | Bajo | Bajo | Bajo | Bajo | Bajo | Bajo |
| Stähli et al.13 2023 | Bajo | Bajo | Bajo | Bajo | Bajo | Bajo |
| Kim et al.18 2025 | Bajo | Bajo | Bajo | Bajo | Bajo | Bajo |
DISCUSIÓN
El presente metanálisis ofrece una comparativa específica entre la ICP inmediata y la ICP por etapas en pacientes con IAMCEST y enfermedad coronaria multivaso. Al integrar evidencia aleatorizada mediante abordajes analíticos adicionales, nuestros hallazgos ofrecen una síntesis actualizada y clínicamente relevante del perfil de seguridad y eficacia de ambas estrategias de revascularización en una población bien definida.
Aunque la mortalidad cardiovascular y por cualquier causa son objetivos relevantes desde el punto de vista clínico, también son episodios relativamente poco frecuentes en poblaciones contemporáneas con IAMCEST sometidas a revascularización multivaso. En el presente análisis no se observaron diferencias estadísticamente significativas entre la ICP inmediata y la ICP por etapas en ninguno de estos objetivos. No obstante, estos hallazgos neutrales se deben interpretar dentro de un contexto con potencial estadístico limitado, tal y como refleja la baja incidencia acumulada de episodios y el análisis secuencial de ensayos que indicó que no se alcanzó el tamaño de información requerido19,20. Los análisis adicionales de IRR informaron resultados consistentes, lo cual refuerza aún más la ausencia de una diferencia clínicamente significativa en materia de supervivencia entre ambas estrategias. En este sentido, los resultados de mortalidad no distinguen entre ICP inmediata y por etapas; por ello, la elección del tratamiento se debe basar en la estabilidad clínica del paciente y en las características específicas de la intervención, no solo en los resultados de mortalidad.
En lo referente al riesgo de reinfarto, la ICP inmediata se asoció de manera consistente con una tasa mucho menor de reinfarto frente a la ICP por etapas. Los análisis exploratorios de metarregresión no identificaron el mejor momento para realizar la intervención ni la prevalencia de diabetes o hipertensión como modificadores significativos de esta relación. Los análisis secuenciales y de sensibilidad informaron resultados consistentes entre los modelos, sin evidencia de heterogeneidad. Aunque no se alcanzó el tamaño de información requerido, la consistencia de los hallazgos a través de múltiples abordajes analíticos avala la relación sólida que existe entre la ICP inmediata y menos episodios isquémicos recurrentes.
Respecto a la LRA, no se observaron diferencias significativas entre la ICP inmediata y la ICP por etapas, con tasas bajas de episodios y ausencia de heterogeneidad entre los estudios. El número limitado de episodios impidió realizar un análisis secuencial significativo, lo cual pone de manifiesto la falta de potencial estadístico para la detección de diferencias mínimas. Aunque la LRA tras la ICP se ve condicionada por factores tales como la exposición al contraste y la complejidad propia de la intervención21, la evidencia actual no avala el supuesto de que la ICP por etapas reduce el riesgo de LRA al distribuir la carga de contraste22. Ninguno de los estudios incluidos fue diseñado específicamente con el potencial estadístico necesario como para poder valorar los resultados renales; además, las definiciones de LRA variaron entre los estudios. En este sentido, hasta que no contemos con estudios debidamente dimensionados con definiciones estandarizadas, las decisiones sobre el mejor momento para realizar la ICP deberán tomarse de forma individualizada teniendo en cuenta la función renal basal y el riesgo global de la intervención23.
No se observaron diferencias significativas en la tasa de accidentes cerebrovasculares entre la ICP inmediata y la ICP por etapas y fueron pocos los episodios comunicados en los estudios, lo cual limita el potencial estadístico. La evidencia disponible sugiere que el riesgo de accidente cerebrovascular tras una ICP en el tratamiento del IAMCEST guarda una estrecha relación con factores derivados de la propia intervención más que con el momento de revascularización de las lesiones no culpables15. En este sentido, el accidente cerebrovascular no parece ser un objetivo clínicamente discriminativo entre la estrategia de revascularización inmediata y por etapas en esta población.
Históricamente, las guías internacionales de práctica clínica han favorecido, siempre, un abordaje por etapas para realizar una revascularización completa en el tratamiento del IAMCEST con enfermedad coronaria multivaso, principalmente porque preocupa la complejidad de la propia intervención, la exposición al contraste y la inestabilidad hemodinámica durante la primera intervención. No obstante, la evidencia aleatorizada acumulada a este respecto ha cuestionado este paradigma y demostrado que la ICP completa inmediata se puede realizar de forma segura en pacientes hemodinámicamente estables, con resultados parecidos o superiores a los que se obtienen con la ICP por etapas13,17,24,25. Se debe mencionar que la mayoría de estudios publicados incluyen principalmente a pacientes clínicamente estables tras reperfusiones exitosas, lo cual limita la extrapolación de los resultados a poblaciones con IAMCEST de mayor riesgo. En este contexto, el estudio OPTION-STEMI amplía la evidencia disponible al incluir a pacientes con inestabilidad hemodinámica transitoria o leve y aporta datos contemporáneos que reflejan mejor la complejidad clínica del mundo real18.
En consonancia con nuestros hallazgos principales, ni la ICP inmediata ni la ICP por etapas variaron en lo referente a la mortalidad cardiovascular o por cualquier causa trascurrido 1 año, si bien la ICP inmediata se asoció a un menor riesgo de reinfarto. Más allá de los resultados clínicos, la revascularización completa inmediata resulta ventajosa a nivel económico al reducir el tiempo de hospitalización, evitar nuevos cateterismos y optimizar el uso de recursos. En cambio, la ICP por etapas precisa una segunda intervención con hospitalización, lo cual incrementa el gasto acumulado en hasta un 50% en algunos estudios26,27 y se asemeja a los gastos adicionales derivados de nuevas hospitalizaciones no programadas en casos de isquemia recurrente. En este contexto, una estrategia de revascularización en un único acto quirúrgico aporta valor clínico y económico, sobre todo, en sistemas de salud con recursos limitados, donde el gasto contemporáneo de la ICP sigue siendo alto28.
Desde una perspectiva de seguridad y eficacia, tanto la ICP inmediata como la ICP por etapas son estrategias aceptables en pacientes adecuadamente seleccionados con IAMCEST y enfermedad coronaria multivaso. En el presente estudio, la ICP inmediata se asoció principalmente a menos episodios isquémicos recurrentes; por su parte, los episodios cardiovasculares adversos mayores, incluida la mortalidad cardiovascular y por cualquier causa, no variaron significativamente entre una y otra estrategia. En este sentido, la elección entre ICP inmediata y por etapas debería basarse, cada vez más, en las características clínicas de cada paciente y consideraciones logísticas y no en cuestiones relacionadas con el perfil de seguridad de la intervención.
Aunque no se estudió directamente en este metanálisis, la evidencia emergente sugiere que factores biológicos sistémicos, tales como inflamación, hipercoagulabilidad y activación simpática, podrían, también, influir en el riesgo isquémico recurrente más allá de la propia gravedad angiográfica29,30. Además, las características de vulnerabilidad de la placa se asocian a la ocurrencia de episodios isquémicos futuros en lesiones no culpables, aun cuando estas características son angiográficamente leves31. En este sentido, la incorporación de marcadores biológicos de riesgo y parámetros de estabilidad clínica para la toma de decisiones sobre la revascularización es una línea de investigación prioritaria, orientada a optimizar estrategias individualizadas en pacientes con IAMCEST y enfermedad coronaria multivaso.
Limitaciones
Se deben tener en cuenta varias limitaciones. En primer lugar, solo se incluyeron 6 ensayos clínicos aleatorizados, lo cual limita el potencial estadístico, particularmente en lo referente a resultados poco habituales. En segundo lugar, el análisis se limitó a pacientes con IAMCEST y enfermedad coronaria multivaso; en este sentido, los hallazgos no deben extrapolarse a otras poblaciones con síndrome coronario agudo; además, el número limitado de estudios que informaron todos los resultados preespecificados podría comprometer la solidez de algunas estimaciones. En tercer lugar, el uso de datos agregados a nivel del estudio impidió ajustar por las características de cada paciente y limitó la evaluación de modificadores de efecto a nivel individual; en consecuencia, los análisis de metarregresión fueron exploratorios y deben interpretarse con cautela ante la falta de estudios y el posible sesgo ecológico. Por último, la variabilidad en el momento de realizar la ICP por etapas entre los ensayos pudo introducir cierta heterogeneidad clínica residual; además, las evaluaciones formales de sesgo de publicación tuvieron un potencial estadístico limitado debido el reducido número de estudios.
CONCLUSIONES
El presente metanálisis integra abordajes analíticos adicionales y ofrece una comparativa específica entre la ICP inmediata y la ICP por etapas en pacientes con IAMCEST y enfermedad coronaria multivaso. La ICP inmediata se asoció consistentemente a un menor riesgo de reinfarto, sin observarse diferencias significativas en la mortalidad cardiovascular o por cualquier causa, el accidente cerebrovascular o la LRA. Aunque la evidencia acumulada sigue estando por debajo del tamaño de información requerido para los resultados clínicos más importantes, la consistencia de los hallazgos en los distintos análisis avala la solidez de la reducción observada en la ocurrencia de reinfartos. Desde una perspectiva clínica, estos resultados sugieren que la revascularización completa inmediata se puede realizar de forma segura en pacientes debidamente seleccionados y reduce la carga de reinfartos. En este sentido, la elección entre una u otra estrategia debería basarse, cada vez más, en las características clínicas de cada paciente y consideraciones prácticas y no en cuestiones relacionadas con el perfil de seguridad de la intervención. Futuros estudios con marcadores biológicos de riesgo podrían perfeccionar aún más las estrategias individualizadas de revascularización de esta población.
FINANCIACIÓN
Ninguna.
CONSIDERACIONES ÉTICAS
El presente metanálisis se basó exclusivamente en datos de estudios previamente publicados y análisis secundarios de información públicamente disponible. En este sentido, no hizo falta la aprobación de ningún Comité de Ética ni comité de revisión institucional. Como no se incluyeron datos individuales de los pacientes ni casos clínicos, el consentimiento informado no fue de aplicación. Todos los estudios incluidos se realizaron de conformidad con los estándares éticos vigentes en cada centro al momento de su publicación original.
De conformidad con las guías SAGER, se evaluó información relativa al sexo y género en los estudios incluidos. Aunque el sexo generalmente fue informado en las características basales, los datos de resultados desagregados por sexo y las variables de género, por lo general, no estuvieron disponibles, lo cual impidió un análisis específico por sexo o género. Esta limitación se debe tener en cuenta al interpretar los resultados.
DECLARACIÓN SOBRE EL USO DE INTELIGENCIA ARTIFICIAL
Durante la preparación de este estudio, los autores utilizaron ChatGPT 5.2 para la revisión sintáctico-gramatical del documento. Tras el uso de esta herramienta, los autores revisaron y editaron el contenido según fuese necesario y se hacen plenamente responsables del contenido del artículo publicado.
CONTRIBUCIÓN DE LOS AUTORES
D. Paulino-González: conceptualización, análisis formal, redacción, revisión y edición. L.H. García-Mena: análisis formal, investigación, redacción, revisión y edición. E. Andrade-Arbaiza: metodología, investigación, redacción, revisión y edición. D.A. Navarro-Martínez: metodología, análisis formal. J.L. Maldonado-García: análisis formal, redacción, revisión y edición. S.A. Xiloj-López: investigación. C.J. Palomino-Ojeda: investigación, redacción, revisión y edición. R.M. Arellano-Sánchez: curación de datos, análisis formal. N.E. Antonio-Villa: recogida de datos, análisis formal, redacción, revisión y edición. A. Ricalde-Alcocer: redacción – revisión y edición, supervisión. D. Araiza-Garaygordobil: redacción, revisión y edición, supervisión.
CONFLICTO DE INTERESES
Ninguno.
AGRADECIMIENTOS
Los autores rinden un sentido homenaje a un familiar muy querido de uno de los coautores; asimismo, expresan su más sincero agradecimiento al Dr. Pavel Pichardo-Rojas por el apoyo prestado.
¿QUÉ SE SABE DEL TEMA?
- La enfermedad coronaria multivaso está descrita en aproximadamente el 40% de los pacientes con IAMCEST y se asocia a un mayor riesgo de reinfarto y mortalidad. La revascularización completa, incluidas lesiones culpables y no culpables, reduce la ocurrencia de episodios cardiovasculares adversos mayores frente a la ICP por etapas solo en la lesión culpable. Las lesiones no culpables se pueden tratar en la primera intervención o por etapas; no obstante, el mejor momento para realizar la revascularización sigue sin estar claro.
¿QUÉ APORTA DE NUEVO?
- El presente metanálisis de 6 ensayos clínicos aleatorizados ofrece una comparativa integral de la ICP inmediata frente a la ICP por etapas en el tratamiento de lesiones no culpables en pacientes con IAMCEST y enfermedad coronaria multivaso. La ICP inmediata se asoció a un menor riesgo de reinfarto, sin observarse diferencias significativas en la mortalidad cardiovascular, por cualquier causa, el accidente cerebrovascular o la LRA. Los análisis exploratorios de metarregresión no identificaron el mejor momento para realizar la intervención ni las comorbilidades basales como modificadores del efecto. En líneas generales, estos hallazgos avalan el perfil de seguridad de la revascularización completa inmediata y sugieren una posible ventaja clínica y económica derivada de menos episodios isquémicos recurrentes y reintervenciones.
BIBLIOGRAFÍA
1. Pimor A, Auffret V, Didier R, et al. Immediate complete revascularization in patients with ST-segment elevation myocardial infarction and multivessel disease treated by primary percutaneous coronary intervention: Insights from the ORBI registry. Arch Cardiovasc Dis. 2018;111:656-665.
2. Muller DWM, Topol EJ, Ellis SG, Sigmon KN, Lee K, Califf RM. Multivessel coronary artery disease: a key predictor of short-term prognosis after reperfusion therapy for acute myocardial infarction. Thrombolysis and Angioplasty in Myocardial Infarction (TAMI) Study Group. Am Heart J. 1991;121(4 Pt 1):1042-1049.
3. Jaski BE, Cohen JD, Trausch J, et al. Outcome of urgent percutaneous transluminal coronary angioplasty in acute myocardial infarction: comparison of single-vessel vs multivessel coronary artery disease. Am Heart J. 1992;124:1427-1433.
4. Wald DS, Morris JK, Wald NJ, et al. Randomized trial of preventive angioplasty in myocardial infarction. N Engl J Med. 2013;369:1115-1123.
5. Gershlick AH, Khan JN, Kelly DJ, et al. Randomized trial of complete vs lesion-only revascularization in patients undergoing primary percutaneous coronary intervention for STEMI and multivessel disease: the CvLPRIT trial. J Am Coll Cardiol. 2015;65:963-972.
6. Mehta SR, Wood DA, Storey RF, et al. Complete Revascularization with Multivessel PCI for Myocardial Infarction. N Engl J Med. 2019;381: 1411-1421.
7. O'Gara PT, Kushner FG, Ascheim DD, et al. 2013 ACCF/AHA guideline for the management of ST-elevation myocardial infarction: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. Circulation. 2013;127:362-425.
8. Ibanez B, James S, Agewall S, et al. 2017 ESC Guidelines for the management of acute myocardial infarction in patients presenting with ST-segment elevation: The Task Force for the management of acute myocardial infarction in patients presenting with ST-segment elevation of the European Society of Cardiology (ESC). Eur Heart J. 2018;39:119-177.
9. Neumann FJ, Sousa-Uva M, Ahlsson A, et al. 2018 ESC/EACTS Guidelines on myocardial revascularization. Eur Heart J. 2019;40:87-165.
10. Page MJ, McKenzie JE, Bossuyt PM, et al. The PRISMA 2020 statement: an updated guideline for reporting systematic reviews. BMJ. 2021;372:71.
11. Higgins JPT, Thomas J, Chandler J, et al. Cochrane Handbook for Systematic Reviews of Interventions version 6.5 (updated August 2024). Cochrane. Disponible en www.cochrane.org/handbook. Consultado 11 Dic 2025.
12. DerSimonian R, Laird N. Meta-analysis in clinical trials. Control Clin Trials. 1986;7:177-188.
13. Stähli BE, Varbella F, Linke A, et al. Timing of Complete Revascularization with Multivessel PCI for Myocardial Infarction. N Engl J Med. 2023;389:1368-1379.
14. Politi L, Sgura F, Rossi R, et al. A randomised trial of target-vessel vs multi-vessel revascularisation in ST-elevation myocardial infarction: major adverse cardiac events during long-term follow-up. Heart. 2010;96:662-667.
15. Park S, Rha SW, Choi BG, et al. Immediate versus staged complete revascularization in patients with ST-segment elevation myocardial infarction and multivessel coronary artery disease: results from a prematurely discontinued randomized multicenter trial. Am Heart J. 2023;259:58-67.
16. Maamoun W, Elkhaeat N, Elarasy R. Safety and feasibility of complete simultaneous revascularization during primary PCI in patients with STEMI and multi-vessel disease. Egypt Heart J. 2011;63:39-43.
17. Wood DA, Cairns JA, Wang J, et al. Timing of Staged Nonculprit Artery Revascularization in Patients With ST-Segment Elevation Myocardial Infarction: COMPLETE Trial. J Am Coll Cardiol. 2019;74:2713-2723.
18. Kim MC, Ahn JH, Hyun DY, et al. Immediate versus staged complete revascularisation during index admission in patients with ST-segment elevation myocardial infarction and multivessel disease (OPTION–STEMI): a multicentre, non-inferiority, open-label, randomised trial. Lancet. 2025; 406:1032-1043.
19. Schoenfeld DA. Sample-Size Formula for the Proportional-Hazards Regression Model. Biometrics. 1983;39:499.
20. Olivier CB, StrußL, Sünnen N, et al. Accuracy of Event Rate and Effect Size Estimation in Major Cardiovascular Trials: A Systematic Review. JAMA Netw Open. 2024;7:248818-248818.
21. Mehran R, Dangas GD, Weisbord SD. Contrast-Associated Acute Kidney Injury. N Engl J Med. 2019;380:2146-2155.
22. Almendarez M, Gurm HS, Mariani J, et al. Procedural Strategies to Reduce the Incidence of Contrast-Induced Acute Kidney Injury During Percutaneous Coronary Intervention. JACC Cardiovasc Interv. 2019;12:1877-1888.
23. Nakamura T, Watanabe M, Sugiura J, et al. Prognostic impact and predictors of persistent renal dysfunction in acute kidney injury after percutaneous coronary intervention for acute myocardial infarction. Scientific Reports.2024;14:1-9.
24. Rao SV, O'Donoghue ML, Ruel M, et al. 2025 ACC/AHA/ACEP/NAEMSP/SCAI Guideline for the Management of Patients With Acute Coronary Syndromes: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation. 2025;151:771-862.
25. Diletti R, den Dekker WK, Bennett J, et al. Immediate versus staged complete revascularisation in patients presenting with acute coronary syndrome and multivessel coronary disease (BIOVASC): a prospective, open-label, non-inferiority, randomised trial. Lancet. 2023;401:1172-1182.
26. Virani SS, Newby LK, Arnold SV, et al. 2023 AHA/ACC/ACCP/ASPC/NLA/PCNA Guideline for the Management of Patients With Chronic Coronary Disease: A Report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. Circulation. 2023;148:E9-E119.
27. Kim LK, Yeo I, Cheung JW, et al. Thirty?Day Readmission Rates, Timing, Causes, and Costs after ST? Segment–Elevation Myocardial Infarction in the United States: A National Readmission Database Analysis 2010-2014. J Am Heart Assoc. 2018;7:009863.
28. Hsia RY, Antwi YA, Weber E, Nath JB. A Cross-Sectional Analysis of Variation in Charges and Prices across California for Percutaneous Coronary Intervention. PLoS One. 2014;9:103829.
29. Seropian IM, Toldo S, Van Tassell BW, Abbate A. Anti-inflammatory strategies for ventricular remodeling following ST-segment elevation acute myocardial infarction. J Am Coll Cardiol. 2014;63:1593-1603.
30. Klingenberg R, Brokopp CE, Grivès A, et al. Clonal restriction and predominance of regulatory T cells in coronary thrombi of patients with acute coronary syndromes. Eur Heart J. 2015;36:1041-1048.
31. Spagnolo M, Giacoppo D, Laudani C, et al. Advances in the Detection and Management of Vulnerable Coronary Plaques. Circ Cardiovasc Interv. 2025; 18:015529.


