RESUMEN
Introducción y objetivos: El estudio EPIC03-BIOSS se llevó a cabo para describir la eficacia del stent farmacoactivo dedicado BIOSS LIM C en el tratamiento de las lesiones en bifurcación, así como la modificación inducida sobre la lesión en bifurcación por angiografía cuantitativa automatizada.
Métodos: Estudio observacional prospectivo en el que se incluyeron 124 pacientes con lesión en bifurcación tratados con stent farmacoactivo BIOSS LIM C, excluidas las lesiones por reestenosis y aquellas en las que no había afección del vaso principal.
Resultados: El stent se implantó con éxito en 121 pacientes (97,6%); en 18 (14,5%) se utilizó una técnica de 2 stents. El análisis por angiografía cuantitativa automatizada mostró una estenosis residual media del 18% en el segmento proximal, de prácticamente el 0% en el segmento distal y del 21% en la rama lateral. Los resultados angiográficos para la técnica de doble stent muestran unos diámetros (2,12 ± 0,30 frente a 1,60 ± 0,42 mm; p < 0,001) y estenosis residuales (18,36 ± 9,94 frente a 28,49 ± 14,19%; p < 0,01) significativamente mejores. La distorsión sobre la angulación nativa del vaso resultó mínima, con una reducción absoluta de unos 5° (52,8 ± 18,4 frente a 47,5 ± 17,2°; p = 0,001).
Conclusiones: El stent BIOSS LIM C consigue una elevada tasa de éxito para el tratamiento de las lesiones en bifurcación. Los resultados angiográficos son buenos, destacando la escasa distorsión sobre la angulación nativa del vaso y los excelentes resultados angiográficos de la técnica de doble stent. Consideramos que puede ser un buen dispositivo para el tratamiento de las bifurcaciones, con la ventaja de poder facilitar la implantación no prevista de un segundo stent.
Palabras clave: Stent dedicado. Lesión en bifurcación. Stent liberador de sirolimus BIOSS LIM C.
ABSTRACT
Introduction and objectives: To describe the efficacy of the BIOSS LIM C dedicated sirolimus-eluting stent to treat coronary bifurcation lesions, and impact on the bifurcation angle and carina through quantitative coronary angiography.
Methods: Observational prospective study including 124 patients with bifurcation lesions treated with a BIOSS LIM C dedicated sirolimus-eluting stent excluding restenotic lesions and those without main vessel involvement.
Results: The stent was successfully deployed in 121 patients (97.6%) while in 18 (14.5%) double stenting was used. The quantitative coronary analysis has shown proper stent expansion with a mean residual stenosis of 18% in the proximal segment, nearly 0% in the distal segment, and 21% in the side branch. The angiographic results of double stenting showed higher mean diameters (2.12 ± 0.30 vs 1.60 ± 0 .42; P < .001), and lower residual stenosis (18.36 ± 9.94 vs 28.49 ± 14.19%, P < .01). Distortion imposed on the bifurcation angulation was minimal with an absolute reduction of 5 degrees (52.8 ± 18.4 vs 47.5 ± 17.2; P = .001).
Conclusions: The dedicated BIOSS LIM C stent has had a very high success rate to treat coronary bifurcation lesions. Angiographic results are good with a remarkably low impact on the native bifurcation angulation, and excellent results from double stenting. We think this can be a very useful device to treat coronary bifurcation lesions with the advantage of easing out the bailout deployment of a second stent into the side branch.
Keywords: Dedicated stent. Bifurcation lesion. BIOSS LIM C sirolimus-eluting stent.
Abreviaturas
OCT: tomografía de coherencia óptica. POT: técnica de optimización proximal. QCA: angiografía cuantitativa automatizada. RL: rama lateral. RP: rama principal.
INTRODUCCIÓN
El tratamiento percutáneo de las bifurcaciones coronarias puede suponer hasta el 20% de las lesiones coronarias tratadas1. La definición de lesión en bifurcación del European Bifurcation Club2 incluye aquellas que afectan una rama lateral (RL) relevante, ya sea por su diámetro angiográfico o por el miocardio en riesgo dependiente de esa RL.
La anatomía pseudofractal de la bifurcación coronaria3 implica una diferencia sensible de calibre entre los segmentos proximal y distal. El estudio de los límites estructurales de los stents tubulares ha favorecido el desarrollo de técnicas de tratamiento4,5 encaminadas a optimizar su implantación en una anatomía que no es completamente cilíndrica, con buenos resultados tanto angiográficos como clínicos6-10. Además, se ha consensuado una estrategia de escalada progresiva, en función de parámetros de afección de la RL, desde el stent provisional hacia la técnica compleja o de 2 stents.
Aunque se han desarrollado plataformas específicas dedicadas al tratamiento de la bifurcación coronaria, estas han quedado limitadas al uso por operadores expertos. Los stents dedicados pueden dividirse en aquellos encaminados a tratar el vaso principal garantizando un buen acceso al RL (Nile Croco & Pax, Minvasys, Francia; Multi-Link Frontier, Abbott Vascular Devices, Estados Unidos; o el TAXUS Petal, Boston Scientific, Estados Unidos) y los dedicados a tratar primero la RL para completar después la rama principal (RP) con un stent tubular (Tryton Side Branch, Tryton Medical, Estados Unidos; Sideguard, Cappella Inc., Estados Unidos). Sin embargo, sea por ofrecer unos resultados discretos o por su complejidad, no se han adoptado de forma universal.
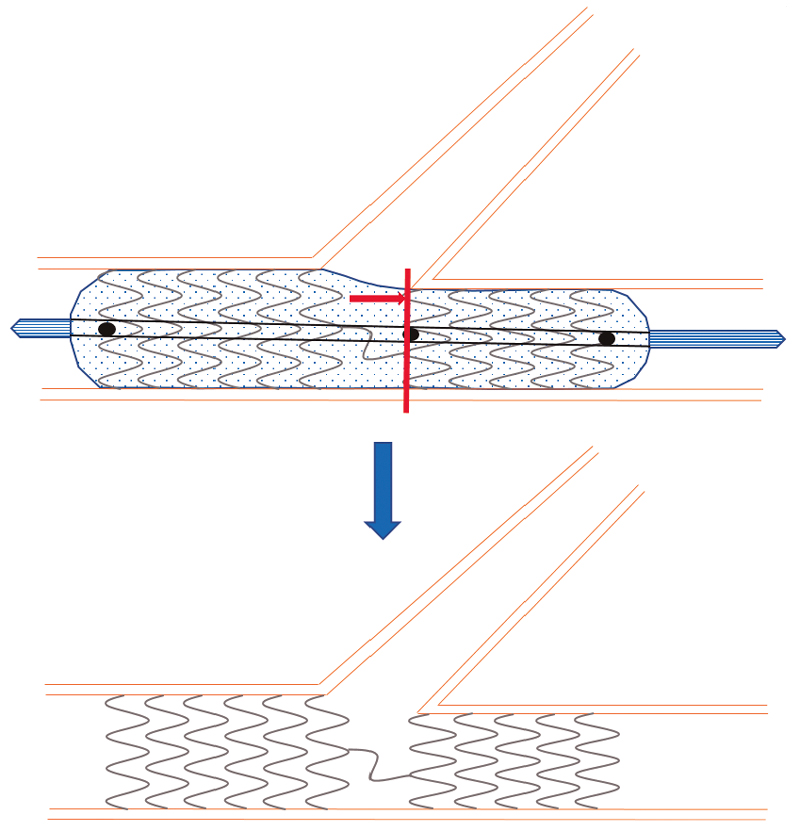
El stent BIOSS LIM C11 (Balton, Polonia) presenta una plataforma de cromo-cobalto de strut ultrafino de 70 µm, recubierta con un polímero biodegradable de ácido poliláctico que libera sirolimus. Es un stent dedicado para bifurcaciones formado por 2 segmentos de distinto tamaño unidos por 2 struts conectores largos (figura 1). Ello persigue mantener la relación pseudofractal entre la porción proximal y distal de la RP, así como facilitar la técnica de acceso a la RL o la técnica de stent provisional. Los estudios previos han mostrado buenos resultados, con una tasa de éxito en el implante del 100% y una incidencia de revascularización de la lesión diana del 6,8-9,8%12-14.
Figura 1. Imagen del diseño del stent BIOSS. Obsérvese la estructura en 2 cuerpos con el espacio central para la rama lateral.
El objetivo del presente estudio es describir los resultados angiográficos inmediatos, evaluados por angiografía cuantitativa automatizada (QCA, quantitative coronary analysis), en términos de deformación de la angulación nativa de la lesión y de expansión, especialmente a nivel del polígono de confluencia y el nacimiento de la RL.
MÉTODOS
Pacientes
Se presenta un registro multicéntrico prospectivo iniciado por investigadores independientes en el que se incluyeron pacientes con cardiopatía isquémica referidos para revascularización coronaria percutánea de una lesión bifurcada, considerando como tal aquella cuyas ramas distales tenían un diámetro mínimo de 2 mm.
Se excluyeron los pacientes con lesiones que afectaban la bifurcación exclusivamente en la RL, reestenosis, oclusiones crónicas completas, contraindicación para la doble antiagregación, shock cardiogénico, menores de edad o con rechazo expreso a ser incluidos en el estudio.
El estudio se realizó de acuerdo de acuerdo con los postulados de la Declaración de Helsinki y su protocolo fue aprobado por los distintos comités de ética de los centros participantes. Se obtuvo el consentimiento firmado específico de todos los pacientes incluidos en el estudio.
Procedimiento
El procedimiento de implantación del stent se realizó siguiendo las recomendaciones de implante específicas del dispositivo (figura 2), realizando el implante y el control final en la proyección angiográfica con mejor despliegue de la bifurcación. La anticoagulación con heparina sódica o de bajo peso molecular se realizó de acuerdo con los estándares habituales en cada sala. El tratamiento específico de la lesión bifurcada se dejó también a cargo del operador. Se permitió el uso de predilatación de ambas ramas, técnica de stent provisional o técnica de 2 stents de inicio, siempre y cuando se utilizara al menos un stent dedicado del estudio para bifurcación.
Figura 2. Esquema del posicionamiento del stent BIOSS para su correcto implante. El marcador central se debe ajustar a la carina de la bifurcación, al ostium de la rama principal distal.
El éxito del procedimiento se definió como la implantación de un stent BIOSS LIM C en la lesión en bifurcación, con estenosis residual por estimación visual < 30% en la RP y < 50% en la RL.
Seguimiento clínico
Se realizó seguimiento telefónico o presencial a los 30 días y a los 12 meses. Se interrogó acerca de eventos cardiacos adversos consistentes en muerte, infarto de miocardio, accidente vascular cerebral, trombosis de stent, necesidad de nueva revascularización o hemorragias.
Análisis angiográfico
El análisis angiográfico lo realizó de forma independiente un laboratorio de imágenes (BARCICORE-Lab, España) mediante un software dedicado para bifurcaciones (QAngio XA 7.3, Países Bajos), con el que se realizaron todas las medidas angiográficas, incluidas las de angulación de la bifurcación. Dos analistas seleccionaron las imágenes previas y posteriores al implante sin presencia de guía intracoronaria y en la misma proyección (menos de 10° de diferencia). El análisis angiográfico se realizó en telediástole siguiendo los protocolos internos del laboratorio.
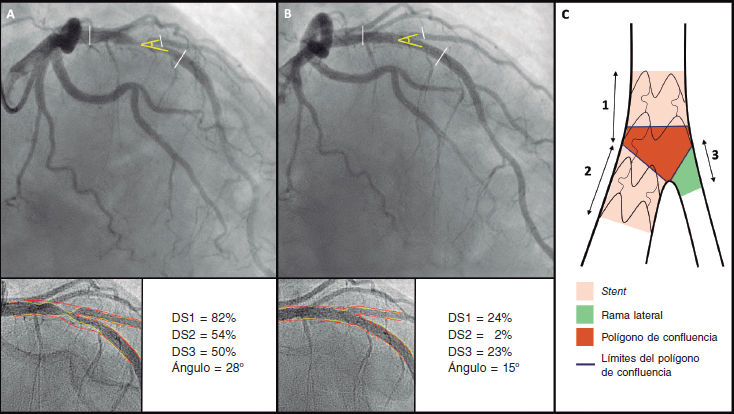
El software utilizado permite la medición simultánea de los 3 segmentos de una bifurcación (RP proximal, RP distal y RL) y obtener resultados por separado de todos los segmentos, incluido el polígono de confluencia de la bifurcación. Todos los análisis se realizaron tomando como referencia los bordes proximal y distal de los stents implantados. En caso de una técnica de implante de 2 stents se utilizó el borde distal del stent implantado en la RL como límite distal de análisis. En caso de implante de un solo stent se utilizaron únicamente los 5 mm proximales de la RL. La figura 3 muestra un ejemplo del análisis angiográfico.
Figura 3. Análisis angiográfico cuantitativo que muestra el tamaño del diámetro de estenosis (DS) en el vaso principal proximal (1), el vaso principal distal (2) y los 5 mm proximales de la rama lateral (3), preintervención (A) y posintervención (B). También se mide el cambio en el ángulo de la bifurcación entre las ramas distales. La imagen C muestra los límites de cada segmento (1, 2 y 3) y los bordes del polígono de confluencia.
Estadística
Todos los datos cuantitativos se presentan como media ± desviación estándar (DE) y los datos cualitativos en número (porcentaje). Para el análisis de QCA entre los valores angiográficos preimplante y posimplante se utilizaron las prueba t de Student para datos apareados (datos cuantitativos) y de McNemar (datos cualitativos) de forma apropiada. Para el análisis comparativo entre las cohortes de stent provisional y doble stent se utilizaron las pruebas t de Student o U de Mann-Whitney (datos cuantitativos) y χ² o exacta de Fisher (datos cualitativos), según procediera. Se estableció como significación estadística un valor de p ≤ 0,05. Los análisis estadísticos se realizaron con el programa SPSS versión 20.
RESULTADOS
Datos clínicos basales
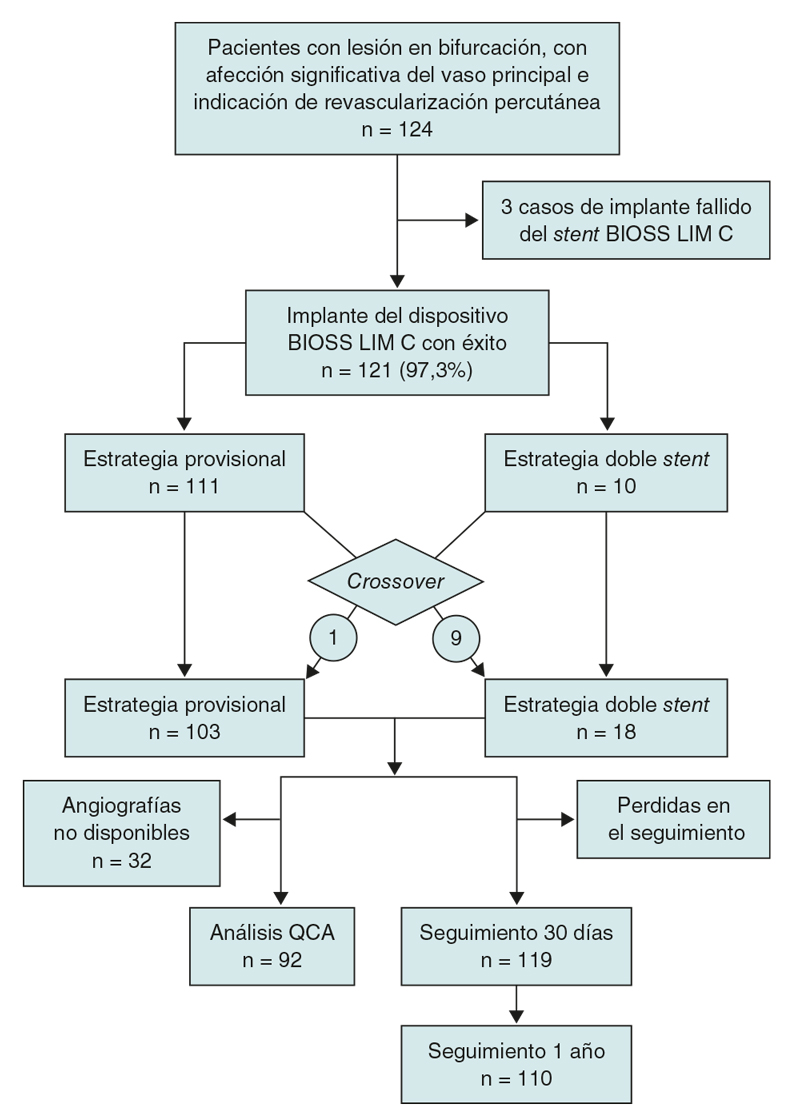
Entre agosto de 2018 y febrero de 2021 se incluyeron 124 pacientes en el estudio (figura 4), cuyos datos demográficos se muestran en la tabla 1. Destacan una proporción de diabéticos del 26,9% (32/124) y una proporción de pacientes con síndrome coronario agudo del 52,8% (66/124), de ellos un 12,8% (16/124) con elevación del segmento ST en curso. No hubo diferencias significativas en cuanto a las características clínicas basales entre la cohorte de estrategia de un stent y la cohorte de doble stent.
Tabla 1. Descripción de la población
| Total | |
|---|---|
| Demográficas basales | 124 |
| Sexo femenino | 23 (18,47%) |
| Edad | 65,48 (11,09) |
| Hipertensión arterial | 79 (63,2%) |
| Dislipemia | 72 (57,6%) |
| Diabetes mellitus | 32 (25,6%) |
| Tratamiento con insulina | 8 (6,4%) |
| Fumador | 39 (31,2%) |
| Insuficiencia renal crónica | 10 (8%) |
| Vasculopatía periférica | 8 (6,4%) |
| Tratamiento de base | |
| Ácido acetilsalicílico | 81 (64,8%) |
| Clopidogrel | 34 (27,2%) |
| Ticagrelor | 18 (14,4%) |
| Prasugrel | 2 (0,6%) |
| Anticoagulantes orales | 9 (7,2%) |
| Inhibidores vitamina K | 1 (0,8%) |
| Anticoagulantes orales de acción directa | 8 (6,4%) |
| Indicación | |
| Angina estable | 37 (29,6%) |
| Isquemia silente | 12 (9,6%) |
| Disfunción ventricular | 3 (2,4%) |
| SCACEST | 6 (4,8%) |
| SCASEST/angina inestable | 16 (12,8%) |
| SCASEST/infarto de miocardio | 34 (27,2%) |
| SCACEST | 16 (12,8%) |
| IAM | 25 (20%) |
| CABG previa | 4 (3,2%) |
| ICP previa | 29 (23,2%) |
| Fracción de eyección (%) | 54,31 (12,29) |
| Fibrilación auricular | 9 (7,2%) |
| Insuficiencia cardiaca | 16 (12,8%) |
| CABG: cirugía de revascularización coronaria; IAM: infarto agudo de miocardio; ICP: intervencionismo coronario percutáneo; SCACEST: síndrome coronario agudo con elevación del segmento ST; SCASEST: síndrome coronario sin elevación del segmento ST. | |
Figura 4. Diagrama de flujo del estudio EPIC03-BIOSS. QCA: angiografía cuantitativa automatizada.
Datos angiográficos y de procedimiento
Los datos angiográficos y de procedimiento se muestran en la tabla 2 y la tabla 3. Destaca que la gran mayoría de los procedimientos se realizaron por vía radial (120, el 96,8%) y que la angiografía mostró enfermedad coronaria de 3 vasos en 19 pacientes (15,3%). En 10 casos (8%) la lesión tratada fue en el tronco común izquierdo. En cuanto a complejidad, en 55 pacientes (44,3%) las lesiones tratadas fueron de las categorías B2/C de la American Heart Association/American College of Cardiology y 32 lesiones (25,8%) tenían una calcificación moderada o grave.
Tabla 2. Datos angiográficos por estimación visual
| Total | Provisional | Compleja | p | |
|---|---|---|---|---|
| Acceso radial | 120 (96%) | 110 (97,3%) | 10 (90,9%) | 0,314 |
| Lesión de TC | 11 (8,8%) | 10 (8,8%) | 1 (9,1%) | 0,830 |
| DA proximal | 77 (61,6%) | 71 (62,8%) | 6 (54,5%) | 0,746 |
| Enfermedad coronaria | 0,524 | |||
| 1 vaso | 55 (44%) | 51 (46,4%) | 4 (36,4%) | |
| 2 vasos | 47 (37,6%) | 43 (39,1%) | 4 (36,4%) | |
| 3 vasos | 19 (15,2%) | 16 (14,5%) | 3 (27,3%) | |
| Dominancia derecha | 109 (87,2%) | 99 (87,6%) | 10 (90,9%) | 0,773 |
| Bifurcación afectada | 0,693 | |||
| TC-DA/Cx | 10 (8%) | 8 (7,3%) | 2 (18,2%) | |
| DA/diagonal | 71 (56,8%) | 53 (57,5%) | 4 (54,6%) | |
| Cx/OM | 28 (22,4%) | 25 (22,2%) | 3 (27,3%) | |
| CD/PL | 15 (12,0%) | 15 (13,2%) | 0 (0%) | |
| Clasificación de Medina | 0,001 | |||
| 100 | 8 (6,4%) | 8 (7,3%) | 0 (0%) | |
| 010 | 18 (14,4%) | 18 (15,9%) | 0 (0%) | |
| 001 | 0 (0%) | 0 (0%) | 0 (0%) | |
| 110 | 38 (30,4%) | 38 (33,6%) | 0 (0%) | |
| 101 | 5 (4%) | 5 (4,4%) | 0 (0%) | |
| 011 | 10 (8%) | 6 (5,3%) | 4 (36,4%) | |
| 111 | 44 (35,2%) | 38 (33,6%) | 6 (54,5%) | |
| Verdadera | 59 (47,2%) | 49 (43,3%) | 10 (100%) | |
| Calcificación (moderada o grave) | 32 (25,6%) | 28 (24,8%) | 4 (36,4%) | 0,542 |
| Tortuosidad proximal | 25 (20%) | 20 (17,7%) | 5 (45,5%) | 0,04 |
| Trombo | 15 (20%) | 14 (12,4%) | 1 (0,9%) | 1,000 |
| Tipo de lesión | 0,362 | |||
| A | 3 (2,4%) | 3 (2,7%) | 0 (0%) | |
| B1 | 37 (29,6%) | 31 (27,4%) | 6 (54,5%) | |
| B2 | 45 (36%) | 43 (38,1%) | 2 (18,2%) | |
| C | 10 (8%) | 10 (8,8%) | 0 (0,0%) | |
| CD: coronaria derecha; Cx: circunfleja; DA: descendente anterior; OM: oblicua marginal; PL: posterolateral; TC: tronco común. | ||||
Tabla 3. Descripción del procedimiento y seguimiento
| Total | Provisional | Compleja | p | |
|---|---|---|---|---|
| Procedimiento | 124 | 106 (85,5%) | 18(14,5%) | |
| Estrategia inicial | 124 | 113 (90,4%) | 11 (9,6%) | |
| Catéter guía | 0,289 | |||
| 6 Fr | 113 (90,4%) | 104 (92%) | 9 (81,8%) | |
| 7 Fr | 10 (8%) | 8 (7,1%) | 2 (18,2%) | |
| 8 Fr | 1 (0,8%) | 1 (0,9%) | 0 (0%) | |
| Predilatación RL | 100 (80%) | 90 (79,6%) | 10 (90,9%) | 0,690 |
| Aterectomía rotacional | 0 (0%) | 0 (0%) | 0 | 1,000 |
| Implantación de stent | 121 (97,6%) | 111 (98,2%) | 10 (90,9%) | 0,314 |
| Longitud del stent | 19,73 (3,23) | 19,57 (3,21) | 21,45 (3,04) | 0,064 |
| POT | 33 (26,6%) | 30 (26,5%) | 3 (27,3%) | 0,800 |
| Dilatación RL | 47 (37,9%) | 43 (38,1%) | 4 (36,4%) | 0,449 |
| Kissing tras stent en RP | 21 (44,7%) | 21 (48,8%) | 0 (0%) | |
| Solo dilatación RL | 26 (55,3%) | 22 (51,2%) | 4 (100%) | |
| Stent adicional | 17 (13,7%) | 16 (14,2%) | 1 (9,1%) | |
| Stent en RL | 18 (14,5%) | 9 (8%) | 9 (81,8%) | 0,000 |
| Kissing tras stent en RL | 16 (88,9%) | 7 (77,8%) | 9 (100%) | |
| Imagen | 11 (8,9%) | 8 (7,1%) | 3 (27,3%) | 0,023 |
| IVUS | 9 (7,3%) | 7 (6,2%) | 2 (18,2%) | |
| OCT | 2 (1,6%) | 1 (0,9%) | 1 (9,1%) | |
| Complicaciones | 1 (0,8%) | 1 (0,9%) | 0 | |
| Oclusión RL | 1 (0,8%) | 1 (0,9%) | 0 (0%) | |
| Éxito (ausencia de estenosis ≥ 50%) | 114 (91,2%) | 104 (92%) | 10 (90,9%) | 0,338 |
| TIMI RP | 0,638 | |||
| 3 | 114 (91,9%) | 103 (91,2%) | 11 (100%) | |
| 2 | 0 (0%) | 0 (0%) | 0 (0%) | |
| 1 | 3 (2,4%) | 3 (2,7%) | 0 (0%) | |
| TIMI RL | 0,638 | |||
| 3 | 114 (91,9%) | 103 (91,2%) | 11 (100%) | |
| 2 | 0 (0%) | 0 (0%) | 0 (0%) | |
| 1 | 3 (2,4%) | 3 (2,7%) | 0 (0%) | |
| Estenosis RP | 3,27% (6,14) | 3,24% (6,25) | 3,57% (4,76) | 0,892 |
| Estenosis RL | 14,74% (19,94) | 15,55% (20,45) | 4,29% (4,5) | 0,211 |
| Estenosis ≥ 50% RP | 0 (0%) | 0 (0%) | 0 (0%) | 1,000 |
| Estenosis ≥ 50% RL | 7 (7,1%) | 7 (7,7%) | 0 (0%) | 0,585 |
| Estenosis ≥ 30% RL | 22 (22,4%) | 22 (24,2%) | 0 (0%) | 0,158 |
| Seguimiento 12 meses | 110 (88,7%) | 92 (86,8%) | 18 (100%) | |
| Muerte | 0 (0%) | 0 (0%) | 0 (0%) | |
| IAM relacionado con stent | 2 (1,8%) | 1 (1,1%) | 1 (5,5%) | 0,223 |
| ReICP | 6 (5,4%) | 5 (5,4%) | 1 (5,5%) | 0,555 |
| Trombosis | 1 (0,9%) | 0 (0%) | 1 (5,5%) | 0,115 |
| IAM: infarto agudo de miocardio; IVUS: ecocardiografía intravascular; ReICP: reintervencionismo coronario percutáneo; RL: rama lateral; RP: rama principal; OCT: tomografía de coherencia óptica; POT: técnica de optimización proximal; TIMI: Thrombolysis in Myocardial Infarction. | ||||
Cuando analizamos las diferencias entre las cohortes tratadas con técnica de stent provisional y de doble stent (tabla 2 y tabla 3) observamos que, en la segunda, la proporción de bifurcaciones verdaderas, la tortuosidad proximal y el uso de técnicas de imagen eran significativamente mayores.
Durante el procedimiento (tabla 3) se consiguió implantar el stent BIOSS LIM C con éxito en 121 pacientes (97,6%). En los 3 casos en que no se implantó el stent, las lesiones presentaban calcificación moderada o grave y tortuosidad proximal. Un paciente de los 121 que recibieron el implante se complicó con oclusión de la RL por disección, que no pudo ser revascularizada. De los 113 casos (90,4%) en que se adoptó una estrategia inicial de stent provisional, en 30 (26,5%) se realizó una técnica de optimización proximal (POT, proximal optimization technique) y en 43 (38,1%) fue preciso dilatar la RL, ya fuera mediante kissing-balón o dilatación simple (tabla 3). Finalmente, en 9 pacientes (7,2%) en los que inicialmente se adoptó una estrategia de un solo stent se requirió un segundo stent en la RL. La estrategia de doble stent se adoptó de entrada en 11 pacientes (9,6%); sin embargo, tras la dilatación de la RL y la implantación del stent en la RP, en 2 de ellos (18,2%) se consideró que no era necesaria la implantación del segundo stent. Así, finalmente, 18 pacientes (14,5%) fueron tratados con una técnica de 2 stents. Las proporciones de predilatación, aterectomía rotacional, uso de POT y éxito del implante fueron similares en ambas cohortes.
Angiografía cuantitativa de la bifurcación
Se dispuso de imágenes angiográficas de 92 pacientes (tabla 4), en las que se observó una estenosis residual media del 18% en el segmento proximal y de prácticamente el 0% en el segmento distal de la RP. En la RL, la estenosis residual media tras el procedimiento fue del 21%, con una estenosis residual significativa en el 5% de los pacientes, todos ellos tratados con técnica de stent provisional.
Tabla 4. Análisis por angiografía cuantitativa automatizada de la bifurcación en el conjunto de la cohorte. Comparación entre stent simple y doble stent
| N = 92 lesiones | Toda la población (n = 92) | Técnica 1 stent (n = 75) | Técnica 2 stents (n = 17) | ||||||
|---|---|---|---|---|---|---|---|---|---|
| Total | Pre | Post | p | Pre | Post | p | Pre | Post | p |
| Diámetro luminal mínimo, mm | 0,97 ± 0,48 | 1,70 ± 0,44 | < 0,001 | 0,99 ± 0,48 | 1,60 ± 0,42 | < 0,001 | 0,85 ± 0,47 | 2,12 ± 0,30 | < 0,001 |
| Estenosis máxima por diámetro, % | 62,78 ± 17,70 | 26,62 ± 14,03 | < 0,001 | 61,63 ± 17,92 | 28,49 ± 14,19 | < 0,001 | 67,86 ± 16,25 | 18,36 ± 9,94 | < 0,001 |
| Ángulo carinal, grados | 52,8 ± 18,4 | 47,5 ± 17,2 | 0,001 | 52,3 ± 13,4 | 46,4 ± 18,1 | 0,002 | 55,3 ± 13,3 | 51,9 ± 12,5 | 0,161 |
| Rama principal proximal | |||||||||
| Longitud, mm | 11,15 ± 5,28 | 10,86 ± 5,22 | 0,154 | 11,56 ± 5,59 | 11,21 ± 5,53 | 0,155 | 9,06 ± 2,50 | 8,97 ± 2,69 | 0,776 |
| Diámetro luminal de referencia, mm | 3,83 ± 1,13 | 3,88 ± 0,80 | 0,674 | 3,65 ± 0,98 | 3,84 ± 0,71 | 0,089 | 4,75 ± 1,42 | 4,10 ± 1,12 | 0,066 |
| Diámetro luminal mínimo, mm | 1,63 ± 0,85 | 2,96 ± 0,62 | < 0,001 | 1,60 ± 0,77 | 2,85 ± 0,46 | < 0,001 | 1,78 ± 1,15 | 3,50 ± 0,93 | < 0,001 |
| Estenosis por diámetro, % | 55,36 ± 20,81 | 18,09 ± 10,34 | < 0,001 | 54,12 ± 20,78 | 19,44 ± 10,01 | < 0,001 | 61,16 ± 20,58 | 11,77 ± 9,78 | < 0,001 |
| Estenosis binaria (ED ≥ 50%), n (%) | 58 (63,0) | 0 | < 0,001 | 45 (60,0) | 0 | < 0,001 | 13 (76,5) | 0 | < 0,001 |
| Rama principal distal (BIOSS) | |||||||||
| Longitud, mm | 10,35 ± 5,36 | 9,96 ± 5,46 | 0,190 | 10,61 ± 5,69 | 10,28 ± 5,76 | 0,105 | 9,13 ± 3,24 | 8,66 ± 3,43 | 0,082 |
| Diámetro luminal de referencia, mm | 2,33 ± 0,45 | 2,34 ± 0,42 | 0,797 | 2,29 ± 0,45 | 2,32 ± 0,42 | 0,547 | 2,49 ± 0,39 | 2,42 ± 0,40 | 0,409 |
| Diámetro luminal mínimo, mm | 1,19 ± 0,56 | 2,28 ± 0,36 | < 0,001 | 1,24 ± 0,56 | 2,27 ± 0,37 | < 0,001 | 0,99 ± 0,53 | 2,34 ± 0,30 | < 0,001 |
| Estenosis por diámetro, % | 48,43 ± 23,07 | 0,12 ± 15,00 | < 0,001 | 46,67 ± 22,98 | −0,62 ± 15,06 | < 0,001 | 60,61 ± 19,77 | 3,40 ± 14,74 | < 0,001 |
| Estenosis binaria (ED ≥ 50%), n (%) | 43 (46,7) | 0 | < 0,001 | 31 (41,3) | 0 | < 0,001 | 12 (70,6) | 0 | < 0,001 |
| Rama lateral | |||||||||
| Longitud, mm | 6,32 ± 3,81 | 6,27 ± 3,47 | 0,689 | 5,20 ± 0,99 | 5,21 ± 0,89 | 0,905 | 11,58 ± 6,88 | 11,25 ± 6,08 | 0,549 |
| Diámetro luminal de referencia, mm | 2,18 ± 0,48 | 2,22 ± 0,49 | 0,199 | 2,12 ± 0,46 | 2,16 ± 0,42 | 0,268 | 2,42 ± 0,51 | 2,49 ± 0,71 | 0,536 |
| Diámetro luminal mínimo, mm | 1,41 ± 0,64 | 1,75 ± 0,52 | < 0,001 | 1,46 ± 0,57 | 1,62 ± 0,43 | 0,022 | 1,19 ± 0,88 | 2,31 ± 0,50 | < 0,001 |
| Estenosis por diámetro, % | 34,16 ± 27,52 | 20,94 ± 19,14 | < 0,001 | 30,06 ± 25,34 | 24,35 ± 17,13 | 0,070 | 52,24 ± 30,19 | 5,88 ± 20,77 | < 0,001 |
| Estenosis binaria (ED ≥ 50%), n (%) | 22 (23,9) | 5 (5,4) | < 0,001 | 13 (17,3) | 5 (6,6) | 0,044 | 9 (52,9) | 0 | < 0,001 |
| ED: estenosis por diámetro. | |||||||||
Si se comparan los pacientes tratados con una técnica de un solo stent con aquellos tratados con 2 stents (tabla 4), se observa que, en el segmento proximal, los resultados de expansión son mejores con la técnica de doble stent, con una estenosis residual del 11% (frente al 19% con un solo stent), aunque partiendo de unos mayores diámetros de referencia basales (3,65 ± 0,98 frente a 4,75 ± 1,42 mm). La técnica de doble stent mostró un excelente resultado sobre la RL, con un diámetro luminal mínimo significativamente mayor (2,31 ± 0,50 frente a 1,62 ± 0,43 mm; p = 0,01) y una estenosis residual mínima del 5,9% (frente al 24,3% con la técnica provisional), destacando especialmente la ausencia de estenosis > 50%. En el segmento distal, los resultados fueron similares.
Angiografía cuantitativa del polígono de confluencia
En el polígono de confluencia (tabla 5) los resultados indican estenosis residuales del 17,15 ± 10,96% en el núcleo del polígono y del 19,21 ± 20,56% para el ostium de la RL. Al comparar las técnicas provisional y de doble stent (tabla 5), los datos del análisis QCA muestran unos diámetros luminales mínimos mejores para la técnica de 2 stents en el núcleo de la bifurcación y en el ostium de la RL, resultando prácticamente iguales para el ostium del segmento distal.
Tabla 5. Análisis por angiografía cuantitativa automatizada. Polígono de confluencia. Comparación entre stent simple y doble stent
| N = 92 lesiones | Toda la población (n = 92) | Técnica 1 stent (n = 75) | Técnica 2 stents (n = 17) | ||||||
|---|---|---|---|---|---|---|---|---|---|
| Pre | Post | p | Pre | Post | p | Pre | Post | p | |
| Núcleo de la bifurcación | |||||||||
| Diámetro luminal de referencia, mm | 4,04 ± 1,13 | 3,97 ± 0,80 | 0,531 | 3,83 ± 0,97 | 3,88 ± 0,69 | 0,618 | 4,82 ± 1,34 | 4,35 ± 1,10 | 0,095 |
| Diámetro luminal mínimo, mm | 2,09 ± 0,94 | 3,28 ± 0,78 | < 0,001 | 1,87 ± 0,72 | 2,93 ± 0,49 | < 0,001 | 2,25 ± 0,98 | 3,63 ± 0,90 | < 0,001 |
| Estenosis por diámetro, % | 48,49 ± 17,94 | 17,15 ± 10,96 | < 0,001 | 47,57 ± 18,23 | 18,76 ± 10,68 | < 0,001 | 52,39 ± 15,70 | 10,31 ± 9,63 | < 0,001 |
| Estenosis binaria (ED ≥ 50%), n (%) | 46 (50,0) | 0 | < 0,001 | 35 (46,7) | 0 | < 0,001 | 11 (64,7) | 0 | 0,001 |
| Ostium rama principal distal (BIOSS) | |||||||||
| Diámetro luminal de referencia, mm | 2,34 ± 0,45 | 2,35 ± 0,43 | 0,842 | 2,29 ± 0,45 | 2,32 ± 0,42 | 0,544 | 2,55 ± 0,40 | 2,48 ± 0,43 | 0,406 |
| Diámetro luminal mínimo, mm | 1,38 ± 0,53 | 2,40 ± 0,37 | < 0,001 | 1,40 ± 0,50 | 2,39 ± 0,36 | < 0,001 | 1,32 ± 0,67 | 2,45 ± 0,41 | < 0,001 |
| Estenosis por diámetro, % | 40,59 ± 21,36 | −3,67 ± 15,54 | < 0,001 | 38,61 ± 20,61 | −4,57 ± 15,76 | < 0,001 | 48,95 ± 23,07 | 0,13 ± 14,37 | < 0,001 |
| Estenosis binaria (ED ≥ 50%), n (%) | 34 (37,0) | 0 | < 0,001 | 23 (30,7) | 0 | < 0,001 | 11 (64,7) | 0 | 0,001 |
| Ostium rama lateral | |||||||||
| Diámetro luminal de referencia, mm | 2,21 ± 0,50 | 2,24 ± 0,51 | 0,280 | 2,14 ± 0,46 | 2,17 ± 0,41 | 0,375 | 2,51 ± 0,56 | 2,57 ± 0,72 | 0,553 |
| Diámetro luminal mínimo, mm | 1,56 ± 0,52 | 1,80 ± 0,55 | < 0,001 | 1,58 ± 0,47 | 1,65 ± 0,45 | 0,219 | 1,47 ± 0,71 | 2,40 ± 0,52 | < 0,001 |
| Estenosis por diámetro, % | 28,21 ± 21,77 | 19,21 ± 20,56 | 0,004 | 24,91 ± 20,30 | 23,13 ± 17,97 | 0,501 | 42,19 ± 22,82 | 2,58 ± 22,99 | < 0,001 |
| Estenosis binaria (ED ≥ 50%), n (%) | 16 (17,4) | 5 (5,4) | 0,012 | 9 (12,0) | 5 (6,7) | 0,267 | 7 (41,2) | 0 | 0,016 |
| ED: estenosis por diámetro. | |||||||||
El ángulo de la bifurcación (tabla 4) mostró una ligera modificación tras la implantación del stent, con una reducción estadísticamente significativa desde 52,8 ± 18,4° hasta 47,5 ± 17,2° (p = 0,001). En la cohorte de doble stent, la modificación de la angulación en términos absolutos fue similar, con una reducción de unos 4°, pero esta diferencia no alcanzó la significación estadística (tabla 4). No se observó una correlación significativa entre el grado de modificación de la angulación y la estenosis residual de la RL (p = 0,86).
Resultados clínicos
Durante el procedimiento se comunicó una sola complicación, que consistió en la oclusión de la RL en un paciente a quien se implantó el stent con la técnica provisional, que no se consiguió recuperar. A 30 días no hubo ningún evento clínico mayor, ningún caso de trombosis de stent ni ninguna revascularización de la lesión diana.
Al año del implante se pudo contactar con 110 pacientes (88,7%) y se observó un caso de trombosis definitiva del dispositivo (0,91%), concretamente en un doble stent, que fue tratado mediante angioplastia primaria. Este, junto con otros 5 casos de nueva revascularización de la lesión diana por reestenosis (4,54%), suponen una incidencia de fracaso de la lesión diana del 5,45% a los 12 meses. De estas reestenosis, 2 se localizaron en el ostium de la RL, mientras que las otras 3 afectaron al vaso principal. No hubo ningún fallecimiento y se produjeron 3 infartos (2,72%), todos ellos relacionados con el dispositivo, por trombosis de un stent y, en los otros 2 casos, por reestenosis con mínima movilización de troponina.
DISCUSIÓN
Los principales hallazgos del presente estudio son: a) el stent dedicado BIOSS LIM C obtiene una alta tasa de éxito a 30 días en los pacientes con lesiones bifurcadas complejas; b) dicho dispositivo se utiliza básicamente con una estrategia de stent provisional y se asocia con una necesidad muy reducida de implante de stent en la RL; y c) los resultados angiográficos inmediatos demuestran un correcto comportamiento del stent en los 3 segmentos de la bifurcación y en el polígono de confluencia, donde la superficie de contacto entre el stent y la arteria es mínimo.
Los datos demográficos confirman que se trata de una población no seleccionada, con una prevalencia de factores de riesgo, comorbilidad y patología cardiaca, así como unas características anatómicas de las lesiones, que se corresponden con el día a día de cualquier unidad de hemodinámica.
El dispositivo mostró una elevada proporción de éxito de implante, acorde con la sencillez de su diseño, pues fue implantado con éxito en más del 97% de los casos. Se trata de una tasa de éxito similar a la descrita en la mayoría de los estudios con stents tubulares en bifurcación, lo que no siempre se había comunicado en las series previas de stents dedicados (estudios Axxess, Frontier y Nile). El stent Frontier15, por ejemplo, presentaba una incidencia de reestenosis del 29,9%. El stent Nile16,17 sí se usó con éxito en arterias tortuosas y segmentos distales, con aceptables resultados, con un 8,4% de revascularización de la lesión diana; sin embargo, requería una distribución de la estenosis angiográfica centrada en la carina. El stent Axxess18, autoexpandible, mostró resultados favorables, con una incidencia de eventos cardiovasculares al año del 7,7% y de reestenosis del 6,4%, pero en realidad solo trataba el polígono de confluencia y el segmento inmediatamente proximal a los ostia de las ramas, y además se limitaba a determinados ángulos y longitudes, requiriendo en muchas ocasiones del uso de stents adicionales.
En el 14,5% de los casos se realizó una técnica con 2 stents. Se trata de un stent dedicado, de forma que, al cruzar a la RL, la ausencia de struts en el polígono de confluencia facilita su avance sin requerir la apertura previa. Los resultados del estudio parecen apoyar su facilidad de uso para realizar una técnica de 2 stents. En todos los casos en que se intentó, se consiguió implantar el segundo stent en la RL. De los 9 casos en que se planteó una estrategia de doble stent de entrada, en 6 (66%) el stent de la RL se implantó directamente, sin mediar dilatación. Este dato, aunque muy limitado, podría señalar una posible ventaja del dispositivo dedicado BIOSS LIM C para facilitar el acceso a la RL a un segundo stent, en caso de que fuera necesario. Por otra parte, los resultados angiográficos tras el implante son especialmente destacables para la técnica de 2 stents: tanto los diámetros luminales mínimos como la estenosis residual en los segmentos proximal y la RL son mejores que en la cohorte de la técnica provisional.
Al analizar los datos del procedimiento, llama la atención la predilatación de la RL en 47 casos en los que esta no presentaba afección significativa. El protocolo no definía la obligación de predilatar la RL; se hizo a criterio del investigador en cada caso, por observar la presencia de una lesión que, aunque no alcanzara el 50% de estenosis, se considerara que presentaba riesgo de desplazamiento de la carina.
Otro de los aspectos destacables es el uso llamativamente bajo de la POT, que se realizó en 33 casos (26%), y de forma similar en ambas cohortes. A este respecto, cabe recordar que el dispositivo está diseñado con un segmento proximal de mayor calibre, de forma que con el simple inflado lleva incorporada esta posdilatación proximal. En los estudios POLBOS I19 y II14 se observó que la realización de POT mejoraba la incidencia de revascularización de la lesión diana, con una tendencia a una menor pérdida luminal tardía, pero se realizó POT en una proporción del 37%, similar a la de nuestra cohorte.
Uno de los objetivos principales del estudio era valorar la potencial desventaja del diseño en 2 segmentos del stent. Este diseño propicia un espacio para el polígono de confluencia, de 0,9-1,5 mm entre ambos segmentos, unidos por 2 conectores. En este espacio, la relación metal/arteria es significativamente menor, lo cual podría redundar en una relativa infraexpansión sistemática.
Los resultados sobre el polígono de confluencia de la cohorte provisional muestran que la estenosis residual media es de alrededor del 19% en el propio núcleo del polígono y del 23% en el ostium de la RL. Estos datos sugieren un cierto impacto en los resultados angiográficos de esta relativa falta de armazón entre ambos segmentos, que consideramos podría ser la causa de cierto grado de infraexpansión en el polígono de confluencia.
Otro de los objetivos principales del estudio era valorar la afección en la angulación nativa de la bifurcación. Godino et al.20 analizaron la modificación del ángulo de la bifurcación tras una angioplastia con técnica de 1 o 2 stents en una cohorte de 215 pacientes. Describieron una reducción media de alrededor de 10° del ángulo en el tronco coronario y de 7° en el resto de las bifurcaciones con la implantación de 2 stents, mientras que con la técnica provisional no encontraron diferencias significativas. En nuestro estudio, los resultados en el conjunto de la población muestran una modificación estadísticamente significativa, aunque numéricamente poco relevante, del ángulo de la bifurcación, que pasó de unos 53° a unos 47°. Al contrario que lo descrito por Godino et al.20, en nuestro estudio, en la cohorte de 2 stents, la modificación del ángulo no resultó significativa, con una reducción media de unos 3°. Sin embargo, en la cohorte provisional se observó una reducción significativa del ángulo, de unos 6°. En todo caso, consideramos que se trata de una simple significación estadística; parece poco probable que 5° de variación del ángulo de la bifurcación sean perceptibles en la estimación visual, y menos que aporten alguna desventaja en términos clínicos.
Los resultados en el seguimiento fueron globalmente buenos y en la línea de lo observado en estudios previos14,19. Hubo una pérdida significativa de casos para el análisis por QCA, pues solo se dispuso de 92 resultados. Otra de las limitaciones del estudio concierne al análisis de la técnica de 2 stents. A pesar de que los datos de QCA sugieren un buen resultado de la técnica de 2 stents, el estudio no estaba diseñado para hacer una comparación entre las técnicas provisional y de doble stent, la información recogida es limitada y el número de pacientes tratados con doble stent resulta insuficiente para llegar a ninguna conclusión.
Una limitación adicional que cabe señalar es el escaso uso de las técnicas de imagen; probablemente, en las lesiones en bifurcación su uso sistemático aportaría beneficio.
Para concluir, consideramos que el presente estudio, realizado en varios centros con distintos operadores, pone de relieve la sencillez de uso del stent BIOSS LIM C para el tratamiento de las lesiones en bifurcación. Nos parece especialmente destacable para simplificar el abordaje con la técnica de 2 stents, en la que nos llama la atención la escasa distorsión que se sobreimpone a la angulación nativa de la bifurcación. Por otra parte, como punto débil reseñaríamos el débil armazón metálico que queda en el polígono de confluencia, que consideramos relacionado con cierto grado de infraexpansión. Sin embargo, los buenos resultados clínicos en el seguimiento al año parecen indicar que este diseño no supone un problema relevante.
Limitaciones
Se trata de un estudio observacional prospectivo, por lo que cualquier comparación con las técnicas de tratamiento habitual de las lesiones en bifurcación puede resultar limitada. No se obtuvo el seguimiento de todos los pacientes; aunque se contó con información del 88% de la cohorte, las pérdidas en el seguimiento fueron ligeramente mayores de lo debido.
CONCLUSIONES
El stent dedicado BIOSS LIM C muestra un buen comportamiento en el abordaje de las lesiones en bifurcación. Angiográficamente, el stent tiene un espacio a nivel del polígono de confluencia para permitir un acceso más fácil a la RL. Ello supone una ratio metal/arteria más baja, lo que condiciona una estenosis residual de alrededor del 20%. Sin embargo, esta estenosis residual no supone un aumento relevante de eventos al año, y a la postre el diseño carinal permite un fácil acceso a la RL en caso de requerir un segundo stent, con excelentes resultados. Finalmente, la distorsión inducida por el stent sobre el ángulo de la carina es limitada, de unos 5°.
FINANCIACIÓN
El estudio contó con una beca de la fundación EPIC, financiada de forma no condicionada por el grupo LOGSA.
CONTRIBUCIÓN DE LOS AUTORES
B. García del Blanco y A. Pérez de Prado, como coinvestigadores principales del estudio, escribieron el protocolo, gestionaron la financiación y la realización del proyecto, incluyeron pacientes, escribieron parte del artículo e hicieron aportaciones a la redacción general del artículo. J. Gómez-Lara realizó los análisis angiográficos en el laboratorio centralizado, participó en el análisis estadístico, escribió parte del artículo e hizo aportaciones a la redacción general. I. Otaegui Irurueta, como subinvestigador, incluyó pacientes en el estudio y realizó los procedimientos y seguimientos del protocolo, introdujo la información requerida en el cuaderno de recogida de datos, realizó la depuración y la finalización de los datos introducidos, participó en el análisis estadístico, escribió parte del artículo, concluyó la redacción general aunando las diferentes secciones del resto de los autores y respondió a las correcciones solicitadas por los revisores. M.A. Carmona Ramírez se encargó de las gestiones regulatorias necesarias para iniciar el estudio e incluir los diferentes centros, tanto con la Agencia Española de Medicamentos y Productos Sanitarios como con los diferentes centros y comités de ética. El resto de los autores, como subinvestigadores del estudio, incluyeron pacientes, realizaron los procedimientos y los seguimientos según el protocolo, rellenaron el cuestionario de recogida de datos y respondieron a todas las cuestiones que se les solicitó.
CONFLICTO DE INTERESES
A. Pérez de Prado es editor asociado de REC: Interventional Cardiology; se ha seguido el procedimiento editorial establecido en la revista para garantizar la gestión imparcial del manuscrito. A. Pérez de Prado ha recibido ayudas a la investigación de entidades promotoras de investigación (Fundación EPIC): Abbott, Biosensors, Biotronik, Bristol-Myers-Squibb, Boston Scientific, Cardiva, iVascular, Shockwave Ltd., Terumo y Volcano Philips; y honorarios por consultoría teórica o práctica (proctoring): Braun, Boston Scientific y Terumo. Los demás autores declaran no tener ningún conflicto de intereses.
¿QUÉ SE SABE DEL TEMA?
- Los stents dedicados ofrecen la posibilidad de adaptarse mejor a la anatomía fractal de las lesiones en bifurcación, con una menor distorsión del ángulo de bifurcación y permitiendo un acceso facilitado para la rama lateral. El stent BIOSS LIM C ha mostrado resultados favorables en ensayos aleatorizados comparado con stents tubulares de segunda generación.
¿QUÉ APORTA DE NUEVO?
- En este estudio se muestra el comportamiento angiográfico de la lesión en bifurcación tras el implante del stent dedicado BIOSS LIM C. También se comprueba la factibilidad de su uso sistemático, con una alta tasa de éxito y una escasa afección de la angulación de la bifurcación. La infraexpansión residual en el polígono de confluencia es aceptable para la técnica provisional, pese a una reducida ratio metal/arteria, y excelente para la técnica de doble stent.
BIBLIOGRAFÍA
1. Ojeda S, Romaguera R, Cruz-González I, Moreno R. Spanish Cardiac Catheterization and Coronary Intervention Registry. 29th Official Report of the Interventional Cardiology Association of the Spanish Society of Cardiology (1990-2019). Rev Esp Cardiol. 2020;73:927-936.
2. Burzotta F, Lassen JF, Lefèbre T, et al. Percutaneous coronary intervention for bifurcation coronary lesions: the 15th consensus document from the European Bifurcation Club. EuroIntervention. 2021;16:1307-1317.
3. Huo Y, Kassab GS. Scaling laws of coronary circulation in health and disease. J Biomech. 2016;49:2531-2539.
4. Foin N, Sen S, Allegria E, et al. Maximal expansion capacity with current DES platforms: a critical factor for stent selection in the treatment of left main bifurcations? EuroIntervention. 2013;8:1315-1325.
5. Finet G, Derimay F, Motreff P, et al. Comparative Analysis of Sequential Proximal Optimizing Technique Versus Kissing Balloon Inflation Technique in Provisional Bifurcation Stenting: Fractal Coronary Bifurcation Bench Test. JACC Cardiovasc Interv. 2015;8:1308-1317.
6. Maeng M, Hom NR, Erglis A, et al. Long-term results after simple versus complex stenting of coronary artery bifurcation lesions: Nordic Bifurcation Study 5-year follow-up results. J Am Coll Cardiol. 2013;62:30-34.
7. Hildick-Smith D, Behan MW, Lassen JF, et al. The EBC TWO Study (European Bifurcation Coronary TWO): A Randomized Comparison of Provisional T-Stenting Versus a Systematic 2 Stent Culotte Strategy in Large Caliber True Bifurcations. Circ Cardiovasc Interv. 2016;9:e003643.
8. Ferenc M, Gick M, Kienzle R-P, et al. Randomized trial on routine vs. provisional T-stenting in the treatment of de novo coronary bifurcation lesions. Eur Heart J. 2008;29:2859.
9. Ferenc M, Ayoub M, Büttner HJ, et al. Long-term outcomes of routine versus provisional T-stenting for de novo coronary bifurcation lesions: five-year results of the Bifurcations Bad Krozingen I study. EuroIntervention. 2015;11:856-859.
10. Erglis A, Kumsars I, Niemelä M, et al. Randomized comparison of coronary bifurcation stenting with the crush versus the culotte technique using sirolimus eluting stents: the Nordic stent technique study. Circ Cardiovasc Interv. 2009;2:27-34.
11. Gil RJ, Bil J, Kern A, Pawłowski T. First-in-man study of dedicated bifurcation cobalt-chromium sirolimus-eluting stent BIOSS LIM C® - Three-month results. Kardiol Pol. 2018;76:464-470.
12. Gil RJ, Bil J, Grundeken MJ, et al. Long-term effectiveness and safety of the sirolimus-eluting BiOSS LIM® dedicated bifurcation stent in the treatment of distal left main stenosis: an international registry. EuroIntervention. 2016;12:1246-1254.
13. Gil RJ, Bil J, Vassiliev D, Garcia LAI. First-in-man study of dedicated bifurcation sirolimus-eluting stent: 12-month results of BiOSS LIM® Registry. J Interv Cardiol. 2015;28:51-60.
14. Gil RJ, Bil J, Grundeken MJ, et al. Regular drug-eluting stents versus the dedicated coronary bifurcation sirolimus-eluting BiOSS LIM® stent: the randomised, multicentre, open-label, controlled POLBOS II trial. EuroIntervention. 2016;12:e1404-e1412.
15. Lefèvre T, Ormiston J, Guagliumi G, et al. The Frontier stent registry: safety and feasibility of a novel dedicated stent for the treatment of bifurcation coronary artery lesions. J Am Coll Cardiol. 2005;46:592-598.
16. Costa RA, Abizaid A, Abizaid AS, et al. Procedural and early clinical outcomes of patients with de novo coronary bifurcation lesions treated with the novel Nile PAX dedicated bifurcation polymer-free paclitaxel coated stents: results from the prospective, multicentre, non-randomised BIPAX clinical trial. EuroIntervention. 2012;7:1301-1309.
17. TCT-50: Complex Coronary Bifurcation Lesions Treated with the Novel Polymer-Free Dedicated Bifurcation Paclitaxel-Eluting Stent (Nile Pax): 9-Month Clinical and Angiographic Results of the Prospective, Multicenter BIPAX Clinical Trial. J Am Coll Cardiol. 2011;58:B15.
18. Verheye S, Agostoni P, Dubois CL, et al. 9-Month clinical, angiographic, and intravascular ultrasound results of a prospective evaluation of the Axxess self-expanding biolimus A9-eluting stent in coronary bifurcation lesions: the DIVERGE (Drug-Eluting Stent Intervention for Treating Side Branches Effectively) study. J Am Coll Cardiol. 2009;53:1031-1039.
19. Gil RJ, Bil J, Džavík V, et al. Regular Drug-Eluting Stent vs Dedicated Coronary Bifurcation BiOSS Expert Stent: Multicenter Open-Label Randomized Controlled POLBOS I Trial. Can J Cardiol. 2015;31:671-678.
20. Godino C, Al-Lamee R, C La Rosa C, et al. Coronary left main and non-left main bifurcation angles: how are the angles modified by different bifurcation stenting techniques? J Interv Cardiol. 2010;23:382-393.