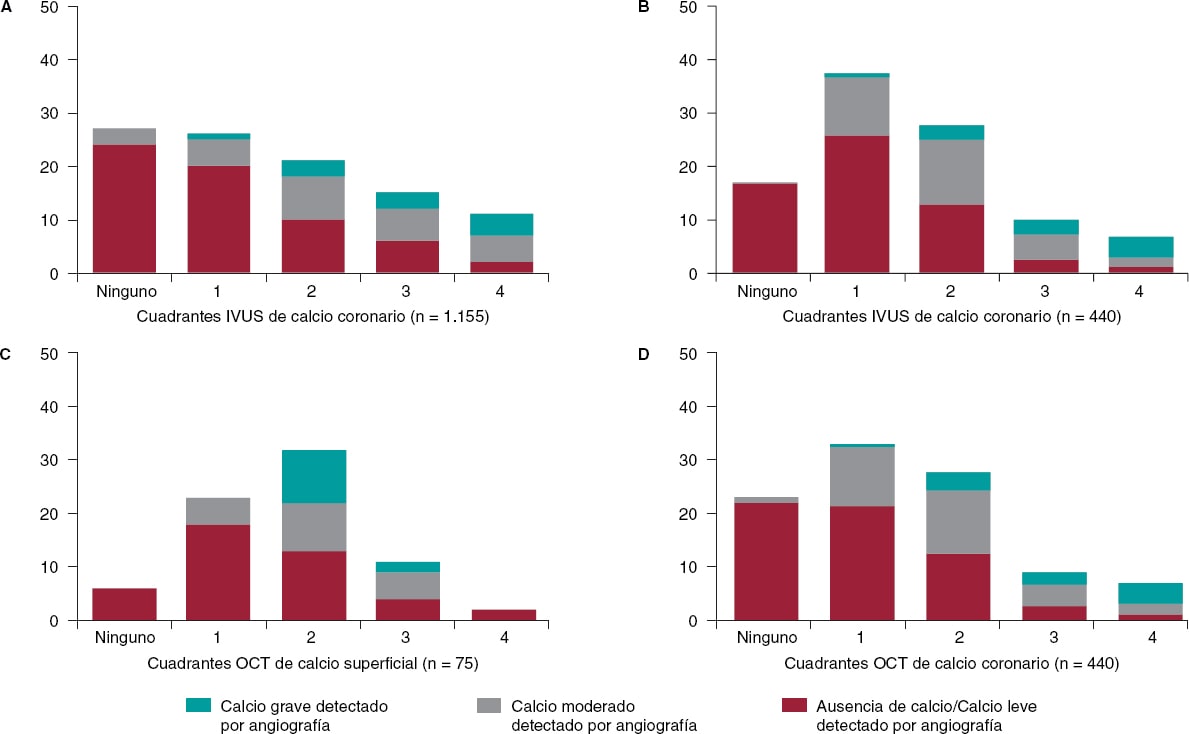
En 1995, mis colegas del Washington Hospital Center (Washington, DC, Estados Unidos) y yo publicamos cuantificaciones del calcio coronario observadas mediante ecocardiografía intravascular (IVUS) o angiografía de 1.155 lesiones destinadas a ser tratadas mediante intervención coronaria percutánea (figura 1)1. La angiografía detectó la presencia de calcio en 440 lesiones (38%) y la IVUS hizo lo propio en 841 lesiones (73%). El 27% de estas 1.155 lesiones no presentaban calcificación en la IVUS, el 26% presentaban calcificación solo en 1 cuadrante de la IVUS, el 21% en 2 cuadrantes, el 15% en 3 cuadrantes y el 11% en 4 cuadrantes de la IVUS. Cuando se observó una calcificación, solo fue superficial en el 48% de las lesiones, profunda en el 28% y superficial y profunda en el 24% de las lesiones. Así pues, pudo confirmarse la presencia de calcio coronario superficial en el 72% de 841 lesiones calcificadas (1 cua- drante con calcio superficial en el 35% de las lesiones, 2 cuadrantes en el 31%, 3 cuadrantes en el 18% y 4 cuadrantes con calcio superficial en el 18% de las lesiones). La capacidad diagnóstica de la angiografía para cuantificar el calcio se basó principalmente en el arco y longitud del mismo, aunque también en si este fue, o no, superficial (figura 1). No obstante, también se observó un curioso índice de falsos positivos angiográficos del 10% que se atribuyó a la dificultad de diferenciar el calcio perivascular o del segmento de referencia del calcio intralesional. En cualquier caso, nunca quedó claro si se trataba de un problema sistemático propio de la detección de calcio mediante angiografía o si se debió a que, a principios de la década de 1990, la angiografía era todavía una técnica primitiva de imágenes sin el nivel de desarrollo que tiene en la actualidad.
Figura 1. Tres estudios (en el sentido de las agujas del reloj empezando en la esquina superior izquierda) realizaron comparativas de la detección de calcio coronario en lesiones diana mediante imágenes intravasculares o angiografía. A: estudio de Mintz et al.1 en 1995. B y C: estudio de por Wang et al.2 en 2017. D: estudio de McGuire et al.3 en 2021. IVUS: ecocardiografía intravascular; OCT: tomografía de coherencia óptica.
Este mismo estudio lo repitieron Wang et al. más de 20 años después en una pequeña cohorte de 440 lesiones utilizando un equipo angiográfico de última generación acompañado de imágenes por IVUS y por tomografía de coherencia óptica (OCT) (figura 1)2. La coronariografía fue capaz de detectar cualquier cantidad de calcio coronario en el 40,2% de las lesiones (177 de 440), la IVUS en el 82,7% de las lesiones (364 de 440) y la OCT en el 76,8% de las lesiones (338 de 440). Cabe destacar que, comparado con el estudio de 1995, casi todo el calcio detectado fue superficial, hubo menos lesiones sin ninguna cantidad calcio y más lesiones con calcio coronario en 1 o 2 cuadrantes (figura 1). En el 13,2% de las lesiones con calcio detectado mediante IVUS, este no fue visible en la OCT principalmente por la presencia de atenuación debida a la acumulación superficial de placa con contenido lipídico. En un artículo publicado recientemente en REC: Interventional Cardiology, McGuire et al.3 realizaron una comparativa de la detección de calcio coronario mediante angiografía u OCT en 75 lesiones. La OCT detectó calcio coronario en 69 lesiones y la angiografía, que no detectó ningún falso positivo, hizo lo propio en 30 lesiones (figura 1)3. Comparada con la IVUS, la OCT es capaz de medir el grosor, área y volumen que influyen en la detección angiográfica del calcio, además de su arco y longitud2,3.
Aparte del índice más bajo de falsos positivos descrito en los 2 estudios contemporáneos, algo que podría atribuirse a la mayor resolución de los equipos actuales de radiología, a las dosis más bajas de radiación que se utilizan en la actualidad comparado con las que se empleaban en 1995 y al reconocimiento clínico de la existencia de calcio perivascular, los resultados fueron muy similares a los de 1995. Así pues, parece haber una limitación fundamental inherente a los rayos x que no es susceptible de mejora con los avances técnicos.
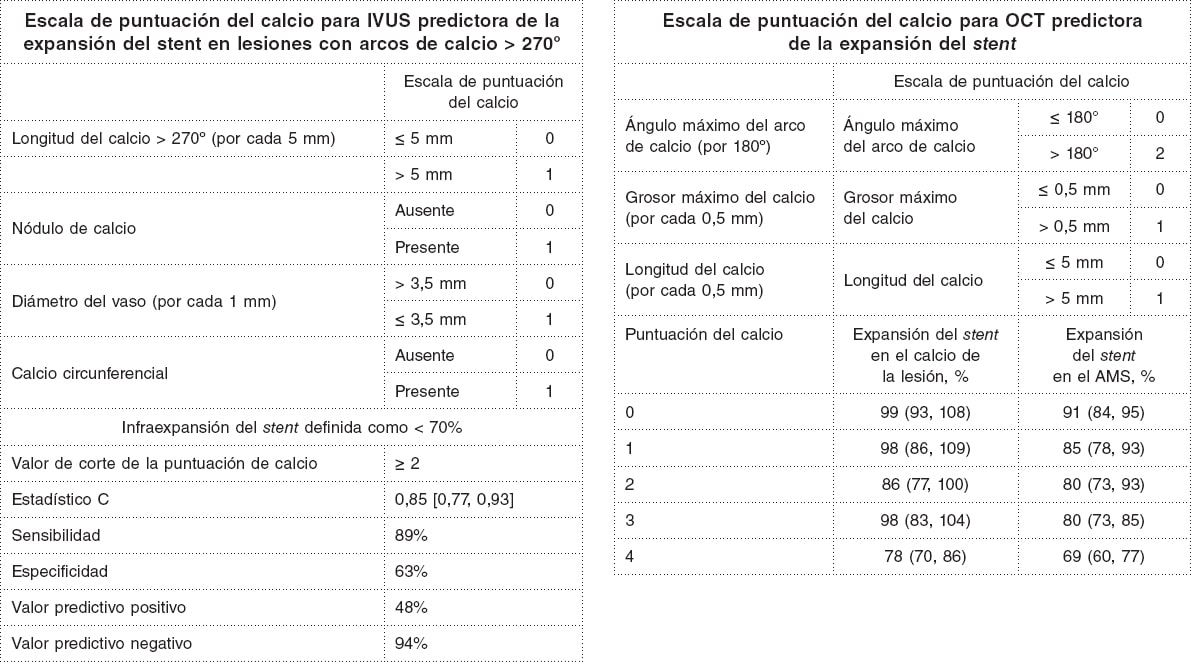
¿Por qué es tan importante detectar el calcio coronario? La principal causa de la restenosis del stent es la infraexpansión del mismo y el principal causante de dicha infraexpansión es el calcio coronario. Por otro lado, la historia natural de la restenosis del stent no es benigna, con una tasa anual de mortalidad que se sitúa entre el 5 y el 7% (y que se asocia al tratamiento y durante el seguimiento)4-7. Existen escalas de puntuación del calcio coronario tanto para la OCT como para la IVUS capaces de predecir con fiabilidad la infraexpansión del stent asociada a la calcificación (figura 2)8,9; también existen tecnologías y abordajes que se pueden usar para modificar el calcio coronario y propiciar una mejor expansión del stent4,10.
Figura 2. Escalas de puntuación del calcio coronario para la tomografía de coherencia óptica y la ecocardiografía intravascular para predecir la infraexpansión del stent 8,9. AMS: área mínima del stent; IVUS: ecocardiografía intravascular; OCT: tomografía de coherencia óptica.
Existen predictores del calcio en lesiones diana tanto a nivel del paciente (mayor edad, diabetes insulinodependiente, angina estable más que síndrome coronario agudo, insuficiencia renal crónica—sobre todo si un paciente está a diálisis—y presencia de calcio en cualquier punto del árbol coronario) como de la propia lesión (vasos más pequeños, estenosis más graves)11-15. No obstante, en su mayoría, las lesiones suelen comportarse independientemente de la acumulación de calcio. Solo las imágenes intravasculares son capaces de detectar y cuantificar, con fiabilidad, la presencia de calcio en lesiones diana y de predecir la infraexpansión del stent en un contexto de calcificación grave en lesiones diana.
FINANCIACIÓN
Ninguna.
CONFLICTO DE INTERESES
G.S. Mintz declara haber recibido honorarios de Boston Scientific, Philips, Medtronic y Abiomed fuera del ámbito de este estudio.
BIBLIOGRAFÍA
1. Mintz GS, Popma JJ, Pichard AD, et al. Patterns of calcification in coronary artery disease. A statistical analysis of intravascular ultrasound and coronary angiography in 1155 lesions. Circulation. 1995;91:1959-1965.
2. Wang Z, Matsumura M, Mintz GS, et al. In vivo calcium detection by comparing optical coherence tomography, intravascular ultrasound, and angiography. JACC Cardiovasc Imaging. 2017;10:869-879.
3. McGuire C, Shlofmitz E, Melaku GD, et al. Comparison of quantitative calcium parameters in optical coherence tomography and invasive coronary angiography. REC Interv Cardiol. 2022;4:6-11.
4. Mintz GS, Ali ZA, Maehara A. Use of intracoronary imaging to guide optimal percutaneous coronary intervention procedures and outcomes. Heart. 2021;107:755-764.
5. Wiebe J, Kuna C, Ibrahim T, et al. Long-term prognostic impact of restenosis of the unprotected left main coronary artery requiring repeat revascularization. JACC Cardiovasc Interv. 2020;13:2266-2274.
6. Tamez H, Secemsky EA, Valsdottir LR, et al. Long-term outcomes of percutaneous coronary intervention for in-stent restenosis among Medicare beneficiaries. EuroIntervention. 2021;17:e380-e387.
7. Shlofmitz E, Torguson R, Zhang C, et al. Impact of intravascular ultrasound on Outcomes following PErcutaneous coronary interventioN for In-stent Restenosis (iOPEN-ISR study). Int J Cardiol. 2021 https://doi.org/10.1016/j.ijcard.2021.08.003.
8. Fujino A, Mintz GS, Matsumura M, et al. A new optical coherence tomography-based calcium scoring system to predict stent underexpansion. EuroIntervention. 2018;13:e2182-e2189.
9. Zhang M, Matsumura M, Usui E, et al. Intravascular ultrasound-derived calcium score to predict stent expansion in severely calcified lesions. Circ Cardiovasc Interv. 2021;14:e010296.
10. De Maria GL, Scarsini R, Banning AP. Management of calcific coronary artery lesions:Is it time to change our interventional therapeutic approach?JACC Cardiovasc Interv. 2019;12:1465-1478.
11. Mintz GS, Pichard AD, Popma JJ, et al. Determinants and correlates of target lesion calcium in coronary artery disease:a clinical, angiographic and intravascular ultrasound study. J Am Coll Cardiol. 1997;29:268-274.
12. Mintz GS, Pichard AD, Kent KM, Satler LF, Popma JJ, Leon MB. Interrelation of coronary angiographic reference lumen size and intravascular ultrasound target lesion calcium. Am J Cardiol. 1998;81:387-391.
13. Tuzcu EM, Berklap B, DeFranco AC, et al. The dilemma of diagnosing coronary calcification:angiography versus intravascular ultrasound. J Am Coll Cardiol. 1996;27:832-838.
14. Gruberg L, Rai P, Mintz GS, et al. Impact of renal function on coronary plaque morphology and morphometry in patients with chronic renal insufficiency as determined by intravascular ultrasound volumetric analysis. Am J Cardiol. 2005;96:892-896.
15. Chin CY, Matsumura M, Maehara A, et al. Coronary plaque characteristics in hemodialysis-dependent patients as assessed by optical coherence tomography. Am J Cardiol. 2017;119:1313-1319.