RESUMEN
Introducción y objetivos: Las guías clínicas recomiendan la realización de una coronariografía en los pacientes con infarto agudo de miocardio sin elevación del segmento ST (IAMSEST). Sin embargo, no está claramente establecido el mejor momento para hacerla. Por ello, el objetivo del presente trabajo fue analizar si practicar un cateterismo precoz (durante las primeras 24 h) se relaciona con un mejor pronóstico, en comparación con hacerlo de manera diferida (más allá de las 24 h).
Métodos: De enero de 2014 a junio de 2016 ingresaron en la unidad de cuidados agudos cardiológicos de un hospital terciario 447 pacientes consecutivos con diagnóstico de IAMSEST a los que se hizo una coronariografía. Se clasificó de forma retrospectiva a los pacientes en 3 grupos en función del momento de realización del cateterismo: durante las primeras 24 h, entre las 24 y 72 h tras el diagnóstico, y después de las primeras 72 h.
Resultados: El cateterismo se llevó a cabo en las primeras 24 h en 285 pacientes (63,8%). No se identificaron diferencias entre los grupos en cuanto a sexo, prevalencia de factores de riesgo cardiovascular ni presencia de comorbilidad. Tampoco se encontraron diferencias en las variables pronósticas analizadas ni en la mortalidad. En el seguimiento a los 12 meses, la incidencia de eventos cardiovasculares y la mortalidad fueron similares entre los grupos.
Conclusiones: En el presente estudio, la realización de una coronariografía precoz (en las primeras 24 h) a los pacientes ingresados por IAMSEST no mostró beneficio clínico en términos de supervivencia o reducción de eventos cardiovasculares.
Palabras clave: Síndrome coronario agudo. GRACE score. Cateterismo precoz. Pronóstico. Mortalidad.
ABSTRACT
Introduction and objectives: According to the recommendations of the latest clinical practice guidelines, non-ST-elevation acute myocardial infarction (NSTEMI) patients should undergo an invasive coronary angiography. However, the best moment to perform this coronary angiography has not been stablished yet. Our main objective was to see if performing an early angiography (within the first 24 h) in NSTEMI patients was associated with better prognosis compared to delayed angiography (beyond the first 24 h).
Methods: From January 2014 to June 2016, 447 consecutive patients were admitted to the acute cardiac care unit of a tertiary hospital with a diagnosis of NSTEMI. They all underwent catheterization. We classified them into 3 groups depending on the moment when the coronary angiography was performed (within the first 24 h after diagnosis, 24 h to 72 h later, and > 72 h after diagnosis).
Results: Coronary angiography was performed within the first 24 h in 285 patients (63.8%). There were no differences among the groups regarding gender, distribution of cardiovascular risk factors, past medical history of coronary disease or presence of other comorbidities. We found no differences among the 3 groups in variables with known prognostic impact. The cardiovascular events and 1-year mortality at follow-up were similar among the 3 groups.
Conclusions: In our study, in the whole spectrum of NSTEMI, early coronary angiography (within the first 24 h) did not show any clinical benefits regarding survival or fewer major adverse cardiovascular events.
Keywords: Acute coronary syndrome. GRACE score. Early angiography. Prognosis. Mortality.
Abreviaturas AC: angiografía coronaria. IAMSEST: infarto agudo de miocardio sin elevación del segmento ST.
INTRODUCCIÓN
La angiografía coronaria (AC) es un paso clave en el tratamiento de pacientes que sufren infarto agudo de miocardio sin elevación del segmento ST (IAMSEST). La AC reduce la mortalidad y la incidencia de nuevos eventos cardiovasculares adversos comparado con el abordaje conservador1,2. De ahí que las actuales guías de práctica clínica europeas sobre el manejo de IAMSEST recomienden una estrategia invasiva para el tratamiento de estos pacientes1.
El mejor momento para realizar una AC en pacientes con IAMSEST sigue siendo objeto de debate. La AC precoz (que se realiza durante las primeras 24 horas después del diagnóstico) sigue recomendándose en pacientes con un alto riesgo de IAMSEST, definido como una puntuación > 140 en la escala GRACE. No obstante, el posible beneficio de este abordaje todavía no se ha establecido de una manera concluyente3.
El objetivo de nuestro estudio fue analizar el impacto pronóstico de la AC precoz (realizada durante las primeras 24 horas después del diagnóstico) en pacientes con IAMSEST comparado con la estrategia AC tardía (transcurridas 24 horas).
MÉTODOS
Este es un estudio retrospectivo, observacional de cohorte. Entre enero de 2014 y junio de 2016 se recopilaron los datos de 447 pacientes con IAMSEST hospitalizados en un centro terciario de referencia y tratados con angiografía coronaria invasiva.
El IAMSEST se definió según las guías y todos los pacientes recibieron tratamiento siguiendo las recomendaciones establecidas por las mismas1.
Los datos de todos los casos se incluyeron prospectivamente en una base de datos continua multipropósito. Los datos recopilados incluyeron historias clínicas, exámenes físicos, mediciones pulsioximétricas, electrocardiogramas de 12 derivaciones, monitorización mediante electrocardiograma continuo, pruebas sanguíneas, ecocardiografías y AC. Se calcularon las puntuaciones de riesgo de cada paciente en la escala GRACE (Global Registry of Acute Coronary Events) y CRUSADE (Can Rapid Risk Stratification of Unstable Angina Patients Suppress Adverse Outcomes With Early Implementation of the American College of Cardiology/American Heart Association Guidelines)1.
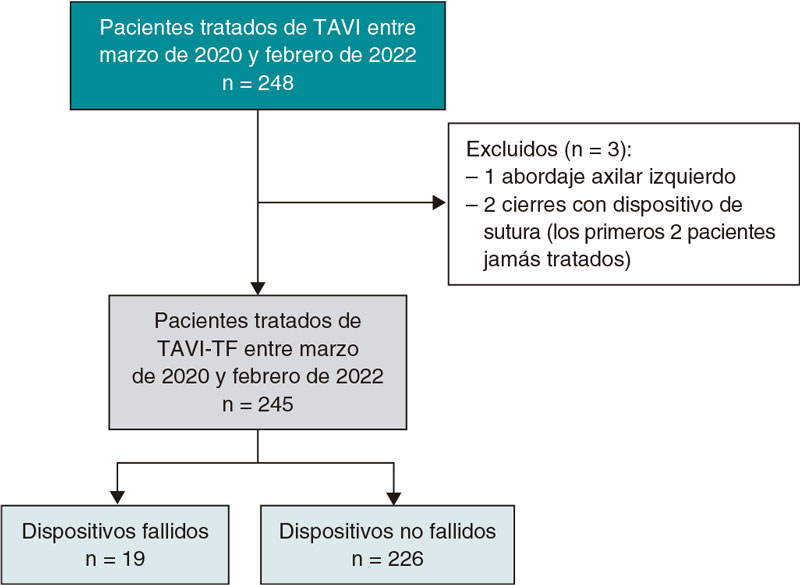
Los pacientes se clasificaron en 3 grupos según el tiempo transcurrido hasta que se realizó la AC (figura 1): cateterismo durante las primeras 24 horas después del diagnóstico (grupo 1, n = 285 pacientes), entre 24 y 72 horas después (grupo 2, n = 102 pacientes) y transcurridas 72 horas (grupo 3, n = 60 pacientes). La decisión de cuándo realizar la AC la tomó el médico al cargo en cada caso. Después de ser dados de alta del hospital, el seguimiento a 12 meses de los pacientes se llevó a cabo en una visita clínica específica.
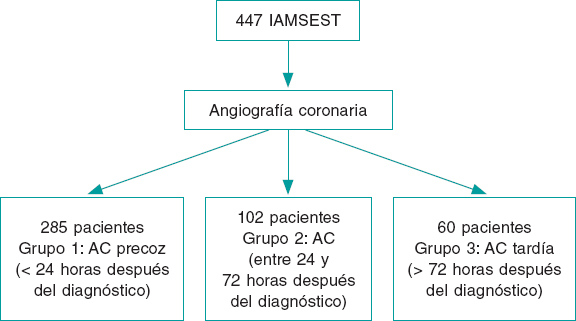
Figura 1. Diagrama de flujo. AC: angiografía coronaria; IAMSEST: infarto agudo de miocardio sin elevación del segmento ST.
Los objetivos primarios de nuestro estudio fueron la mortalidad y los eventos cardiovasculares adversos mayores (accidente cerebrovascular, nuevo síndrome coronario agudo, nueva revascularización) durante la hospitalización y dependiendo de cuándo se realizó la AC en pacientes con IAMSEST. Los objetivos secundarios fueron la mortalidad, la incidencia de eventos cardiovasculares adversos mayores al cabo de 1 año y los eventos hemorrágicos según los criterios propuestos por el Bleeding Academy Research Consortium (BARC)4. También se analizó el tratamiento antiagregante plaquetario prescrito en el momento del alta hospitalaria y su correlación con los MACE durante el seguimiento.
Análisis estadístico
Las variables continuas se expresaron como media y desviación estándar o mediana y rango intercuartílico [IQR], lo más apropiado en cada caso. La prueba de Kolmogorov-Smirnov se empleó para estudiar la distribución normal de las variables. En lo que se refiere a las variables cuantitativas, se realizó una comparativa de los grupos usando la prueba t de Student bilateral o la U de Mann-Whitney, lo más apropiado en cada caso. Las variables categóricas se expresaron como frecuencia y porcentaje y se compararon mediante la prueba de χ2 o la prueba exacta de Fisher, lo más apropiado en cada caso. Ninguna variable tuvo pérdidas > 15%.
Se realizó un análisis de regresión logística multivariado para valorar el posible impacto del momento elegido para realizar la AC sobre la mortalidad hospitalaria. El modelo incluyó todas las variables significativas a nivel estadístico en el análisis univariado de mortalidad además del tiempo transcurrido hasta la realización de la AC. Se calcularon las odds ratios (OR) ajustadas con intervalos de confianza del 95% (IC95%) para cada variable. En lo que al objetivo secundario de mortalidad al cabo de 1 año se refiere, se optó por realizar un análisis de regresión de Cox para valorar cualquier posible factor pronóstico.
Todas las pruebas fueron bilaterales y las diferencias se consideraron estadísticamente significativas con valores p < 0,05. El análisis estadístico se llevó a cabo utilizando el programa IBM SPSS Statistics V 22.0.
RESULTADOS
La tabla 1 muestra las características basales de la población de pacientes. Los pacientes del grupo 1 eran más jóvenes (66,5 ± 13,5 años frente a 71,1 ± 12,7 años en el grupo 2 y 70,7 ± 13,5 en el grupo 3, p = 0,016). No se observó ninguna diferencia de género entre los grupos (p = 0,565). Los factores de riesgo cardiovascular, la enfermedad coronaria previa (p = 0,314) y la presencia de otras comorbilidades fueron similares entre los distintos grupos (tabla 1).
Tabla 1. Características basales entre los 3 grupos del estudio y tratamiento antiagregante plaquetario en el momento del alta hospitalaria
| Grupo 1 (n = 285) | Grupo 2 (n = 102) | Grupo 3 (n = 60) | p | |
|---|---|---|---|---|
| Edad (años) | 66,5 (13,5) | 70,7 (13,5) | 71,1 (12,7) | 0,016 |
| Sexo (varón) | 78,9% | 80,2% | 73,3% | 0,565 |
| Diabetes | 34,9% | 37,6% | 35,0% | 0,880 |
| Hipercolesterolemia | 63,4% | 54,5% | 55,9% | 0,195 |
| Hipertensión | 71,1% | 71,3% | 73,3% | 0,942 |
| Puntuación GRACE | 157 (44,9) | 161 (45,7) | 170 (39,6) | 0,041 |
| Puntuación CRUSADE | 32,8 | 34,8 | 36,4 | 0,251 |
| TFG | 72 | 69,8 | 66 | 0,118 |
| Niveles máximos de CK | 659,9 | 479,4 | 590 | 0,623 |
| FEVI en el momento del alta | 49,6 | 54,2 | 52 | 0,229 |
| Clase Killip | 0,604 | |||
| I | 194 (71,3%) | 75 (72,7%) | 37 (62,7%) | |
| II | 32 (11,8%) | 15 (15,2%) | 9 (15,3%) | |
| III | 23 (8,5%) | 7 (7,1%) | 8 (13,6%) | |
| IV | 23 (8,5%) | 5 (5,1%) | 5 (8,5%) | |
| Ventilación mecánica | 29 (10,7%) | 6 (6,1%) | 5 (8,3%) | 0,636 |
| Número de vasos con estenosis grave | 0,488 | |||
| 1 | 133 (46,8%) | 45 (44,6%) | 23 (38,6%) | |
| 2 | 77 (27,1%) | 23 (22,8%) | 22 (36,7%) | |
| 3 | 68 (23,9%) | 29 (28,7%) | 14 (23,3%) | |
| Revascularización exitosa | 211 (89,8%) | 70 (92,1%) | 42 (91,3%) | 0,930 |
| Tratamiento antiagregante plaquetario en el momento del alta | ||||
| Ticagrelor | 154 (54%) | 52 (50,9%) | 29 (48,3%) | 0,154 |
| Clopidogrel | 105 (36,8%) | 40 (39,2%) | 24 (40%) | 0,358 |
| Prasugrel | 26 (9,2%) | 10 (9,9%) | 7 (11,7%) | 0,469 |
CK: creatincinasa; FEVI: fracción de eyección del ventrículo izquierdo; TFG: tasa de filtración glomerular. Grupo 1: angiografía coronaria durante las primeras 24 horas después del diagnóstico; grupo 2: entre 24 y 72 horas después; grupo 3: angiografía coronaria > 72 horas después del diagnóstico. | ||||
Se realizó una AC durante las primeras 24 horas en 285 pacientes (63,8%). Sorprendentemente, advertimos que las puntuaciones GRACE de los pacientes del grupo 1 [157,67 ± 44,9 puntos frente a 170 ± 39,5 puntos en el grupo 3, (p = 0,041)] fueron más bajas y las puntuaciones CRUSADE parecidas a las de los otros 2 grupos (p = 0,251).
No se observaron diferencias significativas entre los distintos grupos en la clase Killip durante el ingreso hospitalario (tabla 1). La fracción de eyección del ventrículo izquierdo y los valores máximos de los biomarcadores cardiacos fueron similares entre los distintos grupos. La presencia de enfermedad multivaso fue, también, parecida entre los 3 grupos (tabla 1). Tampoco se observaron diferencias significativas en el objetivo primario entre los 3 grupos del estudio (tabla 2). Durante la hospitalización, los accidentes cerebrovasculares y los eventos hemorrágicos sobrevinieron de forma similar entre los 3 grupos (tabla 2). Es importante resaltar la baja incidencia de eventos hemorrágicos (5 pacientes con eventos hemorrágicos BARC tipo 2 y 2 pacientes con eventos BARC tipo 3 en el grupo 1, mientras que en los grupos 2 y 3 hubo 3 pacientes con eventos BARC tipo 2 y 2 pacientes con eventos BARC 3, sin eventos mortales). Durante el seguimiento a 1 año, los eventos cardiovasculares adversos y la mortalidad año fueron similares entre los 3 grupos (tabla 2).
Tabla 2. Incidencia hospitalaria y durante el seguimiento de eventos adversos y mortalidad (expresado como porcentaje) entre los 3 grupos
| Grupo 1 (n = 285) | Grupo 2 (n = 102) | Grupo 3 (n = 60) | p | |
|---|---|---|---|---|
| Eventos hospitalarios | ||||
| Insuficiencia cardiaca | 74 (25,9%) | 26 (25,4%) | 21 (36%) | 0,246 |
| IAM no fatal | 3 (1%) | 4 (3,9%) | 3 (6%) | 0,371 |
| Daño renal agudo | 47 (16,5%) | 18 (17,6%) | 15 (25%) | 0,334 |
| Accidente cerebrovascular | 3 (1%) | 2 (1,9%) | 2 (3,3%) | 0,548 |
| Eventos hemorrágicos | 20 (7%) | 6 (5,8%) | 6 (10%) | 0,213 |
| Mortalidad hospitalaria | 19 (6,6%) | 7 (6,8%) | 2 (3,4%) | 0,358 |
| Eventos al año de seguimiento | ||||
| Muerte | 17 (5,9%) | 5 (4,9%) | 5 (8,3%) | 0,114 |
| Accidente cerebrovascular | 3 (1,05%) | 3 (2,9%) | 1 (1,6%) | 0,271 |
| Hemorragia mayor | 7 (2,45%) | 6 (5,8%) | 4 (6,6%) | 0,427 |
| Infarto de miocardio | 16 (5,6%) | 5 (4,9%) | 4 (6,6%) | 0,907 |
IAM: infarto agudo de miocardio. Grupo 1: angiografía coronaria durante las primeras 24 horas después del diagnóstico; grupo 2: entre 24 y 72 horas después; grupo 3: angiografía coronaria > 72 horas después del diagnóstico. | ||||
En lo que al tratamiento médico se refiere en el momento del alta hospitalaria, un porcentaje similar de pacientes recibieron clopidogrel, prasugrel y ticagrelor en los 3 grupos del estudio (tabla 1). En nuestra cohorte, el tratamiento antiagregante plaquetario no se asoció a diferencias en la incidencia de eventos cardiovasculares adversos mayores y mortalidad en el seguimiento a 12 meses.
El análisis de regresión logística multivariado realizado para predecir la mortalidad reveló que la hipertensión, la clase Killip IV durante el ingreso hospitalario, la fracción de eyección del ventrículo izquierdo y el daño miocárdico (definido como niveles máximos de creatincinasa) se asociaron independientemente a una incidencia más alta de la mortalidad hospitalaria. El tiempo transcurrido hasta la realización de la AC no fue un predictor independiente de la mortalidad hospitalaria después de realizar el correspondiente ajuste multivariado (tabla 3).
Tabla 3. Análisis de regresión logística multivariado para predecir la mortalidad hospitalaria
| Variable | Odds ratio (IC95%) | p |
|---|---|---|
| AC después de 72 horas | referencia | |
| AC durante las primeras 24 horas | 0,98 (0,26-3,74) | 0,978 |
| AC entre 24 y 72 horas después | 1,33 (0,28-6,24) | 0,716 |
| Hipertensión | 6,25 (1,09-33,3) | 0,04 |
| Edad (por año) | 1,03 (0,98-1,08) | 0,292 |
| Revascularización exitosa | 0,51 (0,12-2,21) | 0,371 |
| Niveles máximos de CK (por pg/ml) | 1,00 (1,00-1,01) | 0,010 |
| FEVI | 0,93 (0,90-0,97) | < 0,001 |
| Clase Killip en el ingreso hospitalario | ||
| I | referencia | 0,026 |
| II | 3,39 (0,98-11,75) | 0,054 |
| III | 3,24 (0,92-11,36) | 0,067 |
| IV | 15,34 (2,19-107,58) | 0,006 |
AC: angiografía coronaria; CK: creatincinasa; FEVI: fracción de eyección del ventrículo izquierdo; IC95%: intervalo de confianza del 95%. | ||
En lo referente a la mortalidad al cabo de 1 año, el análisis de regresión de Cox arrojó resultados similares. El tiempo transcurrido hasta la realización de la AC no fue significativo en el análisis multivariado. La hipertensión, la edad, la fracción de eyección del ventrículo izquierdo y la clase Killip durante el ingreso hospitalario se asociaron independientemente a una incidencia más alta de mortalidad al cabo de 1 año (tabla 4).
Tabla 4. Análisis de regresión de Cox multivariado para predecir la mortalidad a 1 año
| Variable | Hazard ratio (IC95%) | p |
|---|---|---|
| AC después de 72 horas | referencia | |
| AC durante las primeras 24 horas | 0,96 (0,46-2,03) | 0,919 |
| AC entre 24 y 72 horas después | 0,82 (0,33-2,07) | 0,677 |
| Hipertensión | 3,64 (1,30-10,3) | 0,014 |
| Edad (por año) | 1,04 (1,01-1,07) | 0,022 |
| Revascularización exitosa | 0,94 (0,41-2,13) | 0,876 |
| Niveles máximos de CK (por pg/ml) | 1,00 (1,00-1,01) | 0,198 |
| FEVI | 0,96 (0,94-0,98) | < 0,001 |
| Clase Killip en el ingreso hospitalario | ||
| I | referencia | |
| II | 2,83 (1,32-6,08) | 0,008 |
| III | 2,78 (1,27-6,09) | 0,010 |
| IV | 2,91 (0,83-10,2) | 0,096 |
AC: angiografía coronaria; CK: creatincinasa; FEVI: fracción de eyección del ventrículo izquierdo; IC95%: intervalo de confianza del 95%. | ||
DISCUSIÓN
Nuestro estudio incluyó una extensa cohorte de 447 pacientes consecutivos con IAMSEST analizados retrospectivamente. Nuestros resultados revelaron que la AC precoz (definida como aquella AC que se realiza durante las primeras 24 horas después del diagnóstico) en pacientes con IAMSEST no mejoró el pronóstico de esta cohorte de pacientes comparado con la AC tardía. Tampoco se observaron diferencias entre los 3 grupos en lo referente al tiempo transcurrido hasta la realización de la AC en la incidencia de eventos cardiovasculares adversos mayores, mortalidad ni el seguimiento a 12 meses.
Las guías de práctica clínica recomiendan realizar una AC precoz durante las primeras 24 horas después del diagnóstico en el manejo de pacientes con IAMSEST. No obstante, esta recomendación se basa en los resultados de ensayos clínicos relativamente viejos y en un metanálisis4-8. Varios estudios recientes han explorado el impacto pronóstico que tiene el momento en que se realiza la AC sobre pacientes IAMSEST para hallar evidencias más sólidas en este escenario clínico9,10.
Los resultados del TIMACS (Timing of Intervention in Acute Coronary Syndromes) revelaron que la AC precoz se asoció a un descenso del objetivo compuesto de muerte, infarto de miocardio o isquemia refractaria comparado con la estrategia de AC tardía11.
Entre el 1 de enero de 2005 y el 31 de diciembre de 2011 se realizó un estudio de cohorte retrospectivo que incluyó a 19.704 pacientes emparejados por puntuación de propensión y hospitalizados con un primer síndrome coronario agudo. Este estudio reveló que el uso de una estrategia de tratamiento invasivo inicial se asoció a un menor riesgo de mortalidad cardiovascular y rehospitalización por infarto de miocardio comparado con el abordaje invasivo conservador12. No obstante, es importante resaltar la naturaleza retrospectiva de este estudio y el hecho de que el seguimiento de los pacientes solo duró 60 días.
Sin embargo, un metanálisis que recopiló datos de 83.229 pacientes no reveló ninguna diferencia significativa a nivel estadístico en la mortalidad, infarto de miocardio ni hemorragias mayores entre las 2 estrategias13.
Otro metanálisis incluyó 8 ensayos clínicos controlados y aleatorizados (n = 5.324 pacientes) con un seguimiento medio de 180 días [180-360] y comparó a un grupo de pacientes IAMSEST que recibieron una estrategia invasiva precoz con una estrategia tardía. El metanálisis confirmó que la estrategia invasiva precoz no redujo la mortalidad, incluidos pacientes de alto riesgo con > 140 puntos en la escala GRACE14.
Un reciente metanálisis que combinó los resultados de 10 ensayos clínico tampoco halló diferencia alguna en la mortalidad, infarto de miocardio ni hemorragias mayores entre pacientes con IAMSEST asociada al momento de realización de la AC. En cualquier caso, la estrategia de AC precoz sí se asoció a menos anginas recurrentes y a estancias hospitalarias más cortas15.
El estudio LIPSIA-NSTEMI aleatorizó a pacientes con IAMSEST a los que realizaron una AC durante las primeras 2 horas después de la aleatorización (estrategia de AC inmediata), entre 10 y 48 horas después de la aleatorización (AC precoz) y al llamado grupo invasivo selectivo, en el que los pacientes recibieron, inicialmente, tratamiento médico. No se observó diferencia alguna en el tamaño del infarto entre los 3 grupos del estudio16.
El reciente ensayo clínico controlado y aleatorizado VERDICT, realizado por Kofoed et al., incluyó a 2.147 pacientes de los cuales 1.075 recibieron una evaluación invasiva muy precoz (durante las primeras 12 horas después del diagnóstico) y 1.072 a recibir tratamiento invasivo estándar (AC realizada 61,6 horas después de la aleatorización)17. El objetivo primario fue un compuesto de mortalidad por cualquier causa, infarto de miocardio recurrente no fatal, ingreso hospitalario por isquemia miocárdica refractaria o por insuficiencia cardiaca. En este estudio, la estrategia de evaluación coronaria invasiva muy precoz no mejoró, en líneas generales, los resultados clínicos a largo plazo comparado con la estrategia invasiva realizada a los 2-3 días en pacientes con síndrome coronario agudo sin elevación del segmento ST. No obstante, en los pacientes de mayor riesgo, el tratamiento invasivo muy precoz sí mejoró los resultados a largo plazo17, lo cual coincide con los resultados descritos por el estudio TIMACS.
A pesar de todos estos datos, saber cuál es el mejor momento para realizar una AC en pacientes con IAMSEST sigue siendo objeto de debate.
Una importante limitación de anteriores estudios es la heterogeneidad existente en la definición de AC precoz y tardía, así como las diferencias observadas en los objetivos primarios4-14. La falta de criterios uniformes hace que sea difícil comparar los resultados. La definición de IAMSEST ha ido cambiando con el paso del tiempo. Así, los antiguos estudios clínicos empleaban un criterio distinto para la definición de IAMSEST e incluían a pacientes distintos de los que se incluyen en los estudios actuales. Habría que intentar identificar qué pacientes de mayor riesgo son los que se beneficiarían de una estrategia invasiva precoz. En este sentido, estudios publicados con anterioridad no empleaban sistemas de estratificación del riesgo para clasificar a los pacientes. Sin embargo, en nuestro estudio sí calculamos los riesgos isquémicos y hemorrágicos de todos los pacientes. Como nuestro objetivo fue valorar el posible beneficio de una estrategia invasiva precoz en pacientes con IAMSEST, se calculó la puntuación de riesgo GRACE de toda la población del estudio. No obstante, a pesar del alto riesgo isquémico de nuestros pacientes, no se observó ninguna diferencia significativa a nivel estadístico entre las 2 estrategias (AC precoz o tardía) en lo que se refiere a la mortalidad o a los eventos adversos.
Limitaciones
Nuestro estudio tiene varias limitaciones que conviene tener en cuenta a la hora de interpretar los resultados. Aunque incluimos a un amplio número de pacientes IAMSEST con una serie de datos de una calidad alta, este es un estudio observacional, retrospectivo y de un único centro con las limitaciones propias de un estudio de estas características. Además, las actuales guías de práctica clínica recomiendan emplear la escala PRECISE-DAPT para valorar el riesgo hemorrágico en este escenario clínico. En nuestro estudio, el riesgo hemorrágico durante el ingreso hospitalario se clasificó empleando la escala de riesgo CRUSADE.
CONCLUSIONES
Los resultados de nuestro estudio revelan que la estrategia de AC precoz no mejoró el pronóstico ni redujo la mortalidad en pacientes IAMSEST. No obstante, se deben realizar estudios más extensos que aclaren qué grupo de pacientes son los que se benefician de estrategias de AC precoces.
CONFLICTO DE INTERESES
Ninguno.
¿QUÉ SE SABE DEL TEMA?
- La AC precoz está recomendada por la actual guía de práctica clínica en pacientes de alto riesgo con infarto agudos de miocardio sin elevación del segmento ST.
- En la actualidad, tanto los ensayos clínicos como los metanálisis arrojan resultados contradictorios sin diferencias pronósticas claras entre la estrategia AC precoz y el cateterismo tardío.
¿QUÉ APORTA DE NUEVO?
- Se estudió a una extensa cohorte de pacientes IAMSEST consecutivos. Valoramos los eventos cardiovasculares y la mortalidad hospitalarios y en el seguimiento al año.
- Los resultados de nuestro estudio revelan que la estrategia AC precoz no mejoró el pronóstico ni redujo la mortalidad de pacientes IAMSEST.
- No se observaron diferencias entre los 3 grupos asociadas al momento en que se realizó la AC en lo que respecta a los eventos cardiovasculares adversos durante la estancia hospitalaria ni en el seguimiento a 12 meses.
- No obstante, se necesitan estudios más extensos que aclaren qué grupo de pacientes son los que se benefician de una estrategia AC precoz.
BIBLIOGRAFÍA
1. Roffi M, Patrono C, Collet JP, et al. 2015 ESC guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation:Task Force for the Management of Acute Coronary Syndromes in Patients Presenting Without Persistent ST-Segment Elevation of the European Society of Cardiology (ESC). Eur Heart J. 2016;37:267-315.
2. Amsterdam EA, Wenger NK, Brindis RG, et al. 2014 AHA/ACC guideline for the management of patients with non-ST-elevation acute coronary syndromes:executive summary:a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. Circulation. 2014;130:2354-2394.
3. Reuter PG, Rouchy C, Cattan S, et al. Early invasive strategy in high-risk acute coronary syndrome without ST-segment elevation. The Sisca randomized trial. Int J Cardiol. 2015;182:414-418.
4. Vranckx P, White HD, Huang Z, et al. Validation of BARC Bleeding Criteria in Patients With Acute Coronary Syndromes:The TRACER Trial. J Am Coll Cardiol. 2016;67:2135-2144.
5. Montalescot G, Cayla G, Collet JP, et al. ABOARD Investigators. Immediate vs delayed intervention for acute coronary syndromes:a randomized clinical trial. JAMA. 2009;302:947-954.
6. De Winter RJ, Windhausen F, Cornel JH, et al. Early invasive versus selectively invasive management for acute coronary syndromes. N Engl J Med. 2005;353:1095-1104.
7. Hirsch A, Windhausen F, Tijssen JG, et al. Long-term outcome after an early invasive versus selective invasive treatment strategy in patients with non-ST-elevation acute coronary syndrome and elevated cardiac troponin T (the ICTUS trial):a follow-up study. Lancet. 2007;369:827-835.
8. O'Donoghue M, Boden WE, Braunwald E, et al. Early invasive vs conservative treatment strategies in women and men with unstable angina and non- ST-segment elevation myocardial infarction:a meta-analysis. JAMA. 2008;300:71-80.
9. Badings EA, The SH, Dambrink JH, el al. Early or late intervention in high-risk non-ST-elevation acute coronary syndromes:results of the ELISA-3 trial. EuroIntervention. 2013;9:54-61.
10. Milosevic A, Vasiljevic-Pokrajcic Z, Milasinovic D, et al. Immediate Versus Delayed Invasive Intervention for Non-STEMI Patients:The RIDDLE-NSTEMI Study. JACC Cardiovasc Interv. 2016;9:541-549.
11. Mehta SR, Granger CB, Boden WE, et al. Early versus delayed invasive intervention in acute coronary syndromes. N Engl J Med. 2009;360:2165-2175.
12. Hansen KW, Sorensen R, Madsen M, et al. Effectiveness of an early versus a conservative invasive treatment strategy in acute coronary syndromes:a nationwide cohort study. Ann Intern Med. 2015;163:737-746.
13. Navarese EP, Gurbel PA, Andreotti F, et al. Optimal timing of coronary invasive strategy in non-ST-segment elevation acute coronary syndromes:a systematic review and meta-analysis. Ann Intern Med. 2013;158:261-270.
14. Jobs A, Mehta SR, Montalescot G, et al. Optimal timing of an invasive strategy in patients with non-ST-elevation acute coronary syndrome:a meta-analysis of randomized trials. Lancet. 2017;390:737-746.
15. Bonello l, Laine M, Puymirat E, et al. Timing of Coronary Invasive Strategy in Non-ST-Segment Elevation Acute Coronary Syndromes and Clinical Outcomes:An Updated Meta-Analysis. JACC Cardiovasc Interv. 2016;9:2267-2276.
16. Thiele H, Rach J, Klein N, et al. Optimal timing of invasive angiography in stable non-ST-elevation myocardial infarction:the Leipzig Immediate versus early and late PercutaneouS coronary Intervention triAl in NSTEMI (LIPSIA-NSTEMI Trial). Eur Heart J. 2012;33:2035-2043.
17. Kofoed KF, Kelbæk H, Hansen PR, et al. Early Versus Standard Care Invasive Examination and Treatment of Patients With Non-ST-Segment Elevation Acute Coronary Syndrome. Circulation. 2018;138:2741-2750.
Autor para correspondencia: Hospital Clínico Universitario San Carlos, Prof. Martín Lagos s/n, 28040 Madrid, España.
Correo electrónico: carlosferreraduran@gmail.com (C. Ferrera).