Sr. Editor:
La transposición de grandes arterias congénitamente corregida es un defecto congénito infrecuente caracterizado por una discordancia auriculoventricular y ventriculoarterial. Como resultado, la válvula tricúspide y el ventrículo derecho anatómico mantienen la circulación sistémica. Típicamente el paciente se mantie- ne asintomático a temprana edad, pero el ventrículo derecho y la válvula tricúspide tienden a deteriorarse con el tiempo. El único tratamiento curativo para esta afección es el trasplante cardiaco. En este escenario, la reparación valvular percutánea borde a borde se ha utilizado para tratar la insuficiencia tricuspídea en pacientes no candidatos a trasplante; sin embargo, la evidencia existente es escasa y basada en comunicaciones de casos en escenarios clínicos heterogéneos1-3.
Se presenta el caso de un joven con transposición de grandes arterias congénitamente corregida, insuficiencia cardiaca avanzada e insuficiencia tricuspídea torrencial que fue rechazado para trasplante cardiaco por hipertensión pulmonar grave no reversible, y se consideró la reparación valvular percutánea borde a borde. El paciente firmó un consentimiento informado que autoriza la publicación del caso y fue aprobado por el comité de ética de nuestro centro.
Se trata de un varón diagnosticado a los 7 meses de edad de transposición de grandes arterias congénitamente corregida y bloqueo auriculoventricular congénito que permaneció asintomático hasta los 29 años, cuando hubo que implantarle un marcapasos por incompetencia cronotrópica. Posteriormente perdió el seguimiento hasta que ingresó a los 35 años en la unidad de cuidados críticos por edema pulmonar. En ese momento se encontraron disfunción sistólica biventricular, insuficiencia valvular auriculoventricular sistémica grave e hipertensión pulmonar. Debido a una parada cardiaca, se indicó un desfibrilador automático implantable con terapia de resincronización, además de optimización del tratamiento médico.
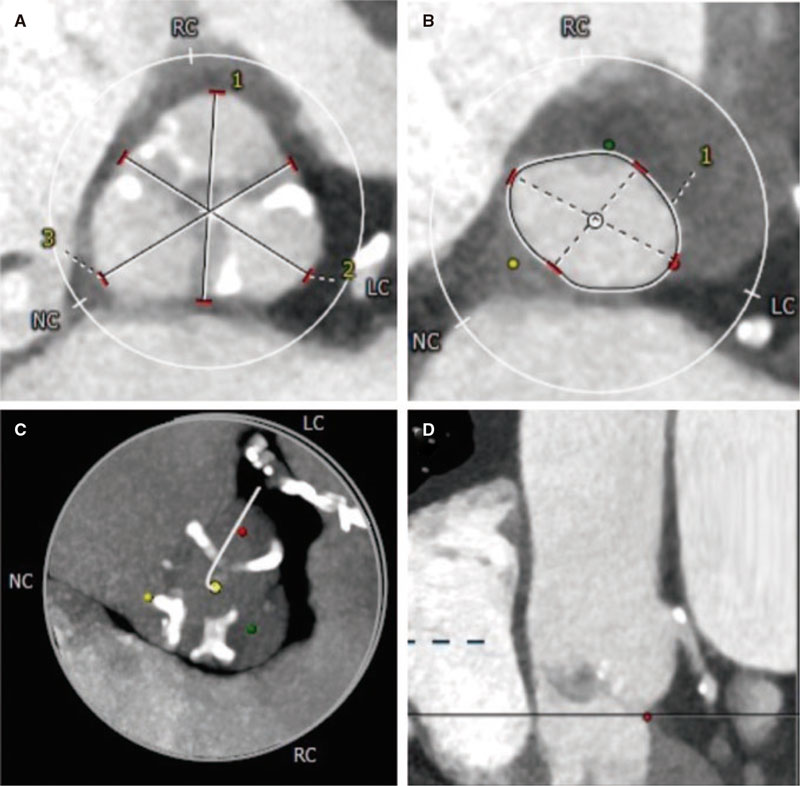
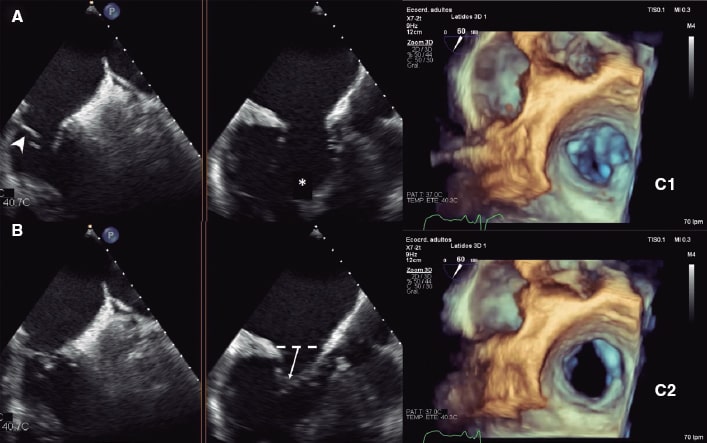
A pesar del tratamiento, el paciente permaneció sintomático en clase III de la New York Heart Association e INTERMACS 4. La evaluación ecocardiográfica mostró disfunción sistólica ventricular sistémica grave (fracción de eyección del ventrículo derecho del 35%) con insuficiencia grave de la válvula auriculoventricular sistémica. La válvula presentaba una anomalía Ebstein-like (8,3 mm/m2), así como cuerdas con implantación anómala, engrosamiento y restricción de los velos, lo que provocaba un amplio defecto de coaptación, principalmente entre las valvas septal y posterior, que generaba insuficiencia torrencial (V/V) (figura 1). El cateterismo cardiaco mostró hipertensión pulmonar grave (presión media en la arteria pulmonar de 55 mmHg) con componentes precapilar y poscapilar (gradiente transpulmonar de 30 mmHg y resistencia vascular pulmonar de 6,4 UW). La prueba vasodilatadora con óxido nítrico resultó en una respuesta máxima, pero sin cambios significativos. Teniendo en cuenta toda la información, el equipo multidisciplinario decidió que el paciente no era elegible para trasplante ni cirugía cardiaca, y se le ofreció la reparación valvular percutánea borde a borde de la válvula tricúspide con un dispositivo MitraClip (Abbott Vascular, EE.UU.) como tratamiento paliativo.
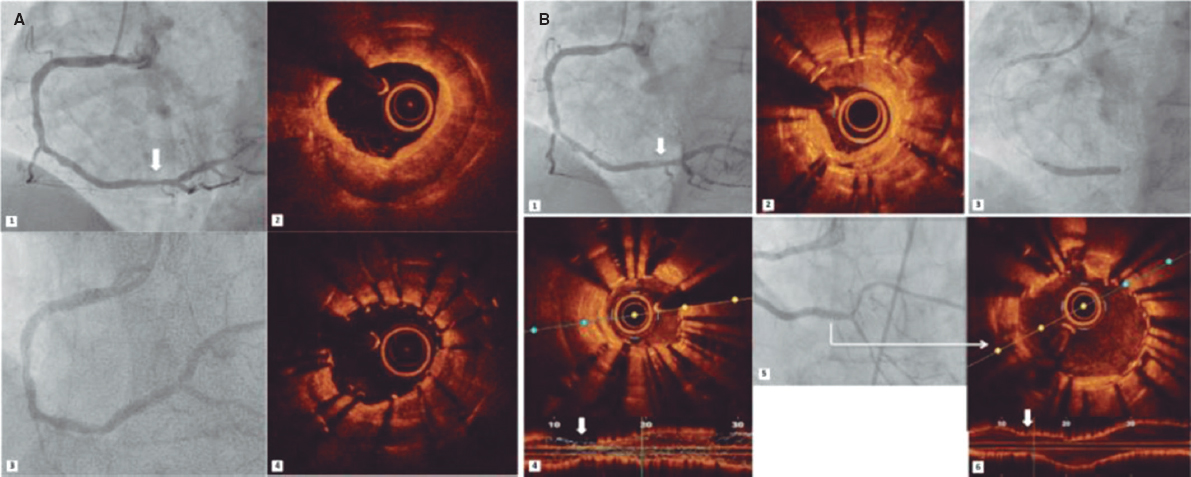
Figura 1. Evaluación detallada de la anatomía de la válvula tricúspide con ecocardiograma transesofágico bidimensional y tridimensional. Vistas del plano X en 55° (izquierda) y 145° (centro), en telediástole (A) y telesístole (B). Valvas marcadamente displásicas (punta de flecha) con inserción desplazada apicalmente (Ebstein-like) e implantación anómala de las cuerdas tendinosas (asterisco), lo que provoca tensión y abombamiento (flecha). C: evaluación de la válvula mitral con zoom tridimensional que evidencia una amplia brecha de coaptación, predominantemente entre las valvas septales y posteriores en telesístole (C1) y en telediástole (C2).
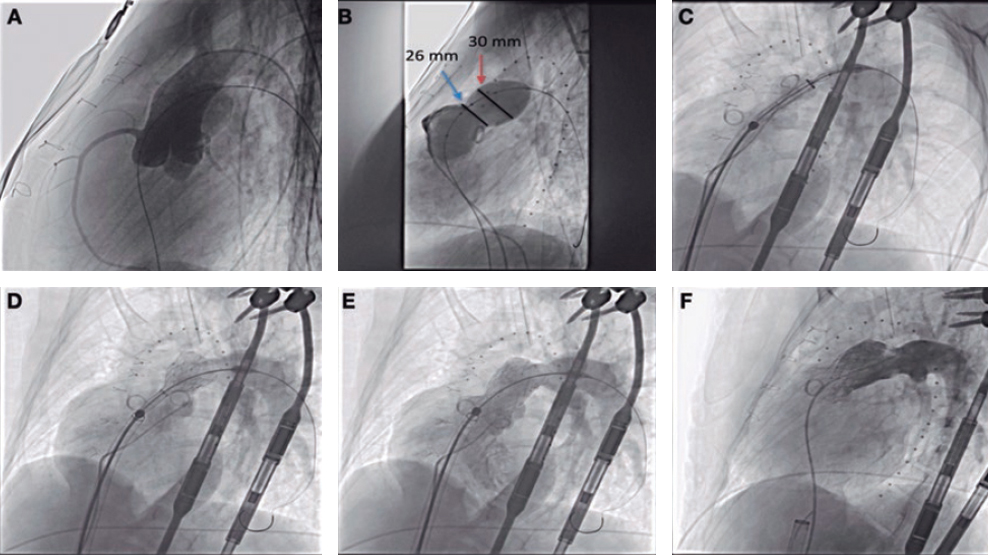
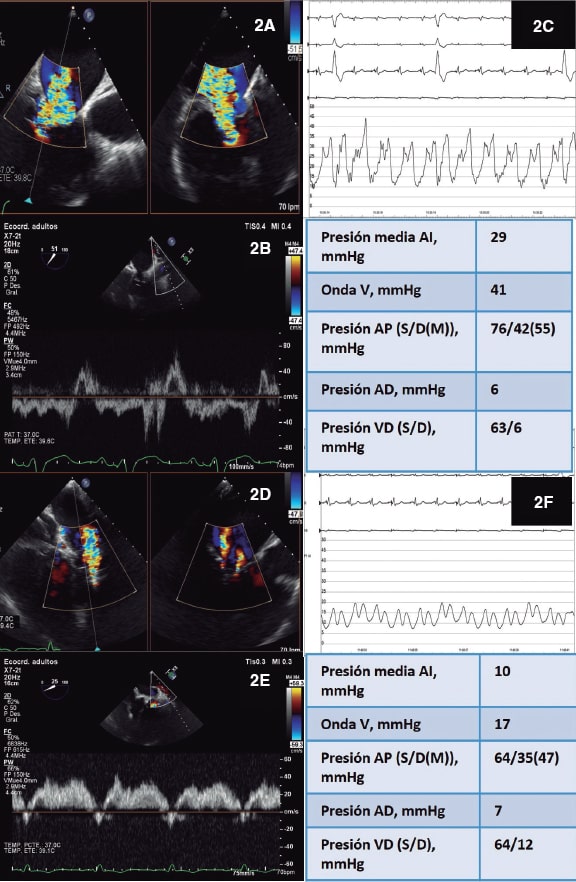
En la intervención se confirmó la regurgitación tricuspídea torrencial (figura 2A,B) con hallazgos hemodinámicos invasivos concordantes (figura 2C). El implante inicial de un MitraClip XTR se realizó en la zona de origen del chorro de insuficiencia, en el centro de la línea de coaptación septal-posterior, y se logró una reducción significativa de la regurgitación. Sin embargo, dada la persistencia de la insuficiencia moderada a grave (II-III/V) sin estenosis significativa, se colocó un segundo dispositivo entre las valvas anterior y septal por ser la zona de mayor regurgitación residual. La evaluación del resultado mostró insuficiencia tricuspídea residual de leve a moderada (II/V) (figura 2D,E), sin estenosis. El buen resultado también se confirmó en la evaluación invasiva (figura 2F), por lo que el procedimiento se dio por finalizado.
Figura 2. Regurgitación tricuspídea antes y después del procedimiento. A,D: color biplano ETE. B,E: doppler pulsado en la vena pulmonar superior izquierda. C,F: trazados y valores de evaluación hemodinámica invasiva. AD: aurícula derecha; AI: aurícula izquierda; AP: arteria pulmonar; VD: ventrículo derecho.
A pesar de un leve empeoramiento de la insuficiencia tricuspídea en el seguimiento a los 6 meses (grado III/V), la disfunción ventricular sistémica (fracción de eyección del ventrículo derecho del 35%) y la hipertensión pulmonar grave (presión sistólica en la arteria pulmonar > 60 mmHg), el paciente mostró una mejoría mantenida de su clase funcional (New York Heart Association II), una reducción significativa de los valores de fracción aminoterminal del propéptido natriurético cerebral tipo B (de 9.787 a 2.083 pg/ml) y menores requerimientos de diuréticos. Todo ello se tradujo en una notable mejoría de su calidad de vida, con una mejor capacidad funcional y sin rehospitalizaciones 1 año después del procedimiento.
Este caso refuerza el papel de la reparación valvular percutánea borde a borde de la válvula tricúspide incluso en un escenario tan sumamente adverso como es la transposición de grandes arterias congénitamente corregida. Pocos reportes han descrito previamente esta indicación1-3 y siempre en situaciones clínicas más favorables. Nuestro caso presenta varias limitaciones técnicas que lo hacen de interés, en especial la presencia de una válvula displásica, con una marcada restricción y un extenso defecto de coaptación. Así pues, se optó por el mayor dispositivo disponible, dirigiéndonos inicialmente a la zona con mayor regurgitación (septal-posterior) y realizando una captura profunda de los velos por el importante abombamiento, aun a riesgo de capturar inadvertidamente una cuerda tendinosa. No obstante, fue necesario un segundo dispositivo para reducir de manera significativa la regurgitación tricuspídea. A pesar del empirismo inherente a la situación clínica y las condiciones hemodinámicas desfavorables, con una hipertensión pulmonar grave y disfunción grave del ventrículo derecho sistémico, el paciente experimentó una franca mejoría clínica mantenida en el tiempo. Esta fue independiente de la falta de mejoría en las cifras de presión arterial pulmonar y de fracción de eyección del ventrículo derecho, por lo cual se cree que la reducción mantenida de la regurgitación tricúspide tuvo impacto clínico. En este sentido, solo en un caso se ha descrito mejoría de la hipertensión pulmonar1, lo que permitió reevaluar la idoneidad del trasplante cardiaco. Por lo tanto, se podría considerar la reparación valvular percutánea borde a borde como un tratamiento alternativo eficaz en los pacientes con transposición de grandes arterias congénitamente corregida no candidatos a trasplante ni a cirugía.
FINANCIACIÓN
No se ha recibido financiación.
CONTRIBUCIÓN DE LOS AUTORES
A. Salinas Gallegos y E. Pozo Osinalde: diseño y redacción del manuscrito. L. Nombela-Franco, P. Jiménez Quevedo y R. Estevez-Loureiro: manejo del paciente y revisión del manuscrito. J.A. de Agustín: revisión del manuscrito.
CONFLICTO DE INTERESES
L. Nombela-Franco y R. Estévez-Loureiro son consultores, proctors y han recibido honorarios por conferencias de Abbott Vascular, Edwards Lifesciences y Boston Scientific.
BIBLIOGRAFÍA
1. Gaydos SS, Capps CD, Judd RN, et al. Hemodynamic impact of MitraClip procedure for systemic tricuspid regurgitation in congenitally-corrected transposition of great arteries: A case report. Cardiovasc Revasc Med. 2020. https://doi.org/10.1016/j.carrev.2020.08.034.
2. Picard F, Tadros VX, Asgar AW. From tricuspid to double orifice morphology: Percutaneous tricuspid regurgitation repair with the MitraClip device in congenitally corrected-transposition of great arteries. Catheter Cardiovasc Interv. 2017;90:432-436.
3. Van Melle JP, Schurer R, Willemsen M, Hoendermis ES, van den Heuvel AF. Percutaneous tricuspid valve repair using MitraClip(R) for the treatment of severe tricuspid valve regurgitation in a patient with congenitally corrected transposition of the great arteries. Neth Heart J. 2016;24:696-697.
* Autor para correspondencia: Departamento de Cardiología, Instituto Cardiovascular, Hospital Clínico San Carlos, Profesor Martín Lagos s/n, 28040 Madrid, España.
Correo electrónico: eduardopozoosinalde@yahoo.es (E. Pozo Osinalde).